Preparados glucocorticoides: indicacións e contraindicacións para o seu uso, sobredose e posibles efectos secundarios
Maior irritabilidade nerviosa.
Do sistema cardiovascular:
Trombose de veas profundas.
Do sistema dixestivo:
Úlceras esteroides do estómago e dos intestinos.
Sangrado do tracto dixestivo.
Dexeneración graxa do fígado.
Dos sentidos:
Catarata posterior subcapsular.
Do sistema endocrino:
Inhibición da función e atrofia da córtex suprarrenal.
Por parte da pel:
Do sistema músculo-esquelético:
Fracturas e necrosis aséptica dos ósos.
Retraso do crecemento nos nenos.
Desde o sistema reprodutivo:
Irregularidades menstruais.
Violacións das funcións sexuais.
O desenvolvemento sexual atrasado.
Por parte de indicadores de laboratorio:
Retención de sodio e auga.
Exacerbacións de procesos infecciosos e inflamatorios crónicos.
EFECTOS LOCAIS.
Candidiasis da cavidade oral e da faringe.
Secura e queimadura da mucosa nasal e da faringe.
Perforación do septo nasal.
Supresión do eixe hipotalámico-hipofisario-suprarrenal (HPA)
A supresión do HPA é un dos efectos máis perigosos do uso de esteroides. A capacidade de resposta ao estrés fisiolóxico global (por exemplo, durante a cirurxía ou o trauma) pode ser debilitada, poñendo o paciente en risco de hipotensión e hipoglucemia. Entre os síntomas inclúense trastornos do comportamento, náuseas, hipotensión postural e hipoglucemia. O risco de aparición depende da dose, duración e réxime do tratamento, aínda que tamén son posibles outros factores. Existen diferenzas individuais significativas nos efectos da terapia con esteroides. Algúns pacientes tiveron supresión do HPA ao usar 15 miligramos de prednisona tomada diariamente durante varias semanas, mentres que outros non mostraron signos de supresión do HPA a pesar de usar doses diarias máis altas durante períodos máis longos. Así, é difícil prever o risco de supresión do HPA nun determinado paciente baseándose só na dosificación e na duración da terapia. A planificación da dose afecta o grao de supresión do HPA. As doses fisiolóxicas de glucocorticosteroides (5-7,5 miligramos de prednisona) tomadas pola mañá non provocan a supresión do HPA, pero se se dan as mesmas doses durante a noite, a secreción diaria normal de cortisol suprímese. As doses superiores ao nivel fisiolóxico comezan a exercer un efecto inhibidor ao redor dun mes. Coa terapia cada dous días (unha dose de dous días ás 8 horas todos os días), non hai unha supresión clínicamente significativa do HPA. Ademais, os programas de terapia diaria cíclica de 5 a 4 semanas non conducen á supresión. Non obstante, un ciclo de terapia de dúas semanas e unha interrupción de dúas semanas de terapia levan á supresión do HPA. Unha dose farmacolóxica diaria de glucocorticosteroides tomada pola mañá produce menos supresión de HPA que a mesma dose dividida e tomada durante o día.
A recuperación do HPA pode ocorrer dentro dos 12 meses. A función hipotalámico-hipofisaria retorna os primeiros 2-5 meses despois da interrupción da terapia, e maniféstase pola aparición no plasma de niveis normais de hormona adrenocorticotrópica (ACTH). Os signos de recuperación suprarrenal comezarán a aparecer despois de 6-9 meses, e os niveis normais de cortisol volven. A resposta máxima suprarrenal á ACTH non pode aparecer antes dos 9-12 meses despois da interrupción da terapia. Non hai ningún método comprobado para acelerar a recuperación da función HPA normal.
Un aumento dos niveis de ACTH non parece acelerar a recuperación suprarrenal. É moi difícil avaliar canto durará a ausencia clínicamente importante dunha resposta suprarrenal. Debido ás características individuais significativas dos pacientes, non foi posible establecer unha correspondencia fiable entre o grao de supresión do HPA e a concentración de cortisol no sangue. Para resolver esta incerteza, as probas de eixes HPA están a converterse nun importante tomador de decisións. Entre as varias probas (hipoglucemia inducida pola insulina, etc.), a proba máis empregada é a ACTH, polo que os seus resultados se relacionan ben cos niveis de cortisol medidos durante o estrés despois da cirurxía. A concentración de cortisol determínase e despois inxéctase unha ampola (250 cuncas) de ACTH sintético (cosintropina). A concentración de cortisol mídese en mostras de sangue tomadas despois de 30 e 60 minutos. A pesar de que esta proba proporciona unha certa porcentaxe de resultados falsos positivos, moita xente pensa que é moito máis conveniente e máis segura en comparación coa hipoglucemia inducida pola insulina - unha proba que se considera o `` estándar de ouro '' para a proba HPA.
Crese que unha proba que usa hormona liberadora de corticotropina (CRH) combina a sensibilidade dun test de hipoglucemia inducido pola insulina coa conveniencia dun test ACTH. Aínda que é importante detectar a tempo a supresión da HPA, este non é o único factor que determina a capacidade dos pacientes sometidos a terapia con corticosteroides para responder adecuadamente ao estrés. Algúns pacientes teñen unha resposta hipotensiva a pesar da ausencia de supresión do eixo HPA e pode que os pacientes con HPA suprimida non teñan signos clínicos de insuficiencia suprarrenal.
En pacientes con hipotiroidismo, cirrosis, hipoalbuminemia, así como en pacientes anciáns, pódese mellorar o efecto dos glucocorticosteroides.
Cando se prescriben glucocorticosteroides durante o embarazo, hai que ter en conta o efecto terapéutico previsto para a nai e o risco de efectos negativos sobre o feto, xa que o uso destes fármacos pode levar a un deterioro do crecemento do feto, algúns defectos do desenvolvemento (paladar fendido), atrofia da córtex suprarrenal (no terceiro trimestre) embarazo).
En nenos e adultos que toman glucocorticosteroides, as enfermidades infecciosas como o sarampelo e a varicela poden ser difíciles.
Os pacientes que toman doses inmunosupresoras de glucocorticosteroides están contraindicados na administración de vacinas vivas.
A osteoporose desenvólvese nun 30-50% dos pacientes que toman glucocorticosteroides sistémicos durante moito tempo (formas de dosificación oral ou inxectable). Por regra xeral, a columna vertebral, os ósos pélvicos, as costelas, as mans, os pés están afectados.
As úlceras de esteroides durante o tratamento con glucocorticosteroides poden ser asintomáticas ou asintomáticas, manifestando hemorraxia e perforación. Polo tanto, os pacientes que reciben glucocorticosteroides orais a longo prazo deben someterse periodicamente a fibroesofagogastroduodenoscopia e análise de sangue oculta fecal.
En diversas enfermidades inflamatorias ou autoinmunes (artrite reumatoide, lupus eritematoso sistémico e enfermidades intestinais), pódense presentar casos de resistencia aos esteroides.
Co uso simultáneo de glucocorticosteroides con outros fármacos, pódense observar os seguintes efectos:
Con antiácidos - diminución da absorción de glucocorticosteroides.
Con barbitúricos, hexamidina, difenina, carbamazepina, difenhidramina e rifampicina: biotransformación acelerada de glucocorticosteroides no fígado.
Con isoniazida e eritromicina - unha desaceleración na biotransformación de glucocorticosteroides no fígado.
Con eliminación destes medicamentos con salicilatos, butadio, barbitúricos, digitoxina, penicilina e cloramfenicol.
Con isoniazid - trastornos mentais.
Con reserpina, estados depresivos.
Con antidepresivos tricíclicos - aumento da presión intraocular.
Con agonistas adrenérxicos - aumento da acción destes fármacos.
Coa teofilina - o desenvolvemento de efectos cardiotóxicos e un aumento do efecto antiinflamatorio dos glucocorticosteroides.
Con diuréticos, anfotericina, mineralocorticoides - un maior risco de hipokalemia.
Con anticoagulantes indirectos, fibrinolíticos, butadiona, ibuprofeno e ácido etacrino - complicacións hemorráxicas.
Con indometacina e salicilados - lesións ulcerativas do tracto dixestivo.
Con paracetamol - aumento da toxicidade deste medicamento.
Con azatioprina, un maior risco de miopatías, cataratas.
Con mercaptopurina, é posible un aumento na concentración de ácido úrico no sangue.
Con hingamina - é posible aumentar os efectos indesexables deste medicamento (dermatite, miopatía, opacidade da córnea).
Con methandrostenolona - aumento dos efectos terapéuticos e indesexables dos glucocorticosteroides.
Con andrógenos e preparados de ferro - aumento da eritropoyese debido á maior síntese de eritropoetina.
Con medicamentos para reducir o azucre: diminución da eficacia destes medicamentos.
Os glucocorticosteroides inhalados de longa acción e os adadomimétricos β 2 teñen un efecto complementario e sinerxismo. A teofilina pode aumentar a actividade antiinflamatoria dos glucocorticosteroides inhalados.
Cando se usan glucocorticosteroides, é necesario obter o máximo beneficio terapéutico cun mínimo de efectos adversos. Na maioría dos casos, os esteroides non curan a enfermidade, senón que suprimen ou alteran a resposta inmune e inflamatoria e reducen os síntomas da enfermidade. Por iso, débese pesar coidadosamente os beneficios terapéuticos esperados e os riscos potenciais. O risco é insignificante cun breve curso de terapia (7-14 días), incluso co uso de altas doses, que poden ser moi eficaces nalgunhas situacións (por exemplo, con asma aguda). O aumento do apetito e a euforia son os principais efectos secundarios cos cursos curtos. Non hai consecuencias a longo prazo. A decisión de iniciar un curso máis longo de terapia con esteroides require ter en conta os riscos descritos anteriormente.
Os corticoides diferéncianse principalmente pola duración e o grao de acción. Os axentes de acción rápida son menos propensos a suprimir o eixe HPA, especialmente cando se usa unha dose baixa de mañá como parte dun réxime cada día. Os axentes de acción lenta son preferidos para situacións en que se deben usar grandes doses. A actividade mineralocorticoide do fármaco é desexable para insuficiencia suprarrenal, pero non para procesos inflamatorios significativos ou inmunoreactividade. Independentemente do medicamento elixido, é necesario continuar a terapia non esteroide, se isto permite o uso de dosificaciones mínimas de corticosteroides.
A prednisona é a máis usada entre os glucocorticosteroides. A súa curta vida media e baixo prezo fan que esta droga sexa a máis útil en acción inmunosupresora e antiinflamatoria. A prednisona é un metabolito hepático activo da prednisona e úsase en caso de problemas no fígado. A dexametasona é aproximadamente sete veces máis potente que a prednisona e ten unha vida media de 24 horas. Isto fai que sexa útil para probar o eixe HPA. A hidrocortisona (cortisona), unha droga aproximadamente catro veces menos potente que a prednisona. Úsase principalmente en doses farmacolóxicas para terapia adxuntiva en pacientes con supresión de HPA. Florinef (9-alfa-fluorohidroxicortisona) é un poderoso mineralocorticoide (practicamente sen efecto glucocorticoide), e úsase principalmente para a terapia de substitución da insuficiencia cortical suprarrenal.
Teoricamente, o uso de ACTH parecería atractivo porque evitaría a supresión do HPA, pero ACTH tamén estimula unha resposta indesexable de mineralocorticoides e andrógenos. Ademais, non se sabe que resposta de glucocorticoides se obterá a partir da dose administrada. Estes inconvenientes limitan o uso de ACTH.
Elección do réxime: todos os días ou outros días
No tratamento da maioría das enfermidades que requiren terapia con corticosteroides (asma, sarcoidosis e outras), un esquema cada dous días aplícase con éxito, aínda que a miúdo no inicio da terapia debe ser diario. As vantaxes importantes do réxime cada día son a prevención dunha supresión significativa do eixe HPA e a minimización do risco de Cushingoid sen perda importante de actividade antiinflamatoria. O risco da maioría dos efectos secundarios descritos anteriormente redúcese ou elimínase completamente aplicando o esquema todos os días.
Un réxime día a día só non pode evitar a supresión do eixo HPA se, por exemplo, se usa dexametasona para a terapia. Ademais, debe observarse estritamente o réxime de tratamento. O incumprimento do horario ou as variacións de dose do primeiro día non impide a supresión do HPA.
A terapia corticosteroide diaria úsase para agravamentos da enfermidade e para o tratamento de certas enfermidades que só poden ser afectadas polo réxime diario (por exemplo, arterite temporal, pemphigus vulgaris). No caso de que un réxime diario sexa inevitable, pódese minimizar a supresión do HPA se a dose diaria completa se toma á hora da mañá, coa dose máis baixa posible. Un réxime de única dose é case tan eficaz coma un réxime de única dose. Non obstante, a diferenza do esquema todos os días, o risco de desenvolver a síndrome de Cushing é maior.
Cambiando de todos os días ao día
A maioría dos pacientes con dinámicas positivas na terapia diaria son candidatos a cambiar ao réxime todos os días (excepcións, ver máis arriba). Isto permítelle cambiar a un esquema menos doloroso sen perder o control da enfermidade. A diferenza da redución da dosificación, a dose total tomada non cambia. A transición realízase por un aumento gradual da dose do primeiro día e unha diminución da dose no segundo día, ata que se toma unha dobre dose cada dous días, sen medicamentos adicionais nun día intermedio.
A taxa de transición depende da actividade da enfermidade subxacente, da duración da terapia, do grao de supresión do HPA e do estado clínico do paciente. Un esquema aproximado de transición consiste en aumentar a dose do primeiro día e diminuír a dose do segundo día en incrementos de 10 miligramos de prednisona (ou o seu equivalente) cando a dosificación diaria era superior a 40 miligramos e en incrementos de 5 miligramos cando a dosificación diaria era de 20 a 40 miligramos. Nunha dosificación inferior a 20 miligramos, o paso debe ser de 2,5 miligramos. O intervalo entre os cambios varía entre un día e varias semanas e determínase empíricamente en función da resposta clínica do paciente. É importante ter en conta que a maioría dos pacientes que toman un tratamento diario de corticoides durante máis de 2-4 semanas teñen supresión do HPA.
Redución da dose e interrupción da terapia
O cesamento brusco da terapia con corticosteroides que dura máis dun mes cunha dosificación de máis de 20-30 miligramos de prednisona ao día pode levar a unha exacerbación brusca da enfermidade subxacente ou levar a síntomas de abstinencia. Non hai xeitos probados de acelerar a recuperación do HPA. É necesario controlar as manifestacións da enfermidade e reducir a dosificación empíricamente, observando unha súbita exacerbación da enfermidade ou signos de insuficiencia suprarrenal (hipotensión postural, debilidade e disfunción gastrointestinal).
Un enfoque empírico para reducir a dosificación a niveis fisiolóxicos é facer cambios en incrementos de 10 miligramos de prednisona ou o seu equivalente cada 1-3 semanas se a dosificación inicial é superior a 40 miligramos ao día. Se a dosificación era inferior a 40 miligramos, o paso é de 5 miligramos.Unha vez que se alcanza a dose fisiolóxica de prednisona (5-7,5 mg), o paciente pódese cambiar a 1 mg de comprimidos de prednisona ou a dose equivalente de hidrocortisona, de xeito que se poidan producir novas reducións da dose por incrementos máis pequenos. Outras reducións semanais ou de dúas semanas pódense facer en incrementos de 1 miligramos.
Durante o proceso de redución da dosificación, algúns pacientes desenvolven a síndrome de abstinencia, caracterizada por depresión, mialxia, artralxia, anorexia, dores de cabeza e náuseas. Os estudos non lograron determinar a relación entre estes síntomas e os niveis de cortisol ou 17-hidroxicorticosteroide. Na maioría dos casos, as queixas producíronse cando os niveis eran normais. A resposta do HPA tamén foi normal en moitos destes pacientes. Descoñécense os mecanismos responsables deste síndrome, pero parecen estar relacionados coa taxa de redución da dosificación.
Identificación de insuficiencia suprarrenal inducida pola terapia de esteroides
Ao agardar estrés (incluso durante intervencións cirúrxicas), é importante saber o estado do eixe HPA e se será necesaria terapia con esteroides adicional. Como se observou anteriormente, é moi difícil predicir o inicio e a duración da supresión do HPA, o que fai que a proba do eixe HPA sexa útil para decidir se un paciente necesitará terapia esteroide adicional. Neste caso, a proba de cosintropina (ACTH sintético) é un xeito cómodo, seguro e eficaz de probar o eixe HPA. Se a concentración de cortisol despois de 60 minutos é superior a 18 cana / dL ou se produce un aumento desde o nivel inicial de polo menos 10 mug / dL, entón a resposta suprarrenal é suficiente para que o paciente poida soportar o estrés equivalente á anestesia xeral. A proba pódese realizar mediante 100 g de CRH por vía intravenosa. Se o paciente non ten unha resposta suprarrenal adecuada, debe realizarse unha terapia corticosteroide adicional para superar o estrés agudo. A hidrocortisona úsase habitualmente. Dependendo da gravidade do estrés, úsanse 100-400 miligramos de hidrocortisona ao día en varias doses. O límite inferior do intervalo de dose (100 miligramos) corresponde ao estrés no caso de sufrir un trastorno gastrointestinal, gripe ou extracción de dentes. En caso de tensión grave (trauma ou cirurxía), o paciente debe administrarse 100 miligramos de hidrocortisona parenteralmente cada 6-8 horas. Debe usarse unha xeringa pre-preparada que conteña 4 miligramos de dexametasona para uso parenteral en situacións de emerxencia. Se non se dispón de asistencia médica de emerxencia, o paciente está inconsciente ou non pode tomar esteroides por vía oral.
Os esteroides deben usarse con precaución en pacientes cuxo estado mental ou intelixencia poidan verse afectados debido ao risco de supresión do HPA. Os pacientes que toman o réxime de corticoides todos os días deben recibir instrucións sobre a importancia de adherirse ao réxime e tomar o medicamento antes das 8 horas para minimizar o risco de supresión do HPA. Os pacientes deben estar informados sobre a necesidade de aumentar a dosificación se hai estrés ou enfermidade durante todo o curso da terapia con corticoides. Os pacientes deben comprender a necesidade de poñerse en contacto cun médico e aumentar a dosificación do medicamento se están sometidos a estrés físico ou psicolóxico.
Moitos pacientes temen a terminación da esteroideoterapia ou se negan a reducir a dose de esteroides debido ao temor á recaída da enfermidade subxacente. Unha revisión detallada dos efectos secundarios da terapia a longo prazo é necesaria para explicar a necesidade de redución da dosificación e a conveniencia de acabar con corticosteroides.Nos casos en que se require unha terapia diaria con altas dosificación, os efectos mentais adversos (incluído o síndrome de Cushing) poden reducirse notificando ao paciente a probabilidade de que se produza e a súa reversibilidade.
Antiinflamatorios básicos e de acción lenta: metotrexato, sulfasalazina, cloroquina, auronofina
Metotrexato concentrado para a preparación dunha solución para inxección, liofilizado para a preparación dunha solución para inxección, unha solución para inxección, comprimidos, comprimidos recubertos - un axente antitumoral - antimetabolita.
Mecanismo de acción. O antitumoral, axente citostático do grupo antimetabolito inhibe a dihidrofolato reductasa, que está implicado na restauración do ácido dihidrofolato ao ácido tetrahidrofolato (un portador de fragmentos de carbono necesarios para a síntese de nucleótidos purinos e os seus derivados).
Inhibe a síntese, a reparación do ADN e a mitose celular. Particularmente sensible á acción de tecidos que se proliferan rapidamente: células de tumores malignos, medula ósea, células embrionarias, células epiteliais da mucosa intestinal, vexiga e cavidade oral. Xunto co antitumoral, ten un efecto inmunosupresor.
Farmacocinética A absorción oral depende da dose: cando se toma 30 mg / m2 está ben absorbida, a biodisponibilidade media é do 60%. A absorción diminúe cando se toma en doses superiores a 80 mg / m2 (crese que se debe a saturación).
En nenos con leucemia, a absorción oscila entre o 23 e o 95%. TCmax - 40 min-4 h con oral e 30-60 min - con administración de i / m. A comida diminúe a absorción e reduce a Cmax. Comunicación con proteínas plasmáticas - aproximadamente o 50%, principalmente con albúmina. Volume de distribución: 0,18 l / kg.
Cando se toma en doses terapéuticas, independentemente da vía de administración, practicamente non penetra no BBB (despois da administración intratecal no LCR, conséguense altas concentracións). Penetra no leite materno.
Tras a administración oral, é metabolizada parcialmente pola flora intestinal, a parte principal - no fígado (independentemente da vía de administración) coa formación dunha forma de poliglutamina farmacológicamente activa, que tamén inhibe a dihidrofolato reductasa e a síntese de timidina.
T1 / 2 en pacientes que reciben menos de 30 mg / m2 da droga na fase inicial é de 2-4 horas, e na fase final (que é longa) - 3-10 horas cando se usa pequeno e 8-15 horas cando se usa grandes doses do medicamento. Na insuficiencia renal crónica, ambas as fases da eliminación dos fármacos pódense prolongar significativamente.
É excretado principalmente polos riles en forma inalterada por filtración glomerular e secreción tubular (con administración iv do 80-90% excretada dentro de 24 horas), ata un 10% se excreta con bilis (con reabsorción posterior no intestino). A retirada do fármaco en pacientes con insuficiencia renal, expresada como ascite ou transudado, diminúe significativamente. Con administración repetida, acumúlase nos tecidos en forma de poliglutamatos.
Indicacións. Cáncer de mama, cancro epidermoide da cabeza e do pescozo, cancro de pulmón (células pequenas e non pequenas), tumores trofoblásticos (coriionepitelioma uterino, deriva quística, incluída a destrución), cancro de útero, cancro de ovario, cancro de vexiga, cancro colorectal, cancro esófago, cancro gástrico, cancro de páncreas, cancro testicular, leucemia linfoblástica aguda, infiltración leucémica das meninges (prevención e tratamento), leucemia mieloide aguda, linfoma non Hodgkin (principalmente linfosarcoma, especialmente en nenos e linfoma de Burkitt), lim. phogranulomatosis, micosis fungica, osteosarcoma non metastática, sarcoma dos tecidos brandos, cancro de meninges.
Formas graves de psoríase, artrite psoriásica, artrite reumatoide, dermatomiosite, LES, espondilitis anquilosante.
Contraindicacións Hipersensibilidade, inmunodeficiencia, embarazo, lactación.
No tratamento da psoríase e enfermidades reumáticas (opcional): inhibición grave da hematopoiese da médula ósea, insuficiencia hepática / renal grave.
Con precaución. Ascites, deshidratación, enfermidades obstructivas do tracto gastrointestinal, efusión pleural ou peritoneal, insuficiencia renal crónica, enfermidades parasitarias e infecciosas de natureza vírica, fúngica ou bacteriana - o risco de desenvolver unha enfermidade xeneralizada grave (actualmente ou transferida recentemente, incluído o contacto recente co paciente) - herpes simplex, herpes zoster herpes (fase viremica), varicela, sarampelo, amoebiasis, forteiloidosis (identificada ou sospeitosa), gota (incluíndo antecedentes) ou nefrourolithiasis de urato (incluíndo antecedentes), infección e inflamación IX mucosa oral, vómitos, diarrea (perda de fluído debido a vómitos intensos e diarrea pode levar a un aumento da toxicidade do metotrexato), úlcera gástrica e úlcera duodenal 12, colite ulcerativa, quimioterapia ou radioterapia, antes, astenia.
No tratamento de neoplasias malignas (opcional): aciduria (pH da orina inferior a 7), inhibición da hematopoiese da médula ósea.
Dosificación No interior, intramuscular, por vía intravenosa, intravenosa ou intratecal (está prohibido o uso dun medicamento cun conservante que conteña alcohol bencílico para a administración intratecal e a terapia de alta dose).
Os comprimidos tómanse por vía oral antes das comidas, sen masticar. As doses e os períodos de tratamento establécense individualmente segundo o réxime de quimioterapia, as indicacións, o réxime de tratamento, a "resposta" do paciente e a tolerancia, calculados en función da superficie corporal ou do peso corporal.
As doses superiores a 100 mg / m2 adminístranse só por vía intravenosa (unha solución ou concentrado é diluído previamente cunha solución de dextrosa ao 5% (10 mg - 0,5-1 l dunha solución de dextrosa) e baixo a cuberta de folinato de calcio.
En artrite reumatoide: a dose inicial normalmente é de 7,5 mg unha vez á semana cada vez ou 2,5 mg cada 12 horas (só 3 veces por semana). Para conseguir o efecto óptimo, a dose semanal pódese aumentar (non superior a 20 mg), entón a dose debe reducirse á máis baixa efectiva.
En psoríase, as doses iniciais son por vía oral, i.v. ou iv, 7,5-25 mg / semana, unha vez, ou 2,5 mg a intervalos de 12 horas 3 veces por semana ata que se consiga un efecto adecuado, pero non superior a 30 mg / semana. A dose adoita aumentar gradualmente, cando se consegue o efecto óptimo, a dose comeza a diminuír ata a menor efectiva.
Efecto secundario.Dos órganos hemopoéticos: leucopenia e trombocitopenia, panitopenia, anemia (incluída a aplástica), neutropenia, agranulocitosis, eosinofilia, linfadenopatía, enfermidades linfoproliferativas, hipogammaglobulinemia.
Do sistema dixestivo: anorexia, náuseas, vómitos, estomatite, xingivite, faringite, enterite, lesións erosivas e ulcerativas e hemorraxias do tracto gastrointestinal (incluíndo melena, hematemese), hepatotoxicidade (hepatite aguda, fibrose e cirrosis do fígado, insuficiencia hepática, hipoalbuminemia, aumento actividade de transaminases "hepáticas"), pancreatite.
Do sistema nervioso: dor de cabeza, somnolencia, disartria, afasia, hemiparesis, paresis, convulsións, cando se usa en altas doses - unha violación transitoria das funcións cognitivas, labilidade emocional, sensibilidade cranial inusual, encefalopatía (incluída leukoencefalopatía).
Por parte da pel: Erupción eritemática, picazón na pel, urticaria, fotosensibilidade, pigmentación da pel alterada, alopecia, ecquimosis, telangiectasia, acne, furunculose, eritema multiforme (incluída a síndrome de Stevens-Johnson), necrólise epidermal tóxica, ulceración e necrose cutánea, exfoli.
Desde o lado do órgano da visión: conxuntivite, deficiencia visual (incluída a cegueira transitoria).
Desde o sistema respiratorio: raramente - fibrose pulmonar, insuficiencia respiratoria, alveolite, pneumonite intersticial (incluída fatal), EPOC.
Do CCC: pericardite, derrame pericárdico, diminución da presión arterial, tromboembolismo (incluíndo trombose arterial, trombose vascular cerebral, trombose de veas profundas, trombose de veas retinais, tromboflebite, embolia pulmonar).
Do sistema xenitourinario: nefropatía grave ou insuficiencia renal, azotemia, cistite, hematuria, proteinuria, esperma e ovoxénese deteriorada, oligospermia transitoria, diminución da libido, impotencia, dismenorrea, secreción vaxinal, ginecomastia, infertilidade, aborto, morte fetal, defectos no desenvolvemento fetal.
Do sistema músculo-esquelético: artralxia, mialxia, osteoporose, osteonecrose, fracturas.
Infeccións: infeccións oportunistas que poñen en risco a vida (incluída a pneumonía por pneumocistis), CMV (incluída a pneumonía CMV), sepsis (incluída fatal), nocardiosis, histoplasmosis, criptococcosis, infeccións provocadas por Herpes zoster e Herpes simplex (incluído divulgado).
Outros: vasculite, diabetes mellitus, linfoma (incluído o reversible), síndrome de lise tumoral, necrose dos tecidos brandos, reaccións anafiláctidas, morte súbita.
No tratamento da artrite reumatoide: máis do 10% - aumento da actividade de transaminases "hepáticas", náuseas, vómitos, 3-10% - estomatite, trombocitopenia (menos de 100 mil / μl), 1-3% - erupción cutánea, picazón, dermatite, diarrea, alopecia, leucopenia ( menos de 3000 / μl), panitopenia, mareos, pneumonite intersticial, outras - diminución de hematocrito, cefalea, infeccións (incluídas as vías respiratorias superiores), anorexia, artralxia, dor no peito, tose, disuria, molestias nos ollos, hemorragias, febre, sudoración excesiva, tinnitus, secreción vaxinal.
No tratamento da psoríase: alopecia, fotosensibilidade, sensación de ardor da pel, raramente - placas erosivas dolorosas na pel.
No tratamento da artrite reumatoide xuvenil: aumento da actividade de transaminases "hepáticas" (14%), disfunción do tracto gastrointestinal (11%), incluída náuseas, vómitos, diarrea, estomatite (2%), leucopenia (2%), cefalea (1,2%), alopecia (0,5%), mareos (0,2%), erupción cutánea (0,2%).
Sobredose. Tratamento: a introdución dun antídoto específico - folinato de calcio, se é posible de inmediato, preferentemente na primeira hora, nunha dose igual ou superior á dose de metotrexato, adóitanse as doses posteriores segundo sexa necesario, segundo a concentración de metotrexato no soro. Para evitar a precipitación de metotrexato e / ou os seus metabolitos nos túbulos renales, o corpo está hidratado e alcalinizado, o que acelera a excreción de metotrexato.
Interacción. Aumenta a actividade anticoagulante de derivados de cumarina ou indandión e / ou aumenta o risco de hemorraxia reducindo a síntese dun factor procoagulante no fígado e deteriorado da formación de plaquetas.
Aumenta a concentración de ácido úrico no sangue, polo tanto, no tratamento de pacientes con hiperuricemia e gota concomitantes, pode ser necesario un axuste da dose de medicamentos antigota (alopurinol, colchicina, sulfinpyrazona), o uso de medicamentos anti-gota uricosúricos pode aumentar o risco de nefropatía asociada ao aumento da formación de ácido úrico durante o tratamento (é preferible usar alopurinol).
A administración simultánea de salicilatos, fenilbutazona, fenitoína, sulfanilamidas, derivados de sulfonilurea, ácido aminobenzoico, pirimetamina ou trimetoprim, unha serie de antibióticos (penicilina, tetraciclina, cloramfenicol), anticoagulantes indirectos e dependencia hipolipidémica ou diminución da secreción tubular, o que nalgúns casos pode levar ao desenvolvemento de efectos tóxicos graves, ás veces incluso mortais.
Os AINE con altas doses de metotrexato aumentan a concentración e frean a eliminación deste último, o que pode provocar a morte por grave intoxicación hematolóxica e gastrointestinal.Recoméndase deixar de tomar fenilbutazona durante 7-12 días, piroxicam durante 10 días, diflunisal e indometacina durante 24-48 horas, ketoprofeno e AINE con T1 / 2 curto entre 12 e 24 horas antes da infusión de metotrexato en doses moderadas e altas e durante polo menos 12 horas (dependendo da concentración de metotrexato no sangue) despois da súa realización. Débese ter precaución ao combinar AINE con doses baixas de metotrexato (pode diminuír a excreción de metotrexato polos túbulos renales).
Os fármacos que bloquean a secreción tubular (por exemplo, probenecid) aumentan a toxicidade do metotrexato reducindo a súa excreción polos riles.
Os antibióticos mal absorbidos no tracto gastrointestinal (tetraciclinas, cloramfenicol) reducen a absorción de metotrexato e perturban o seu metabolismo debido á supresión da microflora intestinal normal.
Retinoides, azatioprina, sulfasalazina, etanol e outros medicamentos hepatotóxicos aumentan o risco de hepatotoxicidade.
Os medicamentos que conteñen folatos (incluíndo multivitaminas) reducen o efecto tóxico do metotrexato sobre a medula ósea.
A L-asparaginase reduce a gravidade do efecto antitumoral do metotrexato inhibindo a replicación celular.
A anestesia usando óxido de dinitróxeno pode levar ao desenvolvemento de imprevisibles mielosopresión grave e estomatite.
Acyclovir para a administración parenteral con administración intratecal de metotrexato aumenta o risco de desenvolver trastornos neurolóxicos.
O uso de citacarina 48 horas antes ou dentro de 10 minutos despois do inicio da terapia con metotrexato pode provocar o desenvolvemento dun efecto citotóxico sinérxico (recoméndase axustar o réxime de dosificación en función do control de parámetros hematolóxicos).
Os medicamentos hematotóxicos aumentan o risco de hematotoxicidade do metotrexato.
Reduce a eliminación da teofilina.
A neomicina para a administración oral pode diminuír a absorción de metotrexato para a administración oral.
Varios pacientes con fungoides psoríase ou micósicos tratados con metotrexato en combinación con terapia PUVA (metoxaleno e UFO) foron diagnosticados con cancro de pel.
A combinación con radioterapia pode aumentar o risco de depresión da medula ósea.
O metotrexato pode reducir a resposta inmune á vacinación, polo que o intervalo entre a introdución de vacinas víricas vivas e inactivadas varía de 3 a 12 meses.
Nome químico. (1 - tio - beta - D - glucopirazinato) (trietilfosfina) ouro 2, 3, 4, 6 - tetraacetato
Acción farmacolóxica. A preparación de ouro para a administración oral (contén un 29% de Au), ten un efecto antiinflamatorio. Non se entende completamente o mecanismo de acción: crese que a supresión da inmunidade celular débese á captación de Au 3+ por monocitos e leucocitos nucleares polimórficos, o que conduce á inhibición da fagocitosis e ao bloqueo de encimas lisosómicas. Reduce a actividade dos sistemas sulfhidrilo e complexos enzimáticos de leucocitos e linfocitos, o que conduce a unha diminución da concentración de Ig e factor reumatoide, inhibe a síntese de coláxeno e Pg.
O efecto terapéutico desenvólvese gradualmente e obsérvase despois de 3-4 meses (ás veces 6 meses) desde o momento de tomar o medicamento.
Farmacocinética Absorción despois da administración oral - 25%. Comunicación con proteínas plasmáticas - 60%. Css nótase 3 meses despois do inicio do tratamento, cunha dose de 6 mg / día é de 68 μg / ml.
Metabolízase rapidamente no fígado (a auofofina non modificada practicamente non se detecta no sangue). T1 / 2 no sangue - 21-31 días, nos tecidos - 42-128 días. É excretado polos riles (60%) e coa bilis.
Indicacións. Artrite reumatoide (tratamento e prevención na detección de cambios radiolóxicos precoz nas articulacións), artrite psoriásica, síndrome de Felty.
Contraindicacións Hipersensibilidade, CHF, insuficiencia renal crónica, hepatite (fase activa), inhibición da hematopoiese da médula ósea, dermatite exfoliativa, enterocolite, embarazo, lactación, cachéxia, urticaria, eccema, erupción cutánea.
Réxime de dosificación.Interior: adultos - 6 mg / día, nenos - 0,1 mg / kg / día en 2 doses divididas.
Se a recepción é ineficaz durante 4 meses e está ben tolerada, é posible aumentar a dose ata adultos ata 9 mg / día en 3 doses divididas e para nenos ata 0,2 mg / kg / día. En caso de falla de tratamento durante os próximos 3 meses, o medicamento é cancelado.
Efectos secundarios. Do sistema nervioso e órganos sensoriais: letarxia, alucinacións, convulsións epilépticas, conxuntivite.
Do sistema respiratorio: faringite, traquite, pneumonía intersticial, pneumofibrose.
Do sistema dixestivo: xingivite, glosite, estomatite, vómitos, diarrea ou estreñimiento, gastralxia, gastrite, enterite necrótica, enterocolite ulcerosa, colite, hemorraxia gastrointestinal, colestase, colelitiasis, hepatite, insuficiencia hepática.
Do sistema xenitourinario: síndrome nefrótico con proteinuria masiva, insuficiencia renal, vaginite.
Do sistema hematopoietico: agranulocitosis, panitopenia, anemia, leucopenia, trombocitopenia.
Reaccións alérxicas: erupcións cutáneas, coceira da pel, eosinofilia, dermatite, hipertermia.
Interacción. Incompatible con penicilinas, levamisol, cloroquina, compatible con AINEs.
Os efectos secundarios son reforzados por citostáticos, hepato e nefrotóxicos, penicilamina.
As drogas mielotóxicas potencian o efecto hematotóxico da droga.
Instrucións especiais. Antes e durante a terapia, é necesario controlar o cadro de sangue periférico (contido de Hb, conteo de plaquetas), función renal (concentración de urea, creatinina, contido de proteínas na urina), función hepática (actividade de transaminases "hepáticas") durante o primeiro ano de tratamento - mensualmente, o segundo - cada 2-3 meses. Con proteinuria superior a 1 g / día, a terapia debe ser interrompida.
Sulfasalazina, comprimidos recubertos entéricos.
O grupo farmacolóxico é un axente intestinal antimicrobiano e antiinflamatorio.
Acción farmacolóxica. Un axente intestinal antimicrobiano, a sulfonamida, tamén ten un efecto antiinflamatorio. A posibilidade de usar colite non específica no tratamento está asociada á capacidade da sulfasalazina de acumularse selectivamente no tecido conectivo da parede intestinal coa liberación de ácido 5-aminosalicílico (5-ASA), que ten actividade antiinflamatoria, e a sulfapiridina, que ten un efecto bacteriostático competitivo, un antagonista competitivo de PAB.
Actúa contra diplococos, estreptococos, gonococos, E. coli.
Farmacocinética A absorción - 10%, é sometida a escisión por microflora intestinal coa formación de sulfapiridina - 60-80 e 25% 5-ASA. Comunicación con proteínas plasmáticas de sulfasalazina - 99%, sulfapiridina - 50%, 5-ASA - 43%.
A sulfiridina metabolízase no fígado por hidroxilación para formar metabolitos inactivos, 5-ASA por acetilación. T1 / 2 de sulfasalazina - 5-10 horas, sulfapiridina - 6-14 horas, 5-ASA - 0,6-1,4 horas. É excretada polos intestinos - 5% sulfapiridina e 67% 5-ASA, riles - 75-91% de sulfasalazina absorbida (en dentro de 3 días).
Indicacións. Colite ulcerativa inespecífica.
Contraindicacións Hipersensibilidade, insuficiencia hepática e / ou renal, anemia, porfiria, deficiencia conxénita de glicosa-6-fosfato deshidroxenase, lactación, idade infantil (ata 5 anos).
Categoría de acción sobre o feto. B
Dosificación No interior, 1 g 4-6 veces ao día, durante 2-3 semanas, seguido dunha diminución gradual da dose en 0,5-1 g cada 5-7 días, o curso do tratamento pode durar ata 4-6 meses. Nenos de 5-7 anos - 0,25-0,5 g 3-6 veces ao día, maiores de 7 anos - 0,5 g 3-6 veces ao día.
Efecto secundario. Cefalea, mareos, dispepsia: náuseas, vómitos, diarrea, dor abdominal, perda de apetito, mestura de sangue nas feces, pneumonite intersticial, hepatite inducida por fármacos, fotosensibilidade, cor laranxa amarela de ouriños, agranulocitosis, leucopenia, trombocitopenia, hemeolite, reaccións alérxicas: necrólise epidérmica tóxica (síndrome de Lyell), eritema exudativo maligno (síndrome de Stevens-Johnson), choque anafiláctico.
Interacción.Aumenta o efecto de anticoagulantes, antiepilépticos e medicamentos hipoglicémicos orais, así como os efectos secundarios de citostáticos, inmunosupresores, hepato e nefrotóxicos.
Os fármacos que inhiben a hematopoiese da medula ósea aumentan o risco de mielosupresión.
Cloroquina (Delagil) comprimidos. O grupo farmacolóxico é un axente antimalarial.
Acción farmacolóxica. O antiprotozoal tamén ten un efecto inmunosupresor e antiinflamatorio. Provoca a morte de formas de eritrocitos asexuais de todo tipo de plasmodia. Ten un efecto gametocida, con excepción de Plasmodium falciparum (presenta un efecto antigametocida). Debido á inhibición da síntese de ácidos nucleicos, ten un efecto antiinflamatorio inmunosupresor e non específico.
Farmacocinética Despois da administración oral, absorbe rapidamente e case por completo do tracto dixestivo. Cmax alcánzase ás 2-6 horas. O 55% únese á albumina plasmática. Esténdese axiña aos órganos e tecidos do corpo (fígado, riles, bazo, pulmóns). Penetra facilmente o BBB e a placenta.
Metabolízase en pequena cantidade (25%). É excretado polos riles (70% - sen cambios) lentamente. T1 / 2 - 1-2 meses.
Con insuficiencia renal, pode acumularse. Cunha reacción ácida de orina aumenta a velocidade de eliminación e aumenta a reacción alcalina.
Indicacións. Malaria (prevención e tratamento de todo tipo), amoebiasis extraintestinal, absceso hepático amoebico, LES (formas crónicas e subagudas), artrite reumatoide, esclerodermia, fotodermatose, porfiria cutánea tardía.
Contraindicacións Hipersensibilidade, insuficiencia hepática e / ou renal, inhibición da hematopoiese da médula ósea, trastornos graves do ritmo, artrite psoriásica, neutropenia, porfirinuria, embarazo.
Dosificación No interior, para a prevención da malaria - 0,5 g na primeira semana 2 veces, e despois 1 vez sempre o mesmo día da semana. O tratamento da malaria realízase segundo o seguinte esquema: 1 día unha vez 1 g, despois de 6-8 horas - 0,5 g, os días 2 e 3 do tratamento - 0,75 g diarias en 1 dose. Se é necesario - goteo iv.
Para a amebiasis, 0,5 g 3 veces ao día durante 7 días, logo 0,25 g 3 veces ao día durante outros 7 días, logo 0,75 g 2 veces por semana durante 2-6 meses.
Con artrite reumatoide - 0,25 g dúas veces ao día durante 7 días, logo - 0,25 g diariamente durante 12 meses.
Con SLE - diariamente 0,25-0,5 g.
En fotodermatose, 0,25 g diarias durante 1 semana, logo 0,5-0,75 g semanais.
Efecto secundario. Do sistema dixestivo: náuseas, vómitos, gastralxia.
Do sistema nervioso: mareos, dores de cabeza, trastornos do sono, psicoses, convulsións epilépticas.
Do CCC: dano miocárdico con cambios no ECG, diminución da presión arterial.
Dende os órganos sensoriais: con uso prolongado - nublado da córnea, danos na retina, visión alterada, chamada nas orellas.
Reaccións alérxicas: dermatite, fotosensibilidade.
Outros: mialxia, leucopenia, decoloración da pel e do pelo.
Indicacións para o uso de glucocorticoides
As indicacións para o uso de glucocorticoides son as seguintes:

- tratamento das enfermidades suprarrenais (os glucocorticoides úsanse para a insuficiencia aguda, unha forma crónica de insuficiencia, hiperplasia cortical conxénita), na que non son capaces de producir completamente (nin incluso) hormonas en abundancia,
- terapia para enfermidades autoinmunes (reumatismo, sarcoidosis) - baseada na capacidade destas hormonas para influír nos procesos inmunitarios, suprimilos ou activalos. Os glucocorticoides tamén se usan para a artrite reumatoide,
- tratamento de enfermidades do sistema urinario, incluídas as inflamatorias. Estas hormonas poden combater eficazmente as inflamacións violentas,
- Os glucocorticoides para alerxias úsanse como axentes que afectan á produción de compostos bioloxicamente activos que provocan e potencian as reaccións de intolerancia individuais,
- tratamento das enfermidades do sistema respiratorio (prescríbense glucocorticoides para o asma, pneumonía pneumocista, rinite alérxica). Cómpre destacar que diferentes fármacos teñen farmacodinámica diferente. Algunhas drogas actúan o suficientemente rápido, outras lentas.Non se poden usar medios cun efecto demorado e prolongado se é necesario aliviar manifestacións agudas (por exemplo, cun ataque asmático),
- Os glucocorticoides en odontoloxía úsanse no tratamento da pulpite, a periodontite, outros fenómenos inflamatorios, así como na composición de mesturas de recheo e como axente anti-choque para choques anafilácticos causados por drogas,
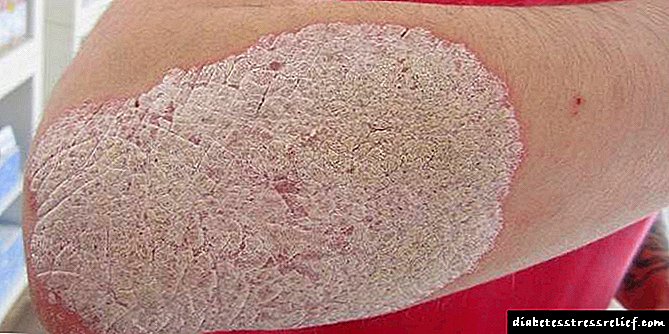
- tratamento de problemas dermatolóxicos, procesos inflamatorios na derme,
- tratamento de enfermidades do tracto gastrointestinal. A indicación de glucocorticoides é a enfermidade de Crohn,
- O tratamento dos pacientes despois das lesións (incluída a espalda) débese ao efecto anti-choque e antiinflamatorio dos fármacos.
- como parte da terapia complexa - con edema cerebral.

A partir de substancias pertencentes ao grupo dos glucocorticosteroides, creáronse preparados médicos en forma de pomadas, comprimidos, solucións en ampolas, líquidos inhalados:
- Cortisona
- Prednisona
- Dexametasona
- Hidrocortisona
- Beclometasona
- Triamcinolona.
Só un médico, en función das indicacións, pode prescribir glucocorticoides locais e decidir sobre a duración da terapia.
Efectos secundarios
A masa de efectos positivos que provocaron os glucocorticoides provocou o seu uso xeneralizado na medicina.
 A terapia hormonal non era nada segura, caracterízase pola presenza de moitos:
A terapia hormonal non era nada segura, caracterízase pola presenza de moitos:
- deterioración da calidade do cabelo e da pel, aparición de estrías, puntos negros,
- crecemento intensivo do cabelo en áreas atípicas do corpo en mulleres,
- diminución da forza vascular,
- a aparición de cambios hormonais,
- provocando ansiedade, psicose,
- violación do metabolismo da auga-sal.
O uso de glucocorticoides pode levar á aparición de moitas enfermidades:

- úlcera péptica
- obesidade
- inmunodeficiencia
- dismenorrea.
Hai casos en que os glucocorticosteroides provocan o rápido desenvolvemento de infeccións, cuxos axentes causantes estaban no corpo antes, pero non tiñan a capacidade de multiplicarse intensamente debido á actividade do sistema inmune.
Os efectos negativos ocorren non só co uso prolongado de glucocorticosteroides ou a súa sobredose. Tamén se detectan cunha forte abolición de fármacos, porque despois de recibir análogos artificiais de hormonas, as glándulas suprarrenais detéñenas por si soas.
Despois do final da terapia hormonal, a manifestación é posible:

- debilidades
- a aparición de dor muscular
- perda de apetito
- aumento de temperatura
- exacerbación doutras patoloxías existentes.
O efecto máis perigoso provocado pola cancelación brusca de tales hormonas é a insuficiencia suprarrenal aguda.
O seu principal síntoma é unha caída da presión arterial, síntomas adicionais - trastornos dixestivos, acompañados de dor, letarxia, convulsións epilépticas.
É tan perigoso cancelar voluntariamente a toma de glucocorticosteroides como auto-medicar co seu uso.
Contraindicacións
A abundancia de efectos secundarios causados polo uso de glucocorticosteroides, causa moitas contraindicacións para o seu uso:
- hipertensión grave
- fallo circulatorio
- embarazo
- sífilis
- tuberculose
- diabete
- endocardite
- xade.
Non está permitido o uso de medicamentos que conteñan glucocorticoides para o tratamento de infeccións a non ser que se dispoña dunha protección adicional do corpo contra o desenvolvemento doutras enfermidades infecciosas. Por exemplo, manchando pel con pomadas con glucocorticoides, unha persoa reduce a inmunidade local e corre o risco de desenvolver enfermidades fúngicas.
Cando prescriben glucocorticoides, as mulleres en idade reprodutiva deben estar seguros de que non hai embarazo; unha terapia hormonal pode levar á insuficiencia suprarrenal no feto.
Vídeos relacionados
Sobre os posibles efectos secundarios dos glucocorticosteroides no vídeo:
Os glucocorticoides merecen realmente unha atención e recoñecemento dos médicos, porque poden axudar en situacións tan difíciles. Pero as drogas hormonais requiren especial atención ao desenvolver a duración do tratamento e dosificación. O médico debe informar ao paciente sobre todos os matices que poden xurdir ao usar glucocorticoides, así como os perigos que agardan cunha negativa brusca do medicamento.
Diferentes grupos de drogas úsanse para tratar enfermidades dos riles. Un deles son os glucocorticosteroides. Os medicamentos teñen un efecto versátil sobre o corpo. A miúdo úsanse como medio de atención de emerxencia para complicacións e agravamentos de enfermidades.
Glucocorticosteroides (GCS): o nome xeralizado para as hormonas producidas pola capa cortical das glándulas suprarrenais. Este grupo inclúe glucocorticoides (cortisona, hidrocortisona) e mineralocorticoides (aldosterona). Hoxe, os corticoides sintéticos úsanse activamente para o tratamento. Pero ata o momento aínda se está estudando a súa seguridade e eficacia para o corpo, moitos aspectos de uso son bastante controvertidos.
Clasificación e forma de liberación

Os glicocorticosteroides son producidos pola cortiza suprarrenal baixo a influencia do sistema nervioso central e da glándula pituitaria. Regula a síntese de hormonas - o hipotálamo. Con falta de GCS no sangue a nivel de hidrocortisona e situacións estresantes (trauma, infección), sintetiza a corticoliberina, que é un estimulante da liberación de ACG da glándula pituitaria. Baixo a influencia desta hormona prodúcense glucocorticosteroides na cortiza suprarrenal.
Os GCS teñen un efecto antiinflamatorio, regulan os carbohidratos, os lípidos, o metabolismo das proteínas, controlan a función renal, a resposta do corpo a situacións estresantes. Na práctica médica úsanse hormonas naturais e os seus análogos sintéticos.
Como drogas GCS comezou a usarse a mediados do século pasado. As hormonas sintéticas teñen as mesmas propiedades que as naturais. Suprimen o proceso inflamatorio, pero non afectan aos axentes causantes da infección. Unha vez que os corticoides deixen de funcionar, a infección pode reanudarse.
Os glucocorticosteroides por un lado producen un poderoso efecto terapéutico, permítenche obter un resultado positivo en pouco tempo. Por outra banda, o seu uso está cheo de numerosas reaccións adversas de diversos sistemas e órganos.
As hormonas provocan estrés, o que leva a un debilitamento do sistema inmunitario, xa que normalmente se proporciona en estado tranquilo. Ademais, os corticoides sintéticos suprimen o traballo dos naturais, o que pode levar a unha función adrenal deteriorada. Polo tanto Os corticoides deben ser estrictamente regulados por un médico e só se deben prescribir se outras drogas son ineficaces.
Os glucocorticosteroides son liberados baixo a forma de:
- pastillas
- solucións de inxección
- aerosol
- pomadas, cremas.
Indicacións e contraindicacións
A acción de GCS é moi diversa:
- antiinflamatorios
- antialérxicos,
- inmunomodulador.

Os fármacos úsanse para deter o proceso inflamatorio en moitas enfermidades:
- reumatismo
- enfermidades do sangue
- lupus eritematoso sistémico,
- asma bronquial,
- pneumonía
- dermatite
- enfermidades neurolóxicas
- alerxias e moitas outras.
Os corticoides pódense usar para tales patoloxías renales:
- hinchazón do ril
- disfunción conxénita da corteza suprarrenal,
- lupus eritematoso
- síndrome nefrótico.
- intolerancia individual,
- varicela
- vacinación viva
- infeccións graves.
Os hormonas son prescritos con moito coidado na presenza das seguintes enfermidades:
- diabetes mellitus
- hipertensión
- úlcera do estómago
- insuficiencia cardíaca
- trombose
- glaucoma e catarata
- tuberculose
- trastornos mentais.
Non se poden tomar mineralocorcoides con deficiencia hepática e hipertensión, diabetes e potasio no plasma sanguíneo.
Nota! O GCS pode causar moitos efectos secundarios en varias áreas do corpo. Hormonas débiles e moderadamente activas con uso a curto prazo, por regra xeral, raramente causan complicacións graves. Para reducir o risco de desenvolver efectos non desexados, cómpre responder a tempo ante calquera cambio no corpo e axustar a dosificación dos medicamentos.
Enfermidade renal

Non hai recomendacións específicas sobre o uso de GCS. Non son medios de terapia específica. Unha excepción é a insuficiencia suprarrenal, na que os glucocorticoides realizan a función da terapia de reposición. Antes de prescribir calquera fármaco hormonal para enfermidades do sistema urinario, o médico debe pesar os pros e os contras.
Para cada paciente, a dose é seleccionada empíricamente para lograr o efecto desexado. De cando en vez, revísase, baseándose nun cambio de síntomas e no desenvolvemento de efectos secundarios. 1 dose de corticoides é seguro para a saúde. E un curso de ingreso de 1 semana sen contraindicacións practicamente non prexudica o corpo. Pola contra, se se sospeita de insuficiencia suprarrenal grave, unha única administración intramuscular de GCS pode salvar a vida do paciente.
Hai que ter en conta que unha forte cesación de medicamentos hormonais pode causar insuficiencia suprarrenal iatrogénica. Se se espera a administración a longo prazo de corticoides na enfermidade renal, seleccionarase a dose mínima suficiente para lograr a dinámica positiva. Pero normalmente prescríbense cursos longos, se a enfermidade ameaza directamente a vida do paciente.
A terapia de enfermidades renais con corticoides pode ser:
- Intenso - usado en condicións de risco de vida, administradas por vía intravenosa.
- Limitación - Para enfermidades crónicas prolongadas, prefírese os comprimidos que hai que tomar durante moito tempo. Úsase un esquema de recepción discontinua.
- Alternando - aplicar corticoides de acción curta e cunha duración media de acción, unha vez pola mañá, unha vez cada 2 días.
- Intermitente - tomar cursos de 3-4 días, despois pausa 4 días.
- Terapia de pulso - unha única inxección de corticoides nunha vea de polo menos 1 g como emerxencia.
O tratamento das enfermidades renales con fármacos hormonais debe ir acompañado da inxestión de vitamina D e calcio para previr a osteoporose. Para reducir o efecto dos corticoides sobre o estómago, recoméndase usar Almagel, Fosfalugel.
Hai moitos desacordos entre os especialistas sobre o uso de glucocorticosteroides nas enfermidades dos riles. A forma leve pode normalmente ser terapéutica con corticoides; os medicamentos son medicamentos de primeira liña para a enfermidade. A primeira semana, os pacientes reciben prednisona nunha dose de 1-2 mg / kg. Ao longo das 6-8 semanas, reduciuse gradualmente a cantidade de fármaco tomado. Algúns médicos recomendan tomar o medicamento todos os días.
Moitas veces despois da abolición dos glucocorticosteroides, ocorren recaídas. Estes pacientes considéranse resistentes ao GCS e son tratados con outros inmunosupresores (azatioprina). A nefritis con lupus tamén se pode tratar con medicamentos hormonais. Cando son membranosas, prescríbense hormonas (prednisona 120 mg) durante 2-2,5 meses cada dous días, cunha diminución gradual da dose nos próximos 1-2 meses.
Vexa a lista e características de patoloxías renales baratas.
As instrucións de uso do medicamento Nolicin para a cistite descríbense na páxina.
Na dirección, lea sobre o que mostra unha ecografía da vexiga en homes e como prepararse para o estudo.
Regras de retirada de drogas
Se tomar hormonas é longo, entón tes que cancelalas gradualmente. Os medicamentos inhiben o traballo da córtex suprarrenal, se interrompe bruscamente a inxestión, entón isto ameaza ao paciente con insuficiencia suprarrenal.
Non hai un esquema claramente establecido para reducir a dosificación de GCS. Todo depende da duración do curso da terapia e da actividade do medicamento.Se a terapia é de curta duración, tomar GCS pódese reducir en 2,5 ml cada 3-4 días (empregando o prednisolon como exemplo). Se o tratamento é máis longo, entón a redución da dosificación debe ser máis lenta - 2,5 mg cada 7-20 días.
Con coidado, precisa reducir a dose a menos de 10 mg - 1,25 mg cada 3-7 días. Se o GCS foi inicialmente prescrito nunha alta dosificación, entón a redución pode levarse a cabo con máis intensidade (en 3 días, 5-10 mg). Se se chega a unha dose do 30% da dose inicial, posteriormente cada 1,2 semanas redúcese 1,25 mg. Así, é posible conseguir unha cantidade de mantemento do medicamento durante un tempo suficientemente longo.
Lista de glucocorticosteroides
Os GCS divídense en varios grupos segundo a duración da súa acción.

- Cortisona
- Hidrocortisona
- Mazipredon
- Solu Cortef,
- Fluticasona
- Cyclesonide.
- Dexametasona (Dexamed, Megadexan),
- Betametasona (Celeston),
- Triamcinolona (Kenalog, Berlicort, Triacort).
O custo dos glucocorticosteroides pode ser diferente segundo o fabricante, a forma de liberación e a política de prezos da cadea de farmacia.
O custo medio das drogas máis comúns:
- Prednisolona -100 pezas de comprimidos 5 mg 103 rublos, 3 ampolas de 1 ml (30 mg) 48 rublos,
- Dexametasona - 1 ml solución de 25 ampollas 130-180 rublos, comprimidos de 0,5 mg 10 pezas 45 rublos,
- Hidrocortisona - ampollas 2 ml 2,5% 10 pezas 148 rublos,
- Metipred - comprimidos de 4 mg 30 pezas 175-190 rublos,
- Diprospan - 1 ampolla de 1 ml de 217 rublos.
Os glucocorticosteroides son hormonas sintetizadas polas glándulas suprarrenais. Distribúense por todos os tecidos do noso corpo e realizan varias funcións. Nalgunhas enfermidades, incluído o ril, empregan corticoides sintéticos e naturais para combater a inflamación e outros problemas. Pero a terapia con glucocorticosteroides ten dous lados. O seu uso pode levar a moitas consecuencias desagradables. Polo tanto, debe ser estrictamente regulado por un médico.
Vídeo: unha revisión e revisión das características do uso de glucocorticosteroides e como evitar efectos secundarios do uso de drogas:
O mecanismo de acción e efectos farmacolóxicos
O mecanismo do efecto antiinflamatorio dos corticoides é suprimir todas as fases da inflamación. Estabilizando as membranas das estruturas celulares e subcelulares, incl. A lise, os antiinflamatorios esteroides impiden a liberación de enzimas proteolíticas da célula, inhiben a formación de radicais libres de osíxeno e peróxidos de lípidos nas membranas. No foco da inflamación, os corticoides restrinxen vasos pequenos e reducen a actividade da hialuronidasa, inhibindo así a etapa de exudación, evitan a fixación de neutrófilos e monócitos ao endotelio vascular, limitan a súa penetración nos tecidos e reducen a actividade dos macrófagos e fibroblastos.
Na aplicación do efecto antiinflamatorio xoga un papel importante a capacidade do GCS de inhibir a síntese e liberación de mediadores inflamatorios (PG, histamina, serotonina, bradiquinina, etc.). Inducen a síntese de lipocortinas, inhibidores da biosíntese da fosfolipase A2 e reducen a formación de COX-2 no foco da inflamación. Isto leva a unha liberación limitada de ácido araquidónico dos fosfolípidos das membranas celulares e a unha diminución da formación dos seus metabolitos (PG, leucotrienos e factor activador das plaquetas).
O GCS pode inhibir a fase de proliferación, porque restrinxen a penetración de monocitos no tecido inflamado, impedindo a súa participación nesta fase da inflamación, inhiben a síntese de mucopolisacáridos, proteínas e inhiben os procesos de linfopoiese. Con inflamación da xénese infecciosa de corticosteroides, dada a presenza dun efecto inmunosupresor, é recomendable combinar con terapia antimicrobiana.
O efecto inmunosupresor do GCS débese a unha diminución do número e actividade dos linfocitos T que circulan polo sangue, unha diminución da produción de inmunoglobulinas e o efecto dos auxiliares de T nos linfocitos B, unha diminución do contido do complemento no sangue, a formación de complexos inmunitarios fixos e unha inhibición da formación da inhibición da formación da inmaginación .
O efecto antialérxico do GCS débese a unha diminución do número de basófilos circulantes, unha violación da interacción dos receptores Fc situados na superficie das mastocitos, coa rexión Fc de IgE e o compoñente C3 do complemento, que impide que o sinal entre na célula e vaia acompañado dunha diminución da liberación de histamina, heparina e serotonina das células sensibilizadas. e outros mediadores de alerxias de tipo inmediato e impiden o seu efecto sobre as células efectoras.
O efecto anticuerpo débese á participación de corticoides na regulación do ton vascular, fronte aos seus antecedentes aumenta a sensibilidade dos vasos sanguíneos ás catecolaminas, o que leva a un aumento da presión sanguínea, o metabolismo da auga salada, o sodio e a auga retéñense, o volume do plasma aumenta e a hipovolemia diminúe.
Glucocorticosteroides (GCS): o que é na medicina
Os glucocorticoides e os glucocorticosteroides son o mesmo, sinónimos que indican as hormonas producidas pola córtex suprarrenal, tanto naturais como sintéticas, ás veces empregando o acrónimo GKS para a brevidade.
Xunto cos mineralocorticoides, os corticoides constitúen un grupo extenso de corticoides, pero os corticoides son especialmente necesarios como medicamentos. Podes ler sobre que tipo de drogas son os corticoides.
Proporcionan ao médico grandes oportunidades para o tratamento de enfermidades graves, "extinguen" os focos da inflamación, poden mellorar o efecto doutros medicamentos, aliviar o inchazo e amordecer a sensación de dor.
Ao aumentar artificialmente a cantidade de corticosteroides no corpo do paciente, os médicos resolven problemas que antes parecían imposibles.
A ciencia médica tamén conseguiu que a GCS hoxe se poida aplicar "dirixida" - para actuar exclusivamente na área de problemas, sen molestar a outros que están sans.
Como resultado desta aplicación tópica, redúcese o risco de efectos secundarios.
O alcance dos medicamentos glucocorticoides é o suficientemente amplo. Estes fondos úsanse:
Ademais, o GCS úsase no tratamento de lesións (teñen un efecto anti-choque eficaz), e tamén para restaurar as funcións do corpo despois de operacións complexas, radiación e quimioterapia.

O réxime de tomar corticoides ten en conta a posible retirada de glucocorticoides, é dicir, o risco de deterioración no benestar do paciente despois de deixar de usar estes medicamentos.
O paciente pode incluso desenvolver o que se denomina insuficiencia glucocorticoide.
Para evitalo, é habitual completar o tratamento con glucocorticoides suavemente, reducindo coidadosamente a dose do medicamento ao finalizar o tratamento.
 Todos os procesos sistémicos máis importantes teñen lugar baixo a influencia de corticosteroides a nivel celular, incluído o xenético.
Todos os procesos sistémicos máis importantes teñen lugar baixo a influencia de corticosteroides a nivel celular, incluído o xenético.
Isto significa que só os especialistas poden traballar con preparados médicos deste tipo A auto-medicación está estrictamente prohibida, xa que pode causar todo tipo de complicacións.
O mecanismo de acción dos glucocorticoides sobre o corpo aínda non está completamente comprendido. Segundo descubriron os científicos, os corticosteroides fórmanse segundo o "mando" da glándula pituitaria: libera unha substancia chamada "corticotropina" ao torrente sanguíneo, que envía o seu propio sinal - sobre cantos corticosteroides deberían darse as glándulas suprarrenais.
Un dos seus principais produtos é un glucocorticoide activo chamado "cortisol", tamén se lle chama "hormona do estrés".
Tales hormonas prodúcense por varias razóns, a súa análise axuda aos médicos a identificar anormalidades do sistema endócrino, patoloxías graves e seleccionar tales medicamentos (incluído o GCS) e métodos de tratamento que serán máis eficaces en cada situación particular.

Os glucocorticoides afectan o corpo de varias maneiras á vez. Un dos máis importantes é o seu efecto antiinflamatorio.
Os GCS son capaces de reducir a actividade de encimas que destruen os tecidos do corpo, illando as áreas afectadas das saudables.
Os GCS actúan sobre as membranas celulares, tornándoas máis grosas, o que significa complicar o metabolismo, como resultado de infección non dan a posibilidade de estenderse por todo o corpo, situándoo nun "marco axustado".
Entre outras formas da influencia dos corticosteroides no corpo humano:
- Efecto inmunoregulador: en diferentes circunstancias, a inmunidade aumenta lixeiramente ou, ao contrario, a inmunidade é suprimida (os médicos usan esta propiedade de corticoides durante o transplante de tecidos de doantes),
- antialérxicos,
- anticuerpos - eficaz, por exemplo, nun choque anafiláctico, cando un medicamento debe proporcionar un resultado rápido para salvar o paciente.
O GCS pode afectar á produción de insulina (isto axuda a pacientes con hipoglucemia), acelerar a produción dunha sustancia como a eritropoetina (coa súa participación no sangue aumenta o contido de hemoglobina), pode elevar a presión sanguínea, afectar o metabolismo das proteínas.
Á hora de prescribir medicamentos, os médicos teñen que ter en conta moitos matices, incluído o chamado efecto resorptivo, cando o medicamento entra no torrente sanguíneo xeral despois da absorción e desde alí no tecido. Moitos tipos de corticoides permiten o uso de drogas máis localmente.
Por desgraza, non toda a "actividade" de glucocorticoides é completamente útil para os humanos.
O exceso de corticosteroides como consecuencia dun uso prolongado do medicamento leva, por exemplo, a que a bioquímica interna cambie - o calcio é lavado, os ósos fanse quebradizos, a osteoporose desenvólvese.
Os glucocorticoides distínguense polo tempo que traballan dentro do corpo.
Os medicamentos de acción curta permanecen no sangue do paciente desde dúas horas ata media xornada (os exemplos son Hydrocortisone, Cyclesonide, Mometasone). Pódense atopar as instrucións de uso de hidrocortisona.
GCS de acción media - ata un día e medio (Prednisolona, Metilprednisolona), a longo prazo - 36-52 horas (Dexametasona, Beclometasona).
Hai unha clasificación segundo o método de administración do medicamento:
Os glucocorticoides fluorados teñen un efecto especialmente potente no corpo do paciente. Estes fondos tamén teñen clasificación propia.
Dependendo da cantidade de flúor contida neles, son monofluorurados, di- e trifluorinados.
Unha variedade de medicamentos que utilizan GCS ofrécelle aos médicos a elección da forma adecuada (comprimidos, crema, xel, pomada, inhalador, parche, gotas nasais) e o "contido" correspondente para obter exactamente os efectos farmacolóxicos necesarios e en ningún caso. Non agrave o estado do paciente, provocando efectos secundarios no corpo.
A farmacoloxía é o destino dos especialistas, só un médico comprende en todas as sutilezas que efectos poden ter ou non este medicamento no corpo, cando e segundo que esquema se usa.
Como exemplo, damos o nome de glucocorticoides:
Métodos de tratamento
Desenvolvéronse diferentes tipos de métodos de tratamento con corticoides:
- substitución - úsase se as glándulas suprarrenais non poden producir de forma independente a cantidade necesaria de hormonas para o corpo,
- supresivo: para nenos con anormalidades conxénitas no funcionamento da cortiza suprarrenal,
- farmacodinámica (inclúe tratamentos intensivos, limitantes e de longa duración) - en terapia antialerxica e antiinflamatoria.

En cada caso, proporciónanse determinadas doses do medicamento tomado e a frecuencia do seu uso.
Entón, a terapia alternativa implica tomar glucocorticoides unha vez cada dous días, a terapia con pulso significa a pronta administración de polo menos 1 g do medicamento para coidados urxentes ao paciente.
Por que son perigosos os glucocorticoides para o corpo? Cambian o seu equilibrio hormonal e ás veces provocan as reaccións máis inesperadas. , especialmente se por algún motivo se produciu unha sobredose da droga.
As enfermidades provocadas por corticoides inclúen, por exemplo, a hiperfunción da córtex suprarrenal.
O feito é que o uso dunha droga que axuda ás glándulas suprarrenais a realizar as súas funcións, dálles a oportunidade de "relaxarse". Se a droga se interrompe bruscamente, as glándulas suprarrenais xa non poden dedicarse a un traballo completo.
Que outros problemas pode esperar despois de tomar GCS? Isto é:
Se o perigo se pon a tempo, case todos os problemas xurdidos poden resolverse con éxito. O principal non é agravalos coa auto-medicación, senón actuar exclusivamente de acordo coas recomendacións do médico.
Información xeral
A cortiza suprarrenal produce 3 tipos de hormonas:
- controlar o metabolismo de sodio potásico (mineralocorticoides),
- responsable da función reprodutiva (esteroides sexuais),
- glucocorticosteroides, responsables da regulación do metabolismo intermedio.

A produción de corticosteroides está controlada pola hipófise e o hipotálamo, pero lévase a cabo en órganos endocrinos emparellados, situados por encima dos riles, para os que levaron o seu nome.
Por primeira vez estas hormonas usáronse como medicamentos nos anos 40 do século pasado, obtiveron o seu nome debido á súa capacidade para regular o metabolismo da glicosa. Outros estudos clínicos demostraron que as hormonas non só afectan o metabolismo de lípidos, carbohidratos, proteínas, senón que tamén regulan a actividade do sistema circulatorio, riles, sistema inmunitario do corpo, participan no desenvolvemento e metabolismo do tecido óseo e afectan significativamente o sistema nervioso central.
O uso de hormonas na súa forma natural, a pesar da eficacia significativa do efecto, está limitado debido ao gran número de efectos secundarios negativos.
Análogos estruturais e funcionais
Os glucocorticoides son análogos estruturais e funcionais daquelas hormonas sintetizadas na córtex suprarrenal, na súa zona de paquete. As drogas presentadas neste grupo divídense en:
- glucocorticoides de orixe natural (cortisona, como prodróxeno que forma un metabolito activo),
- preparados sintéticos obtidos a base de hidrocortisona () unindo varios compostos químicos á súa molécula.

Son eles os que determinan a diferenza nas direccións aplicadas, un cambio significativo nas propiedades que dá a sustancia química adherida.
A fludrocortisona, formada pola adición dun átomo de flúor á cortisona, é 12 veces superior na actividade do glucocorticoide e 125 veces na cortisona mineralocorticoide.
A dexametasona, co grupo 16-metilo engadido á molécula de flucrocortisona, conserva a actividade glucocorticoide, pero ten un lixeiro mineralocorticoide.
A metilprednisolona, á que se lle engadiu 1 radical, supera o prodrogo por 5 veces no grao de actividade dos glucocorticoides.
Os análogos medicinais artificiais das hormonas da cortiza suprarrenal úsanse en medicina en casos graves cando o beneficio medicinal deles supera o dano dos seus efectos secundarios. Ás veces, á vista da afección extrema ou da gravidade concomitante da lesión, non hai outra opción que usar medicamentos hormonais. Os medicamentos corticosteroides úsanse para proporcionar:
- antiinflamatorios
- desensibilizador
- antitóxico
- anti-choque,
- acción inmunosupresora.

Estes están lonxe de todos os efectos medicinais que se poden obter coa dosificación calculada e un enfoque individual da cita. Nas enfermidades da columna vertebral, os fármacos glucocorticoides tamén se usan debido á súa capacidade de multiplicar en paralelo o efecto das drogas utilizadas no curso da terapia complexa.
O principio principal de prescribir medicamentos HA é lograr o máximo efecto, ás doses máis baixas posibles.Para este propósito, estanse a desenvolver análogos sintéticos que teñen un efecto significativamente máis pronunciado, o que permite reducir a dosificación e a duración do curso prescrito.
Clasificación e subdivisións de fármacos
Aínda non se desenvolveu unha clasificación xeralmente aceptada de fármacos con hormonas suprarrenais. Os practicantes subdividen GC segundo o lugar e o método de solicitude. Segundo isto, unha división moi condicionada en subgrupos, distínguense os seguintes tipos de fármacos:
- inxectable
- comprimido
- preparados tópicos en forma de pomadas, cremas, xeles e suspensións.

O segundo principio de asignación de categorías é a separación da principal substancia activa na composición do medicamento. Os medicamentos diferencian segundo o compoñente dominante:
- prednisona
- metilprednisolona,
- betametasona
- dexametasona, etc.
Existe unha diferenza clínica en medicamentos hormonais segundo a duración da exposición, que se establece usando investigación científica. Os glucocorticoides divídense en medios:
- exposición curta
- duración media
- acción longa (prolongada).

Por medio de breve exposición refírese, que é un análogo sintético da hormona. Debido á relativa inmutabilidade da súa composición, practicamente non afecta o equilibrio do metabolismo auga-sal e non viola o metabolismo celular.
A betametasona e a dexametasona, cunha fórmula estrutural modificada, poden ter un efecto a longo prazo, mentres que a prednisolona e a metilprednisolona son fármacos de media duración de influencia.
Na medicina, hai outra división dos glucocorticoides, que os distingue polo uso da sustancia principal, e implica a asignación:
- compostos endóxenos (naturais),
- análogos sintéticos (oleosos),
- análogos sintéticos (que conteñen flúor).
Ningunha das gradacións existentes, debido ao uso xeneralizado de varias formas de HA, non inclúe as características completas dun medicamento hormonal, e úsase na terminoloxía profesional de certos círculos científicos cualificados.
Drogas hormonais de influencia interna
As drogas de acción interna tamén se dividen en:
- intranasal (aplicado a través do nariz),
- parenteral
- oral (inxerido)
- inhalación
Tal separación dos medicamentos proporciona unha gradación clara das enfermidades ao prescribir a forma do medicamento. Intranasal úsanse comunmente para tratar:
- rinite alérxica
- inflamación idiopática da mucosa nasal,
- con pólipos no nariz.
Os parenterais son aplicables a enfermidades da cortiza suprarrenal, algunhas enfermidades da tiroides e outras patoloxías complexas.
Os fármacos inhalados son específicos para a exposición e son prescritos para disfuncións respiratorias complexas. O asma bronquial, a EPOC, a rinite alérxica son tratados con estes fármacos, como terapia básica. Entre as drogas de inhalación máis comúns, pódese destacar:
- acetonida de triamcinolona,
- beclometasona dipropionada,
- furoato de mometasona,
- budesonida
- propionato de fluticasona.

Casos de patoloxías graves do sistema respiratorio obrigados a realizar ensaios clínicos de novos fármacos inhalados para o tratamento do asma bronquial durante o embarazo. Demostraron que o tratamento con vapores de drogas no sitio patolóxico non só non aumentou a incidencia de nenos con enfermidades endócrinas, senón que posibilitou notar a súa aparición en nenos que naceron de nais con asma e que non usaron inhaladores para aliviar o seu estado.
A aparición dunha forma intranasal e inhalada de liberación de drogas salvou aos pacientes dalgúns dos riscos comúns ao usar medicamentos parenterais usando HA.
Co desenvolvemento de formas farmacoterapéuticas e novos análogos sintéticos, o uso de hormonas glucocorticoides, que se utilizan sen afectar os órganos internos e os sistemas metabólicos, faise menos perigoso.
Farmacodinámica e mecanismo de acción
A conexión natural das hormonas producidas polas glándulas suprarrenais está coordinada pola glándula pituitaria e o hipotálamo e realízase usando a correspondencia complementaria dun determinado código hormonal ao receptor celular. A procura de correspondencia entre os compoñentes de unión pódese realizar tanto dentro da membrana celular como fóra se a hormona non pode difundirse na célula. Os HA únense a receptores especiais de glucocorticoides dentro da membrana celular, o que provoca a aparición de ARN e a síntese que acompaña de proteínas reguladoras.

Existe un mecanismo citostático que pode frear os efectos das hormonas e substancias químicas e enzimáticas que aceleran o proceso de interacción.
Os principais efectos conseguidos polo uso de corticosteroides no corpo humano poden chamarse os seguintes:
- violación da síntese de mediadores inflamatorios (e leucotrienos), ao bloquear e inhibir o encima fosfolipase,
- a diferentes dosificación, a subministración de efectos inmunosupresores e inmunostimulantes, a inhibición da produción de anticorpos, a produción de linfocinas e citocinas,
- obstrución á retirada, estabilización da membrana celular mastular,
- efecto sobre o metabolismo de proteínas, carbohidratos, calcio, graxas, metabolismo de auga-electrólitos,
- aumento da sensibilidade das paredes dos vasos sanguíneos e do músculo cardíaco cara e,
- estimulación da formación de glóbulos vermellos e plaquetas,
- inhibición da produción de leucocitos, basófilos e eosinófilos,
- efectos sobre outras hormonas, incluídas as hormonas xenitais, luteinizantes, tiroides.

Cando se toman por vía oral, absorbense rapidamente, no intestino delgado, alcanzando a concentración máxima en menos dunha hora. A introdución é variable parenteral, e vén proporcionada polas características do medicamento. Son excretados polos riles, únense ás proteínas no sangue e son parcialmente degradadas polo fígado. A vía de administración depende da natureza do fármaco e das características da enfermidade. No tratamento do sistema músculo-esquelético tamén se usan inxeccións intraarticulares.
Lista de medicamentos hormonais
A lista de medicamentos do grupo hormonal glucocorticoide é bastante extensa, pero na práctica clínica considéranse os máis comúns:
- Prednisona
- Triamcinolona
- Dexametasona
- Betametasona.

Os análogos de fármacos baixo nomes comerciais, ou certas variedades cunha forma modificada, considéranse menos comúns e requiren o estudo das instrucións de uso, cunha descrición clara de contraindicacións e indicacións, a estrutura da fórmula química e as características do propósito.
Pertence á lista B, esixen certas condicións de almacenamento. Antes do uso independente de tales drogas, debes consultar ao teu médico, prestar especial atención á posibilidade ou contraindicación do medicamento no seu uso para recentemente nados, nenos e mulleres embarazadas.
Todos os fármacos do grupo hormonal glucocorticoides están descritos na clasificación anatómico-terapéutica-química (ATX), que ten unha estrutura xerárquica e facilita a busca do medicamento adecuado. Calquera medicamento deste grupo é sometido a probas clínicas indispensables, e é descrito por especialistas.
Indicacións de uso
Ata a data, non só se estudaron ben os efectos secundarios e terapéuticos, senón tamén a interacción do HA con moitos fármacos, as dosas necesarias e os esquemas de terapia complexa. Isto posibilitou o uso de drogas en moitas ramas da medicina, como medicamentos básicos e auxiliares.
Condicións patolóxicas nas que o indubidable beneficio de GK converterá nunha lista moi incrible de patoloxías crónicas, sistémicas e agudas. En reumatoloxía úsanse para tratar:
- lupus eritematoso sistémico,
- espondilite anquilosante,
- esclerodermia sistémica,
- polimialxia reumática.
Os glucocorticoides úsanse no tratamento da vasculite e a pielonefrite, en endocrinoloxía que tratan:
- insuficiencia suprarrenal
- tireotoxicose e deficiencia.

- colite ulcerativa,
- hepatite grave
- A enfermidade de Crohn en fase aguda.
Pero o alcance das drogas que conteñen hormonas non está limitado a isto. Usos de cardioloxía para:
- algúns tipos de pericardite,
- miocardite post-viral e non específica de leucocitos.
- con asma bronquial,
- pneumonía eosinofílica,
- alveolite e bronquiolite,
- sarcoidosis dos pulmóns.

En hematoloxía, as drogas hormonais tratan a trombocitopenia e a anemia.
HA - un medicamento de elección indispensable en condicións agudas e en transplantoloxía. A pesar das contraindicacións e efectos secundarios, os glucocorticoides están entre os remedios amplamente usados, e ás veces insubstituíbeis, para lesións graves e condicións agudas. No tratamento de enfermidades da columna vertebral úsanse para a terapia:
- osteocondrose,
- aliviar a dor
- artrite non infecciosa,
- Espondilite anquilosante,
- danos na columna vertebral e nas súas membranas.
A creación de fármacos sintéticos acelerou e aumentou o grao de impacto deste grupo de drogas, ampliando aínda máis o alcance das súas actividades.
Características do uso terapéutico de hormonas e precaucións
Os glucocorticosteroides, debido ao seu uso xeneralizado, úsanse en varias ramas da medicina para o tratamento dun espectro variable de enfermidades. Durante case todas as condicións coñecidas, desenvolvéronse esquemas terapéuticos e protocolo en estados de diferente gravidade.
A duración da acción do medicamento, o grao da súa recomendación, a duración do curso de tratamento, a curta duración ou a prolongación, e incluso unha certa dosificación son todos competencia do médico que sabe manexar un medicamento específico.
É por iso que se di moito sobre a inadmisibilidade da autoadministración de fármacos hormonais sintéticos, sobre a extrema precaución do seu uso, o manexo coidadoso e reflexivo dos fármacos deste grupo. Calquera, o remedio máis curativo, con cita non cualificada e recepción inxustificada, pode causar danos importantes ao corpo humano. Polo tanto, o tratamento só debe facelo un médico que estea familiarizado con todas as sutilezas dos efectos dun determinado medicamento.
Instrucións de uso:
Glucocorticosteroide: unha sustancia de orixe natural ou sintética procedente dunha subclase de hormonas da córtex suprarrenal.
O efecto dos glucocorticosteroides no corpo
Pola súa natureza química, estas substancias son esteroides. En humanos e animais, o principal lugar da súa formación é a corteza suprarrenal. Os glucocorticosteroides xeralmente aumentan a resistencia do corpo a efectos estresantes, e esta é precisamente a importancia biolóxica destas substancias hormonais.
Os glucocorticosteroides afectan o metabolismo no corpo, principalmente sobre hidratos de carbono, minerais, proteínas e auga.
Os medicamentos glucocorticosteroides creados artificialmente actúan como fármacos antiinflamatorios, desensibilizantes, inmunosupresores, antitóxicos e anti-choque.
Os principais efectos dos glucocorticosteroides
Os glucocorticosteroides dan conta do seu efecto ao difundirse a través das membranas celulares no citoplasma. Alí únense a receptores intracelulares especiais a través dos cales afectan á síntese de proteínas.Tamén se coñece o efecto inhibidor destas hormonas sobre a fosfolipase A2 e a hialuronidasa, que son encimas de inflamación.
As substancias deste grupo estabilizan as membranas celulares, o que inhibe a liberación de substancias bioloxicamente activas (histamina, leucotrienos, tromboxano) das mastocitos. Retardan a formación de citocinas proinflamatorias a partir do ácido araquidónico.
O efecto inmunosupresor das hormonas dos glucocorticosteroides úsase na medicina para suprimir unha excesiva agresión do sistema inmunitario dirixida ao propio corpo. Isto é necesario para transplantes de órganos (por exemplo, ril, medula ósea), tumores malignos e enfermidades autoinmunes. Un efecto positivo do tratamento con glucocorticosteroides conséguese ao suprimir a migración de células nai e linfocitos, así como a interacción de distintos grupos de linfocitos entre si.
A capacidade dos glucocorticosteroides para aumentar a presión arterial realízase aumentando a liberación de adrenalina e restablecendo a sensibilidade dos receptores de adrenalina, estreitando o lumen dos vasos e reducindo a súa permeabilidade. Esta propiedade permítelles afrontar condicións de choque en situacións críticas.
Os glucocorticosteroides aumentan a formación de glicosa no fígado e a descomposición de proteínas, o que aumenta o contido en aminoácidos libres e glicosa no sangue. Neste caso, o organismo recibe unha cantidade suficiente de substancias de alta enerxía.
Tratamento con glucocorticosteroides
Na medicina, os preparados de glucocorticosteroides segundo a duración da acción divídense en 3 grupos: curta, media duración e acción a longo prazo.
Os glucocorticosteroides de acción curta inclúen hidrocortisona. Este é un análogo da propia hidrocortisona do corpo, en comparación con outras drogas, ten un efecto mínimo no metabolismo da sal da auga.
Medicamentos de glucocorticosteroides de duración media: metilprednisolona e prednisolona.
Os glucocorticosteroides de longa acción inclúen betametasona e dexametasona.
No tratamento de glucocorticosteroides úsanse formas de administración orais, inhalación, intranasal e parenteral.
Os fármacos para administración oral absorbense ben do tracto dixestivo, no sangue únense ás proteínas do plasma. Úsanse para tratar a disfunción conxénita da córtex suprarrenal, insuficiencia suprarrenal primaria e secundaria, con tiroidite subaguda, enfermidade de Crohn, enfermidades pulmonais intersticiais e EPOC en fase aguda.
Dos glucocorticosteroides inhalados, úsanse máis frecuentemente budesonida, triamcinolona acetonida, dipropionato de beclometasona, furoato de mometasona, propionato de fluticasona. Son moi adecuados para o tratamento básico do asma e a EPOC, rinite alérxica.
Os glucocorticosteroides intranasais prescríbense para a polipose nasal, a rinite alérxica e idiopática. A peculiaridade da súa administración suxire que unha parte do fármaco entrará na mucosa nasal e nas vías respiratorias, e unha parte será tragada e entrará no tracto dixestivo.
Que son os glucocorticoides
Os glucocorticoides son un tipo de hormona humana que é producido polas glándulas suprarrenais, ou máis ben pola súa casca. Toman parte activa nos procesos que se producen no corpo. Tales hormonas comezan a actuar, principalmente en situacións de emerxencia: choque, estrés, trauma. Isto determina o seu uso en medicina para proporcionar efectos antiinflamatorios e antialerxicos.

O mecanismo do seu traballo é aproximadamente o seguinte:
- a hormona, que entra na célula, afecta aos receptores,
- actúan os xenes que regulan a resposta inmune do corpo,
- o traballo activo dos xenes reduce a inflamación e inhibe o sistema inmunitario do paciente.
Ademais, as hormonas glucocorticoides estimulan que os vasos sanguíneos se constrinxan, a partir dos cales se fan menos permeables, mentres se activa o traballo das células do fígado. Así, o corpo está protexido de toxinas e un estado de choque.
Indicacións para terapia con glucocorticoides:
- trastornos das glándulas suprarrenais,
- enfermidades do sistema músculo-esquelético,
- alerxias
- asma
- enfermidades da pel
- sarcoidosis
- Enfermidade de Crohn.
Se o paciente está cargado de asma ou alerxias, entón as hormonas prescríbense en forma de inhalacións.
Efectos secundarios
Os glucocorticoides teñen un gran efecto na produción doutras hormonas no corpo. A tiroides é máis susceptible a este efecto. Baixo a influencia das hormonas suprarrenais, a súa actividade diminúe.
Os efectos secundarios da terapia con glucocorticoides pódense dividir en dous grupos: local e sistémico.
Efectos secundarios locais
Na maioría das veces, consecuencias indesexables deste tipo xorden despois do uso de preparados por inhalación que conteñen hormonas.
Innovación en diabetes: basta beber todos os días.

O paciente pode estar perturbado por:
- nariz coceira
- estornudos frecuentes
- transpiración na nasofaringe,
- candidiasis na boca
- tose.
Por regra xeral, son temporais e desaparecen completamente unha vez que se suspende a terapia hormonal.
Efectos secundarios sistémicos
A lista de efectos secundarios de natureza sistémica é moito máis impresionante. Depende principalmente de que sistema sexa o máis vulnerable.
Os esteroides suprimen completamente o efecto das glándulas suprarrenais. E incluso despois da abolición dos esteroides, hai moito tempo que non son capaces de volver a traballar "a toda forza". A síndrome de retirada é perigosa porque o corpo pode presentar unha escaseza aguda de glucocorticoides. Incluso unha pequena lesión ou estrés pode causar un dano no corpo. Unha persoa con falta de tal hormona séntese letárgica, apática. Non hai apetito e perda de peso importante.

A maior preocupación é a capacidade hipotensiva dos esteroides. A diminución da presión baixo a súa influencia é extremadamente difícil de tratar con drogas tradicionais.
Os esteroides suprimen a inmunidade humana, principalmente ao diminuír a resistencia do corpo a infeccións de natureza bacteriana. O risco de infección depende directamente da dose de glucocorticoides: dose maior - maior risco. Este efecto é a causa raíz do desenvolvemento de complicacións, a miúdo cun desenlace fatal.
Coa terapia de substitución hormonal, as infeccións no corpo están latentes, só é posible un aumento da temperatura corporal. Para evitar tales efectos secundarios, recoméndase aos pacientes vacinas contra a gripe e o pneumococo antes do tratamento. Ademais, non será bo facer unha proba de tuberculina.
A miúdo os glucocorticoides causan trastornos mentais nos pacientes. Isto pódese manifestar tanto en lixeira irritabilidade como en depresión e psicosis severa.
Moitas veces a consecuencia da terapia hormonal pode incluso ser un cambio na aparencia do paciente: aumento de peso, redondeo da cara, acne, estrías lila, hematomas. Por regra xeral, tales efectos indesexables redúcense ou desaparecen completamente despois dunha redución da dose.
Ofrecemos un desconto aos lectores do noso sitio.
Sobredose
A superación da dose requirida, de calquera tipo de medicamento, afecta negativamente á saúde e ao benestar do paciente. Non se sucede tan a miúdo unha sobredose de glucocorticoides.

- hinchazón
- violación do equilibrio de electrólitos no corpo
- calambres.
En casos extremadamente raros, é posible dor abdominal, azia, náuseas e vómitos.
Nos primeiros síntomas dunha sobredose dun medicamento hormonal, debe deterse a súa administración. O tratamento é sintomático. Non se realiza terapia específica.
Interacción con outros medicamentos
Se o paciente toma algún medicamento con regularidade, é necesario informalo ao médico antes do nomeamento de glucocorticoides. A interacción dalgunhas drogas entre si pode provocar efectos non desexados.

O uso simultáneo de fármacos para reducir a acidez do estómago con esteroides debilita o efecto destes últimos. O uso combinado de hormonas e aspirina pode provocar a formación de úlceras no tracto dixestivo, e con paracetamol - un aumento múltiple na súa toxicidade.
Os medicamentos deseñados para baixar os niveis de glicosa perden o seu efecto se se usan en paralelo con glucocorticoides. As hormonas esteroides en combinación con diuréticos poden provocar lixiviación de potasio do corpo.
Con precaución, é necesario tomar tales medicamentos para persoas de idade avanzada, pacientes con cirrosis do fígado, xa que neste caso pódese mellorar o efecto das hormonas.
Os pacientes sometidos a terapia hormonal inmunosupresora están contraindicados nas inxeccións de vacinas vivas.

Como minimizar os efectos secundarios
Hai algúns grupos de pacientes contraindicados na terapia con glucocorticoides.
Estes inclúen:
- pacientes con diabetes
- pacientes con antecedentes de anormalidades mentais,
- pacientes do tracto gastrointestinal
- pacientes con hipertensión arterial pronunciada e / ou insuficiencia cardíaca.

O resto pódese empregar terapia hormonal. Para minimizar o risco de efectos secundarios, debes controlar coidadosamente a túa saúde. Se se detectan patoloxías, o médico debe ser informado sobre isto.
A todos os pacientes sometidos a tratamentos con esteroides, independentemente do seu tipo e tipo, recoméndase que tome complexos vitamínicos-minerais, debendo prestar especial atención ao calcio e á vitamina D. Nalgúns casos, é posible que necesite tomar insulina.
Para maior claridade e facilidade de percepción, todos os efectos secundarios e métodos para detelos están presentados na táboa.
Táboa: "Efectos indesexables da terapia con esteroides e formas de reducilos"
| Efecto secundario | Principais sinais | Hormonas con efecto negativo (casos frecuentes) | Accións de redución de efectos |
|---|---|---|---|
| Retención de fluídos no corpo | O inchazo, por regra xeral, ocorre na cara, nas pernas. | Cortisona, hidrocortisona. | O uso de diuréticos, adhesión a unha dieta baixa en sodio. |
| Osteoporose | Dor severa nas articulacións, costas, fracturas de ósos e vértebras (especialmente en persoas maiores) | Dexametasona | O uso de vitamina D, sales de calcio |
| Dano muscular | Sensación de debilidade nas extremidades, debilidade. | Dexametasona, Prednisona, Prednisona. | O uso de anabolicos, a abolición da dexametasona. |
| Úlcera péptica | Na maioría dos casos, é asintomático. En 1 de cada 10 casos, pode haber hemorraxia gástrica. | Prednisona, prednisolona. | Recoméndase metilprednisolona. A vía óptima de administración é parenteral. |
| Diabetes hormonais | Por regra xeral, non se observan complicacións diabéticas. | Betametasona | O uso de tratamentos alternativos. |
| Trastornos mentais | Ansiedade, axitación extrema, insomnio, depresión, psicosis. | Ocorre extremadamente raramente cando se usa metilprednisolona. | Se é posible, excluír a terapia hormonal en persoas con psique inestable. A falta de tal oportunidade de usar psicotrópicos con esteroides. |
| Aumento de peso | Sensación de fame constante, aumento do apetito. | Dexametasona | Nutrición dietética, a excepción da hormona que provoca aumento de peso. |
| Perda de peso severa | Non hai signos evidentes. | Triamcinolona | O uso de esteroides anabólicos, aminoácidos. |
Por desgraza, o tratamento con glucocorticoides case sempre está asociado á aparición de certos efectos secundarios. A responsabilidade disto recae no médico e co paciente.O médico debe examinar minuciosamente a historia do paciente para excluír a posibilidade de incompatibilidade dos medicamentos tomados. O paciente, á súa vez, debe observar estrictamente a dosificación e o tempo de tomar os fármacos.
Os glucocorticoides son medicamentos graves. O seu uso debe argumentarse só por extrema necesidade. A terapia debe ser o máis curta posible.
A recepción de hormonas en todo caso altera o equilibrio no corpo. O principal é que as consecuencias para o paciente sexan mínimas.
Se hai unha oportunidade sen prescindir da terapia hormonal, paga a pena usala.

A diabetes sempre leva a complicacións mortais. O exceso de azucre no sangue é extremadamente perigoso.
Aronova S.M. deu explicacións sobre o tratamento da diabetes. Ler completo
Mecanismo de acción e efectos
Os corticosteroides son hormonas esteroides na súa orixe, o seu mecanismo de acción é diferente das hormonas de natureza proteica. O GCS entra nas células diana e penetra no seu citoplasma a través da membrana celular, onde se unen aos receptores e exercen o seu efecto específico.
Estes medicamentos hormonais afectan a función da maioría das células do corpo e teñen unha gran importancia práctica. Os seus principais efectos son os seguintes:
- 1. Participa na regulación do metabolismo normal:
- Afectan o metabolismo dos carbohidratos (aumentan a concentración de glicosa no sangue de varias formas).
- 2. Afectar o metabolismo das proteínas (estimular a formación de ARN e proteínas no fígado, potenciar a descomposición de proteínas nos músculos e outros tecidos).
- 3. Afectar o metabolismo das graxas (en diferentes áreas prodúcense 2 procesos opostos - o crecemento e a descomposición do tecido adiposo).
- Posúe actividade mineralocorticoide. Son capaces de estimular receptores de mineralocorticoides (aínda que en menor medida que as hormonas mineralocorticoides), o que como resultado leva á absorción inversa de sodio no corpo. Isto provoca en última instancia a retención de líquidos, o aumento do volume de sangue e unha maior excreción de ións de potasio na orina.
- A resistencia do corpo ao estrés aumenta. Un aumento da glicosa no sangue baixo a influencia dos glucocorticoides proporciona a enerxía necesaria para protexerse contra o estrés causado por trauma, infección, enfermidades, etc.
- Teñen un efecto inmunosupresor (reduce o número de clases diferentes de glóbulos brancos).
- Teñen un poderoso efecto antiinflamatorio, o que se explica por unha diminución do nivel, distribución da función dos linfocitos T e B e unha violación da formación de mediadores inflamatorios. Estabilizan as membranas lisosomas, reducen a liberación de histamina por basófilos. Como resultado, as tres etapas da inflamación están inhibidas.
- Participa na regulación do sistema endocrino: ralentiza a secreción de ACTH e tirotropina, aumenta a produción de hormona de crecemento.
- Afectar o sistema respiratorio. No feto no último mes de embarazo, os corticoides contribúen á formación de tensioactivo, que cobre os alvéolos pulmonares por dentro e é necesario tanto para a súa apertura no momento do primeiro alento como para protexer o seu tecido do colapso no futuro.
- Afectar o sistema cardiovascular. O GCS aumenta a presión arterial e estabilizala a este nivel elevado. O efecto está asociado, por un lado, a un aumento do volume sanguíneo debido á retención de líquidos debido á actividade mineralocorticoide e, por outro, a un aumento da sensibilidade do músculo cardíaco e dos vasos sanguíneos ás catecolaminas endóxenas (adrenalina e norepinefrina).
- Afecta o proceso de hematopoiese. O GCS inhibe a formación de factores hematopoieticos necesarios para a división das células nai da medula ósea vermella. Neste contexto, o nivel de basófilos, eosinófilos e monocitos no sangue diminúe. A formación de neutrófilos está a aumentar.
Hydrocortisone: formas de dosificación e instrucións de uso
Glucocorticoides: un lugar na terapia
Para a terapia farmacodinámica (en contraposición á substitución), é preferible usar fármacos con baixa actividade mineralocorticoide. Os glucocorticoides empregados na práctica clínica teñen certas diferenzas na forza dos principais efectos terapéuticos, farmacocinética e no espectro de efectos secundarios que hai que ter en conta á hora de prescribir.
Os glucocorticoides úsanse na práctica de anestésico e de reanimación nas seguintes condicións: en hipotensión con hemorraxia masiva e as súas recaídas, en hipotensión en falla cardiovascular aguda,
- traumático, hemorrágico
- choque tóxico infeccioso,
- reaccións alérxicas ou anafilácticas (edema de Quincke, urticaria aguda, estado asmático, reaccións tóxico-alérxicas agudas, etc.),
- reaccións alérxicas a analxésicos estupefacientes ou outros medicamentos farmacolóxicos,
- insuficiencia suprarrenal aguda.
Para o tratamento de emerxencia de condicións como choque, reaccións alérxicas, intoxicación, administráronse glucocorticoides iv. A introdución pode ser única ou repetida durante varios días.
A principal indicación para o uso de glucocorticoides durante a anestesia e no período postoperatorio precoz é unha diminución do SBP por baixo dos 80 mm Hg. Art., Que se pode observar en moitas condicións patolóxicas. A administración intravenosa de corticosteroides durante a indución da anestesia e o seu mantemento permítenos unha rápida estabilización da hemodinámica no fondo do tratamento complexo aos 10 minutos da introdución da dose inicial.
Normalmente durante a cirurxía, os glucocorticoides úsanse nunha ampla gama de doses: de 20 a 100 mg cando se calcula na dose de prednisolona. Por outra banda, a eficacia do seu uso en terapia complexa pode chegar ao 96%. Só un pequeno número de casos son ineficaces as drogas. A maioría das veces obsérvase a ausencia dun efecto hemodinámico en pacientes cunha diminución da presión arterial como resposta á introdución dun anestésico local (por exemplo, a cortina). Non houbo efectos de doses únicas de glucocorticoides en pacientes con intoxicación grave se se conservase a súa fonte, así como en poucas ocasións, a resistencia inicial do corpo ás drogas.
En trastornos circulatorios graves, o efecto terapéutico dos glucocorticoides realízase mediante un aumento da perfusión tisular, un aumento da saída venosa, normalización da resistencia periférica e SV, estabilización das membranas celulares e lisosómicas e outros efectos. A pesar do uso tradicional de glucocorticoides en varios tipos de choque, a súa eficacia nestas condicións segue sendo demostrada. Isto débese á complexidade de contabilizar toda a variedade de factores, que subxace no desenvolvemento dunha condición de choque e afecta á eficacia da terapia. O uso de glucocorticoides nestas condicións debe realizarse en combinación con todo o arsenal sintomático farmacolóxico de corrección de complicacións.
O uso xeneral de glucocorticoides atópase no tratamento das reaccións alérxicas que se producen durante o manexo anestésico das intervencións cirúrxicas. En manifestacións alérxicas graves, a administración iv de doses adecuadas de glucocorticoides ten un efecto esmagador. A aparición de glucocorticoides en enfermidades alérxicas atrasa. Así, por exemplo, os principais efectos biolóxicos da hidrocortisona desenvólvense só 2-8 horas despois da súa administración. Polo tanto, os pacientes con reaccións alérxicas graves para evitar o broncospasmo necesitan administración inmediata de epinefrina.
Os glococorticoides teñen un efecto pronunciado na insuficiencia suprarrenal, que se desenvolveu antes e durante a cirurxía. A terapia de substitución úsase hidrocortisona, cortisona e prednisona.
A administración a curto prazo de GCS de longa duración practícase para a prevención da síndrome de angustia respiratoria en bebés prematuros, o que reduce o 40-50% o risco de morte e complicacións desta enfermidade.
Metabolismo dos carbohidratos
Un dos efectos importantes dos corticoides é o seu efecto estimulante na gluconeoxénese. Os glucocorticoides provocan un aumento da formación de glicóxeno e produción de glicosa no fígado, inhiben a acción da insulina e reducen a permeabilidade das membranas para a glicosa nos tecidos periféricos. Como resultado, pode producirse hiperglicemia e glucosuria.
Intercambio de proteínas
Os glucocorticoides reducen a síntese de proteínas e aumentan a súa ruptura, que se manifesta por un saldo negativo de nitróxeno. Este efecto maniféstase especialmente no tecido muscular, na pel e no tecido óseo. As manifestacións de equilibrio negativo de nitróxeno son a perda de peso, a debilidade muscular, a atrofia da pel e os músculos, as estrías e a hemorraxia. Unha diminución da síntese de proteínas é un dos motivos do atraso nos procesos rexenerativos. Nos nenos, a formación de tecidos, incluído o óso, é perturbada, o crecemento é máis lento.
Metabolismo dos lípidos
Os glucocorticoides provocan a redistribución da graxa. O efecto sobre o metabolismo da graxa maniféstase por acción lipolítica local na rexión das extremidades, mentres que tamén se induce a lipoxénese na rexión do tronco. Como resultado, co uso sistemático de drogas, acumulan cantidades importantes de graxa na cara, parte dorsal do corpo, ombreiros cunha diminución do tecido adiposo das extremidades. Os glucocorticoides aumentan a síntese de ácidos graxos e triglicéridos, provocando hipercolesterolemia.
Intercambio auga-sal
A administración a longo prazo de GCS leva á realización da súa actividade mineralocorticoide. Obsérvase un aumento da reabsorción de ións de sodio dos túbulos renais distales e un aumento da secreción tubular de ións potásicos. O atraso de ións de sodio no corpo provoca un aumento gradual de cc e un aumento da presión arterial. Os efectos mineralocorticoides do GCS son máis inherentes ao GCS natural - cortisona e hidrocortisona e, en menor medida, a GCS semisintética.
Os glucocorticoides tenden a provocar un equilibrio negativo de calcio no corpo, reducindo a absorción de calcio do tracto dixestivo e aumentando a súa excreción polos riles, o que pode provocar hipocalcemia e hipercalciuria. Con administración prolongada, unha violación do metabolismo do calcio, unida á ruptura da matriz proteica, leva ao desenvolvemento da osteoporose.
Células do sangue
Os glucocorticoides reducen a cantidade de eosinófilos, monocitos e linfocitos no sangue. Ao mesmo tempo, aumenta o contido de glóbulos vermellos, reticulocitos, neutrófilos e plaquetas. A maioría destes cambios obsérvanse despois de tomar unha única dose de corticoides coa máxima severidade do efecto despois de 4-6 horas.A restauración do estado inicial prodúcese despois de 24 horas .Con tratamento prolongado con corticosteroides, os cambios no cadro sanguíneo teñen unha duración de 1-4 semanas.
Segundo o principio de retroalimentación, os glucocorticoides teñen un efecto deprimente sobre o sistema hipotalámico-hipofisario-suprarrenal (GGNS), como resultado da cal diminúe a produción de ACTH. Unha insuficiencia da función da cortiza suprarrenal que se desenvolve ao mesmo tempo pode producirse cunha forte descontinuación de glucocorticoides. O risco de desenvolver insuficiencia suprarrenal aumenta significativamente co uso regular de glucocorticoides durante máis de 2 semanas.
Acción antiestrés
Os glucocorticoides son hormonas adaptativas que aumentan a resistencia do corpo ao estrés. En condicións graves de estrés, a produción de cortisol aumenta significativamente (polo menos 10 veces). Hai evidencias dun vínculo entre o sistema inmunolóxico e o GNSS. Estas interaccións poden representar polo menos un dos mecanismos da acción antiestrés dos glucocorticoides. Demostrouse que a función do GNS está regulada por moitas citocinas (IL-1, -2, -6, factor de necrose tumoral TNF-a). Todos eles teñen un efecto estimulante.Moitos teñen unha ampla gama de efectos. Por exemplo, a IL-1 estimula a liberación de hormona liberadora de corticotropina por neuronas hipotálamas, afecta directamente á glándula pituitaria (aumenta a liberación de ACTH) e ás glándulas suprarrenais (aumenta a liberación de glucocorticoides). Ao mesmo tempo, os glucocorticoides son capaces de inhibir a expresión de moitas partes do sistema inmune, por exemplo, a produción de citocinas. Así, as GGNS e o sistema inmunitario teñen conexións bidireccionais durante o estrés e estas interaccións son probablemente de gran importancia para manter a homeostase e protexer o corpo das consecuencias potencialmente mortais dunha reacción inflamatoria desenvolvida.
Acción permisiva
Os glucocorticoides poden afectar á acción doutras hormonas, potenciando enormemente os seus efectos. Este efecto dos glucocorticoides sobre os efectos doutras hormonas reguladoras denomínase permisivo e reflicte os cambios na síntese de proteínas provocados polos corticoides, que cambian a resposta dos tecidos a determinados estímulos.
Entón, pequenas doses de glucocorticoides provocan unha potenciación significativa da acción lipolítica das catecolaminas. Os glucocorticoides tamén aumentan a sensibilidade dos receptores adrenérxicos ás catecolaminas e aumentan o efecto de presión da angiotensina II. Crese que debido a isto, os glucocorticoides teñen un efecto tónico no sistema cardiovascular. Como resultado, o ton vascular normalízase, aumenta a contractilidade do miocardio e diminúe a permeabilidade capilar. Pola contra, a insuficiencia na produción de GCS natural caracterízase por unha baixa SV, a expansión de arteriolas e unha débil reacción á adrenalina.
Demostrouse que os glucocorticoides tamén potencian o efecto broncodilatante das catecolaminas, restablecendo a sensibilidade dos receptores beta-adrenérxicos a eles, o que está asociado a un aumento da biosíntese dos receptores adrenérxicos da parede vascular.
Farmacocinética
Os glucocorticoides son pequenas moléculas lipofílicas que pasan ben polas barreiras celulares por simple difusión. Cando se administran, os glucocorticoides son ben absorbidos desde o xunio superior. O Cmax no sangue créase en 0,5-1,5 horas. A taxa de desenvolvemento dos efectos e a duración da acción do GCS dependen da forma de dosificación, da solubilidade e da taxa metabólica dos fármacos.
Os glucocorticoides son producidos en moitas formas de dosificación. As características das formas de inxección débense tanto ás propiedades do propio glucocorticoide como ao éster asociado con el. Os succinatos, hemisuccinados e fosfatos son solubles en auga e teñen un efecto rápido, pero relativamente a curto prazo. Pódense introducir en / m e / in. Os acetatos e os acetonidos son pequenas suspensións cristalinas, son insolubles en auga e son absorbidas lentamente durante varias horas. Os ésteres insolubles en auga están destinados á introdución na cavidade da articulación e nas bolsas articulares. A súa acción alcanza un máximo despois de 4-8 días e dura ata 4 semanas.
No sangue, os glucocorticoides forman complexos con proteínas plasmáticas: albúmina e transcortina. Se os glucocorticoides naturais se unen á transcortina nun 90% e á albumina nun 10%, entón os glucocorticoides sintéticos, con excepción da prednisolona, únense principalmente á albúmina (aproximadamente o 60%) e ao redor do 40% circulan de forma libre. O 25-35% dos glucocorticoides libres son depositados por glóbulos vermellos e glóbulos brancos.
Só os glucocorticoides non proteicos son bioloxicamente activos. Pasan facilmente as membranas mucosas e barreiras histohematolóxicas, incluíndo cerebro en sangue e placentario, rapidamente eliminado do plasma.
O metabolismo dos glucocorticoides ocorre principalmente no fígado, en parte nos riles e outros tecidos. No fígado, os glucocorticoides están hidroxilados e conxúganse con glucuronida ou sulfato.Os esteroides naturais cortisona e prednisona adquiren actividade farmacolóxica só despois da metabolización no fígado coa formación de hidrocortisona e prednisona, respectivamente.
A metabolización de corticoides sintéticos no fígado mediante a recuperación e a conxugación é máis lenta en comparación cos esteroides naturais. A introdución de iones de halóxeno flúor ou cloro na estrutura de GCS retarda o metabolismo das drogas e prolonga a súa T1 / 2. Debido a isto, o efecto dos corticoides fluorados dura máis tempo, pero ao mesmo tempo inhiben máis a función da cortiza suprarrenal.
Os glucocorticoides son excretados polos riles a través da filtración glomerular en forma de metabolitos inactivos. A maioría dos corticoides (85%) reabsorban nos túbulos e só preto do 15% son excretados do corpo. En insuficiencia renal, o axuste da dose non se realiza.
Advertencias
En pacientes con hipotiroidismo, cirrosis, hipoalbuminemia, así como en pacientes maiores, pódese mellorar o efecto dos glucocorticoides.
Os glucocorticoides penetran ben na placenta. Os dispositivos naturais e non fluorados son xeralmente seguros para o feto e non conducen ao desenvolvemento intrauterino da síndrome de Cushing e á inhibición do GNSS.
A administración a longo prazo de glucocorticoides fluorados pode causar reaccións non desexadas, incluída e fealdade. Unha muller que leva tomando glucocorticoides nos últimos 1,5-2 anos, co fin de evitar unha insuficiencia suprarrenal aguda, debe administrarse ademais 100 mg de hidrocortisona hemisuccinado cada 6 horas.
Cando se amamanta, as doses baixas de glucocorticoides, equivalentes a 5 mg de prednisolona, non son perigosas para o bebé, xa que os glucocorticoides penetran mal no leite materno. As doses máis altas de fármacos e o seu uso a longo prazo poden provocar acrobacias e inhibición de HHF.
No tratamento de varias enfermidades do sistema músculo-esquelético, especialmente de natureza inflamatoria, as drogas como os glucocorticosteroides atoparon un uso xeneralizado. Antes de comprender os principais efectos terapéuticos, indicacións e contraindicacións, debes saber que son os glucocorticosteroides (GCS).
Os glucocorticosteroides son fármacos que pertencen ao grupo de hormonas esteroides e teñen propiedades antiinflamatorias, antialérxicas, anti-choque, inmunosupresoras e outras propiedades.
Cando se usa?
No tratamento de enfermidades das articulacións e da columna vertebral, a principal indicación para o uso de glucocorticosteroides considérase un proceso inflamatorio grave, especialmente intensivo e que non responde á terapia con antiinflamatorios non esteroides. Que patoloxías articulares se poden usar:
- Artrite (reumatoide, postraumática, gota, psoriatica, etc.).
- Poliartrite
- Osteoartrose (en presenza de signos dun proceso inflamatorio).
- Espondilite anquilosante.
- Periartrite.
- Inflamación da bolsa sinovial ou articular.
Ao prescribir GCS, o médico intenta conseguir o máximo efecto terapéutico usando a dosificación mínima do medicamento. O réxime de tratamento con glucocorticosteroides depende principalmente da gravidade da enfermidade, da condición do paciente e da súa resposta á terapia, que da idade e do peso.
Eficacia clínica
Varios estudos científicos recentes demostraron que os glucocorticosteroides son altamente eficaces no tratamento da inflamación articular grave. Tamén se pode conseguir un efecto clínico rápido co uso simultáneo de GCS en doses baixas e antiinflamatorios non esteroides. Estableceuse que para a maioría dos pacientes con discapacidade debido á poliartrite, resulta moito máis doado en termos funcionais despois de varios días de tratamento con corticoides. O que conta o médico para prescribir glucocorticosteroides:
- Reducir significativamente a gravidade da dor nas articulacións afectadas.
- Mellora o estado funcional das articulacións.
- Retardar os procesos destrutivos.
- Afrontar a inflamación.
- Reducir significativamente a necesidade de antiinflamatorios non esteroides.
- Para aumentar a eficacia do uso de antiinflamatorios básicos.
A experiencia clínica demostrou que moitos pacientes que sofren artrite reumatoide adoitan depender funcionalmente da terapia con glucocorticosteroides e son obrigados a cambiar a longos cursos da súa administración, o que sen dúbida leva ao desenvolvemento de efectos secundarios.
Como se solicita?

Varias vías de administración de drogas GCS son posibles. Por regra xeral, no tratamento da patoloxía inflamatoria do sistema músculo-esquelético, inxectanse glucocorticosteroides na articulación. Actuando directamente sobre o foco da inflamación, conséguese o máximo efecto terapéutico.
Cómpre sinalar que con frecuencia pode acumularse un fluído (exudado) na cavidade das grandes articulacións. Nestes casos, primeiro debes eliminar este fluído e só despois realizar a administración intra-articular do medicamento. Ás veces, para conseguir un mellor efecto, a administración de GCS na articulación combínase con terapia con glucocorticosteroides en comprimidos. Un tipo de tratamento similar úsase para formas graves do proceso inflamatorio cunha tendencia á progresión pronunciada.
As inxeccións intraarticulares de drogas son realizadas só por un médico especialista en condicións estériles (vestiario limpo).
Os preparados de GCS tamén son prescritos con frecuencia en forma oral de comprimidos ou administrados parenteralmente (nunha vea ou músculo).
A duración do curso e a dosificación do medicamento dependen da gravidade e da natureza da enfermidade. Para algúns pacientes, o curso terapéutico é de varios meses ou incluso anos. Cunha alta actividade do proceso patolóxico nas articulacións, utilízase a chamada terapia de pulso. Neste caso, o medicamento adminístrase por vía intravenosa (a través dun contagotas) durante 3 días consecutivos. Na maioría dos casos, a terapia de pulso con glucocorticosteroides permite suprimir rapidamente a actividade do proceso inflamatorio.
Tipos de glucocorticosteroides
Os glucocorticoides, como o cortisol, a cortisona e a corticosterona, son cortiza adrenal natural. A súa produción principal realízase de acordo co ritmo diario. Unha cantidade maior é secretada cun aumento da necesidade destes hormonas. Xorden da proxesterona na capa de malla e malla da córtex suprarrenal. O sangue é transportado a través da transcortina. Os glucocorticoides actúan a través de receptores intracelulares. Afectan o metabolismo de carbohidratos, proteínas e graxas. Estas hormonas tamén inhiben os procesos inflamatorios, polo que chámanse esteroides antiinflamatorios. Son necesarios para superar situacións estresantes graves no corpo humano.
Reaccións adversas
Segundo a observación clínica, a pesar de que a maioría dos efectos secundarios derivados do uso prolongado de GCS en enfermidades inflamatorias das articulacións e da columna vertebral considéranse bastante graves, algúns deles parecen unha orde de magnitude menos frecuentemente que con outros antiinflamatorios. Moitos expertos divide os efectos secundarios condicionalmente co uso sistémico prolongado de glucocorticosteroides en dous grupos:
- Potencialmente controlado (diabetes mellitus, un aumento constante da presión arterial, alteración do sono, glaucoma, insuficiencia cardíaca, ulceración gastrointestinal, osteoporose).
- Non controlado (aumento de peso, cataratas, trastornos mentais, erupcións cutáneas, varias infeccións, osteonecrose, aterosclerose).
Ao mesmo tempo, comprobouse que tomar medicamentos antiinflamatorios non esteroides provoca a miúdo o desenvolvemento dunha patoloxía erosiva e ulcerativa severa do tracto gastrointestinal que o uso de fármacos do grupo GCS.O tratamento con glucocorticoides está asociado xustificadamente cun aumento do risco de complicacións infecciosas, pero isto é típicamente principalmente para pacientes que reciben altas doses de fármacos. Cítanse os criterios para a terapia con glucocorticosteroides inadecuados:
- Dose demasiado alta ou, pola contra, moi baixa.
- Un curso de tratamento razoable.
- Falta de antiinflamatorios básicos.
A administración intraarticular de GCS, unha das complicacións máis perigosas, pero bastante raras, é a infección na cavidade articular durante a inxección. Ademais, a propiedade inmunosupresora dos glucocorticoides contribúe ao desenvolvemento dun proceso inflamatorio purulento. En poucas ocasións, pódese observar a "sinovite post-inxección" cando, despois dunha inxección, obsérvase un aumento do proceso inflamatorio na membrana sinovial da articulación, que pode durar entre varias horas e 2-3 días.
A introdución do medicamento no tecido muscular é altamente indesexable, xa que é posible o desenvolvemento de procesos atróficos ou necróticos.
Hormonas sintéticas
Glicocorticosteroides sintéticos: que é? Os glucocorticosteroides sintéticos (corticoides) úsanse como axentes terapéuticos, tamén chamados coloquialmente simplemente esteroides. Teñen un efecto antiinflamatorio maior que os compostos naturais.
Na terapia farmacolóxica - principalmente menos veces - os glucocorticosteroides úsanse como medicamento antialérxico ou inmunosupresor. O seu uso en terapia está moi estendido en caso de insuficiencia da córtex suprarrenal. O seu principal efecto é inhibir as reaccións inflamatorias, é dicir, bloquear a fosfolipase A 2, o que leva a unha diminución da produción
Por regra xeral, na terapia hormonal úsanse doses estándar do medicamento, que non produce efectos secundarios graves. O mellor é tomar estas drogas nunha única dosificación e de acordo co ritmo fisiolóxico da secreción de cortisol no corpo, é dicir, pola mañá. A terapia con glucocorticosteroides inclúe unha diminución gradual da dose de hormonas administradas na última etapa do tratamento (para evitar a atrofia da córtex suprarrenal).
Os esteroides pódense usar por vía oral e en condicións agudas (en presenza de ameaza vital) - en forma de inxeccións ou infusións intravenosas. O seu uso debería estar baixo control, é dicir, aplicarse só cando hai indicacións claramente definidas para iso, tendo en conta posibles efectos secundarios. As doses deben seleccionarse individualmente para cada paciente, deben cambiarse segundo a gravidade da enfermidade.
Glucocorticosteroides empregados en dermatoloxía
As hormonas da cortiza suprarrenal teñen efectos antiinflamatorios, inmunosupresores e antipruríticos. Son moi empregados en dermatoloxía para enfermidades da pel. Glicocorticosteroides tópicos: fondos relacionados cos medicamentos máis empregados para o tratamento de enfermidades dermatolóxicas. Pódense empregar, especialmente, no tratamento de:
A pomada glucocorticosteroide úsase no tratamento da psoríase. Tamén se usan xeles, cremas, locións para aliviar os síntomas da inflamación e a picazón da pel. Recóllese o líquido hormonal esteroide para o seu coiro cabeludo. Do mesmo xeito que co tratamento continuo, e en poucos casos, o uso de medicamentos esteroides, é preferible o uso de medicamentos máis débiles (para evitar efectos secundarios).

Osteoporose glucocorticosteroide

Unha das complicacións máis adversas do tratamento con glucocorticosteroides prolongado é. Non obstante, segundo algúns expertos, a alta actividade inflamatoria da artrite reumatoide e a diminución da actividade física considéranse factores non menos importantes na aparición da osteoporose.que o tratamento prolongado de corticoides.
Para reducir o risco de desenvolver esta complicación, moitos médicos recomendan axustar substancialmente o seu estilo de vida, especialmente para os pacientes que reciben glucocorticosteroides durante moito tempo. Que hai que facer exactamente:
- Deixar de fumar e beber alcohol.
- Fai exercicio regularmente.
- Coma alimentos ricos en calcio e vitamina D.
- Moitas veces estar ao sol.
- Se é necesario, tome medicamentos prescritos polo seu médico (calcitonina, etc.).
Esteroides no tratamento do sistema respiratorio
As drogas hormonais de todas as drogas utilizadas para tratar a inflamación dos bronquios teñen o efecto máis poderoso. Despois da súa introdución, hai unha diminución do inchazo da membrana mucosa e da secreción de moco, restablece o epitelio bronquial normal. A introdución de esteroides no corpo suprime a fase tardía das alerxias, así como unha maior reacción dos bronquios. Distinguir:
- Glucocorticosteroides en forma de anestésicos inhalados. Son a forma máis preferida de medicamentos para o seu uso no tratamento de todas as formas de asma bronquial.
- Glucocorticosteroides, usados como inxeccións sistémicas no sangue. Este tipo úsase só en formas graves de asma bronquial, cando outros métodos médicos non dan resultados.
- Os esteroides de uso oral tamén se poden usar para o tratamento a curto prazo durante períodos de exacerbación da enfermidade.
Embarazo e lactación
Non se realizaron estudos clínicos dirixidos sobre a seguridade do uso de glucocorticosteroides durante o embarazo. Non obstante, os médicos poden prescribir este medicamento a unha muller embarazada, pero só se o efecto esperado do tratamento supera significativamente o risco esperado para o neno. Ademais, as nais en lactación están fortemente animadas a suspender a lactación durante a terapia con glucocorticosteroides.
Glucocorticoides na práctica clínica
Kharkov Institute for Advanced Medical Studies
En condicións fisiolóxicas, as células da zona de feixe de córtega suprarrenal segregan dous principais glucocorticoides no torrente sanguíneo: cortisona e cortisol (hidrocortisona). A secreción destas hormonas está regulada pola corticotropina da adenohipófise (antes chamada hormona adrenocorticotrópica). Un aumento do nivel de cortisol no sangue polo mecanismo de retroalimentación inhibe a secreción de corticoliberina no hipotálamo e corticotropina na glándula hipofisaria.
A intensidade da secreción de glucocorticoides no sangue durante o día varía significativamente. O contido máximo de hormonas no sangue obsérvase nas primeiras horas da mañá (6-8 horas), o mínimo - pola noite e pola noite.
Os efectos fisiolóxicos dos glucocorticoides son en gran parte os contrarios aos causados pola insulina. As hormonas teñen un efecto catabólico no metabolismo das proteínas (é dicir, axudan a descompoñer moléculas de proteínas complexas en substancias simples) e a efecto anti-anabólico (é dicir, prevén a biosíntese de moléculas proteicas). Como resultado, o corpo descompón proteínas e aumenta a excreción de produtos nitroxenados. A ruptura de proteínas prodúcese nos tecidos musculares, conectivos e ósos. A albumina no sangue é reducida.
Os glucocorticoides estimulan o catabolismo de triglicéridos e inhiben a síntese de graxa dos carbohidratos. Ao mesmo tempo, unha diminución do tecido adiposo das extremidades combínase a miúdo cun aumento da deposición de graxa na parede abdominal e entre as omoplatos. A hiperglucemia baixo a influencia das hormonas prodúcese debido á aumento da formación de glicosa no fígado a partir de aminoácidos (gluconeoxénese) e a supresión do seu uso por tecidos, e tamén aumenta o contido de glicóxeno no fígado. Os glucocorticoides reducen a sensibilidade do tecido á insulina e á síntese de ácidos nucleicos.
As hormonas aumentan a sensibilidade dos adrenoreceptores ás catecolaminas, aumentan os efectos presores da angiotensina II, reducen a permeabilidade capilar e participan no mantemento do ton arteriol normal e a contractilidade do miocardio. Baixo a influencia de glucocorticoides, os niveis sanguíneos de linfocitos, monocitos, eosinófilos e basófilos diminúen, os neutrófilos saen da medula ósea e se estimula o seu aumento no sangue periférico. As hormonas conservan sodio e auga no corpo no fondo da perda de potasio, inhiben a absorción de calcio no intestino e contribúen á liberación deste último do tecido óseo e á súa excreción na urina. Os glucocorticoides aumentan a sensibilidade sensible e a excitabilidade do sistema nervioso, participan na implementación de reaccións ao estrés, afectan á psique humana.
Os glucocorticoides naturais e os seus análogos sintéticos son moi empregados na clínica principalmente porque teñen varias calidades máis valiosas: teñen efectos antiinflamatorios, inmunosupresores, antialérxicos e anti-choques. Os resultados finais da terapia dependen de moitos factores, incluíndo a duración do tratamento, a dose de fármacos, o método e modo de administración, as características inmunolóxicas e inmunoxenéticas das propias enfermidades, etc. Ademais, diferentes glucocorticoides teñen diferentes graos de severidade, efectos inmunosupresores e antiinflamatorios. sen relación directa. Así, a dexametasona ten unha poderosa actividade inmunosupresora antiinflamatoria e relativamente baixa.
Características comparativas dos glucocorticoides
Na práctica clínica, úsanse glucocorticoides naturais (cortisona e hidrocortisona) e os seus derivados semisintéticos. Á súa vez, estes últimos divídense en non fluorados (prednisona, prednisolona, metilprednisolona) e fluorados (triamcinolona, dexametasona e betametasona).
Cando se administran, os glucocorticoides absorbense rápidamente e case por completo no xunio superior. A alimentación non afecta o grao de absorción de hormonas, aínda que a velocidade deste proceso se ralentiza.
As peculiaridades do uso de formas inxectables débense tanto ás propiedades do propio glucocorticoide como ao éster asociado a el. Por exemplo, sucinatos, hemisuccinados e fosfatos disólvense na auga e, cando se administran parenteralmente, teñen un efecto rápido, pero relativamente a curto prazo. Pola contra, os acetatos e os acetonidos son suspensións cristalinas finas e non son solubles en auga. A súa acción desenvólvese lentamente ao longo de varias horas, pero dura moito tempo (semanas). Os ésteres glucocorticoides solubles en auga pódense empregar por vía intravenosa; non poden ser suspensións de cristal fino.
Dependendo da duración da acción terapéutica, todos os glucocorticoides divídense en 3 grupos (táboa 1). Coñecer as doses equivalentes de corticoides permítelle substituír un medicamento por outro se é necesario. O principio xa existente - "pastilla para píldora" (é dicir, se é necesario trasladar o paciente a outro glucocorticoide, recetáronlle tantas tabletas do novo medicamento como recibiu antes da substitución) - na actualidade non funciona. Isto débese á introdución na práctica clínica de formas de dosificación de glucocorticoides con diferentes contidos do principio activo.
| Duración da acción | Nome da droga | Dose equivalente (mg) |
| Acción curta | Hidrocortisona | 20 |
| Cortisona | 25 | |
| Prednisona | 5 | |
| Prednisona | 5 | |
| Metilprednisolona | 4 | |
| Triamcinolona | 4 | |
| Zona de parámetro | 2 | |
| Longa actuación | Dexametasona | 0,75 |
| Betametasona | 0,6 |
Os glucocorticoides naturais teñen actividade mineralocorticoide, aínda que máis débiles que os verdadeiros mineralocorticoides.Os glucocorticoides semisintéticos non fluorados tamén exercen efectos mineralocorticoides (a gravidade dos cales á súa vez é inferior aos efectos dos glucocorticoides naturais). Nas preparacións fluoradas, a actividade mineralocorticoide está ausente (táboa 2). A actividade glucocorticoide dos fármacos semisintéticos é maior que a da cortisona e a hidrocortisona, o que se explica pola menor unión ás proteínas en comparación cos glucocorticoides naturais. Unha característica dos medicamentos fluorados é un metabolismo máis lento no corpo, o que implica un aumento da duración da acción dos medicamentos.
| Duración da acción | Nome da droga | Gluco actividade corticoide | Mineral actividade corticoide |
| Acción curta | Hidrocortisona | 1 | 1 |
| Cortisona | 0,8 | 1 | |
| Prednisona | 4 | 0,8 | |
| Prednisona | 4 | 0,8 | |
| Metilprednisolona | 5 | 0,5 | |
| Duración media | Triamcinolona | 5 | - |
| Longa actuación | Dexametasona | 30 | - |
| Betametasona | 30 | - |
Os seguintes termos son moi utilizados na literatura médica: doses "baixas" de glucocorticoides, "altas", etc. As doses "baixas" de corticosteroides indícanse se a dose diaria non supera os 15 mg (3 comprimidos) de prednisona (ou a dose equivalente) calquera outra droga). Estas doses normalmente son prescritas para o tratamento de mantemento. Se a dose diaria de prednisolona é de 20-40 mg (4-8 comprimidos), falan de doses "medias" de glucocorticoides e máis de 40 mg / día - de "alto". Os valores próximos aos dados obtéñense tamén ao calcular a dose diaria de corticoides por 1 kg de peso corporal do paciente. A fronteira condicional entre as doses "medias" e "altas" é de 0,5 mg de prednisona por 1 kg de peso corporal do paciente ao día.
Nos últimos vinte anos, a clínica tamén usou administración intravenosa de doses moi grandes de glucocorticoides (polo menos 1 g de metilprednisolona ao día) durante varios días. Este tratamento chámase "terapia de pulso".
A dose de glucocorticoides prescritos ao comezo do tratamento para unha determinada enfermidade depende principalmente da forma nosolóxica e da gravidade da enfermidade. A idade do paciente, a presenza ou a ausencia de enfermidades concomitantes, o uso simultáneo doutros medicamentos e outros factores tamén afectan a dose.
As principais opcións para o uso clínico de glucocorticoides pódense representar a seguinte:
| externa: pel, ollos, orellas (en forma de pomadas, pingas, cremas, loções, aerosoles), | msimagelist>
| inhalación - nos pulmóns ou na cavidade nasal, | msimagelist>
| subfolia (epidural), | msimagelist>
| intradérmico: en cicatrices, | msimagelist>
| intracavitaria: dentro da cavidade pleural, intrapericárdica, etc. | msimagelist>
| intraarticular e periarticular, | msimagelist>
| aplicación do sistema: | msimagelist>
| dentro | msimagelist>
| en velas (supositorios), | msimagelist>
| parenteral (principalmente intramuscular e intravenosamente). | msimagelist>
En termos de persistencia e severidade do efecto antiinflamatorio terapéutico, así como tolerancia, a prednisolona e a metilprednisolona son as mellores.
Prednisona considerado como un medicamento estándar para a terapia farmacodinámica. A relación de glucocorticoides e mineralocorticoides da prednisolona é de 300: 1.
Metilprednisolona En comparación coa prednisona, ten unha actividade glucocorticoide lixeiramente maior (nun 20%) e ten un débil efecto mineralocorticoide. A vantaxe da droga é unha estimulación moi moderada da psique e o apetito, o que xustifica o seu nomeamento a pacientes cunha psique inestable e sobrepeso.
A prednisona está hidroxilada no fígado (onde se converte en prednisona) e, polo tanto, non se recomenda para enfermidades hepáticas graves.Sen embargo, na práctica clínica úsase menos frecuentemente que a prednisona.
Triamcinolona - glucocorticoides fluorados, carentes de actividade mineralocorticoide. Polo tanto, menos en comparación con outras drogas, a capacidade de reter sodio e auga. En comparación coa prednisona, ten un efecto glucocorticoide máis pronunciado (nun 20%) e prolongado. Por outra banda, adoita provocar reaccións non desexadas do tecido muscular (miopatía "triamcinolona") e da pel. Polo tanto, o uso prolongado deste medicamento non é desexable.
Dexametasona na actividade glucocorticoide é 7 veces maior que a prednisona. É un glucocorticoide fluorado e non ten un efecto mineralocorticoide. En comparación con outros fármacos, suprime en maior medida a función da cortiza suprarrenal. Non se recomenda o uso a longo prazo debido ao perigo de efectos secundarios graves (principalmente, inhibición do eixe hipotalámico-hipofisario-suprarrenal, alteracións metabólicas, efectos psicostimulantes).
Betametasona - glucocorticoide fluorado, que ten unha forza e duración próximas á dexametasona. Supera lixeiramente este último na actividade dos glucocorticoides (8-10 veces superior á da prednisona) e en menor medida afecta ao metabolismo dos carbohidratos. O fosfato de betametasona é soluble en auga e pódese administrar por vía intravenosa e subconxuntiva. Para a administración intramuscular, intraarticular e periarticular, úsase unha mestura de dous ésteres de betametasona: o fosfato (absorbido rapidamente) e o dipropionato (absorbido lentamente). Esta mestura é unha suspensión cristalina fina que non se pode administrar por vía intravenosa. O fosfato proporciona un efecto rápido (dentro de 30 minutos) e o diproprionato ten un efecto longo, de ata 4 semanas ou máis.
Cortisona actualmente practicamente non se usa debido a unha menor eficiencia e unha peor tolerancia. Xunto coa hidrocortisona, ten a actividade mineralocorticoide máis pronunciada entre todos os glucocorticoides. A principal área de aplicación é a terapia de substitución da insuficiencia suprarrenal en pacientes con función hepática normal (xa que a cortisona convértese en hidrocortisona no fígado, non se recomenda o uso do medicamento para danos graves a este órgano).
Hidrocortisona É case o único glucocorticoide que podería usarse para tratamento parenteral a longo prazo, pero é significativamente inferior ás drogas modernas en tolerabilidade. Máis débil que a prednisona na actividade dos glucocorticoides (4 veces), pero superala en severidade da acción mineralocorticoide. A hidrocortisona úsase normalmente para a substitución fisiolóxica e a cobertura estresante en pacientes con insuficiencia hipotálamo-pituitaria-suprarrenal. En insuficiencia suprarrenal aguda e outras condicións de emerxencia de hidrocortisona, o hemisuccinato é o fármaco escollido.
Beclometasona, flunisólido, budesonida, acetonida de triamcinolona e fluticasona administrado por inhalación. A Beclometasona (beclometh, becotida, etc.) é a máis frecuentemente prescrita para a terapia de mantemento a longo prazo do asma bronquial. Ten un efecto sistémico leve, aínda que en grandes doses (1000-2000 mcg / día) provoca osteoporose e outros efectos secundarios. O uso de flunisolid (ingacort) en comparación coa beclometasona é algo menos probable que leve ao desenvolvemento da candidiasis da cavidade oral. Cando se inhala, o budesonida (pulmicort) é lixeiramente máis efectivo e afecta menos á función renal que a beclometasona. A fluticasona (flixotida, flixonase) en afinidade para os receptores de glucocorticoides é 30 veces maior que a prednisona e 2 veces superior á budesonida. Ten un efecto antiinflamatorio local dúas veces máis forte que a beclometasona.
Uso sistémico de glucocorticoides
Ata a data continúan as discusións sobre a selección de doses adecuadas e formas de dosificación óptimas de fármacos, vías de administración, duración da terapia, efectos secundarios. En xeral, a decisión sobre o uso tópico de corticoides normalmente non causa dificultades médicas. Por iso, na seguinte presentación, o foco principal estará no uso sistémico de hormonas.
Se é necesaria a administración sistémica de glucocorticoides, é preferible a administración oral. Se é imposible introducir estes medicamentos no seu interior, pódense usar en supositorios, a dose neste caso aumenta entre un 25 e un 50%. Os glucocorticoides existentes en formas inxectables metabolízanse rapidamente no corpo durante a administración intramuscular e, especialmente, por vía intravenosa, e polo tanto o seu efecto é a curto prazo e na maioría dos casos insuficiente para o tratamento a longo prazo. Para obter un equivalente, en comparación coa administración oral, o efecto terapéutico, terían que administrarse doses parenterais de 2-4 veces maiores e deberíanse empregar inxeccións frecuentes. Os medicamentos parenterais prolongados (por exemplo, acetonida de triamcinolona ou kenalog) non se usan para o tratamento "supresivo" activo, pero principalmente como terapia de apoio ou local (por exemplo, intraarticular).
Pola mañá, o eixe hipotalámico-hipofisario-suprarrenal é o menos sensible aos efectos inhibidores dos corticoides exóxenos. Ao dividir a dose diaria de glucocorticoides en 3-4 partes e tomalas a intervalos regulares, aumenta o risco de suprimir o eixe hipotálamo-hipofisario-suprarrenal. Polo tanto, na maioría dos casos, as hormonas prescríbense baixo a dose dunha mañá (principalmente medicamentos de longa acción), ou 2/3/4 da dose diaria tómase pola mañá e o resto tómase ao mediodía. Este esquema de aplicación permite reducir o risco de inhibición do eixe hipotalámico-hipofisario-suprarrenal e reducir o risco de osteoporose.
A eficacia terapéutica dos glucocorticoides aumenta aumentando a dose e a frecuencia de administración, pero a severidade das complicacións tamén aumenta. Co uso alternativo de hormonas (cada día), o número de reaccións adversas é menor, pero en moitos casos este modo de administración non é o suficientemente eficaz (por exemplo, con enfermidades do sangue, colite ulcerativa (inespecífica), tumores malignos, así como en casos graves de enfermidades). A terapia alternativa, por regra xeral, úsase despois da supresión da actividade inmunolóxica e inflamatoria cunha diminución da dose de glucocorticoides e a transición ao tratamento de mantemento. No réxime alterno, a dose de hormonas necesaria para o período de 48 horas é administrada cada segundo día pola mañá cada vez. Este enfoque permite reducir o efecto inhibidor dos glucocorticoides exóxenos sobre a función da cortiza suprarrenal do paciente e, polo tanto, evitar a súa atrofia. Ademais, co uso alternativo de glucocorticoides, o risco de complicacións infecciosas diminúe e o retraso do crecemento nos nenos non é tan pronunciado como coa inxestión diaria de hormonas.
Só nos casos raros (por exemplo, con síndrome nefrótico nos nenos), prescríbese terapia alternativa desde os primeiros días de tratamento. Normalmente, este réxime de administración de hormonas está reservado a pacientes que conseguiron estabilización usando glucocorticoides diarios. O seguinte é un exemplo de transferencia dun paciente a terapia alternativa, na que a dose inicial de prednisolona foi de 50 mg.
Con tratamento alternativo, só se usan corticosteroides de acción media (prednisona, prednisolona, metilprednisolona). Despois de tomar unha dose destes fármacos, o eixe hipotalámico-hipofisario-suprarrenal suprímese durante 12-36 horas.Co nomeamento de glucocorticoides de acción longa todos os días (triamcinolona, dexametasona, betametasona), mantense o risco de opresión do eixe hipotálamo-hipofisario-suprarrenal, polo que é irracional usalos para tratamento alternativo. A área de aplicación de hormonas naturais (cortisona e hidrocortisona) está actualmente limitada pola terapia de substitución por insuficiencia suprarrenal e tratamento supresor da síndrome adrenogenital.
Con agudización dos síntomas da enfermidade no segundo día ("sen hormonas"), recoméndase aumentar a dose do medicamento o primeiro día, ou tomar unha pequena dose adicional no segundo día.
As doses altas (por exemplo, 0,6-1,0 mg de prednisolona por 1 kg de peso corporal ao día) ou as doses divididas en varias doses ao longo do día están indicadas nas fases iniciais das enfermidades máis agresivas. É necesario esforzarse para trasladar o paciente nun prazo de 1-2 semanas a unha única dose de mañá de toda a dose diaria. As circunstancias clínicas específicas determinan a redución adicional á dose mínima de mantemento efectiva (prefírese administración alternativa). Unha redución demasiado gradual combínase cun aumento do número e da gravidade dos efectos secundarios do tratamento con glucocorticoides e demasiado rápido - predispón á agravación da enfermidade.
Para reducir os efectos secundarios, debes considerar a posibilidade de "gardar esteroides". En reumatoloxía, por exemplo, isto conséguese mediante o uso de antiinflamatorios non esteroides ou terapia básica (inmunosupresores, antimalarios, etc.). A alternativa é outra opción para reducir as complicacións da terapia con esteroides.
A terapia con altas doses de glucocorticoides pode resultar insatisfactoria debido á falta de eficacia e / ou á aparición de complicacións graves. En tales casos, debes considerar a posibilidade dunha terapia de pulso, é dicir, administración intravenosa de doses moi grandes de hormonas durante un curto espazo de tempo. Aínda que aínda non hai unha definición clara da terapia de pulso, este termo normalmente refírese á administración intravenosa rápida (dentro dos 30-60 minutos) de grandes doses de glucocorticoides (polo menos 1 g) unha vez ao día durante 3 días. Dunha forma máis xeral, a terapia de pulso pode ser representada como a administración intravenosa de metilprednisolona (este fármaco é máis frecuentemente usado por outras) cunha dose de ata 1 g / m². contador de superficie corporal durante 1-5 días. Na actualidade, a terapia de pulso con hormonas esteroides úsase a miúdo no inicio do tratamento para varias enfermidades mediadas inmunoloxicamente rapidamente. A utilidade deste método para a terapia de mantemento a longo prazo é aparentemente limitada.
En xeral, co uso local de esteroides desenvólvense menos efectos tóxicos que con un uso sistémico. O maior número de eventos adversos con uso sistémico de hormonas prodúcese se a dose diaria divídese en varias doses. Cando a dose diaria se toma nunha dose, o número de efectos adversos é menor e o réxime de administración alternativa é o menos tóxico.
Co uso diario, os análogos de glucocorticoides sintéticos cunha longa vida media (por exemplo, dexametasona) causan efectos secundarios con máis frecuencia que os fármacos con vida media curta e media. O nomeamento de doses máis altas de esteroides é relativamente seguro se a duración do seu uso non supera a semana, podéndose prever unha maior achega de tales doses, efectos secundarios clínicamente significativos e efectos tóxicos.
O uso de glucocorticoides naturais e non fluorados durante o embarazo é xeralmente seguro para o feto. Con un uso prolongado de medicamentos fluorados, é posible o desenvolvemento de efectos indesexables no feto, incluídas deformidades.Se unha muller traballadora leva tomando glucocorticoides durante os 1,5-2 anos anteriores, adminístrase ademais 100 mg de hidrocortisona hemisuccinado cada 6 horas para previr a insuficiencia suprarrenal aguda.
Cando se amamanta, as doses baixas de hormonas equivalentes a 5 mg de prednisona non son prexudiciais para o bebé. As doses máis altas de fármacos poden provocar acrobacias e inhibición do eixe hipotalámico-hipofisario-suprarrenal no bebé. Por iso, ás mulleres que toman doses moderadas a altas de glucocorticoides non se lles recomenda amamantar.
Para a prevención da síndrome de angustia respiratoria en bebés prematuros, úsanse medicamentos de longa duración (a miúdo dexametasona). Recoméndase a administración intramuscular de dexametasona á muller en parto con período de xestación de ata 34 semanas 24-48 horas antes do parto previsto. A readministración do medicamento é posible se non se produciu o nacemento prematuro nos próximos 7 días.
| Traslado á terapia alternativa | Redución da dose de glucocorticoides | ||||
| Día | Prednisona mg | Día | Prednisona mg | Día | Prednisona mg |
| 1 | 60 | 11 | 90 | 21 | 85 |
| 2 | 40 | 12 | 5 | 22 | 5 |
| 3 | 70 | 13 | 90 | 23 | 80 |
| 4 | 30 | 14 | 5 | 24 | 5 |
| 5 | 80 | 15 | 90 | 25 | 80 |
| 6 | 20 | 16 | 5 | 26 | 5 |
| 7 | 90 | 17 | 85 | 27 | 80 |
| 8 | 10 | 18 | 5 | 28 | 5 |
| 9 | 95 | 19 | 85 | 29 | 80 |
| 10 | 5 | 20 | 5 | 30 | 0 |
Adestramento do paciente
O paciente debe ser consciente das posibles consecuencias clínicas da insuficiencia do eixe da hipotálamo hipofisario-suprarrenal, que pode producirse como consecuencia do uso sistémico de glucocorticoides. Precaución do paciente sobre a inadmisibilidade da auto-interrupción do tratamento ou unha rápida redución da dose de hormonas sen asesoramento médico adecuado. A resposta do eixe hipotálamo-hipofisaria-suprarrenal ao estrés pode diminuír incluso despois da administración diaria de glucocorticoides durante 7 días. Se o tratamento regular de hormonas orais se interrompe durante máis de 24 horas, entón o paciente pode desenvolver un colapso circulatorio como resposta a estrés fisiolóxico, trauma, infección e cirurxía, que a miúdo require administración parenteral de glucocorticoides. É imposible predecir de forma fiable a aparición de insuficiencia do eixe hipotalámico-hipofisario-suprarrenal nin pola dose de hormonas, nin pola duración do tratamento, nin polo nivel de cortisol no plasma de xexún (aínda que a miúdo se produce insuficiencia cando se prescriben altas doses de glucocorticoides).
Cómpre salientar que o tratamento con hormonas estimula o apetito e causa aumento de peso e destaca a importancia da dieta antes de comezar o tratamento. O médico debería describir ao paciente os síntomas da diabetes, a miopatía esteroideal, as neuropsíquicas, infecciosas e outras complicacións da terapia con glucocorticoides.
Interacción con outros medicamentos
Algúns medicamentos poden afectar á concentración de glucocorticoides no sangue. Así, o fenobarbital e a rifampicina intensifican o metabolismo das hormonas no fígado e reducen así o seu efecto terapéutico. O uso combinado de esteroides e diuréticos tiazídicos aumenta significativamente o risco de hiperglicemia e hipocalemia. A administración simultánea de glucocorticoides e ácido acetilsalicílico reduce o nivel deste último no sangue que a súa concentración é inferior á terapéutica.
Conclusión
As hormonas glucocorticoides ocupan un lugar digno no arsenal médico. En moitos casos, o uso oportuno e adecuado destes fármacos salva a vida dos pacientes, axuda a previr (retrasar) o inicio da discapacidade ou mitigar as súas manifestacións. Ao mesmo tempo, na sociedade, incluído o médico, é moi común o temor ás "hormonas". A clave para a desmitologización dos glucocorticoides é o seu uso racional na práctica clínica.
- Belousov Yu. B., Omelyanovsky V.V. Farmacoloxía clínica das enfermidades respiratorias.- M .: Edición Universum, 1996.- P. 119-130.
- Bereznyakov I.G.Glucocorticosteroides: uso clínico (unha guía para médicos) .- Kharkov, 1995.- 42 p.
- Fundamentos da fisioloxía humana (baixo a dirección de B. I. Tkachenko) .- San Petersburgo: Fundación Internacional para a Historia da Ciencia .- T. 1.- S. 178-183.
- Sigidin Ya. A., Guseva N.G., Ivanova M. M. Enfermidades difusas do tecido conectivo.- M .: Medicina, 1994.- 544 p.
- Strachunsky L.S., Kozlov S. H. Preparados glucocorticoides - Smolensk, 1997.- 64 p.
- Libro de referencia terapéutica da Universidade de Washington (baixo a dirección de M. Woodley, A. Whelan) .- M.: Practice, 1995.- 832 p.
- Boumpas D. T., Chrousos G. P., Wilder R. L., Cupps T. R. Terapia glucocorticoide para enfermidades mediadas pola inmunidade: correlacións básicas e clínicas.- Anais de medicina interna.- 1993.- Vol.119, nº 12.- P. 1198-1208.
O sitio proporciona información de referencia con fins informativos só. O diagnóstico e o tratamento das enfermidades deben realizarse baixo a supervisión dun especialista. Todas as drogas teñen contra-indicacións. Requírese consulta especializada.
Esteroides no tratamento de enfermidades reumatoides
Entre os fármacos usados para combater o reumatismo inclúense glucocorticosteroides. Que é e que medicamentos se usan para tratar o reumatismo, consideraremos con máis detalle. A enfermidade reumatoide ten limitacións no proceso de tratamento. Os medicamentos esteroides só se poden usar por un curto período de tempo. Non obstante, adoitan usarse na loita contra as manifestacións da febre (durante a activación da enfermidade). As drogas deste grupo tamén se usan no tratamento da inflamación das articulacións da columna vertebral. Glucocorticosteroides de uso máis frecuente no tratamento de enfermidades reumatoides:

Os glucocorticoides e a súa importancia nas enfermidades hematolóxicas
Os glucocorticosteroides (cortisona, prednisona, prednisona, dexametasona) están entre os fármacos inmunosupresores máis usados para enfermidades do sistema hematopoietico. Na súa patoxénese son posibles reaccións inflamatorias e fenómenos autoinmunes. A prednisona e, en casos graves, a metilprednisona, úsase por vía intravenosa no tratamento da anemia asociada á trombocitopenia. Os esteroides pódense usar para o sangrado, xa que levan a un aumento no número de plaquetas.
Drogas esteroides por insuficiencia suprarrenal
En caso de enfermidade, úsanse glucocorticosteroides sintéticos. Que é, que síntomas se manifestan na enfermidade? Está asociado principalmente a unha diminución da produción de hormonas corticoides e os corticoides úsanse no tratamento da insuficiencia suprarrenal aguda ou crónica. Dos medicamentos empregados: o cortisol (ou hidrocortisol).

Glucocorticosteroides para reaccións alérxicas
No tratamento de manifestacións alérxicas tamén se usan glucocorticosteroides. Este tratamento pódese levar a cabo con síntomas leves de rinitis alérxica estacional, conxuntivite, así como con urticaria ou reaccións inflamatorias asociadas a picaduras de insectos. Para evitar a reaparición de reaccións anafilácticas, adoita utilizarse hidrocortisona (200 mg por vía intravenosa) ou prednisolona (20 mg por vía intravenosa). E dos medicamentos máis populares tomados con arrefriado causado por unha alerxia son: flunisolida e fluticasona, que contribúen a unha eliminación máis rápida da conxestión nasal.
Efecto antiinflamatorio

É grazas ao forte efecto antiinflamatorio que as hormonas atoparon e ocuparon firmemente o seu nicho en medicina. Especialmente a miúdo úsanse en reumatoloxía.
A alta actividade dos corticoides en relación á inflamación permítelles tratar con éxito enfermidades como:
- Artrite reactiva.
- SLE, ou lupus eritematoso sistémico.
- e outros procesos autoinmunes.
Os glucocorticoides inhiben os procesos de inflamación e destrución nas articulacións, sen as cales ningunha enfermidade reumatolóxica pode facer. Os traumatólogos ortopédicos tamén os prescriben para a artrosis con dor severa e complicada polo proceso inflamatorio.
Como teñen un efecto antiinflamatorio os corticoides?
As hormonas levan a cabo o seu efecto antiinflamatorio suprimindo o traballo dun encima especial - a fosfolipase A2. Indirectamente, afectan ás funcións doutras substancias responsables do desenvolvemento do proceso inflamatorio.
Ademais, os corticoides reducen significativamente a saída de fluído do leito vascular debido ao estreitamento dos capilares, é dicir, eliminan o edema.
No contexto da súa acción, a microcirculación mellora a lesión e a restauración da función do órgano danado prodúcese máis rápido.
Na artrite reumatoide, os glucocorticoides protexen a cartilaxe e os ósos da destrución, permitíndolle manter a estrutura e a función das articulacións.
Efecto inmunomodulador

Unha característica dos glucocorticoides é a inhibición da inmunidade celular. Tamén inhiben o crecemento do tecido linfoide. Isto explica a maior susceptibilidade a infeccións virais no tratamento de corticoides.
Non obstante, en individuos con inmunodeficiencia previa, estas hormonas poden, pola contra, restaurar o nivel necesario de anticorpos de inmunoglobulina.
O efecto da supresión da inmunidade por glucocorticoides é moi utilizado na transplantoloxía para evitar que o paciente rexeite os tecidos transplantados.
Efecto antiallérxico
O mecanismo de desenvolvemento de calquera reacción alérxica é bastante complicado. Cando unha substancia estranxeira entra no corpo, o sistema inmunitario comeza a sintetizar anticorpos específicos: inmunoglobulinas.
Interactuan con certas estruturas - mastocitos. Como resultado deste proceso, libéranse varias substancias bioloxicamente activas, unha das cales é a histamina. É el quen provoca a aparición de síntomas desagradables e perigosos característicos das alerxias.
Os glucocorticoides bloquean a interacción das inmunoglobulinas con mastocitos e inhiben o desenvolvemento dunha reacción alérxica. GCS úsase para combater o choque anafiláctico, o edema de Quincke, a urticaria e outras formas de alerxias.
Efectos metabólicos

As hormonas esteroides afectan todo tipo de metabolismo. Non obstante, a súa participación no metabolismo dos carbohidratos é de especial perigo. Teñen os seguintes efectos:
- Aumentar os niveis de glicosa no sangue - leva ao desenvolvemento de hiperglicemia.
- Contribuír á aparición de azucre na orina: glucosuria.
- Levan á diabetes, que tamén se chama esteroides.
O efecto das hormonas no metabolismo das proteínas tamén é seguro para os pacientes. Inhiben a súa síntese e aceleran a caries. Estes procesos son especialmente pronunciados nos músculos e na pel.
O resultado desta acción catabólica dos glucocorticoides é a atrofia muscular, as estrías, a perda de peso, a dor do pes, a curación lenta das feridas.
Debido ao efecto negativo do GCS no metabolismo das graxas, prodúcese unha distribución asimétrica da graxa subcutánea no corpo. En tales pacientes, practicamente está ausente nas extremidades, pero deposítase en exceso na cara, pescozo e peito.
As hormonas esteroides conservan a auga e o sodio no corpo, pero ao mesmo tempo estimulan a liberación de calcio e a súa eliminación dos ósos. Xunto coa deterioración do metabolismo proteico, a hipocalcemia leva a.
Efectos no sistema cardiovascular

O efecto dos glucocorticoides sobre o sistema cardiovascular é un proceso complexo e diverso. Pero para o paciente é importante a súa capacidade para estreitar os vasos sanguíneos cun aumento da presión arterial. Este efecto prensor pode servir tanto para o beneficio do paciente como para o prexuízo.
Cunha forte caída da presión sanguínea, vasodilatación, choque, é a introdución de hormonas que moitas veces salva vida. Pero ao mesmo tempo, o seu uso sistemático contribúe ao desenvolvemento de hipertensión e dano cardíaco.
Efecto sobre o sistema endocrino
O uso a longo prazo de medicamentos hormonais para enfermidades articulares ou outras patoloxías desencadea un mecanismo de retroalimentación. No cerebro, inhibe a síntese de hormonas estimulantes, as glándulas suprarrenais deixan de cumprir as súas funcións.
Debido ao desequilibrio no traballo das glándulas endócrinas, todos os procesos metabólicos no corpo son perturbados. Ademais, o GCS inhibe a produción de hormonas sexuais.Isto pode causar varios trastornos na vida sexual e reprodutiva. Os niveis de hormonas sexuais reducidos tamén levan a osteoporose.
Como tratar os efectos non desexados dos corticoides?
Efectos negativos
A pesar dunha impresionante lista de efectos secundarios perigosos, as hormonas seguen a ser un tratamento popular para moitas enfermidades - articulacións, pel e sistema inmunitario.
Ás veces, o GCS é o medicamento que máis elixe. Isto adoita notarse en enfermidades autoinmunes, cando outros medicamentos fallan.
Reducir a frecuencia e gravidade dos efectos secundarios permite unha selección minuciosa da dose e do tipo de terapia en si. Hai tratamento en grandes doses, pero a curto prazo - puloterapia. Pola contra, pódense tomar medicamentos hormonais ao longo da vida, pero nunha dosificación reducida.
É importante que o tratamento se realice baixo a supervisión dun médico que avaliará regularmente o estado do corazón e os músculos, o nivel de azucre no sangue e calcio e a aparencia do paciente.
Por regra xeral, cunha dose adecuadamente seleccionada do medicamento, a terapia con glucocorticoides non fai moito dano ao paciente, pero mellora notablemente o seu benestar e o seu estado de saúde.
O corpo humano é un sistema complexo, de funcionamento continuo, capaz de producir substancias activas para a eliminación independente dos síntomas das enfermidades e a protección contra factores negativos do ambiente externo e interno. Estas substancias activas chámanse hormonas e, ademais da función protectora, tamén axudan a regular moitos procesos no corpo.
Que son os glucocorticosteroides
 Os glucocorticosteroides (glucocorticoides) son hormonas corticoides producidas pola córtex suprarrenal. O órgano hipofisario, que produce unha substancia especial no sangue, a corticotropina, é a responsable da liberación destas hormonas esteroides. Estimula a corteza suprarrenal a secreción dunha gran cantidade de glucocorticoides.
Os glucocorticosteroides (glucocorticoides) son hormonas corticoides producidas pola córtex suprarrenal. O órgano hipofisario, que produce unha substancia especial no sangue, a corticotropina, é a responsable da liberación destas hormonas esteroides. Estimula a corteza suprarrenal a secreción dunha gran cantidade de glucocorticoides.
Os especialistas cren que dentro das células dunha persoa hai mediadores especiais responsables da reacción da célula ante os produtos químicos que actúan sobre ela. Así explican o mecanismo de acción de calquera hormona.
Os glucocorticosteroides teñen un efecto moi extenso no corpo:
- ten efectos antiestrés e anti-choque,
- acelerar a actividade do mecanismo de adaptación humana,
- estimular a produción de células do sangue na médula ósea,
- aumentar a sensibilidade do miocardio e dos vasos sanguíneos, provocar un aumento da presión arterial,
- aumentar e ter un efecto positivo na gluconeoxénese que se produce no fígado. O corpo pode deter de forma independente un ataque de hipoglucemia provocando a liberación de hormonas esteroides no sangue,
- aumentar o anabolismo graxo, acelerar o intercambio de electrólitos beneficiosos no corpo,
- ten un poder inmuneregulador,
- reducir a liberación de mediadores, proporcionando un efecto antihistamínico,
- teñen un poderoso efecto antiinflamatorio, reducindo a actividade de encimas que causan procesos destrutivos en células e tecidos. A supresión de mediadores inflamatorios leva a unha diminución do intercambio de fluídos entre células saudables e enfermas, como resultado da cal a inflamación non crece e non progresa. Ademais, o GCS non permite que se produzan lipocortinas do ácido araquidónico - catalizadores do proceso inflamatorio,
Todas estas habilidades das hormonas esteroides da cortiza suprarrenal foron descubertas por científicos no laboratorio, debido a que houbo unha exitosa introdución de glucocorticosteroides no campo farmacolóxico. Máis tarde notouse o efecto antiprurítico das hormonas con uso externo.
A adición artificial de glucocorticoides ao corpo humano, internamente ou externamente, axuda ao corpo a facer fronte a moitos problemas con máis rapidez.
A pesar da alta eficacia e beneficios destas hormonas, as industrias farmacolóxicas modernas usan exclusivamente os seus análogos sintéticos, xa que as hormonas ticantosteroides utilizadas na súa forma pura poden provocar un gran número de efectos secundarios negativos.
Indicacións para tomar glucocorticosteroides
Os glicocorticosteroides son prescritos polos médicos nos casos en que o corpo require unha terapia de apoio adicional. Estes medicamentos raramente se prescriben como monoterapia, inclúense principalmente no tratamento complexo dunha determinada enfermidade.
Na maioría das veces, as indicacións para o uso de hormonas sintéticas de glucocorticoides inclúen as seguintes condicións:
- corpo, incluída rinitis vasomotora,
- e condicións pre-asmáticas,,
- inflamacións da pel de diversas etioloxías. Os glucocorticosteroides úsanse incluso para lesións infecciosas na pel, en combinación con medicamentos que poden facer fronte ao microorganismo que provocou a enfermidade,
- de calquera orixe, incluído o traumático, causado pola perda de sangue,
- e outras manifestacións de patoloxías do tecido conectivo,
- diminución significativa debido a patoloxías internas,
- longa recuperación despois de trasplantes de órganos e tecidos, transfusións de sangue. As hormonas esteroides deste tipo axudan ao corpo a adaptarse rapidamente a corpos e células estranxeiras, aumentando significativamente a tolerancia,
- Os glucocorticosteroides están incluídos no complexo de recuperación despois da radioterapia e oncoloxía,
- a reducida capacidade do seu córtex para provocar unha cantidade fisiolóxica de hormonas e outras enfermidades endócrinas nos estadios agudos e crónicos,
- algunhas enfermidades do tracto gastrointestinal:,,
- enfermidade hepática autoinmune,
- edema cerebral,
- enfermidades dos ollos: queratite, córnea iritis.
Debe tomar glucocorticosteroides só despois do nomeamento dun médico, xa que se o tomas incorrectamente e a dose está calculada incorrectamente, estes medicamentos poden provocar rápidamente efectos secundarios perigosos.

As hormonas esteroides sintéticas poden causar síntomas de abstinencia - deterioración do benestar do paciente despois de deixar o medicamento, ata unha insuficiencia de glucocorticoides. Para evitar que isto suceda, o médico non só está a calcular a dose terapéutica de fármacos con glucocorticoides. Tamén necesita construír un réxime de tratamento cun aumento gradual da cantidade de sustancia farmacéutica para o alivio da etapa aguda da patoloxía e unha diminución da dose ao mínimo despois da transición do pico da enfermidade.
Clasificación dos glucocorticoides
Os expertos medíronse a duración da acción dos glucocorticosteroides artificialmente, pola capacidade dunha única dose dun determinado medicamento de inhibir a hormona adrenocorticotrópica, que se activa en case todas as condicións patolóxicas anteriores. Esta clasificación subdivide as hormonas esteroides deste tipo nos seguintes tipos:
- De curto alcance - inhibir a actividade de ACTH por un período de algo máis dun día (Cortisol, Hidrocortisona, Cortisona, Prednisolona, Metipred),
- Duración media - período de validez de aproximadamente 2 días (traimcinolona, policortolona),
- Drogas de longa acción - o efecto dura máis de 48 horas (Batmethasona, Dexametasona).
Ademais, existe unha clasificación clásica dos fármacos segundo o método da súa introdución no corpo do paciente:
- Oral (en comprimidos e cápsulas),
- gotas nasais e aspersións
- formas inhaladas do medicamento (máis frecuentemente usado por asmáticos),
- pomadas e cremas de uso externo.
Dependendo do estado do corpo e do tipo de patoloxía, pódense prescribir tanto 1 como varias formas de medicamentos que conteñen glucocorticosteroides.
Lista de medicamentos populares con glucocorticosteroides
Entre os moitos fármacos que conteñen glucocorticosteroides, os médicos e farmacólogos distinguen varios fármacos de varios grupos moi eficaces e teñen un baixo risco de provocar efectos secundarios:


Dependendo da condición do paciente e da etapa de desenvolvemento da enfermidade, selecciónase a forma do fármaco, a dose e a duración do uso. O uso de glucocorticosteroides ten lugar necesariamente baixo a supervisión constante dun médico para supervisar calquera cambio na condición do paciente.
Corticosteroides naturais
Os corticosteroides realizan moitas funcións moi importantes no corpo.
Glucocorticoides relacionarse con esteroides tendo efecto antiinflamatorio, participan na regulación do metabolismo de hidratos de carbono, graxas e proteínas, controlan a puberdade, a función renal, a resposta do corpo ao estrés, contribúen ao curso normal do embarazo. Os corticoides no fígado inactúanse e excrétanse na urina.
A aldosterona regula o intercambio de sodio e potasio. Influenciado mineralocorticoides Na + mantense no corpo e aumenta a excreción de ións K + do corpo.
Corticosteroides sintéticos
Os corticoides causan tensión e estrés no corpo, e isto leva a unha diminución da inmunidade, xa que a inmunidade se proporciona a un nivel suficiente só nun estado relaxado. Tendo en conta o anterior, podemos dicir que o uso de corticosteroides contribúe ao percorrido prolongado da enfermidade, bloquea o proceso de rexeneración.
Ademais, os corticoides sintéticos inhiben a función das hormonas naturais dos corticosteroides, o que leva a unha función adrenal deteriorada en xeral. Os corticosteroides afectan o funcionamento doutras glándulas endocrinas, o equilibrio hormonal do corpo é perturbado.
Os corticosteroides, eliminando a inflamación, tamén teñen un efecto analxésico. Os corticosteroides sintéticos inclúen Dexametasona, Prednisolona, Sinalar, Triamcinolona e outros. Estas drogas teñen unha actividade maior e causan menos efectos secundarios que os naturais.
Preparativos para aplicación local (actualidade)
- Prednisona (pomada),
- Hidrocortisona (pomada),
- Lokoid (pomada),
- Cortade (pomada),
- Afloderma (crema),
- Laticort (crema),
- Dermoveit (crema),
- Fluorocort (pomada),
- Lorinden (pomada, loción),
- Sinaflan (pomada),
- Flucinar (pomada, xel),
- Clobetasol (pomada), etc.
Débil significa: Prednisona, Hidrocortisona, Cortade, Lokoid,
Moderadamente activo: Afloderm, Laticort, Dermoveit, Fluorocort, Lorinden,
Altamente activo: Akriderm, Advantan, Kuterid, Apulein, Kutiveyt, Sinaflan, Sinalar, Sinoderm, Flucinar.
Moi activo: Clobetasol.
Como usar corticoides?
O réxime de dosificación é prescrito polo médico. A preparación do comprimido debe tomarse a partir das seis da mañá (primeira dose) e non máis tarde de 14 horas despois. Tales condicións de admisión son necesarias para aproximar a inxestión fisiolóxica de glucocorticoides no sangue durante a súa produción pola córtex suprarrenal.
Nalgúns casos, a altas doses e segundo a natureza da enfermidade, o médico distribúe a dose para o ingreso uniforme durante o día durante 3-4 doses.
Os comprimidos deben tomarse con comida ou inmediatamente despois dunha comida cun pouco de auga.
Tratamento con corticoides
Terapia limitante usado durante longos procesos crónicos: as formas das tabletas normalmente úsanse durante varios meses ou incluso anos.
Para reducir o efecto inhibidor sobre a función das glándulas endócrinas, úsanse réximes de medicamentos intermitentes:
- terapia alternativa - Os glucocorticoides con curta e media duración da acción (Prednisolona, Metilprednisolona) úsanse de 6 a 8 da mañá cada 48 horas,
- terapia intermitente - cursos curtos de 3-4 días de tomar a droga con pausas de 4 días entre eles,
- terapia de pulso - administración rápida intravenosa dunha gran dose (polo menos 1 g) do medicamento para atención de urxencia. O medicamento escollido para este tratamento é a metilprednisolona (é máis accesible para a súa administración ás áreas afectadas e dá menos efectos secundarios).
- Baixo - inferior a 7,5 mg
- Medio - 7,5-30 mg,
- Alta - 30-100 mg
- Moi alto - por riba dos 100 mg,
- A terapia de pulso está por encima dos 250 mg.
Para a profilaxe os efectos indesexables dos corticosteroides no tracto gastrointestinal antes de tomar os comprimidos, pode recomendarse o uso de Almagel e xelea. Recoméndase excluír o tabaquismo, o abuso de alcol, exercicio moderado.
Corticosteroides para nenos
Os nenos con dependencia hormonal (por asma bronquial, por exemplo) tras a administración intravenosa do fármaco transfírense gradualmente a unha dose de mantemento de prednisolona. Con frecuentes recaídas de asma, Beklamethasone dipropionate úsase en forma de inhalación: a dose é seleccionada individualmente. Despois de recibir o efecto, a dose redúcese gradualmente a unha dose de mantemento (seleccionada individualmente).
Glucocorticoides tópicos (cremas, pomadas, locións) úsanse na práctica dos nenos, pero os nenos teñen unha maior predisposición ao efecto sistémico das drogas que os pacientes adultos (retraso e crecemento do desenvolvemento, síndrome de Itsenko-Cushing, inhibición da función das glándulas endocrinas). Isto débese a que nos nenos a relación entre a superficie corporal e o peso corporal é maior que nos adultos.
Por este motivo, os glucocorticoides tópicos en nenos deberían usarse só en áreas limitadas e cun curso curto. Isto é especialmente certo para os recentemente nados. Para nenos do primeiro ano de vida, só se poden usar pomadas que conteñan non máis dun 1% de hidrocortisona ou un medicamento de cuarta xeración - Prednicarbat (Dermatol) e ata 5 anos de idade - hidrocortisona 17-butirrato ou pomadas con medicamentos de forza media.
Para o tratamento de nenos maiores de 2 anos, pódese usar Mometasona segundo o prescrito polo médico (ungüento, ten un efecto prolongado, aplicado 1 día por día).
Hai outros medicamentos para o tratamento da dermatite atópica en nenos con efecto sistémico menos pronunciado, por exemplo, Advantan. Pode usarse ata 4 semanas, pero o seu uso está limitado debido á posibilidade de reaccións adversas locais (sequedad e adelgazamento da pel). En calquera caso, a elección do medicamento para tratar ao neno queda co médico.
Corticosteroides durante o embarazo e a lactación
Este efecto negativo dos glucocorticoides amplifícase como resultado de que as drogas modernas de longa duración (Metipred, Dexamethasone) non son desactivadas polas encimas da placenta e teñen un efecto a longo prazo sobre o feto. Os glucocorticoides, que suprimen o sistema inmunitario, axudan a reducir a resistencia dunha muller embarazada ante infeccións bacterianas e virais, que tamén poden afectar negativamente ao feto.
Os fármacos glucocorticoides pódense prescribir a unha muller embarazada só se o resultado do seu uso supera significativamente o risco de posibles consecuencias negativas para o feto.
Tales indicacións poden ser:
1. A ameaza do nacemento prematuro (un breve curso de hormonas mellora a prematura do feto prematuro para o nacemento), o uso de tensioactivo para o bebé despois do nacemento fixo posible minimizar o uso de hormonas nesta indicación.
2. Reumatismo e enfermidades autoinmunes en fase activa.
3. A hiperplasia hereditaria (intrauterina) no feto da capa cortical da glándula suprarrenal é unha enfermidade difícil de diagnosticar.
Anteriormente, había unha práctica de prescribir glucocorticoides para preservar o embarazo. Pero non se obtiveron datos convincentes sobre a eficacia dunha tal técnica, polo tanto, actualmente non se usa.
Na práctica obstétrica Úsense máis comúnmente metipred, prednisona e dexametasona. Penetran a placenta de diferentes xeitos: A prednisolona é destruída por encimas na placenta en maior medida, e Dexametasona e Metipred só nun 50%. Polo tanto, se se utilizan preparacións hormonais para tratar a unha muller embarazada, é preferible prescribir prednisolona e se para o tratamento do feto - Dexamethasona ou Metipred. Neste sentido, as reaccións adversas do prednisolona e do feto son menos comúns.
Os glucocorticoides en alerxias graves son prescritos tanto sistémicos (inxeccións ou comprimidos) como locais (pomadas, xeles, pingas, inhalacións). Teñen un poderoso efecto antialérxico. Úsanse principalmente os seguintes medicamentos: Hidrocortisona, Prednisolona, Dexametasona, Betametasona, Beclometasona.
Dos glucocorticoides tópicos (para o tratamento local), na maioría dos casos úsanse aerosoles intranasais: con febre do feno, rinitis alérxica, conxestión nasal (estornudos). Normalmente teñen un bo efecto. Fluticasona, dipropionato, propionato e outros atoparon un uso xeneralizado.
Na conxuntivite alérxica, os glucocorticoides raramente se utilizan debido a un maior risco de efectos secundarios. En calquera caso, con manifestacións alérxicas, é imposible empregar medicamentos hormonais por si mesmos para evitar consecuencias indesexables.
Corticosteroides para a psoríase
Os glucocorticoides para uso tópico (pomadas, cremas) adoitan utilizarse 2 p. ao día: cremas durante o día sen apósitos e pola noite con alcatrán de carbón ou antralina usando un aderezo oclusivo. Con lesións extensas, úsanse aproximadamente 30 g do medicamento para tratar todo o corpo.
A elección da preparación de glucocorticoides segundo o grao de actividade para aplicación tópica depende da gravidade do curso da psoríase e da súa prevalencia. A medida que os focos de psoríase diminúen durante o tratamento, o fármaco debe cambiarse a menos activo (ou menos usado normalmente) para minimizar a aparición de efectos secundarios. Cando o efecto se obtén despois de aproximadamente 3 semanas, é mellor substituír o medicamento hormonal por un axente suavizante durante 1-2 semanas.
O uso de glucocorticoides en grandes áreas durante un longo período pode agravar o proceso. A reaparición da psoríase despois da interrupción do medicamento prodúcese antes que durante o tratamento sen glucocorticoides.
, Coaxil, Imipramine e outros) en combinación con glucocorticoides poden causar un aumento da presión intraocular.
Regras de retirada de corticoides
Se a duración do curso de glucocorticoides é de ata varios meses, a dose de prednisolona pode reducirse en 2,5 mg (0,5 comprimidos) cada 3-5 días. Cun curso máis longo, a dose diminúe máis lentamente - por 2,5 mg cada 1-3 semanas. Con moita atención, a dose redúcese por baixo dos 10 mg - 0,25 comprimidos cada 3-5-7 días.
Se a dose inicial de prednisolona foi alta, entón inicialmente a diminución é máis intensa: por 5-10 mg cada 3 días. Ao chegar a unha dose diaria igual a 1/3 da dose inicial redúcese 1,25 mg (1/4 comprimidos) cada 2-3 semanas. Como resultado de tal diminución, o paciente recibe doses de mantemento durante un ano ou máis.
O médico prescribe o réxime de redución do medicamento e a violación deste réxime pode levar a unha agravación da enfermidade - o tratamento terá que comezar de novo cunha dose maior.
Prezos corticoides
No corpo humano prodúcense constantemente procesos químicos e bioquímicos, como resultado de determinadas substancias. Afectan a funcionalidade de órganos e sistemas, todos os procesos que se producen a nivel celular. O estudo de tales compoñentes - hormonas, permite non só comprender a súa funcionalidade e mecanismos de acción, senón que tamén se poden usar con fins terapéuticos. O tratamento de substitución hormonal para moitos pacientes é o único xeito de saír das enfermidades que non responden á terapia con outras drogas. Os glucocorticosteroides úsanse en prácticas dentais, xinecolóxicas, urolóxicas, dermatolóxicas e outras. Entón, glucocorticosteroides, que é?
Acción farmacolóxica dos corticoides
Os glucocorticosteroides (outro nome - glucocorticoides) son substancias esteroides hormonais que forman parte dunha subclase de corticoides que son producidos no corpo pola cortiza suprarrenal. Este é o cortisol (ten a maior actividade biolóxica), a corticosterona, etc.
Paga a pena sabelo: os glucocorticoides teñen un poderoso efecto antiestrés e efecto anti-choque. A súa concentración no sangue aumenta bruscamente ante o fondo dunha situación estresante, un trauma, acompañada de perda de sangue. Un aumento do nivel de hormonas en tales imaxes está asociado coa adaptación do corpo á perda intensa de sangue, ao choque, ás consecuencias do trauma e outras influencias negativas.
O efecto das hormonas esteroides da glicosa sobre o corpo humano é o seguinte:
- Contribuír a un aumento da presión sistólica e diastólica,
- Aumenta a susceptibilidade das paredes celulares do músculo cardíaco aos efectos das catecolaminas,
- Evitan a perda de susceptibilidade ao receptor cun alto contido en catecolaminas,
- Estimula a produción de glóbulos brancos no corpo,
- Aumente a síntese de glicosa no fígado,
- Aumenta a concentración de azucre
- Inhibir a penetración de glicosa nos tecidos periféricos,
- Acelerar a produción de glicóxeno
- Inhibir o proceso de produción de sustancias proteicas, o seu reparto,
- Os glucocorticosteroides eliminan o calcio e o potasio, proporcionan a acumulación de auga, cloro e sodio no corpo,
- Retardar o desenvolvemento de reaccións alérxicas.
As hormonas glucocorticoides "controlan" o consumo de lípidos nas células do tecido subcutáneo, afectan a susceptibilidade dos tecidos brandos aos efectos de certas hormonas. Ademais, estas substancias afectan á actividade do sistema inmune - inhiben a actividade dalgúns anticorpos, pero aceleran a formación doutras células, etc. A lista de propiedades hormonais continúa. É posible que participen activamente noutros procesos, que aínda non se coñecen.
Entón, glucocorticosteroides, que é? Trátase de hormonas que se producen no corpo de cada persoa. Teñen moitas propiedades. Pero unha das accións máis valiosas que provoca o uso de GCS é o efecto antiinflamatorio. O GCS inhibe a actividade de certos compoñentes enzimáticos no corpo, o que leva a un alivio rápido dos procesos inflamatorios.
As hormonas evitan a formación de edema no foco da inflamación, xa que proporcionan unha diminución da permeabilidade das paredes vasculares. Tamén desencadean a produción doutras substancias que se caracterizan por propiedades antiinflamatorias.
Importante: os glucocorticosteroides son medicamentos con ampla gama de efectos, cuxo uso está permitido só por razóns médicas estritas. O uso independente está cheo de numerosas complicacións.
Indicacións de uso

Os glucocorticosteroides son prescritos para o tratamento de patoloxías da glándula suprarrenal. É recomendable levalas nun contexto de formas agudas ou crónicas de insuficiencia renal, con hiperplasia da capa cortical de carácter innato. Con estas enfermidades, a produción natural de hormonas é perturbada, polo tanto, é necesario o uso de fármacos para restaurar o equilibrio hormonal.
- Tratamento de enfermidades de natureza autoinmune (por exemplo, con reumatismo, sarcidosis). O seu propósito baséase na capacidade para acelerar ou suprimir certos procesos inmunitarios. O GCS prescríbese para o tratamento da artrite reumatoide.
- Terapia de patoloxías do sistema urinario, incluída a natureza inflamatoria (a cita débese á propiedade antiinflamatoria).
- Os GCS nunha reacción alérxica úsanse como medicamentos que afectan á produción de compoñentes activos que potencian a intolerancia fisiolóxica de irritantes - alérgenos.
- Recoméndase a terapia de substitución hormonal para enfermidades do sistema respiratorio (ante o asma bronquial, rinite alérxica, pneumonía). Teña en conta que os medicamentos hormonais difiren no mecanismo e na velocidade de exposición. Algunhas drogas funcionan relativamente rápido, mentres que outras traballan lentamente. Non se poden usar medicamentos de acción lenta para aliviar unha clínica aguda.
- Na práctica dental, os corticoides prescríbense para pulpite, periodontite e outras enfermidades.
- Terapia de enfermidades dermatolóxicas. Por regra xeral, prescríbese unha crema ou un ungüento a base de substancias hormonais. Eles axudan a aliviar os procesos inflamatorios na derme, alivianse dunha clínica negativa - erupcións cutáneas, lavado da pel, lesións ulcerativas, etc.
- Tratamento de patoloxías gastrointestinais (enfermidade de Crohn).
- O GCS prescríbese para lesións, que se basean en accións antiinflamatorias e anti-choque.
- En tratamento complexo contra o fondo de edema cerebral.
A partir de compostos que pertencen ao grupo de hormonas glucocorticosteroides, creáronse moitos medicamentos. Eles veñen en diferentes formas de dosificación - loções, bálsamo, cremas, pomadas, xeles, spray, comprimidos para uso interno.
Os nomes dos fármacos glucocorticosteroides: cortisona, triamcinolona, hidrocortisona, prednisolona, Beclometasona, dexametasona, etc. A terapia de substitución hormonal ten as súas propias características, só un especialista médico prescribe medicamentos que conteñen substancias hormonais.
Probables efectos secundarios dos glucocorticosteroides

Os medicamentos con glucocorticosteroides úsanse debido á súa eficacia no tratamento de moitas enfermidades. Eles axudan a restaurar o equilibrio hormonal no corpo, o que elimina unha serie de patoloxías. Pero o tratamento hormonal non sempre é seguro, xa que moitas veces leva á aparición de fenómenos negativos. É por iso que as drogas teñen indicacións estritas.
Os fenómenos negativos máis comúns inclúen:
- Deterioro da pel, pelo, aparición de estrías, acne, furúnculos,
- Crecemento intensivo do pelo en mulleres en zonas atípicas do corpo (por exemplo, no peito, na cara, etc.),
- Deterioro do estado dos vasos sanguíneos (diminución da forza, elasticidade e resistencia),
- Efectos adversos sobre o sistema nervioso central. Maniféstase por perturbación do sono, labilidade emocional, irritabilidade sen causas, neurosis, apatía, depresión e outras condicións patolóxicas,
- Discapacidade visual.
Para información: os glucocorticosteroides poden desencadear o desenvolvemento de diabetes mellitus (dixestibilidade deteriorada do azucre no sangue), úlcera péptica, hipertensión arterial (presión arterial crónica), inmunodeficiencia, obesidade, etc.
Na práctica médica, identificáronse casos cando o GCS levou a un proceso infeccioso tormentoso no corpo. Isto débese a que no contexto da presenza de microorganismos patóxenos, as drogas conducen a unha diminución da inmunidade, como resultado, as bacterias comezan a multiplicarse activamente, xa que o sistema inmune non pode facerlles fronte.
Os eventos adversos non se desenvolven só cun uso prolongado ou debido a unha sobredose, senón tamén nos casos en que o paciente toma o medicamento segundo as instrucións. O seu desenvolvemento tamén ocorre no contexto da retirada de drogas (síndrome de retirada), porque cando se reciben hormonas dende o exterior, as glándulas suprarrenais non as producen por si soas.
Ao final da terapia hormonal, a miúdo obsérvanse os seguintes síntomas:
- Dolores musculares.
- Diminución do apetito.
- Letarxia, apatía.
- Un aumento da temperatura corporal.
- Unha exacerbación das enfermidades crónicas na historia.
A consecuencia máis perigosa do uso de glucocorticosteroides é a aparición de insuficiencia suprarrenal aguda. Caracterízase por unha forte diminución da presión arterial, unha violación do proceso dixestivo, dor abdominal, estado de letarxia e convulsións.
Os glucocorticosteroides teñen unha síndrome de retirada, polo que deixar de usar por conta propia non é menos perigoso que a auto-medicación. Remata a terapia baixo a supervisión dun médico. A dose redúcese gradualmente, o que reduce a gravidade dos efectos secundarios.

 Vexa a lista e características de patoloxías renales baratas.
Vexa a lista e características de patoloxías renales baratas.