Apidra SoloStar
Glulisina insulina, que é o ingrediente activo en Apidra, é esencialmente un análogo recombinante insulina humana, pola forza da súa acción equivalente ao humano endóxeno insulina. En comparación con insulina humana soluble a acción deste análogo desenvólvese máis rápido e a duración da súa influencia é algo máis curta.
Acción fundamental insulina, así como os seus análogos análogos, incluídos insulina glulisinaé regulación metabolismo da glicosa. Os efectos deste grupo de drogas teñen como obxectivo baixar a concentración glicosa no plasmaactivación da súa absorción por tecidos periféricos (especialmente tecido adiposo e músculos esqueléticos), así como para suprimir a formación de glicosano tecido hepático. En adipocitosa droga deprime lipóliseretarda o proceso proteólisee sobe síntese de proteínas. Estudos en pacientes diabete e voluntarios saudables confirmaron un inicio máis rápido dos efectos de Apidra coa administración de sc, así como a súa duración máis curta, en comparación con insulina humana soluble. Con vía de administración s / c hipoglucémico a eficacia desta droga obsérvase despois de 10-20 minutos. Ao comparar inxeccións iv insulina humana soluble e insulina glulisina os efectos de ambas drogas seguen ao mesmo nivel. A actividade de redución de glicosa dunha unidade de ambos os dous fármacos coincide completamente.
Na primeira fase dos estudos en curso con pacientes con diabetes mellitus dependente da insulina avaliación da capacidade para reducir a glicosa insulina humana soluble e insulina glulisina con inxeccións s / c a unha dose de 0,15 U / kg, administrada en diferentes momentos en relación cunha comida estándar de 15 minutos. Segundo os resultados dos estudos, comprobouse que a introdución de Apidra 2 minutos antes da comida tiña o mesmo efecto glicémicocomo a introdución insulina humana media hora antes da comida. No caso da introdución de ambos estes medicamentos 2 minutos antes das comidas, os mellores indicadores control glicémico observado en relación a insulina glulisina. A inxección de apidra dada 15 minutos despois do inicio da comida deu a mesma resultado glicémicoque a introdución do homólogo humano 2 minutos antes da comida.
Na primeira fase de investigación en curso insulina lispro, insulina glulisina e insulina humana soluble implicando pacientes con obeso Comprobouse que se mantén a rápida eficacia de Apidra. Durante o transcurso deste estudo, o período para alcanzar o limiar do 20% de AUC completa, respectivamente, para insulina glulisina/insulina lispro/insulina humana foi 114/121/150 minutos, un ASC (0-2 horas), mostrando tamén cedo baixada de glicosa a acción foi de 427 mg / kg / 354 mg / kg / 197mg / kg respectivamente.
Na 3ª fase dun ensaio clínico de 26 semanas entre insulina glulisina e insulina lisproque se administraron s / c pouco (0-15 minutos) antes das comidas a pacientes con diabetes xuvenilusar como droga de fondo - insulina glargina, comprobouse que os efectos de ambos estes fármacos eran comparables en relación a control glicémicoclasificadas pola variación de contido Hba1c(hemoglobina glicosilada) na fase final do estudo, en comparación coa etapa inicial. Notáronse parámetros comparables glicosa no plasmaarranxado por autocontrol. En caso de inxección insulina glulisinaen comparación coa introdución insulina lispro, non se precisou un aumento das dosificacións do medicamento de fondo.
Na 3ª fase dun ensaio clínico de 12 semanas en pacientes con diabetes mellitus dependente da insulinasometido a un tratamento de fondo insulina glarginaeficacia demostrada insulina glulisina, administrado inmediatamente despois dunha comida, non inferior a cando se administrou antes (0-15 minutos) a comida ou a inxección insulina humana solublerealizado 30-45 minutos antes da comida.
No grupo de estudo de pacientes que recibiron insulina glulisina antes das comidas, notouse unha diminución máis importante Hba1cen comparación con pacientes do grupo de uso analóxico humano.
Na 3ª fase dun ensaio clínico de 26 semanas seguido dun test de seguridade de 26 semanas, comparado insulina glulisinaadministrado s / c 0-15 minutos antes das comidas e insulina humana solubleadministrado s / c 30-45 minutos antes da comida, implicando pacientes con diabetes non dependente da insulinarecibindo ademais como droga de fondo - insulina isófano. O índice medio de peso do paciente foi de 34,55 kg / m2. Redución máis significativa Hba1c(-0,46%) observouse en pacientes do grupo insulina glulisinaen comparación co grupo insulina humana (-0,30%). Neste estudo, a maioría dos pacientes (79%) inmediatamente antes da administración combinaron o seu fármaco de acción curta insulina de isofano. Tomaron 58 persoas estudadas no momento da aleatorización axentes hipoglucémicos orais e seguiu tomándolles nunha dose sen cambios.
No caso dunha infusión continua de infusión de sc insulinacoa utilización dun dispositivo bomba (en relación á diabetes xuvenil) en 59 pacientes que usaban medicamentos Apidra ou Aspart, notouse unha baixa frecuencia oclusión do catéter, para a droga Apidra - 0,08 oclusiónaos 30 días, para a droga Aspart - 0,15 oclusiónpara o mesmo período, así como unha frecuencia similar de reaccións negativas no lugar da inxección, respectivamente o 10,3% e o 13,3%.
No grupo de idade infantil con diabetes dependente da insulina, ao comparar a seguridade e eficacia da introdución como droga de fondo - insulina glargina(unha vez ás 24 da noite) ou insulina isófano (dúas veces ao día, mañá e noite) con administración de sc insulina lispro e insulina glulisina (15 minutos antes das comidas), en ambos grupos reveláronse indicadores comparables control glicémicofrecuencias graves episodios hipoglucémicos e frecuencias de formación hipoglucemiarequirindo intervención externa. É máis, despois de realizar a terapia durante 26 semanas, no grupo Apidra, para obter control glicémico requiriuse un aumento significativo da dosificación diaria insulina de acción rápidadroga de fondo e total dose de insulina, en comparación cun grupo que usa insulina lispro.
Durante ensaios clínicos en pacientes adultos, non se detectaron diferenzas na eficacia e seguridade de usar Apidra por pacientes de diferentes sexos e razas diferentes.
Ao usar procesos de substitución de Apidra aminoácidos asparaginainsulina humana en diante lisinaen posición OT, así como lisinaen diante ácido glutámico na posición B29, contribúe á maior absorción do medicamento.
AUC do medicamento en todos os grupos de pacientes (voluntarios sans e pacientes que padecen tipo 1 e 2 diabetes mellitus) amosaron unha absorción dúas veces superior e Cmax Apidra en comparación coninsulina humana soluble.
Ao realizar estudos con pacientes con diabetes xuvenilDespois dunha inxección s / c de 0,15 U / kg de Apidra, a súa Cmax alcanzouse máis de 55 minutos e foi de 82 ± 1,3 μED / ml, mentres que estes parámetros para o análogo humano foron respectivamente 46 ± 1,3 μED / ml e 82 minutos. Duración media insulina glulisina na circulación sistémica foi menor (98 min) que en insulina humana(161 min).
Ao realizar estudos con pacientes con diabetes non dependente da insulina, despois da inxección sc de 0,2 U / kg de Apidra, a media de Cmax do seu ingrediente activo foi de 91 mcU / ml (no rango de 78-104 mcd / ml).
A absorción do medicamento, no caso da inxección sc de Apidra, realizada na rexión da coxa foi a máis baixa e aumentou coa introdución do medicamento na rexión do ombreiro. A maior absorción foi observada cando se inxectou na rexión da parede abdominal anterior. Con administración subcutánea, a biodisponibilidade absoluta de Apidra foi aproximadamente do 70% (cadeira - 68%, ombro - 71%, parede abdominal - 73%) e caracterizouse por unha baixa variabilidade en diferentes pacientes.
Coa on / na distribución insulina glulisina e a súa derivación posterior é semellante á de insulina humana soluble e é respectivamente: Vd - 13 litros e 22 litros, T1 / 2 - 13 minutos e 18 minutos. Con inxección s / c insulina glulisina ocorre máis rápido (con T1 / 2 - 42 minutos) en comparación co homólogo humano (con T1 / 2 - 86 minutos). Ao realizar unha análise cruzada de investigacións e probas insulina glulisinaincluíndo voluntarios saudables e pacientes con tipos 1 e 2 diabete, o aparente T1 / 2 desta droga situábase nun intervalo de 37-75 minutos.
Un estudo no que participan persoas sen diabetes mellituspero tendo patoloxía renal varios graos de severidade (con CC superior a 80 ml / min, 30-50 ml / min e menos de 30 ml / min) mostraron a preservación do parámetro medio da velocidade de acción de Apidra. Non obstante, cando patoloxías renales permita reducir a necesidade de solicitude insulina.
At patoloxías hepáticas non se realizou un estudo sobre os parámetros farmacocinéticos de Apidra.
Non se entende completamente o efecto do paciente ancián sobre as características farmacocinéticas de Apidra.
A farmacodinámica e farmacocinética de Apidra estudáronse en grupos de idade pediátrica de pacientes con diabetes dependente da insulina 7-11 anos e 12-16 anos. Os valores de absorción, Tmax e Cmax do medicamento en ambos os dous grupos foron comparables aos dos pacientes adultos. Ao inxectar Apidra inmediatamente antes de probalo con comida, o mellorcontrol da glicosa no plasma despois de comer contra insulina humana. Aumento de contido glicosa no plasma despois da comida (AUC0-6 horas) foi igual para Apidra - 641 mg / h × dl, durante insulina humana soluble - 801 mg / h × dl.
Efectos secundarios
As manifestacións negativas notadas ao usar o medicamento Apidra foron reaccións características desta clase farmacolóxica de medicamentos e, polo tanto, para todas as existentes insulina.
A manifestación negativa máis significativa insulinoterapiaobservado polo sistema metabólico é hipoglucemia, que ocorre máis frecuentemente co uso razoable de dosificación excesiva insulina.
Simptomatoloxía hipoglucemiaxeralmente aparece de súpeto. Non obstante, violacións neuropsiquiátricopersonaxe que se forma no fondo neuroglicopenia(inusual) debilidadeou fatiga, dores de cabezasentimento fatigadiminución da concentración perturbacións visuais, somnolencia, síndrome convulsivanáuseas confusión/perda de coñecemento) preceden á manifestación contraregulación adrenérxica (irritabilidadefame emoción nerviosapalidez da pel tremor,suor fríaansiedade taquicardiaforte latido do corazón) A gravidade desta sintomatoloxía depende da velocidade e gravidade do desenvolvemento hipoglucemia.
Episodios graves recorrentes hipoglucemiapode causar danos ou trastornos sistema nervioso. Pronunciado e prolongado hipoglucemiapode ser mortal para os pacientes, xa que pode aumentar o aumento dos seus síntomas fatal.
Reaccións o sistema inmune pode manifestar fenómenos locais persoais hipersensibilidadeata Apidra (incluído ruborsentimento coceira e hinchazón no lugar da inxección). Estes fenómenos, por regra xeral, auto-nivelanse uns días despois da inxección. Nalgúns casos, esta sintomatoloxía non aparece por influencia insulina, e por irritación da pel, debido á súa preinxección antisépticoprocesamento, así como debido a unha inxección incorrecta de SC.
Manifestacións sistémicas de persoal hipersensibilidadeA apidra pode estar acompañada dunha erupción cutánea (posiblemente con coceira) en todo o corpo, sensación estanque no peito, baixar a presión arterial, afogaráfrecuencia cardíaca ou hiperhidrose. Episodios pesados alerxias xeneralizadasincluíndo sucesos anafilácticospode estar en perigo.
As reaccións negativas da pel adoitan ser limitadas. lipodistrofiacapaz de, con todo, reducir a absorción insulina glulisina. Á formación lipodistrofiapode levar inxeccións frecuentes ao mesmo lugar, sen cambiar as áreas de administración de fármacos e, polo tanto, é recomendable que os sitios de inxección cambien con frecuencia (coxa, parede abdominal, ombreiro) para evitar o desenvolvemento lipodistrofia.
Apidra, instrucións de uso
A insulina Apidra SoloStar está destinada á administración de sc, realizada pouco antes (0-15 minutos) ou inmediatamente despois da comida.
Esta droga debe usarse en réximes terapéuticos, incluída a compartición insulina prolongada (posiblemente analóxico) ou medio longo eficiencia, e tamén en paralelo coa drogas hipoglicémicas orais acción.
O réxime de dosificación de Apidra determínase individualmente.
A introdución de Apidra SoloStar realízase mediante unha inxección sc, ou beninfusión continuarealizada en graxa subcutánea utilizando sistema de bomba.
A administración de inxección sc realízase no ombreiro, parede abdominal (dianteira) ou coxa. A infusión realízase na graxa subcutánea na rexión da parede abdominal (fronte). Os sitios de inxección s / c (coxa, parede abdominal, ombreiro) deben alternarse con cada inxección posterior. Para a velocidade absorción e a duración da exposición ao medicamento pode influír nos factores realizados actividade física, outras condicións cambiantes, así como o lugar de administración. A inxección na parede abdominal é máis rápida absorciónen comparación coa introdución á coxa ou o ombreiro.
Ao realizar unha inxección, débense ter en conta todas as posibles precaucións para excluír a entrada do medicamento directamente vasos sanguíneos. Despois da inxección está prohibido masaxeen áreas de introdución. Todos os pacientes que usan Apidra SoloStar deben someterse a unha consulta sobre a técnica de administración adecuada. insulina.
A mestura de Apidra SoloStar só está permitida con insulina humana de isófano. No proceso de mestura destes fármacos, primeiro hai que introducir Apidra na xeringa. A administración de SC debe realizarse inmediatamente despois do proceso de mestura. Non se pode realizar a inxección de drogas mixtas.
Se é necesario, pódese eliminar a solución farmacéutica do cartucho incluído na pluma de xiringa e empregarse dispositivo bombadeseñado para continuo sc infusión. No caso da introdución de Apidra SoloStar con sistema de infusión de bombas, a súa mestura con calquera outra droga non está permitida.
Ao usar xogo de infusión e o depósito usado con Apidra, deberían cambiarse polo menos 48 horas despois cumprindo todas as regras asepsia. Estas recomendacións poden ser diferentes das especificadas nas instrucións xerais a dispositivos bombacon todo, a súa execución é moi importante para unha conduta adecuada infusióne evitar a formación de graves consecuencias negativas.
Os pacientes con infusión continua de apidra s / d deben ter sistemas de inxección alternativos para a administración do medicamento, así como ser adestrados nos métodos correctos do seu uso (en caso de danosdispositivo bomba).
Durante infusión continua Apidra, mal funcionamento da infusión conxunto de bombas, unha violación do seu traballo, así como erros nas manipulacións con eles, poden converterse rapidamente na causa hiperglicemia, cetoacidosis diabética e cetose. En caso de detectar estas manifestacións, é urxente establecer a causa do seu desenvolvemento e eliminalo.
Empregando un seringue SoloStar con Apidra
Antes do primeiro uso, a pluma de xiringa SoloStar debe manterse durante 1-2 horas a temperatura ambiente.
Inmediatamente antes de usar a xeringa, debes inspeccionar coidadosamente o cartucho colocado nel, cuxo contido debe ser incoloro, transparentee non inclúe visibles materia sólida estranxeira (lembra a coherencia da auga).
As plumas xiringas SoloStar usadas non se poden reutilizar e hai que desaloxalas.
Para evitar que sexa posible infecciónSó unha persoa pode usar unha pluma de xiringa sen transferila a outra persoa.
Con cada novo uso do bolígrafo de xeringa, conecte coidadosamente unha nova agulla (compatible exclusivamente con SoloStar) e manteña probas de seguridade.
Ao manipular a agulla, deberase ter moito coidado para evitar feridase oportunidades infecciosa transferencia.
Debe evitarse o uso de plumas de xeringa se se danan, así como nos casos de incerteza no seu traballo.
Sempre é necesario ter un bolígrafo de xeringa en reposición en caso de perda ou dano do primeiro.
A pluma de xeringa debe estar protexida da sucidade e do po, é posible que se limpe as súas partes externas pano mollado. Non se recomenda mergullar a xeringa fluído, lavarou graxaxa que isto pode causarlle dano.
Unha pluma de xiringa que se pode empregar SoloStar en funcionamento, diferente dosificación precisa da solución e require unha manipulación coidadosa. Ao realizar todas as manipulacións coa pluma xeringa, é necesario evitar situacións que poidan causar o seu dano. En caso de sospeita da súa capacidade de servizo, use unha xeringa diferente.
Inmediatamente antes da inxección, asegúrese de que insulina recomendadamarcando a etiqueta na etiqueta do bolígrafo. Despois de eliminar o tapón da xeringa, cómpre inspección visual o seu contido, despois do cal instalar a agulla. Só permitido incoloro, transparentesemellante á auga en coherencia e non incluíndo ningunha sólidos estranxeiros a solución insulina. Para cada inxección posterior, debería empregarse unha agulla nova, que debe ser estéril e axustarse á pluma.
Antes da inxección, asegúrese de que probas de seguridade, verifique o correcto funcionamento da pluma de xiringa e da agulla instalada nel e elimínalo tamén da solución burbullas de aire (se o hai)
Para iso, cando se eliminan os tapóns externos e internos da agulla, mídese unha dose da solución igual a 2 PECES. Sinalando a agulla da xeringa cara arriba, toque suavemente o cartucho co dedo, intentando cambiar todo burbullas de aire á agulla instalada. Pulse o botón destinado á administración de medicamentos. Se aparece na punta da agulla, podemos supor que a pluma de xiringa funciona como se espera.Se isto non sucede, repita as manipulacións anteriores ata obter o resultado desexado.
Despois probaspor seguridade, a ventá de dosificación do bolígrafo debe amosar o valor "0", tras o que se pode establecer a dosificación requirida. A dose administrada do medicamento debe medirse cunha precisión de 1 UNIDADE, no rango de dosificación de 1 UNIDADE (mínimo) a 80 UNIDADES (máximo). Se é necesario, realízase unha dose superior a 80 unidades con dúas ou máis inxeccións.
Ao inxectar, hai que introducir coidadosamente a agulla montada na pluma de xiringabaixo a pel. O botón da pluma de xiringa destinado á introdución da solución debe ser presionado completamente e permanecer nesta posición durante 10 segundos ata que se retire a agulla, o que asegura a administración completa da dose prescrita do medicamento.
Despois da inxección, a agulla debe ser eliminada e descartada. Deste xeito, ofrécese un aviso de depósito. infecciónse / ou contaminaciónplumas de xiringa, así como filtracións e aire que entra no cartucho. Despois de eliminar a agulla usada, a pluma de xeringa SoloStar debe pecharse cun gorro.
Ao retirar e eliminar a agulla, hai que guiarse por regras e métodos especiais (por exemplo, a técnica de instalar a tapa da agulla cunha soa man), co fin de reducir o risco de accidentesasí como previr infección.
Sobredose
En caso de administración excesiva insulinapode ocorrer hipoglucemia.
Con luz hipoglucemia, as súas manifestacións negativas pódense deter comendo que contén azucrede produtosou glicosa. Pacientes con diabetesempre recomendo levar galletas, docesanacos azucreou zume doce.
Síntomas graves hipoglucemia(incluídotrastornos neurolóxicos, calambres, perda de coñecemento, a quen) debería ser detido polas segundas persoas (especialmente adestradas) realizando inxeccións v / m ou s / c glucagón ou inxección iv Dextrosa. Se a aplicación glucagónnon deu un resultado durante 10-15 minutos, pasou á administración de iv dextrosa.
Paciente que acudiu concienciarecomendo comer rico hidratos de carbonopé ao final para repetir hipoglucemia.
Determinar as causas graves hipoglucemiae prevención do seu desenvolvemento no futuro, é necesario observar o paciente dentro un hospital.
Interacción
Estudos de interacción farmacocinética dirixidos insulina glulisina non realizado Dado o stock existente de coñecemento empírico acumulado durante o uso doutras drogas similares, é pouco probable a formación de interaccións medicamentosas clínicamente significativas. Hai substancias que poden afectar metabolismo da glicosa e requiren axustes de dosificación insulina glulisina, así como un control máis próximo da terapia.
A substancias que aumentan hipoglucémicoeficiencia insulinae aumentando o risco de hipoglucemiainclúen: fibratosInhibidores da ACE drogas hipoglicémicas oraissalicilatos Disopiramidas, Fluoxetina, PentoxifilinaInhibidores da monoamina oxidasa Propoxifeno, sulfonamidas.
A substancias que reducen hipoglucémicoefectos insulinainclúen: glucocorticoides, Diazoxido, Danazoldiuréticos, derivados Fenotiazina, Isoniazid, Somatropina, hormonas glándula tiroide, simpatomiméticos (Salbutamol, Epinefrina, Terbutalina), progestins (anticonceptivos orais), medicamentos antipsicóticos (Clozapina, Olanzapina), estróxenosinhibidores de proteasas
Sales de litio, beta-bloqueantes, etanol, Clonidina pode cambiar hipoglucémicoa acción de Apidra nunha dirección ou outra. Uso simultáneo Pentamidinapode causar hipoglucemia, e máis adiante hiperglicemia.
Baixo a influencia de fármacos con actividade simpatolítica (Clonidina, Reserpinabloqueadores beta, Guanetidina), manifestacións adrenérxicoa activación (reflexo) pódese expresar menos ou ausente por completo.
Debido á falta de estudos de compatibilidade, Apidra non debe mesturarse con ningún outro medicamento, excepto insulina insulina (humano).
Ao usar bomba de infusión Non se permite a mestura de Apidra con outras drogas.
Instrucións especiais
Cita do paciente insulinaoutra fábrica ou insulina alternativa debería levarse a cabo baixo a estricta supervisión do persoal médico, en conexión coa posible necesidade de cambiar o réxime de dosificación debido ás desviacións en concentración de insulinao seu tipo (insulina isófano, solubleetc.), forma (humano, animal) e / ou método de produción. Os cambios tamén poden ser necesarios en paralelo hipoglucémicoterapia con formas orais. Interrupción do tratamento ou dosificación inadecuada insulinaespecialmente en pacientes con diabetes xuvenilpode causar diabético cetoacidosise hiperglicemiarepresentando un perigo para a vida do paciente.
Lapso de tempo de desenvolvemento hipoglucemiadebido á taxa de formación efecto insulina drogas usadas e, debido a isto, pode cambiar ao axustar o réxime terapéutico. Ás circunstancias que cambian os precursores da formación hipoglucemiaou facelos menos pronunciados, inclúense: intensificación da insulinoterapialonga dispoñibilidade diabetes mellitusexistencia neuropatía diabéticacambiarse por si mesmo insulinatomar certas drogas (p. ex.bloqueadores beta).
Axuste insulinaPode que sexan necesarias dosificación ao aumentar o paciente actividade física ou cambiar a súa dieta diaria. O exercicio xusto despois de comer aumenta o risco de hipoglucemia. Cando se usa alta velocidade insulina desenvolvemento hipoglucemiavai máis rápido.
Non compensado hiper- ou hipoglucémicoas manifestacións poden causar desenvolvemento comaperda de consciencia ou incluso morte.
Necesidade de solicitude insulinapode fluctuar en sobrecarga emocional ou enfermidades.
Cando o paciente realiza un traballo preciso e perigoso, así como conducir vehículos, a posibilidade de formarse hiper- ou hipoglucemiae teña coidado.
- Actrapid (NM, MS),
- Vozulim-R,
- Biosulina P,
- Gensulina r,
- Insulina MK,
- Gansulin r,
- Insulina-Fereína CR,
- Monosuinsulina(MK, MP),
- Insuman Rapid GT,
- NovoRapid(Penfill, FlexPen),
- Insuran P,
- Pensulin(SR, República Checa),
- Humalogo,
- Rinsulina P,
- Humodar R,
- Rosinsulina P,
- Humulina Regular,
- Monoinsulina CR.
Apidra pódese prescribir aos nenos só a partir dos 6 anos.
No embarazo (e lactación)
Estudos clínicos do uso de Apidra con de embarazo están ausentes. Datos limitados da aplicación insulina embarazada as mulleres non indican o seu impacto negativo formación intrauterina do feto, fluxo de embarazoou nun bebé acabado de nacer.
As probas de reprodución realizadas en animais non mostraron diferenzas entre elas insulina humana e insulina glulisina en relación a fetal/fetaldesenvolvemento, por suposto de embarazo, actividade patrimonial e postnataldesenvolvemento.
Asigna Apidra embarazadaas mulleres deben ter coidado co control continuo obrigatorio do plasma nivel de glicosa e control glicemia.
Embarazadamulleres con diabetes gestacional debería ser consciente dunha posible redución da necesidade insulinaao longo Eu trimestre de embarazoaumento en II e III trimestreasí como unha rápida diminución despois parto.
Selección insulina glulisina Non se establece leite dunha nai lactante. Cando se usa durante lactación maternapode ser necesario axustar o réxime de dosificación.
Comentarios sobre a droga Apidra, tamén, e sobre todos os outros insulinaVexamos a unha cousa, se este medicamento se achegaba ou non a unha ou a outra persoa. No caso de que o medicamento Apidra é totalmente adecuado para o paciente, practicamente non hai queixas sobre a súa eficacia e seguridade. Tamén se nota a comodidade de usar as plumas xeringas SoloStar e a precisión da dosificación nelas. insulina.
Forma e composición de liberación
Forma de dosificación: unha solución para a administración subcutánea (subcutánea): transparente, case incoloro ou incoloro (nun paquete de cartón de 5 cartuchos de vidro transparente incoloro de 3 ml, montado en xeringas plumas desbotables e instrucións para o uso de Apidra SoloStar).
Composición de 1 ml de solución:
- substancia activa: insulina glulisina - 100 UI (unidades de acción) (3,49 mg),
- compoñentes auxiliares: ácido clorhídrico, m-cresol (metacresol), hidróxido sódico, polisorbato 20, trometamina (trometamol), cloruro sódico, auga para a inxección.
Farmacocinética
Unha absorción máis rápida facilítase mediante a substitución en insulina glulisina do aminoácido asparagina da insulina humana na posición B3 coa lisina e a lisina na posición B29 con ácido glutámico.
As curvas farmacocinéticas de AUC en pacientes con diabetes tipo 1 e tipo 2 e voluntarios saudables demostraron que a absorción de insulina da glulisina en comparación coa insulina humana soluble foi aproximadamente 2 veces máis rápida e alcanzou ata dúas veces a C maior.máx (concentración máxima da sustancia).
Segundo os resultados dun estudo no que participaron pacientes con diabetes tipo 1, Tmáx (tempo para alcanzar a concentración máxima da sustancia) despois da administración de insulina glulisina a unha dose de 0,15 U / kg s / c e insulina humana soluble foi de 55 e 82 minutos, respectivamente, emáx no plasma sanguíneo - 82 ± 1,3 e 46 ± 1,3 μED / ml. Na insulina glulisina, o tempo medio de residencia na circulación sistémica é menor que na insulina humana común (98 e 161 minutos, respectivamente).
En pacientes con diabetes tipo 2 despois da administración de 0,2 U / kg de insulina glulisina scmáx fai 91 μED / ml con latitud interquartil no rango de 78-104 μED / ml.
A absorción máis rápida obsérvase despois da introdución de Apidra SoloStar na parede abdominal anterior, en comparación coa introdución do medicamento na coxa. A biodisponibilidade absoluta da insulina glulisina é aproximadamente do 70% (da parede abdominal anterior - 73%, do músculo deltoide - 71%, da coxa - 68%), este indicador ten unha baixa variabilidade individual.
Despois da administración intravenosa, a distribución e excreción da insulina glulisina e da insulina humana soluble son similares e son respectivamente: Vd (volume de distribución) - 13 e 22 l, T1/2 (vida media de eliminación) - 13 e 18 minutos.
En comparación coa insulina humana soluble, a insulina glulisina despois da administración de s / c é excretada máis rápido (T aparente1/2 é de 86 e 42 minutos respectivamente). En individuos sans e en pacientes con diabetes tipo 1 e tipo 2, a T aparente1/2 A insulina en glulisina na análise da sección transversal dos estudos foi de 37 a 75 minutos.
En pacientes con insuficiencia renal pódese reducir a necesidade de insulina. En casos de alteración da función hepática non se estudaron parámetros farmacocinéticos.
Hai información moi limitada sobre a farmacocinética da insulina glulisina en pacientes anciáns con diabetes.
En nenos con diabetes tipo 1, a farmacocinética e farmacodinámica da insulina glulisina estudáronse en dous grupos de idade: 7-11 e 12-16 anos.Nos dous grupos, notouse unha rápida absorción da sustancia e valores Cmáx e Tmáx eran semellantes ás dos adultos. Como en pacientes adultos, a insulina glulisina cando se aplica inmediatamente antes da proba cunha comida proporcionou un mellor control da glicosa no sangue despois de comer, en comparación coa insulina humana soluble.
Imaxes en 3D
| Solución para administración subcutánea, 100 pezas / 1 ml | 1 ml |
| substancia activa: | |
| insulina glulisina | 100 Pezas (3,49 mg) |
| excipientes: metacresol (m-cresol), trometamol (trometamina), cloruro de sodio, polisorbato 20, hidróxido de sodio, ácido clorhídrico, auga para inxección |
Embarazo e lactación
Non hai información suficiente sobre o uso de Apidra ® SoloStar ® en mulleres embarazadas.
Unha cantidade limitada de datos obtidos sobre o uso de insulina glulisina en mulleres embarazadas (informáronse menos de 300 resultados do embarazo) non indica o seu efecto adverso sobre o curso do embarazo, o desenvolvemento fetal ou sobre un bebé acabado de nacer. Os estudos reprodutivos en animais non revelaron diferenzas entre a insulina glulisina e a insulina humana con respecto ao embarazo, desenvolvemento embrionario / fetal, parto e desenvolvemento postnatal.
O uso de Apidra ® SoloStar ® en mulleres embarazadas debe realizarse con precaución. É necesario un coidadoso control da concentración de glicosa no sangue e manter o control glicémico.
Os pacientes con diabetes pre-embarazo ou gestacional deben manter o control glicémico durante todo o embarazo. Durante o primeiro trimestre do embarazo, a necesidade de insulina pode diminuír e, durante o segundo e terceiro trimestre, normalmente pode aumentar. Inmediatamente despois do nacemento, a demanda de insulina diminúe rapidamente.
Non se sabe se a insulina glulisina se excreta no leite materno ou non. Para as mulleres durante a lactación, pode ser necesario axustar o réxime de dosificación de insulina e dieta.
Dosificación e administración
S / c pouco despois (0-15 minutos) antes ou pouco despois dunha comida.
Apidra ® SoloStar ® debe usarse en réximes de tratamento que inclúen insulina de acción media ou insulina de acción longa ou un análogo de insulina de acción longa. Ademais, Apidra ® SoloStar ® pódese usar en combinación con axentes hipoglucémicos orais.
O réxime de dosificación do fármaco Apidra ® SoloStar ® está seleccionado individualmente.
O fármaco Apidra ® SoloStar ® administra-se por inxección sc, ou por infusión continua na graxa subcutánea mediante un sistema de bomba.
As inxeccións subcutáneas de Apidra ® SoloStar ® deben realizarse na rexión da parede abdominal anterior, do ombreiro ou da coxa, e o medicamento adminístrase mediante infusión continua na graxa subcutánea na rexión da parede abdominal anterior. Os sitios de inxección e sitios de infusión nas áreas anteriores (parede abdominal anterior, coxa ou ombreiro) deberían alternar con cada nova administración do medicamento. A taxa de absorción e, en consecuencia, o inicio e a duración da acción poden verse afectadas por: o lugar de administración, a actividade física e outras condicións de cambio. A administración subcutánea á parede abdominal proporciona unha absorción algo máis rápida que a administración ás outras partes do corpo antes mencionadas (ver sección "Farmacocinética").
Deben observarse precaucións para evitar que o fármaco entre directamente nos vasos sanguíneos. Despois da administración do medicamento, é imposible facer masaxes na zona de inxección. Os pacientes deben formarse coa técnica de inxección correcta.
Mestura de insulina
Apidra ® SoloStar ® pódese mesturar con insulina humana-isófano.
Ao mesturar Apidra ® SoloStar ® con insulina-isófano humano, primeiro debe introducirse na xeringa Apidra ® SoloStar ®. A inxección SC debe facerse inmediatamente despois da mestura. As insulinas anteriores non se poden introducir / entrar.
Dispositivo de bombeo para infusión continua
Cando se usa Apidra ® SoloStar ® cun sistema de bomba para infusión de insulina, non pode mesturarse con outros fármacos.
Apidra ® tamén se pode administrar mediante un dispositivo de bombeo para a infusión continua de insulina. Se é necesario, a preparación Apidra ® pode ser eliminada do cartucho da pluma de xeringa Apidra ® SoloStar ® e pódese usar mediante un dispositivo de bombeo para a infusión continua de insulina.
Ao mesmo tempo, o conxunto de infusión e o depósito usado con Apidra ® deben substituírse por regras asépticas polo menos cada 48 horas. Estas recomendacións poden diferir das instrucións xerais dos manuais para dispositivos de bombeo. É importante que os pacientes sigan as instrucións especiais anteriores para o uso de Apidra ®. O non seguir estas instrucións especiais para o uso de Apidra ® pode levar ao desenvolvemento de eventos adversos graves.
Cando se usa Apidra ® cun dispositivo de acción da bomba para a infusión continua de insulina, non se pode mesturar con outras insulinas ou disolventes.
Os pacientes que se administran Apidra ® por infusión continua de sc deberían ter sistemas alternativos para a administración de insulina e deberían estar adestrados para administrar insulina por inxección sc (no caso de avería do dispositivo bomba usado).
Cando se usa Apidra ® con dispositivos de bomba para infusión continua de insulina, a interrupción do dispositivo bomba, un mal funcionamento do conxunto de infusión ou erros no manexo poden levar rapidamente ao desenvolvemento de hiperglicemia, cetose e cetoacidosis diabética. No caso do desenvolvemento de hiperglicemia ou cetose ou cetoacidosis diabética, é necesaria a identificación e eliminación rápida das causas do seu desenvolvemento.
Siga as instrucións para o manexo correcto das xeringas precargadas (consulte a sección "Instrucións de uso e manipulación").
Instrucións de uso e manexo da xiringa pre-recargada SoloStar ®
Antes do primeiro uso, a pluma de xiringa debe manterse a temperatura ambiente durante 1-2 horas.
Antes do uso, inspeccione o cartucho dentro da pluma de xeringa. Debe usarse só se a solución é transparente, incolora, non contén partículas sólidas visibles e, en coherencia, aseméllase á auga.
As plumas xeringuillas SoloStar ® baleiras non deben reutilizarse e hai que desaloxalas.
Para previr a infección, un bolígrafo pre-cuberto só o debe usar un paciente e non debe ser transferido a outra persoa.
Manexo da xiringa SoloStar ®
Antes de empregar a pluma xeringa SoloStar ®, debes ler atentamente as instrucións de uso.
Información importante sobre o uso da xiringa SoloStar ®
Antes de cada uso, conecte coidadosamente a nova agulla á pluma de xiringa e realice unha proba de seguridade. Só se deben empregar agullas compatibles con SoloStar ®.
Débense tomar precaucións especiais para evitar accidentes que impliquen o uso dunha agulla e a posibilidade de transmisión de infección.
En ningún caso debes usar a xiringa SoloStar ® se está danada ou se non está seguro de que funcionará correctamente.
Ten sempre na man unha pluma de xeringa SoloStar ® de reposición en caso de perda ou danos no exemplar empregado.
Instrución de almacenamento
Se a pluma de xeringa SoloStar ® se garda nun frigorífico, debería retirarse de 1 a 2 horas antes da inxección prevista para que a solución leve a temperatura ambiente. A administración de insulina refrixerada é máis dolorosa.
A pluma de xiringa SoloStar ® usada debe ser destruída.
A pluma de xiringa SoloStar ® debe estar protexida do po e da sucidade.
A parte exterior da seringa Pen SoloStar ® pódese limpar limpándoa cun pano húmido.
Non mergullarse en líquido, enxágüe e lubrica a pluma xeringa SoloStar ®, xa que pode danala.
A xeringa Pen SoloStar ® dispensa con precisión a insulina e é seguro para a súa utilización. Tamén require unha manipulación coidadosa. Evite situacións nas que poida producirse danos na pluma xeringa SoloStar ®. Se hai sospeita de que a instancia da pluma de xiringa SoloStar ® puidese ser danada, deberase empregar unha nova xeringa.
Etapa 1. Control da insulina
É necesario comprobar a etiqueta na xiringa SoloStar ® para asegurarse de que contén a insulina adecuada. Despois de eliminar o tapón da xeringa, a aparencia da insulina contida nela contrólase: a solución de insulina debe ser transparente, incolora, non conter partículas sólidas visibles e semellar a auga con consistencia.
Etapa 2. Conectando a agulla
Debe empregarse só agullas compatibles coa pluma de xeringa SoloStar ®.
Para cada inxección posterior, use sempre unha nova agulla estéril. Despois de quitar a tapa, a agulla debe instalarse coidadosamente na pluma de xiringa.
Etapa 3. Proba de seguridade
Antes de cada inxección, é necesario realizar unha proba de seguridade e asegurarse de que o bolígrafo e a agulla funcionan ben e que se eliminen as burbullas de aire.
Mide a dose igual a 2 pezas.
Débense retirar os tapóns de agulla exteriores e internos.
Colocando a pluma xeringa coa agulla cara arriba, toque suavemente o cartucho co dedo de insulina para que todas as burbullas de aire se dirixan cara á agulla.
Pulse (completamente) o botón de inxección.
Se a punta da agulla aparece insulina, isto significa que a pluma de xiringa e a agulla funcionan correctamente.
Se a punta da agulla non aparece insulina, repítese o paso 3 ata que a insulina apareza na punta da agulla.
Etapa 4. Selección de dose
A dose pódese establecer cunha precisión de 1 UNIDADE, desde a dose mínima (1 UNIDADE) ata a máxima (80 UNIDADES). Se é preciso introducir unha dose superior a 80 piezas, deberán administrarse 2 ou máis inxeccións.
A xanela de dosificación debe indicar "0" despois da realización da proba de seguridade. Despois, pódese establecer a dose necesaria.
Etapa 5. Dose
Un médico debe informar ao paciente sobre a técnica de inxección.
A agulla debe introducirse baixo a pel.
O botón de inxección debe ser presionado completamente. Mantéñase nesta posición durante outros 10 s ata que se elimina a agulla. Isto garante a introdución da dose seleccionada de insulina por completo.
Etapa 6. Eliminar e descartar a agulla
En todos os casos, despois de cada inxección, a agulla debe ser eliminada e descartada. Isto garante a prevención da contaminación e / ou infección, o aire que entra no recipiente para a insulina e as fugas de insulina.
Ao eliminar e descartar a agulla, hai que tomar precaucións especiais. As precaucións de seguridade recomendadas para retirar e tirar agullas (por exemplo, a técnica de poñer o tapón cunha soa man) deben observarse para reducir o risco de accidentes que implica o uso da agulla e tamén para previr a infección.
Despois de eliminar a agulla, pecha a pluma de xeringa SoloStar ® cunha tapa.
Grupos especiais de pacientes
Función renal deteriorada. A necesidade de insulina na insuficiencia renal pode diminuír.
Función hepática deteriorada. En pacientes con alteración da función hepática, a necesidade de insulina pode diminuír debido a unha capacidade reducida de gluconeoxénese e unha desaceleración do metabolismo da insulina.
Pacientes anciáns. Os datos de farmacocinética dispoñibles en pacientes anciáns con diabetes mellitus son insuficientes. A deterioración da función renal na vellez pode levar a unha diminución dos requirimentos de insulina.
Nenos e adolescentes. Apidra ® pódese usar en nenos maiores de 6 anos e adolescentes. A información clínica sobre o uso da droga en nenos menores de 6 anos é limitada.
Fabricante
1. Sanofi-Aventis Deutschland GmbH, Alemaña.
2. CJSC Sanofi-Aventis Vostok, Rusia. 302516, Rusia, Rexión de Oryol, Distrito de Oryol, s / n Bolshekulikovskoye, ul. Livenskaya, 1.
As reclamacións dos consumidores deben enviarse ao enderezo da oficina de representación da empresa en Rusia: 125009, Moscova, ul. Tverskaya, 22.
Tel .: (495) 721-14-00, fax: (495) 721-14-11.
No caso da produción da droga no Sanofi-Aventis Vostok CJSC, Rusia, as queixas dos consumidores deben enviarse ao seguinte enderezo: 302516, Rusia, Rexión de Oryol, distrito de Oryol, s / n Bolshekulikovskoye, ul. Livenskaya, 1.
Tel./fax: +7 (486) 244-00-55.
Como usar: dosificación e curso do tratamento
S / c no abdome, ombreiro ou coxa ou por infusión continua de Apidra SoloStar na graxa subcutánea do abdome. A droga adminístrase 0-15 minutos antes ou inmediatamente despois dunha comida. Os sitios de inxección e infusión deberían alternar en cada inxección. Non podes masaxear a zona de inxección (para excluír a entrada dos medicamentos nos vasos sanguíneos) O efecto do medicamento exprésase en unidades que son específicas só para a insulina glulisina e difiren de ME ou outras unidades de actividade doutras insulinas. A dose selecciónase individualmente.
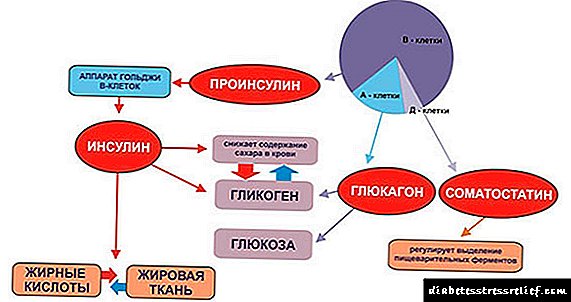
Acción farmacolóxica
Axente hipoglicémico, insulina de acción curta. Análogo recombinante da insulina humana. O uso de Apidra SoloStar reduce a concentración de glicosa no sangue, estimula a absorción de glicosa por tecidos periféricos (músculo esquelético, tecido adiposo) e inhibe a formación de glicosa no fígado. Suprime a lipólise en adipocitos, proteólise, aumenta a síntese de proteínas.
Con a / c administración de Apidra SoloStar, unha diminución da glicosa no sangue comeza despois de 10-20 minutos, cunha administración iv, o efecto sobre unha diminución da glicosa é comparable á forza da insulina humana soluble. Pola forza do efecto hipoglucémico, 1 UI de insulina glulisina é igual a 1 UI de insulina humana soluble.
Información xeral
 Apidra, aínda que se considere un análogo recombinante da hormona humana, caracterízase por un efecto rápido e non duradeiro en comparación con el. O medicamento farmacolóxico preséntase no sistema de radar (rexistro de medicamentos) como insulina curta.
Apidra, aínda que se considere un análogo recombinante da hormona humana, caracterízase por un efecto rápido e non duradeiro en comparación con el. O medicamento farmacolóxico preséntase no sistema de radar (rexistro de medicamentos) como insulina curta.
Apidra é unha solución empregada para inxeccións subcutáneas.
Ademais da sustancia activa (glulisina), o medicamento contén compoñentes adicionais como:
- polisorbato 20 (monolatarado),
- hidróxido de sodio
- trometamol (aceptador de protóns),
- cloruro de sodio
- cresol
- ácido (concentrado) clorhídrico.
A solución farmacéutica colócase en cartuchos que conteñen 3 ml, instalados na xeringa e non se poden substituír. Recoméndase almacenar a droga no frigorífico sen expoñela á conxelación e á penetración do sol. A pluma de xiringa 2 horas antes da primeira inxección debe estar nunha sala con temperatura ambiente.
O prezo de 5 plumas da droga é de aproximadamente 2000 rublos. O prezo recomendado polo fabricante pode diferir dos prezos reais.
Características farmacolóxicas
 O Apidra prescríbese aos diabéticos para normalizar a glicemia. Debido á presenza dun compoñente hormonal na súa composición, o valor do indicador de glicosa no sangue diminúe.
O Apidra prescríbese aos diabéticos para normalizar a glicemia. Debido á presenza dun compoñente hormonal na súa composición, o valor do indicador de glicosa no sangue diminúe.
Unha caída do nivel de azucre comeza dentro dun cuarto de hora despois da inxección subcutánea. As inxeccións intravenosas de insulina de orixe humana e a solución Apidra teñen case o mesmo efecto nos valores da glicemia.
Despois da inxección, no corpo póñense en marcha os seguintes procesos:
- A produción de glicosa é inhibida polo fígado,
- a lipólise suprímese nas células que compoñen o tecido adiposo,
- a síntese de proteínas está optimizada,
- Estímase a captación de glicosa nos tecidos periféricos,
- suprímese a ruptura de proteínas.
Segundo os resultados de estudos realizados entre persoas saudables e pacientes con diabetes, as inxeccións subcutáneas da hormona Apidra non só reducen o tempo de espera para o efecto desexado, senón que tamén reducen a duración do efecto. Esta característica distingue esta hormona da insulina humana.

A actividade hipoglucémica é a mesma tanto na hormona Apidra como na insulina humana. Realizáronse diversos ensaios clínicos para avaliar os efectos destes fármacos. Estiveron implicados pacientes que padecen enfermidade tipo 1. Os resultados obtidos permitiron concluír que unha solución de Glulisina nunha cantidade de 0,15 U / kg, administrada 2 minutos antes da comida, fai posible rastrexar o nivel de glicosa despois de 2 horas exactamente do mesmo xeito que despois das inxeccións de insulina humana realizadas en media hora.
Apidra conserva as propiedades da acción rápida en pacientes con obesidade existente.
Diabetes tipo 1
Os ensaios clínicos realizados entre persoas con primeiro tipo de enfermidade baseáronse nunha comparación das propiedades de Glulisin e Lizpro. Durante 26 semanas, as hormonas que conteñen estes compoñentes foron administradas a pacientes. O glargin utilizouse como preparación basal. Tras a conclusión do período de estudo, avaliouse o cambio na hemoglobina glicosilada.
Os pacientes dentro de 26 semanas mediron ademais o nivel de glicemia usando un glucómetro. O seguimento mostrou que a terapia con insulina con Glulisina, en comparación co tratamento cun fármaco que contén Lizpro, non requiriu un aumento da dosificación da hormona principal.
 A terceira fase de proba durou 12 semanas. Participaron voluntarios de persoas con diabetes que inxectaron Glargin.
A terceira fase de proba durou 12 semanas. Participaron voluntarios de persoas con diabetes que inxectaron Glargin.
Os resultados demostraron que o uso dunha solución co compoñente Glulisin despois de completar unha comida foi tan eficaz como cando se inxectou antes das comidas.
De xeito similar, confirmouse a racionalidade de usar Apidra (e hormonas similares) en comparación coa insulina humana, administrada media hora antes do lanche previsto.
Os pacientes que participaron nos ensaios dividíronse en 2 grupos:
- participantes administrando Apidra
- pacientes con diabetes, realizando terapia con insulina mediante inxeccións de hormona humana.
Os resultados dos ensaios clínicos levaron á conclusión de que o efecto de reducir a hemoglobina glicada foi maior no primeiro grupo de participantes.
Diabetes tipo 2
Durante 26 semanas realizáronse estudos en fase 3 que demostraron o efecto das drogas na glicemia en pacientes con diabetes tipo 2. Despois da súa conclusión, sucedéronse outros ensaios clínicos, que tiveron o mesmo tempo na súa duración.
 A súa tarefa foi determinar a seguridade no uso de inxeccións de Apidra, administradas 15 minutos antes das comidas, e insulina humana soluble, administrada a pacientes 30 ou 45 minutos.
A súa tarefa foi determinar a seguridade no uso de inxeccións de Apidra, administradas 15 minutos antes das comidas, e insulina humana soluble, administrada a pacientes 30 ou 45 minutos.
A insulina principal en todos os participantes foi Isofan. O índice corporal medio dos participantes foi de 34,55 kg / m². Algúns pacientes tomaron oralmente medicamentos adicionais, mentres continuaron a administrar a hormona nunha dose sen cambios.
A hormona Apidra resultou comparable coa insulina de orixe humana ao avaliar a dinámica do nivel de hemoglobina glicada durante seis meses e 12 meses respecto do valor inicial.
O indicador cambiou nos primeiros seis meses do seguinte xeito:
- en pacientes que usan insulina humana - 0,30%,
- en pacientes que se someteron a terapia con insulina que contiña Glulisina - 0,46%.
Cambio de indicador despois dun ano de proba:
- en pacientes que usan insulina humana - 0,13%,
- en pacientes que se someteron a terapia con insulina que contiña Glulisina - 0,23%.
A eficacia, así como a seguridade do uso de drogas baseadas en Glulisin, non cambiaron en persoas de diferentes razas e de xénero diferente.
Grupos especiais de pacientes
A acción de Apidra pode cambiar se os pacientes teñen varias patoloxías relacionadas coa diabetes:
- Insuficiencia renal. Nestes casos, hai unha diminución da necesidade de hormona.
- Patoloxía do fígado. Non se estudou o efecto dos axentes que conteñen glulisina en pacientes con tales trastornos.
 Non hai datos sobre cambios farmacocinéticos en pacientes anciáns. En nenos e adolescentes de 7 a 16 anos, que padecen diabetes tipo 1, o medicamento absorbe rapidamente despois da administración subcutánea.
Non hai datos sobre cambios farmacocinéticos en pacientes anciáns. En nenos e adolescentes de 7 a 16 anos, que padecen diabetes tipo 1, o medicamento absorbe rapidamente despois da administración subcutánea.
Realizar inxeccións de Apidra antes de comer permítelle manter un nivel máis normal de glicemia despois de comer en comparación coa insulina humana.
Indicacións e dosificación
O uso dunha solución medicinal é necesario para persoas con enfermidade dependente da insulina. A categoría de pacientes que reciben o medicamento con máis frecuencia inclúe nenos maiores de 6 anos.
Unha solución que conteña Glulisin debe administrarse inmediatamente despois dunha comida ou pouco antes. Apidra úsase en combinación con insulinoterapia prolongada ou axentes que teñen unha duración media de influencia, así como os seus análogos. Ademais, está permitido o uso doutros fármacos hipoglicémicos xunto coas inxeccións hormonais. A dose de inxección de Apidra só debe ser prescrita por un médico.
A terapia da enfermidade debe realizarse só baixo a supervisión dun especialista. Está prohibido cambiar de xeito independente a dosificación de calquera medicamento, especialmente inxeccións de insulina, así como cancelar o tratamento ou cambiar a outro tipo de hormona sen a aprobación previa do endocrinólogo.
Non obstante, hai un réxime de insulina terapéutica exemplar para as hormonas de acción curta. Implica a contabilidade obrigatoria do número de unidades de pan consumidas ao día (1 XE equivale a 12 g de hidratos de carbono).
Necesidade hormonal:
- para cubrir 1 XE para o almorzo, hai que pinchar 2 unidades,
- no xantar necesitas 1,5 unidades.,
- pola tarde, considérase igual a cantidade de hormona e XE, é dicir, 1: 1, respectivamente.
Manter a diabetes na fase de compensación e a glicemia normal é normal se controlas constantemente a glicosa. Isto pódese conseguir tomando medicións no contador e calculando a necesidade de que unha hormona realice inxeccións de acordo coa cantidade prevista de XE a tomar.
Métodos de administración
A solución de medicamentos Apidra inxéctase baixo a pel se se usa un bolígrafo. No caso de pacientes que usan unha bomba de insulina, o axente entra nunha zona de graxa subcutánea mediante infusión permanente.
Puntos importantes a coñecer antes de inxectar:
- A solución é inxectada na área da coxa, o ombreiro, pero a maioría das veces na área ao redor do ombligo do estómago.
- Ao instalar a bomba, o medicamento debe entrar nas capas subcutáneas no abdome.
- Os sitios de inxección deberían alternar.
- A velocidade e a duración da absorción, o período de inicio do efecto dependen da área de administración da solución, así como da carga realizada.
- Non masaxes as zonas nas que se inxectou a solución para que non entre nos vasos.
- As inxeccións realizadas no estómago garanten un inicio de efecto máis rápido que as inxeccións noutras zonas.
- Apidra pódese combinar coa hormona Isofan.
Non se debe mesturar a solución Apidra empregada para o sistema de bombas con outros medicamentos similares. A instrución deste dispositivo contén información completa sobre o funcionamento do dispositivo.
Material vídeo sobre os beneficios das bombas de insulina:
Reaccións adversas
Durante a terapia con insulina, pode aparecer síndrome convulsiva.A aparición de síntomas neuropsiquiátricos na maioría dos casos vén precedida de signos asociados a un aumento dos valores de presión arterial. De feito, tales manifestacións son características da hipoglucemia.
Esta condición é principalmente unha consecuencia dunha dose mal seleccionada ou dun desaxuste de alimentos consumidos co número de unidades ingresado.
Se se produce unha hipoglucemia, o estado do paciente non se normaliza se non se toman as medidas adecuadas. Consisten no uso de varios hidratos de carbono.
Canto máis rápido poida ter unha picadura dun paciente, máis posibilidades terá para o alivio rápido dos síntomas característicos deste estado. Se non, pode haber coma, é case imposible saír dela sen axuda médica. Os pacientes nesta condición necesitan ser inxectados cunha solución de glicosa.
Trastornos do metabolismo e da pel
Nas zonas de inxección, reaccións como:
Os síntomas que aparecen a miúdo desaparecen por conta propia e non precisan a interrupción da terapia farmacéutica.
Os trastornos no metabolismo exprésanse no desenvolvemento da hipoglucemia, que se acompaña dos seguintes síntomas:
- fatiga
- debilidade e fatiga
 ,
, - perturbacións visuais
- somnolencia
- taquicardia
- ataques de náuseas
- sensación de dor de cabeza
- suor fría
- a aparición de escuridade da conciencia, así como a súa perda completa.
A introdución da solución sen cambiar a zona de punción pode levar a lipodistrofia. É unha reacción tisular ante un trauma permanente e exprésase en lesións atróficas.
Trastornos xerais
Os trastornos sistémicos durante o uso da droga son raros.
A súa aparición vai acompañada dos seguintes síntomas:
- ataques de asma
 ,
, - urticaria
- sensación de picazón
- dermatite causada por alerxias.
Nalgúns casos, unha alerxia xeneralizada pode poñer en perigo a vida do paciente.
Pacientes especiais
As inxeccións da solución deben prescribirse a mulleres embarazadas con extrema precaución. O control da glicemia no marco de tal terapia debe realizarse constantemente.
Puntos importantes da insulinoterapia para nais expectantes:
- Calquera tipo de diabetes, incluída a forma de xestación da enfermidade, require manter o nivel de glicemia dentro de límites normais durante todo o período de embarazo.
- A dosificación de unidades do medicamento administrado diminúe no primeiro trimestre e aumenta gradualmente, a partir dos 4 meses de embarazo.
- Despois do nacemento, a necesidade dunha hormona, incluída Apidra, redúcese. As mulleres con diabetes gestacional requiren a maioría das veces a interrupción da insulinoterapia despois do parto.
É de destacar que non se realizaron estudos sobre a penetración dunha hormona co compoñente Glulisin no leite materno. A partir da información contida nas revisións das nais lactantes con diabetes, durante todo o período de lactación, debes axustar de xeito independente ou coa axuda dos médicos a dose de insulina e dieta.
Apidra non está prescrito para menores de 6 anos. Non hai información clínica sobre o uso do medicamento nesta categoría de pacientes.
Formas de composición e liberación
En 1 mililitro de solución de Apidra Solostar contén o único ingrediente activo: insulina glulisina nunha dose de 100 pezas. Ademais, o medicamento contén:
- Hydroskide e Cloruro de sodio
- Auga preparada
- Metacresol
- Polisobato
- Trometamol
- Ácido clorhídrico.
A solución que contén insulina é un líquido claro e sen pintura, dispoñible en frascos de 3 ml. Un paquete inclúe 1 ou 5 botellas con bolígrafos.
Propiedades curativas
A insulina glulisina contida en Apidra é un análogo recombinante da insulina natural producida no corpo humano. A glulisina actúa moito máis rápido e caracterízase por unha duración da exposición máis reducida en comparación coa insulina natural.
Baixo a acción da insulina glulisina, obsérvase un axuste gradual do metabolismo da glicosa. Cun descenso do nivel de azucre, rexístrase a estimulación da súa absorción directamente polos tecidos periféricos, inhibición da síntese de glicosa nas células do fígado.
A insulina inhibe o proceso de lipólise que se produce nos adipocitos, así como a proteólise. Ao mesmo tempo, a síntese de proteínas aumenta significativamente.
Como resultado de numerosos estudos coa participación de persoas con diabetes, así como de pacientes sans, obtivéronse os seguintes resultados: coa administración subcutánea de Apidra, a acción rápida da insulina obsérvase cun período de exposición máis curto que a insulina soluble natural.
Despois da introdución de glulisina baixo a pel, o seu efecto nótase despois de 10-20 minutos. Pero ao inxectarse nunha vea, o índice de glicosa diminúe do mesmo xeito que despois da introdución da insulina natural. Unha unidade de insulina glulisina caracterízase por case as mesmas propiedades que reducen a glicosa que unha unidade de insulina natural.
En pacientes con patoloxías do sistema renal, a necesidade de insulina adoita reducirse significativamente.
Apidra Solostar: instrucións de uso
A administración subcutánea de Apidra debe realizarse antes das comidas ou inmediatamente despois.
Os medicamentos que conteñen insulina deben usarse segundo o esquema prescrito de terapia antidiabética xunto coa insulina, que se caracteriza por unha duración media de exposición ou insulina de longa acción. Quizais o uso combinado con fármacos hipoglicémicos para a administración oral.
A selección do réxime de dosificación é realizada polo endocrinólogo.
Introducción Apidra
A introdución dunha solución que contén insulina realízase subcutaneamente por inxección ou infusión mediante un sistema especial de bomba.
A inxección subcutánea realízase na parede abdominal (directamente a súa parte dianteira), na rexión femoral ou no ombreiro. A infusión do medicamento realízase na parede abdominal. Os lugares de infusión e inxección deberían estar cambiando constantemente.
Como usar unha pluma xeringa
Antes da introdución de Apidra, a pluma de xiringa deberá ser lixeiramente quentada a temperatura ambiente (aproximadamente 1-2 horas).
A nova agulla se une á xeringa pluma de insulina, entón cómpre realizar unha proba de seguridade sinxela. Despois diso, o indicador "0" estará visible na xanela de dosificación da pluma de xiringa. Entón establécese a dosificación necesaria. O valor mínimo da dose administrada é 1 unidade e o máximo é de 80 unidades. Se hai necesidade de sobredose, fórmanse varias inxeccións.
Durante a inxección, a agulla, que está instalada na pluma da xiringa, necesitará introducirse lentamente baixo a pel. Presionarase o botón da pluma xeringa, que debe permanecer nesta posición inmediatamente ata o momento da extracción. Isto asegura a introdución da dosificación desexada dun medicamento que contén insulina.
Despois da inxección, elimínase a agulla e elimínase. Así, será posible previr a infección da xiringa de insulina. No futuro, a pluma de xeringa debe ser pechada cun gorro.
O medicamento pode prescribirse a mulleres embarazadas e en lactación.
Contraindicacións e precaucións

Prezo: de 421 a 2532 rub.
O medicamento que contén insulina Apidra Solostar non se usa para a manifestación de hipoglucemia e aumenta a susceptibilidade aos compoñentes do medicamento.
Cando se use un medicamento que conteña insulina doutro fabricante, será preciso un control estricto da terapia antidiabética por parte do médico asistente, xa que non se pode descartar a necesidade de axustar a dose tomada. Pode que necesite cambiar o esquema de tratamento hipoglicémico de fármacos para a administración oral.
A realización da terapia antidiabética ou o uso de altas doses de insulina, en particular en persoas con diabetes xuvenil, pode provocar cetoacidosis diabética, así como hipoglucemia, o que representa un grave perigo para a vida.
O intervalo de tempo para a aparición de hipoglucemia está directamente relacionado coa taxa de desenvolvemento da reacción hipoglucémica dos fármacos empregados, pode cambiar coa corrección do tratamento antidiabético.
Algúns factores poden reducir a severidade da hipoglucemia, inclúen:
- Longo curso de diabetes
- Terapia intensiva coa insulina
- O desenvolvemento da neuropatía diabética
- O uso de varias drogas (por exemplo, bloqueadores β).
O cambio na dose de insulina Apidra Solostar realízase cun aumento da actividade física ou cun cambio na dieta diaria.
No caso de aumentar a actividade física inmediatamente despois de comer, aumenta a probabilidade de desenvolver hipoglucemia. A insulina terapia de acción curta pode provocar o inicio da hipoglucemia.
Os síntomas hipoclicémicos non compensados provocan a aparición de precoma, coma ou diabéticos.
Ao cambiar o estado emocional, o desenvolvemento de certas enfermidades, pode ser necesario axustar a dose dun medicamento que conteña insulina.
Cando se traballa con mecanismos precisos, conducir vehículos, aumenta o risco de desenvolver hipoxeclicemia e polo que hai que ter coidado especial.
Interaccións entre drogas
Ao tomar algúns fármacos, pódese rexistrar un efecto no metabolismo da glicosa, en relación con isto, hai que axustar a dosificación de glulisina e controlar estrictamente a condución da terapia antidiabética.
Entre as drogas que aumentan o efecto hipoglucémico da glulisina figuran:
- Inhibidores dunha determinada encima que converte a angiotensina, monoamina oxidasa
- Pentoxifilina
- Fibras Medicamentos
- Medios baseados en axentes antimicrobianos da sulfonamida
- Disopiramidas
- Drogas hipoglicémicas destinadas a uso oral
- Fluoxetina
- Salicilatos
- Propoxifeno.
Destínanse unha serie de medicamentos que reducen significativamente o efecto hipoglucémico dunha solución que contén insulina:
- Isoniazid
- Somatropina
- Danazol
- Algunhas simpatomiméticas
- Medicamentos para estróxenos
- COC
- Diazoxido
- Inhibidores da protease
- Hormonas tiroideas
- Medicamentos antipsicóticos
- GKS
- Derivados de fenotiazina
- Drogas diuréticas.
É de destacar que os bloqueadores β-adrenérxicos, as drogas que conteñen etanol e o litio, a clonidina son capaces de aumentar e diminuír o efecto hipoglucémico de Apidra.
Durante o uso de reserpina, axentes bloqueadores β-adrenérxicos, clonidina e guanetidina, os signos de hipoglucemia poden estar débiles ou ausentes.
Dado que non hai información sobre a compatibilidade farmacéutica da gluzilina, non a mesture con outras drogas, a insulina natural isofan é unha excepción.
No caso de usar unha bomba de infusión para administrar Apidra, non debería ser mestura dunha solución que conteña insulina con outros fármacos.
Efectos secundarios e sobredose
A miúdo, as persoas con diabetes poden desenvolver unha condición tan perigosa como a hipoglucemia.
Nalgúns casos obsérvanse erupcións cutáneas na pel e a aparición de inchazo local.
Non se descarta a aparición de lipodistrofia en caso de incumprimento do réxime prescrito de tratamento antidiabético.
Outras manifestacións alérxicas inclúen:
- Dermatite de xénese alérxica, erupción por tipo de urticaria, asfixia
- Sensación de aperte na zona do peito (bastante rara).
É de notar que as reaccións do sistema inmunitario (manifestacións alérxicas) poden ser niveladas ao día seguinte da inxección. Nalgúns casos, os síntomas negativos non son causados pola exposición á insulina, senón pola irritación da pel como resultado dun tratamento previo á inxección cunha solución antiséptica ou por unha inxección incorrecta.
Cando se diagnostica unha síndrome alérxica xeneralizada, o risco de morte é elevado. Polo tanto, coa menor manifestación de síntomas secundarios, terá que consultar un médico.
Coa introdución de sobredosis de Apidra, a hipoglucemia pode desenvolverse tanto en forma leve como en máis grave. Neste caso, é necesario realizar un tratamento:
- Suave: alimentos ou bebidas que conteñen azucre
- Forma severa (estado inconsciente): para o alto, 1 ml do medicamento Glucagon é administrado baixo a pel ou o músculo, a falta de reacción ao Glucagón, é posible unha solución intravenosa de glicosa.
Despois de que o paciente recupere a conciencia, será necesario proporcionarlle unha comida rica en hidratos de carbono. Posteriormente, recoméndase o seguimento do estado do paciente por parte do médico asistente.
 Eli Lilly and Company, Francia
Eli Lilly and Company, Francia
Prezo de 1602 a 2195 esfregue.
O humalogo é un dos axentes que presentan un pronunciado efecto hipoglucémico. Humalog contén insulina lispro. Baixo a influencia do medicamento, será posible regular o metabolismo da glicosa e mellorar significativamente a síntese de proteínas. Prodúcense medicamentos en forma de solución e suspensión.
Pros:
- Usabilidade
- A aparición dun efecto hipoglicémico rápido
- A probabilidade de desenvolver reaccións adversas graves é baixa.
Contras:
- Non use se se sospeita hipoglucemia.
- Custo elevado
- Pode provocar sudoración excesiva.
Apidra SoloStar, instrucións de uso: método e dosificación
A solución Apidra SoloStar adminístrase s / c 0-15 minutos antes das comidas ou pouco despois das comidas.
O medicamento prescríbese en réximes de tratamento que inclúen insulina de acción media, ou insulina de acción longa, ou un análogo de insulina de acción longa. Apidra SoloStar tamén se pode usar en combinación con axentes hipoglucémicos orais.
O réxime de dosificación debe seleccionarse individualmente.
A introdución da solución Apidra SoloStar pode producirse como inxección sc ou infusión continua na graxa subcutánea coa axuda dun sistema de acción bomba.
Lugares de administración de drogas:
- inxección s / c: na rexión da parede abdominal anterior, coxa ou ombreiro,
- infusión continua: na rexión da parede abdominal anterior.
Con cada nova administración do medicamento, deben alternar os sitios de inxección / infusión indicados. O lugar de administración de Apidra SoloStar, a actividade física e outras condicións cambiantes poden afectar a aparición e duración do medicamento. Cando s / á introdución na parede abdominal, obsérvase unha absorción lixeiramente máis rápida que cando se introduce nas outras áreas do corpo indicadas anteriormente.
Para evitar a entrada de Apidra SoloStar directamente nos vasos sanguíneos, deben observarse as precaucións de seguridade. É imposible facer masaxes na área de administración da droga. Os pacientes deben seguir a técnica de inxección correcta.
A insulina glulisina pódese mesturar co isófano da insulina humana, sendo Apidra SoloStar o primeiro que se atrae á xiringa. A inxección SC debe facerse inmediatamente despois da mestura. Non se poden administrar insulinas mesturadas por vía intravenosa.
Durante infusión continua de sc, Apidra SoloStar non se mestura con outros fármacos, incluídas insulinas ou disolventes.
Se é necesario, pódese extraer o medicamento do cartucho da xeringa e empregarse para a inxección usando un dispositivo de bombeo para a infusión continua de insulina.
O conxunto de infusión e o depósito usado co medicamento deben ser substituídos polo menos cada 48 horas, observando normas asépticas. Estas recomendacións poden diferir das instrucións xerais dos manuais para o uso de dispositivos de bombeo. Non obstante, se non se seguen estas recomendacións especiais, poden producirse eventos adversos graves.
É preciso ter en conta a posibilidade de quebra o dispositivo de bombeo usado, para o que é necesario ter sistemas alternativos para a administración da droga e poder administrar correctamente o axente SC.
Debido a un mal funcionamento do dispositivo bomba, un mal funcionamento do conxunto de infusión ou un erro no seu manexo, é posible o rápido desenvolvemento de hiperglicemia, cetoacidosis diabética e cetose. Nestes casos, a identificación e eliminación rápida das causas destes eventos adversos son necesarias.
Siga as instrucións para o manexo adecuado das xeringas precargadas.
Antes do seu uso, a pluma de xiringa debe manterse a temperatura ambiente durante 1-2 horas (o uso de insulina refrixerada é máis doloroso). Antes da introdución, cómpre inspeccionar o cartucho situado dentro do bolígrafo. No caso de partículas sólidas visibles, así como un cambio na cor e consistencia, Apidro SoloStar non debe empregarse. Despois do uso, debes eliminar a pluma xeringa baleira (prohibida a reutilización).
A pluma de xeringa chea non pode ser transferida a outra persoa, e só debe usala un paciente, o que reduce a probabilidade de infección.
Antes de cada uso, hai que conectarlle unha nova agulla á xeringa. Debería realizarse unha proba de seguridade (o dispositivo e a agulla funcionan ben, elimínanse burbullas de aire). Só se poden usar agullas compatibles.
O dispositivo dispón con precisión de insulina e é seguro para o seu uso. A pluma de xeringa debe estar protexida do po e da sucidade. Pode limpar o exterior limpándoo cun pano húmido. Non mergulla a xeringa en líquido, lubrica e enxágüe.
Ao realizar unha proba de seguridade, mide a dose correspondente a 2 unidades (hai que eliminar os tapóns internos e externos da agulla). A pluma de xeringa colócase coa agulla cara arriba e golpea suavemente cun dedo no cartucho de insulina para que as burbullas de aire se despracen no sentido da agulla. A continuación, prema completamente o botón de inxección de drogas. Se o dispositivo funciona correctamente, aparecerá insulina na punta da agulla.
Despois de completar o exame de seguridade, a xanela de dosificación debería indicar "0". Despois diso, pode establecer a dose requirida.
A dose pódese establecer entre 1 e 80 unidades cunha precisión de 1 unidade. Se precisa introducir unha gran dose, realice dúas ou máis inxeccións.
O médico debe informar ao paciente sobre a técnica de inxección. A agulla debe inserirse baixo a pel. Débese premer completamente o botón de inxección. Mantéñase nesta posición durante outros 10 segundos ata que se retire a agulla. Isto asegura a introdución da dose completa de insulina.
A agulla despois de cada inxección debe eliminarse e eliminarse. Para evitar a contaminación e / ou infección, a entrada de aire no tanque de insulina e as fugas de insulina. Despois de quitar a agulla, pecha a xeringa cun tapón.
A necesidade de insulina ante o fondo da función hepática deteriorada pode diminuír, o que está asociado a unha capacidade reducida de gluconeoxénese e unha desaceleración do metabolismo da insulina.
Con insuficiencia renal, a necesidade de insulina pode diminuír.
En pacientes anciáns con diabetes, a información sobre a farmacocinética é insuficiente. Coa idade, aumenta a probabilidade de deteriorar a función renal, o que pode causar unha diminución dos requirimentos de insulina.
Humulina NPH
 Eli Lilly East S.A., Suíza
Eli Lilly East S.A., Suíza
Prezo de 148 a 1305 esfregue.
Humulin NPH - un medicamento coa sustancia activa insulina-isófano, úsase na diabetes para controlar a glicemia. A Humulina NPH prodúcese en forma de solución en cartuchos que se empregan para unha pluma de xiringa.
Pros:
- Pódese prescribir á embarazada
- Úsase para a primeira diabetes diagnosticada
- A terapia antidiabética a longo prazo está permitida.
Contras:
- Pode causar picazón xeralizada.
- No fondo do tratamento, pódese diagnosticar a frecuencia cardíaca
- É liberado só por receita.
 Novo Nordic, Dinamarca
Novo Nordic, Dinamarca
Prezo de 344 a 1116 rublos.
O LS contén insulina de acción curta. Está prescrito para a diabetes en ausencia de control glicémico doutras drogas. Baixo a influencia de Actrapid, o curso dos procesos intracelulares actívase debido á estimulación específica da biosíntese do cAMP e á rápida penetración nas células musculares. A sustancia activa é insulina soluble. As drogas prodúcense en forma de solución.
Pros:
- Prezo baixo
- Diminución rápida do azucre no sangue
- Pódese usar con insulina de acción longa.
Contras:
- Non se descarta a aparición de signos de lipodistrofia
- Pode desenvolverse edema de Quincke
- Con maior actividade física, requirirase axuste da dose.
Influencia na capacidade para conducir vehículos e mecanismos complexos
Durante o período de tratamento, hai un risco ao conducir. Isto débese á probabilidade de hiperglicemia e hipoglucemia, así como ás perturbacións visuais observadas durante o desenvolvemento destas condicións. Isto é especialmente perigoso para os pacientes debilitados, así como para os pacientes que non presentan síntomas ou teñen episodios frecuentes de hipoglucemia. Para tomar unha decisión sobre a posibilidade / imposibilidade dun paciente para conducir vehículos, estes factores deberían ser avaliados en cada caso. Para evitar a posibilidade de hipoglucemia, aconséllase que os pacientes tomen precaucións durante a condución.
Embarazo e lactación
A experiencia de usar Apidra SoloStar en mulleres embarazadas é insuficiente. Segundo unha cantidade limitada de datos (menos de 300 resultados do embarazo), o fármaco non afecta negativamente nin o curso do embarazo, o desenvolvemento fetal ou o recentemente nado. Nos estudos reprodutivos en animais non se atoparon diferenzas entre insulina glulisina e insulina humana con respecto ao embarazo, desenvolvemento embrionario / fetal, parto e desenvolvemento postnatal.
Apidra SoloStar en mulleres embarazadas debe usarse con precaución co control obrigatorio da concentración de glicosa no sangue e manter o control glicémico.
As mulleres con pre-embarazo ou diabetes gestacional necesitan manter o control glicémico durante todo o período de xestación. A necesidade de insulina durante o primeiro trimestre de embarazo pode diminuír e, durante o segundo e terceiro trimestre, pode aumentar. Inmediatamente despois do parto, prodúcese unha rápida diminución das necesidades de insulina.
Non hai probas que apoien ou neguen que a insulina glulisina se excreta no leite materno. Durante a lactación, pode ser necesario axustar a dieta e o réxime de dosificación de insulina.
Interacción farmacolóxica
Non se realizaron estudos especiais sobre interacción farmacocinética. Con base no coñecemento empírico dispoñible sobre outras drogas similares, crese que é pouco probable o desenvolvemento de interaccións medicamentosas clínicamente significativas. Algunhas substancias / preparados poden afectar o metabolismo da glicosa, neses casos pode ser necesario un axuste da dose de Apidra SoloStar e especialmente un control minucioso do tratamento.
Medicamentos que afectan o efecto hipoglucémico da insulina:
- aumento (incluído un aumento da predisposición á hipoglucemia): inhibidores da enzima de conversión da angiotensina, propoxifeno, axentes hipoglucemicos orais, disopiramida, fluoxetina, fibratos, pentoxifilina, inhibidores da monoamina oxidasa, antimicrobianos da sulfonamida, salicilados,
- diminución: somatropina, glucocorticosteroides, diazoxido, danazol, isoniazido, diuréticos, derivados de fenotiazina, simpatomiméticos, proxestinas, estróxenos, hormonas tiroideas, fármacos antipsicóticos, inhibidores de proteasas.
Outras interaccións posibles:
- clonidina, beta-bloqueantes, alcohol, sales de litio: cando se combinan, é posible potenciar ou debilitar o efecto hipoglucémico da insulina,
- pentamidina: pode producirse unha hipoglucemia con posterior desenvolvemento de hiperglicemia,
- clonidina, beta-bloqueantes, reserpina, guanetidina: cando se combinan con fármacos con actividade simpatolítica, os síntomas da activación adrenérxica reflexa poden ser menos pronunciados ou ausentes.
Non mesture insulina glulisina con outros medicamentos distintos á insulina isofan humana.
No caso da administración coa axuda dunha bomba de infusión, Apidra SoloStar non debe mesturarse con disolventes e outros preparados de insulina.
Os análogos de Apidra SoloStar son: Apidra, Insulin Lyspro, Humalog, Brinsulrapi MK 40 U / ml, Actrapid HM Penfill, etc.
Termos e condicións de almacenamento
Almacenar nun lugar escuro a unha temperatura de 2-8 ºC. Non conxele. Manter fóra do alcance dos nenos.
A vida útil é de 2 anos.
Despois do primeiro uso, a vida útil de Apidra SoloStar nunha xeringa pluma desbotable é de 4 semanas. As plumas de xeringa desbotables despois do seu uso deben gardarse a temperaturas de ata 25 ºC nun lugar protexido da luz e do alcance dos nenos.

 ,
, ,
,