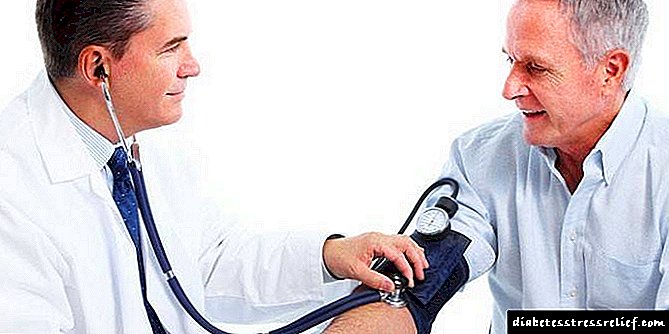
A secuencia de síntese de colesterol no fígado
A transformación do lanosterol en colesterol realízase nas membranas do retículo do hepatocito endoplasmático. Un dobre enlace fórmase na molécula do primeiro composto. Esta reacción consume moita enerxía usando NADPH como doante. Despois da influencia de varias encimas transformadoras sobre o lanosterol, aparece o colesterol.
Transporte Q10
Unha función importante do colesterol tamén é a transferencia Q10. Este composto é o responsable de protexer a membrana dos efectos negativos das enzimas. Un gran número deste composto prodúcese nalgunhas estruturas e só entón entra no torrente sanguíneo. Non ten a capacidade de penetrar de forma independente nas células restantes, polo que para este propósito precisa dun portador. O colesterol afronta con éxito esta tarefa.
Funcións básicas de conexión
Como se mencionou anteriormente, esta sustancia pode ser útil para os humanos, por suposto, só se estamos a falar de HDL.
En base a isto, queda claro que a afirmación de que o colesterol é absolutamente prexudicial para os humanos é un erro.
O colesterol é un compoñente bioloxicamente activo:
- participa na síntese de hormonas sexuais,
- asegura o funcionamento normal dos receptores de serotonina no cerebro,
- é o principal compoñente da bilis, así como a vitamina D, que é a responsable da absorción de graxas,
- impide o proceso de destrución das estruturas intracelulares baixo a influencia de radicais libres.
Pero xunto con propiedades positivas, a sustancia pode ter algún dano para a saúde humana. Por exemplo, a LDL pode provocar o desenvolvemento de enfermidades graves, contribuír principalmente ao desenvolvemento da aterosclerose.
No fígado, o biocomponente sintetízase baixo a influencia da redutase de HMG. Esta é a principal encima implicada na biosíntese. A inhibición da síntese ocorre baixo a influencia da retroalimentación negativa.
O proceso de síntese dunha substancia no fígado ten unha relación inversa coa dose dun composto que entra no corpo humano cos alimentos.
Aínda máis sinxelo, descríbese deste xeito este proceso. O fígado regula de xeito independente os niveis de colesterol. Canto máis unha persoa consome alimentos que conteñan este compoñente, menos substancia se produce nas células do órgano e se temos en conta que as graxas se consumen xunto cos produtos que o conteñen, este proceso regulador é moi importante.
Características da síntese da materia
Os adultos saudables normais sintetizan HDL a unha velocidade de aproximadamente 1 g / día e consumen aproximadamente 0,3 g / día.
 Un nivel relativamente constante de colesterol no sangue ten tal valor - 150-200 mg / dl. Mantido principalmente controlando o nivel de síntese de denovo.
Un nivel relativamente constante de colesterol no sangue ten tal valor - 150-200 mg / dl. Mantido principalmente controlando o nivel de síntese de denovo.
É importante notar que a síntese de HDL e LDL de orixe endóxena está parcialmente regulada pola dieta.
O colesterol, tanto dos alimentos coma no sintetizado no fígado, úsase na formación de membranas, na síntese de hormonas esteroides e ácidos biliares. A maior proporción da sustancia úsase na síntese de ácidos biliares.
A inxestión de HDL e LDL por células mantense a un nivel constante mediante tres mecanismos diferentes:
- Regulación da actividade HMGR
- Regulación do exceso de colesterol libre intracelular a través da actividade de O-aciltransferase esterol, SOAT1 e SOAT2 con SOAT2, que é o compoñente activo predominante no fígado. A designación inicial para estes encimas foi ACAT para acil-CoA: colesterol aciltransferase. Os encimas ACAT, ACAT1 e ACAT2 son acetil CoA acetiltransferases 1 e 2.
- Ao controlar os niveis de colesterol no plasma mediante a captación de receptores mediados por LDL e o transporte inverso mediado por HDL.
A regulación da actividade HMGR é o principal medio para controlar o nivel de biosíntese de LDL e HDL.
O encima está controlado por catro mecanismos diferentes:
- inhibición do feedback,
- control da expresión xénica,
- taxa de degradación da enzima,
- fosforilación-desfosforilación.
Os tres primeiros mecanismos de control actúan directamente sobre a propia sustancia. O colesterol actúa como un inhibidor da retroalimentación de HMGR preexistente e tamén provoca unha rápida degradación do encima. Este último é o resultado da polubiquitinación de HMGR e a súa degradación no proteosoma. Esta capacidade é unha consecuencia do dominio sensible aos esterol de SSD HMGR.
Ademais, cando o colesterol é excesivo, a cantidade de ARNm para HMGR diminúe como resultado da diminución da expresión xénica.
Enzimas implicadas na síntese
 Se o compoñente exóxeno está regulado mediante modificación covalente, este proceso levarase a cabo como resultado da fosforilación e da desfosforilación.
Se o compoñente exóxeno está regulado mediante modificación covalente, este proceso levarase a cabo como resultado da fosforilación e da desfosforilación.
O encima é máis activo en forma non modificada. A fosforilación do encima reduce a súa actividade.
O HMGR está fosforilado pola proteína quinase activada por AMP, AMPK. A propia AMPK está activada por fosforilación.
A fosforilación AMPK está catalizada por polo menos dous encimas, a saber:
- A quinase principal responsable da activación de AMPK é LKB1 (cinasa hepática B1). O LKB1 identificouse por primeira vez como un xene en humanos que levaban unha mutación autosómica dominante na síndrome de Putz-Jegers, PJS. O LKB1 tamén se atopa mutante no adenocarcinoma pulmonar.
- A segunda enzima fosforilante AMPK é a proteína quinase quinasa beta dependente da calodulina (CaMKKβ). O CaMKKβ induce a fosforilación AMPK en resposta a un aumento da Ca2 + intracelular como resultado da contracción muscular.
A regulación de HMGR por modificación covalente permite producir HDL. O HMGR é máis activo no estado desfosforilado. A fosforilación (Ser872) está catalizada pola encima proteína quinase (AMPK) activada por AMP, a actividade da cal tamén está regulada pola fosforilación.
A fosforilación AMPK pode producirse debido a polo menos dous encimas:
A desfosforilación de HMGR, volvéndoa a un estado máis activo, lévase a cabo mediante a actividade das fosfatases proteicas da familia 2A. Esta secuencia permítelle controlar a produción de HDL.
Que afecta o tipo de colesterol?
 PP2A funcional existe en dúas isoformas catalíticas diferentes codificadas por dous xenes identificados como PPP2CA e PPP2CB. As dúas isoformas principais de PP2A son o encima heterodimérica e o holoenzima heterotrimérica.
PP2A funcional existe en dúas isoformas catalíticas diferentes codificadas por dous xenes identificados como PPP2CA e PPP2CB. As dúas isoformas principais de PP2A son o encima heterodimérica e o holoenzima heterotrimérica.
O encima principal PP2A está composto por un sustrato de andamiaxe (chamado orixinalmente subunidade A) e unha subunidade catalítica (subunidade C). A subunidade α catalítica está codificada polo xene PPP2CA, e a subunidade β catalítica está codificada polo xene PPP2CB.
A subestrutura do andamio α está codificada polo xene PPP2R1A e a subunidade β do xene PPP2R1B. O encima principal, PP2A, interactúa cunha subunidade reguladora variable para ensamblarse nun holoenzima.
As subunidades de control PP2A inclúen catro familias (chamadas inicialmente subunidades B), cada unha delas consta de varias isoformas codificadas por xenes diferentes.
Actualmente, hai 15 xenes diferentes para a subunidade reguladora de PP2A B. A función principal das subunidades reguladoras da PP2A é orientar as proteínas do substrato fosforiladas á actividade da fosfatase das subunidades catalíticas de PP2A.
PPP2R é unha das 15 subunidades reguladoras diferentes de PP2A. Hormonas como o glucagón e a adrenalina afectan negativamente á biosíntese do colesterol aumentando a actividade de subunidades reguladoras específicas dos encimas da familia PP2A.
A fosforilación mediada por PKA da subunidade reguladora de PP2A (PPP2R) leva á liberación de PP2A de HMGR, evitando a súa defosforilación. Contrarrestando os efectos da glucagón e da adrenalina, a insulina estimula a eliminación de fosfatos e aumenta así a actividade do HMGR.
A regulación adicional de HMGR prodúcese a través da inhibición da retroalimentación con colesterol, así como a regulación da súa síntese aumentando o nivel de colesterol intracelular e esterol.
Este último fenómeno está asociado ao factor de transcrición SREBP.
Como é o proceso no corpo humano?
 A actividade do HMGR monitorízase adicionalmente mediante unha sinalización con AMP. Un aumento da cAMP activa unha proteína quinasa dependente do cAMP, PKA. No contexto da regulación HMGR, o PKA fosforila a subunidade reguladora, o que leva a un aumento na liberación de PP2A de HMGR. Isto impide que PP2A elimine os fosfatos do HMGR, evitando a súa reactivación.
A actividade do HMGR monitorízase adicionalmente mediante unha sinalización con AMP. Un aumento da cAMP activa unha proteína quinasa dependente do cAMP, PKA. No contexto da regulación HMGR, o PKA fosforila a subunidade reguladora, o que leva a un aumento na liberación de PP2A de HMGR. Isto impide que PP2A elimine os fosfatos do HMGR, evitando a súa reactivación.
Unha gran familia de subunidades proteicas reguladoras da fosfatase regula e / ou inhibe a actividade de numerosas fosfatases, incluídos os membros das familias PP1, PP2A e PP2C. Ademais das fosfatases PP2A que eliminan os fosfatos de AMPK e HMGR, as fosfatases da familia da proteína fosfatase 2C (PP2C) tamén eliminan os fosfatos de AMPK.
Cando estas subunidades reguladoras do fosforilato PKA, a actividade dos fosfatatos unidos diminúe, o que resulta en que AMPK permaneza no estado fosforilado e activo, e HMGR en estado fosforilado e inactivo. A medida que se elimina o estímulo, o que conduce a un aumento da produción de cAMP, o nivel de fosforilación diminúe e o nivel de desfosforilación aumenta. O resultado final é un regreso a un maior nivel de actividade de HMGR. Por outra banda, a insulina conduce a unha diminución do cAMP, que á súa vez activa a síntese. O resultado final é un regreso a un maior nivel de actividade de HMGR.
Por outra banda, a insulina leva a unha diminución do cAMP que, á súa vez, activa a síntese de colesterol. O resultado final é un regreso a un maior nivel de actividade de HMGR. A insulina leva a unha diminución do cAMP, que á súa vez pode usarse para mellorar o proceso de síntese.
A capacidade de estimular a insulina e inhibir o glucagón, a actividade do HMGR é consistente coa influencia destas hormonas noutros procesos metabólicos. A función principal destas dúas hormonas é controlar a accesibilidade e transportar enerxía a todas as células.
O seguimento a longo prazo da actividade de HMGR realízase principalmente controlando a síntese e degradación do encima. Cando os niveis de colesterol son altos, o nivel de expresión xénica de HMGR diminúe e, pola contra, os niveis máis baixos activan a expresión xénica.
A información sobre o colesterol inclúese no vídeo neste artigo.
Cal é a esencia do proceso de produción de moléculas de colesterol?
Moitos alimentos enchen o corpo de colesterol: trátase de produtos de orixe animal, así como graxas trans que se atopan en grandes cantidades en alimentos procesados, así como en alimentos rápidos (comida rápida).
Se usas estes produtos inmensamente, entón a concentración de moléculas de colesterol no sangue converterase en alta e terás que recorrer a unha solución médica para a hipercolesterolemia.
O colesterol, que entra no corpo cos alimentos, ten unha baixa densidade molecular, o que conduce á deposición de tal colesterol nas cunchas internas dos vasos sanguíneos, o que provoca o desenvolvemento da placa de colesterol e a patoloxía da aterosclerose.
Un aumento do índice de colesterol no sangue prodúcese non só porque se obtén do exterior, senón tamén por unha violación no proceso de síntese de moléculas de lipoproteínas polas células do fígado.
 Síntese de colesterol aos contidos ↑
Síntese de colesterol aos contidos ↑
Síntese do colesterol no fígado
A síntese de colesterol no corpo é de aproximadamente 0,50-0,80 gramos por día.
A síntese de moléculas de colesterol no corpo distribúese:
- O 50,0% é producido por células do fígado,
- 15,0% - 20,0% - polos departamentos do intestino delgado,
- 10,0% - sintetízase pola córtex suprarrenal e as células da pel.
Todas as células do corpo humano teñen a capacidade de sintetizar lipoproteínas.
Con comida, ata o 20,0% da molécula de colesterol total entra no corpo - aproximadamente 0,40 gramos ao día.
As lipoproteínas son excretadas fóra do corpo coa axuda do ácido biliar, e por día a utilización de moléculas de colesterol por bile non supera os 1,0 gramos.
A biosíntese de lipoproteínas no corpo
A biosíntese das moléculas lipídicas prodúcese no departamento endoplasmático - o retículo. A base para todos os átomos das moléculas de carbono é a sustancia acetil-SCoA, que entra no endoplasma das mitocondrias nas moléculas de citrato.
Durante a biosíntese de moléculas de lipoproteínas, participan 18 moléculas de ATP e 13 moléculas NADPH fanse participantes na síntese.
O proceso de formación do colesterol atravesa polo menos 30 etapas e reaccións no corpo.
A síntese por fases de lipoproteínas pódese dividir en grupos:
inserir aviso activo - nivel de azucre
- A síntese do ácido mevalónico prodúcese durante a cetoxénese das dúas primeiras reaccións e despois da terceira etapa, 3-hidroxi-3-metilglutaril-ScoA reacciona coa molécula reductasa de HMG-ScoA. A partir desta reacción, sintetízase Mevalonate. Esta reacción require unha cantidade suficiente de glicosa no sangue. Podes compensar con a axuda de doces e cereais,
- A síntese de isopentenil difosfato prodúcese despois da adición de fosfato ás moléculas de ácido mevalónico e a súa deshidratación,
- A síntese do difosfato de farnesilo prodúcese despois da combinación de tres moléculas de isopentenil difosfato,
- A síntese de squalene é a unión de 2 moléculas de difosfato de farnesil,
- A reacción da transición do squaleno á molécula de lanosterol prodúcese,
- Despois da eliminación de grupos metilo innecesarios, o colesterol convértese.


Regulación da síntese de lipoproteínas
O elemento regulador no proceso de síntese é a encima hidroximetilglutarilo-ScoA reductasa. A capacidade deste encima para cambiar a actividade é máis de 100 veces.
A regulación da actividade encimática prodúcese segundo varios principios:
- Regulación da síntese a nivel metabólico. Este principio funciona "do contrario", o encima é inhibido polo colesterol, o que permite manter un contido intracelular constante,
- Regulación hormonal covalente.
A regulación a nivel hormonal prodúcese nas seguintes etapas:
- Un aumento da hormona insulina no corpo activa a proteína fosfatase, o que provoca un aumento da actividade do encima principal HMG-ScoA reductasa,
- A hormona glucagona e a hormona adrenalina teñen a capacidade de activar o elemento da proteína quinase A, que fosforila o encima HMG-ScoA reductasa e reduce a súa actividade,
- A actividade de síntese de colesterol depende da concentración dunha proteína transportadora especial no sangue, que une en tempo e cando as reaccións intermedias dos metabolitos.
Colesterol corporal
O colesterol sintetizado nas células do fígado é necesario para o corpo para diversos procesos vitais:
- Situadas en cada membrana celular, as moléculas de colesterol fortalécenas e fan que sexan elásticas,
- Coa axuda de lipoproteínas, as células coroides aumentan a súa permeabilidade, que as protexe de influencias externas,
- Sen axuda de lipoproteínas, as glándulas suprarrenais non producen o tipo de esteroides das hormonas sexuais,
- Usando lípidos, prodúcese ácido biliar e impide que a vesícula se forme pedra na mesma,
- As lipoproteínas únense ás células neuronais na medular e no cerebro,
- Coa axuda de lipoproteínas, consolídase a funda das fibras nerviosas,
- Coa axuda do colesterol prodúcese vitamina D, que axuda a absorber o calcio e evita a destrución do tecido óseo.
O colesterol axuda ás glándulas suprarrenais a sintetizar estes grupos de hormonas:
- Grupo corticoides
- Grupo de hormonas glucocorticoides,
- Grupo de mineralocorticoides.
 O colesterol axuda a producir a síntese suprarrenal de grupos hormonais
O colesterol axuda a producir a síntese suprarrenal de grupos hormonaisEstas hormonas fornecen os procesos de regulación hormonal dos órganos reprodutores humanos.
As moléculas de colesterol despois da síntese nas células do fígado entran no órgano endocrino da glándula suprarrenal e contribúen á produción de hormonas e a manter o equilibrio na esfera hormonal.
Metabolismo das moléculas de vitamina D no corpo
A produción de moléculas de vitamina D vén da luz solar, que penetra no colesterol baixo a pel. Neste momento prodúcese a síntese de vitamina D, que é moi importante para o corpo para absorber minerais de calcio.
Todos os tipos de lipoproteínas, tras a síntese, son transportados polo corpo polo sistema sanguíneo.
A vitamina D pódese converter só en lipoproteínas de alta densidade molecular e os lípidos de baixo peso molecular provocan o desenvolvemento da patoloxía da aterosclerose, porque teñen a capacidade de establecerse nas membranas internas das arterias en forma de placas de colesterol, que crecen e provocan esta patoloxía.
Ás veces pódense observar placas de colesterol en humanos baixo a pel das mans.
 Metabolismo vitamina D aos contidos ↑
Metabolismo vitamina D aos contidos ↑
Disturbios na síntese de lipoproteínas
En moitos procesos metabólicos no corpo, poden producirse fallos e interrupcións. Tales trastornos poden producirse no metabolismo dos lípidos. Hai moitas razóns e teñen unha etioloxía exóxena e endóxena.
As causas endóxenas de trastornos de síntese de lipoproteínas inclúen:
- A idade dunha persoa. Despois de 40 anos no corpo humano, a produción de hormonas sexuais atenúase e o fondo hormonal perturba, e entre os 45 e os 50 anos, todos os procesos metabólicos se ralentizan, o que tamén pode provocar unha ruptura no metabolismo dos lípidos,
- Xénero - Os homes son máis propensos á acumulación de colesterol que as mulleres. As mulleres antes da menopausa e a menopausa están protexidas pola produción de hormonas sexuais, da acumulación de lipoproteínas,
- Predisposición hereditaria xenética. O desenvolvemento da hipercolesterolemia familiar.
As causas exóxenas de fracaso de lípidos inclúen factores que dependen do estilo de vida do paciente, así como patoloxías asociadas que contribúen a unha violación na síntese de moléculas de colesterol:
- Adicción á nicotina,
- Dependencia crónica de alcol,
- Unha alimentación inadecuada pode levar ao aumento do colesterol no corpo e a súa acumulación non só no sangue,
- Un estilo de vida sedentario causa procesos metabólicos retrasados e síntese de lipoproteínas,
- Hipertensión arterial: a alta presión no torrente sanguíneo dá requisitos previos para que as membranas vasculares estean saturadas con graxas lipídicas, que posteriormente forman unha placa de colesterol,
- A dislipidemia é un trastorno no metabolismo dos lípidos. Con patoloxía, prodúcese un desequilibrio entre lipoproteínas VP, lípidos NP, así como o nivel de triglicéridos no sangue,
- Patoloxía obesidade,
- Diabetes mellitus. Con hiperglucemia, o metabolismo e o metabolismo dos lípidos son perturbados.
 Patoloxía obesidadeaos contidos ↑
Patoloxía obesidadeaos contidos ↑Deficiencia no corpo de moléculas beneficiosas de colesterol
Existen patoloxías que reducen a concentración de colesterol de alto peso molecular no sangue debido á diminución da síntese de moléculas de HDL.
Isto pode levar a patoloxías na glándula tiroide, pode afectar significativamente o nivel de azucre no sangue e provocar diabete, así como causar moitas enfermidades do torrente sanguíneo e órgano cardíaco.
As consecuencias dunha baixa concentración de colesterol de alto peso molecular poden ser:
- A patoloxía do raquitismo, que se desenvolve na infancia debido á síntese reducida de vitamina D e á dixestibilidade das moléculas de calcio,
- Envellecemento precoz das células do corpo. Sen o subministro oportuno de colesterol ás membranas celulares, destrúense e comeza o proceso de envellecemento,
- Unha forte diminución do peso corporal, debido á síntese insuficiente de moléculas de colesterol e ao metabolismo lipídico deteriorado,
- Dores no tecido muscular por falta de células do músculo lipídico,
- Dor no órgano cardíaco que pode desencadear un ataque cardíaco.
Pode corrixir o índice de colesterol de alto peso molecular mediante nutrición dietética, que inclúe peixes de mar, varios aceites vexetais, así como produtos lácteos.
E non te esquezas de froitas frescas, herbas e verduras - deberían prevalecer na dieta.