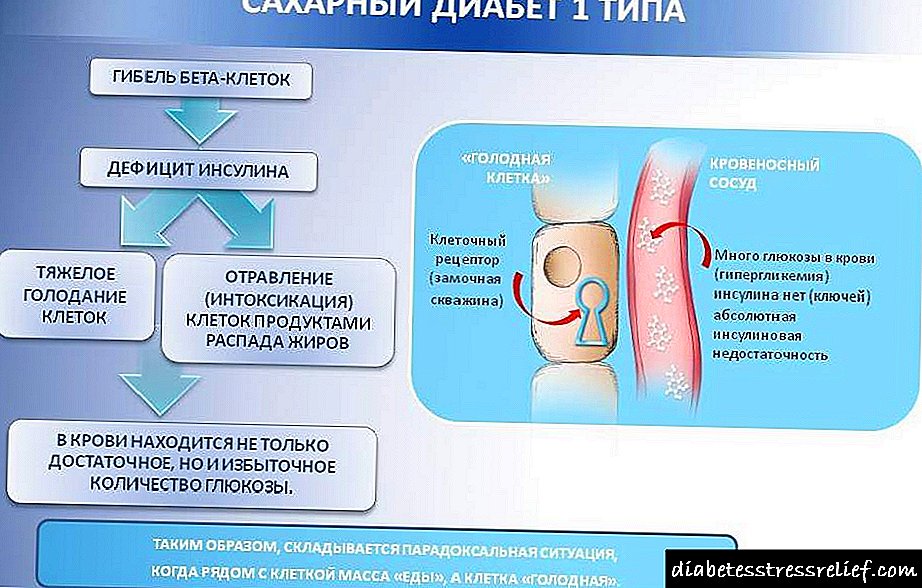
Síntomas da diabetes

A amiotrofia diabética é unha debilidade muscular que conduce a danos nas terminacións nerviosas da medula espiñal. Neste caso, o paciente comeza dores fortes nas pernas, que non son eliminadas polos analxésicos habituais, unha extremidade diminúe de volume. Pode ser difícil para os médicos facer un diagnóstico correcto, xa que a patoloxía ocorre só no 1% dos pacientes con diabetes mellitus, e os seus síntomas son similares ao inchazo, a osteocondrose e outros.
Lea este artigo
Artigos expertos médicos
Os síntomas da diabetes aparecen de dúas formas. Isto é debido á deficiencia aguda ou crónica de insulina, que á súa vez pode ser absoluta ou relativa. A deficiencia aguda de insulina provoca un estado de descompensación de hidratos de carbono e outros tipos de metabolismo, acompañado de hiperglicemia clínicamente significativa, glucosuria, poliuria, polidipsia, perda de peso por hiperfagia, cetoacidosis, ata un coma diabético. A deficiencia crónica de insulina en presenza de diabetes mellitus subcompensado e compensado periódicamente vén acompañada de manifestacións clínicas caracterizadas como "síndrome diabético tardío" (retino-, neuro- e nefropatias diabéticas), que se basean en microangiopatías diabéticas e trastornos metabólicos típicos do curso crónico da enfermidade. .
O mecanismo para o desenvolvemento de manifestacións clínicas de deficiencia aguda de insulina inclúe metabolismo de carbohidratos, proteínas e graxas alteradas, que causan hiperglicemia, hiperaminocidemia, hiperlipidemia e cetoacidosis. A deficiencia de insulina estimula a gluconeoxénese e a glicoxenólise e tamén inhibe a glicogénese hepática. Os carbohidratos dos alimentos (glicosa), en menor medida que nos saudables, metabolízanse no fígado e nos tecidos dependentes da insulina. A estimulación da glucoxénese por glucagón (con deficiencia de insulina) leva ao uso de aminoácidos (alanina) para a síntese de glicosa no fígado. A fonte de aminoácidos é a proteína tisular que está a aumentar a caries. Dado que o aminoácido alanina se usa no proceso de gluconeoxénese, o contido de aminoácidos en cadea ramificada (valina, leucina, isoleucina) no sangue aumenta, a utilización do tecido muscular para a síntese de proteínas tamén se reduce. Así, os pacientes desenvolven hiperglicemia e aminocidemia. O aumento do consumo de proteínas e aminoácidos dos tecidos vai acompañado dun saldo negativo de nitróxeno e é un dos motivos para perder peso nos pacientes, e unha hiperglicemia significativa é causada pola glucosuria e pola poliuria (como resultado da diurese osmótica). A perda de fluído na orina, que pode chegar a 3-6 l / día, provoca deshidratación intracelular e polidipsia. Cun descenso no volume sanguíneo intravascular, a presión arterial diminúe e o hematocrito aumenta. En condicións de deficiencia de insulina, os principais substratos enerxéticos do tecido muscular son os ácidos graxos libres, que se forman no tecido adiposo como resultado do aumento da lipólise: hidrólise dos triglicéridos (TG). A súa estimulación como resultado da activación da lipase sensible ás hormonas provoca un aumento da inxestión de FFA e glicerol no torrente sanguíneo e no fígado. Os primeiros, oxidados no fígado, serven como fonte de corpos cetonas (ácidos beta-hidroxibutíricos e acetoacéticos, acetona), que se acumulan no sangue (parcialmente utilizados polos músculos e as células do sistema nervioso central), contribuíndo á cetoacidosis, unha diminución do pH e da hipoxia tisular.Parcialmente as FFA no fígado úsanse para a síntese de TGs, que provocan infiltración hepática graxa, e tamén entran no torrente sanguíneo, o que explica a hipergliceridemia frecuentemente observada en pacientes e o aumento da FFA (hiperlipidemia).
A progresión e o aumento da cetoacidosis aumentan a deshidratación dos tecidos, a hipovolemia, a concentración de sangue con tendencia ao desenvolvemento da síndrome de coagulación intravascular diseminada, mal suministro de sangue, hipoxia e edema da córtex cerebral e o desenvolvemento de coma diabético. Unha forte diminución do fluxo sanguíneo renal pode causar necrose dos túbulos renais e anuria irreversible.
As características do curso da diabetes, así como as súas manifestacións clínicas, dependen en boa medida do seu tipo.
A diabetes tipo I, por regra xeral, maniféstase por síntomas clínicos graves, que reflicten a deficiencia característica de insulina no corpo. A aparición da enfermidade caracterízase por importantes trastornos metabólicos que provocan manifestacións clínicas de descompensación de diabetes mellitus (polidipsia, poliuria, perda de peso, cetoacidosis), que se desenvolven ao longo de varios meses ou días. Moitas veces a enfermidade maniféstase primeiro por un coma diabético ou por acidosis grave. Despois de realizar medidas terapéuticas, incluída a gran maioría dos casos, insulinoterapia e compensar a diabetes, obsérvase unha mellora no curso da enfermidade. Así, en pacientes, incluso despois de sufrir coma diabético, a necesidade diaria de insulina diminúe gradualmente, ás veces incluso ata que se cancela por completo. En moitos pacientes obsérvase un aumento da tolerancia á glicosa, que conduce á posibilidade de interromper a terapia coa insulina despois de eliminar os trastornos metabólicos pronunciados característicos do período inicial da enfermidade. A literatura describe casos bastante frecuentes de recuperación temporal de tales pacientes. Non obstante, ao cabo duns meses, e ás veces despois dos 2-3 anos, a enfermidade recurriu (especialmente no fondo dunha infección viral), e a terapia con insulina fíxose necesaria ao longo da vida. Este patrón fíxose notar desde hai moito tempo na literatura estranxeira chamada "lúa de mel de diabéticos", cando hai unha remisión da enfermidade e a ausencia da necesidade de insulinoterapia. A súa duración depende de dous factores: o grao de dano ás células beta do páncreas e a súa capacidade para rexenerarse. Dependendo do predominio dun destes factores, a enfermidade pode asumir inmediatamente a natureza da diabetes clínica ou se producirá unha remisión. A duración da remisión tamén está influenciada por factores externos como a frecuencia e a gravidade das infeccións virais concomitantes. Observamos pacientes nos que a duración da remisión alcanzou os 2-3 anos no contexto da ausencia de infeccións virais e intercurrentes. Ademais, non só o perfil glicémico, senón tamén os índices de test de tolerancia á glicosa (GTT) en pacientes non representaron desviacións da norma. Cómpre salientar que en varios traballos, os casos de remisión espontánea da diabetes foron considerados como o resultado do efecto terapéutico de drogas de azucre ou biguanidas de sulfonamida, mentres que outros autores atribuíron este efecto á terapia dietética.
Despois do inicio da diabetes clínica persistente, a enfermidade caracterízase por unha pequena necesidade de insulina, que aumenta durante 1-2 anos e permanece estable. O curso clínico no futuro depende da secreción residual de insulina, que pode variar significativamente dentro dos valores subnormais do péptido C. Cunha secreción residual moi baixa de insulina endóxena, obsérvase un curso lábil de diabetes con tendencia á hipoglucemia e á cetoacidosis, debido á alta dependencia dos procesos metabólicos da insulina administrada, a natureza da nutrición, o estrés e outras situacións.A maior secreción de insulina residual proporciona un curso de diabetes máis estable e unha menor necesidade de insulina exóxena (a falta de resistencia á insulina).
Ás veces o diabete mellitus tipo I combínase con enfermidades endocrinas autoinmunes e non endocrinas, que é unha das manifestacións da síndrome poliendocrina autoinmune. Dado que a síndrome poliendocrina autoinmune pode incluír danos na córtex suprarrenal, cunha diminución da presión arterial, é preciso aclarar o seu estado funcional para poder adoptar medidas adecuadas.
A medida que a duración da enfermidade aumenta (despois de 10-20 anos), as manifestacións clínicas da síndrome diabética tardía aparecen en forma de retino e nefropatía, que progresan máis lentamente cunha boa compensación da diabetes. A principal causa de morte é a insuficiencia renal e, máis raramente, as complicacións de aterosclerose.
En termos de severidade, a diabetes tipo I divídese en formas moderadas e graves. A severidade moderada caracterízase pola necesidade dunha terapia de substitución de insulina (independentemente da dose) para diabetes mellitus sen complicación ou pola presenza de retinopatía de estadios I, II, nefropatía en estadio I, neuropatía periférica sen dor grave e úlceras tróficas. En gran medida, diabetes con deficiencia de insulina en combinación con retinopatía das etapas II e III ou nefropatía das etapas II e III, neuropatía periférica con dor severa ou úlceras tróficas, cegueira neurodistrófica, difícil de tratar, encefalopatía, manifestacións graves de neuropatía autonómica, pendente, coma, curso lábil da enfermidade. En presenza de manifestacións de microangiopatía enumeradas, non se ten en conta a necesidade de insulina e o nivel de glicemia.
O curso clínico de diabetes mellitus tipo II (non dependente da insulina) caracterízase polo seu inicio gradual, sen signos de descompensación. Os pacientes adoitan recorrer a un dermatólogo, xinecólogo, neuropatólogo sobre enfermidades fúngicas, furunculose, epidermofitosis, picazón na vaxina, dor nas pernas, enfermidade periodontal e deficiencia visual. Ao examinar tales pacientes, detéctase diabetes. Moitas veces, por primeira vez, faise un diagnóstico de diabetes durante un infarto de miocardio ou un ictus. Ás veces a enfermidade debuta cun coma hiperosmolar. Debido ao inicio da enfermidade imperceptible na maioría dos pacientes, a determinación da súa duración é moi difícil. Isto, posiblemente, explica a aparición relativamente rápida (despois de 5-8 anos) de signos clínicos de retinopatía ou a súa detección incluso durante o diagnóstico inicial da diabetes. O curso da diabetes tipo II é estable, sen tendencia á cetoacidosis e condicións hipoglucémicas no contexto de usar só unha dieta ou en combinación con medicamentos orais que reducen o azucre. Dado que a diabetes deste tipo adoita desenvolverse en pacientes maiores de 40 anos, obsérvase a súa frecuente combinación con aterosclerose, que ten unha tendencia ao progreso rápido debido á presenza de factores de risco en forma de hiperinsulinemia e hipertensión. As complicacións da aterosclerose adoitan ser as causas da morte nesta categoría de pacientes con diabetes mellitus. A nefropatía diabética desenvólvese con moita menos frecuencia que en pacientes con diabetes tipo I.
A diabetes mellitus tipo II segundo a gravidade divídese en 3 formas: leve, moderada e grave. A forma leve caracterízase pola capacidade de compensar a dieta só con diabetes. Probablemente a súa combinación con retinopatía en estadio I, nefropatía en fase I, neuropatía transitoria. Para a diabetes moderada, é típica a compensación pola enfermidade con medicamentos orais que diminúen o azucre.Quizais unha combinación con retinopatía das etapas I e II, nefropatía do estadio I, neuropatía transitoria. En casos graves, a compensación da enfermidade conséguese con fármacos que baixan o azucre ou a administración periódica de insulina. Nesta fase obsérvanse retinopatías en fase III, nefropatía en fase II e III, manifestacións graves de neuropatía periférica ou autonómica, encefalopatía. Ás veces diagnostícase unha forma grave de diabetes en pacientes compensados por unha dieta, en presenza das manifestacións anteriores de microangiopatía e neuropatía.
A neuropatía diabética é unha manifestación clínica característica da diabetes mellitus, observada no 12-70% dos pacientes. A súa frecuencia entre os pacientes aumenta significativamente despois de 5 anos ou máis da existencia de diabetes mellitus, independentemente do seu tipo. Non obstante, a correlación da neuropatía coa duración da diabetes non é absoluta, polo que existe a opinión de que a natureza da compensación por diabetes mellitus está máis influída pola frecuencia da neuropatía, independentemente da súa gravidade e duración. A falta de datos claros na literatura sobre a prevalencia da neuropatía diabética débese en gran parte a información insuficiente sobre as súas manifestacións subclínicas. A neuropatía diabética inclúe varias síndromes clínicas: radiculopatía, mononeuropatía, polineuropatía, amiotrofia, neuropatía autonómica e encefalopatía.
A radiculopatía é unha forma bastante rara de neuropatía periférica somática, que se caracteriza por dores de tiro agudas dentro do mesmo dermatoma. Esta patoloxía baséase na desmielinización dos cilindros axiais nas raíces posteriores e nas columnas da medula espiñal, que se acompaña dunha violación da sensibilidade muscular profunda, desaparición dos reflexos do tendón, ataxia e inestabilidade na posición de Romberg. Nalgúns casos, o cadro clínico da radiculopatía pódese combinar con alumnos desiguales, considerados como pseudotabes diabéticos. A radiculopatía diabética debe diferenciarse da osteocondrose e a espondilose deformante da columna vertebral.
A mononeuropatía é o resultado de danos nos nervios periféricos individuais, incluídos os nervios craniais. Son características dores espontáneas, paresis, trastornos de sensibilidade, diminución e perda de reflexos do tendón na zona do nervio afectado. O proceso patolóxico pode danar os troncos nerviosos dos pares de nervios craniais III, V, VI-VIII. Significativamente máis frecuentemente que outros, os pares III e VI son afectados: aproximadamente o 1% dos pacientes con diabetes mellitus teñen parálise extraocular muscular, que se combina coa dor na parte superior da cabeza, diplopia e ptose. A derrota do nervio trigeminal (par V) maniféstase por ataques de dor intensa na metade da cara. A patoloxía do nervio facial (par VII) caracterízase por unha paresis unilateral dos músculos faciais e unha perda de audición par VIII. A mononeuropatía detéctase tanto no contexto da diabetes mellitus que existe desde hai tempo coma na tolerancia á glicosa deteriorada.
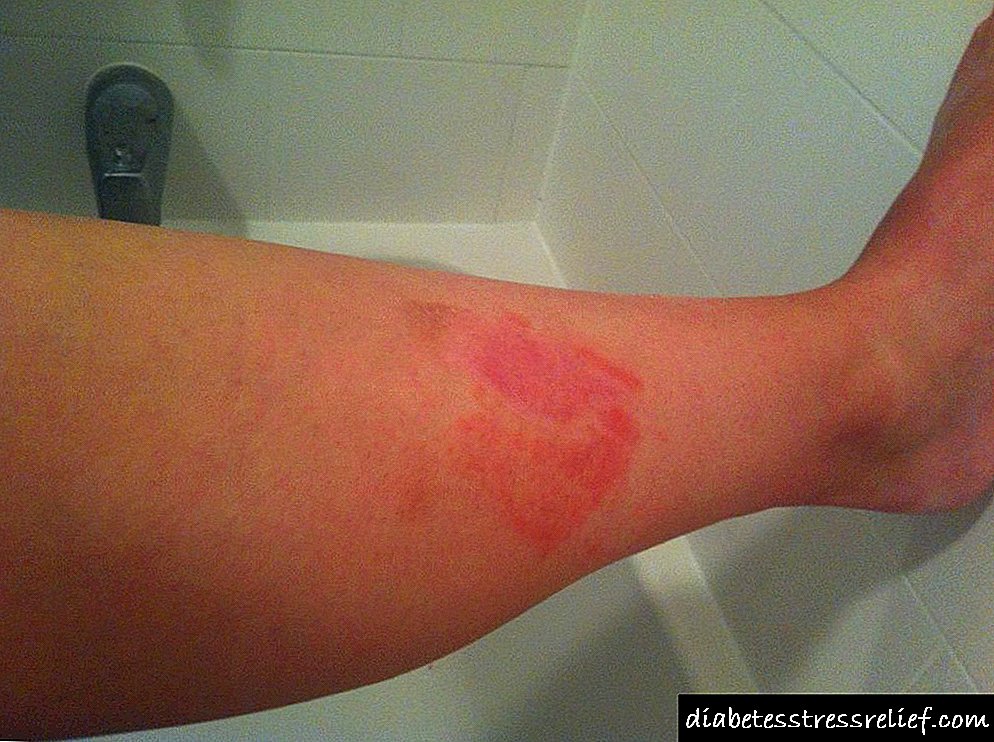
A polineuropatía é a forma máis común de neiroopatía diabética periférica somática, que se caracteriza por trastornos distais, simétricos e predominantemente sensibles. Estes últimos obsérvanse en forma de "síndrome de medias e luvas", e esta patoloxía é moito máis cedo e máis pesada nas pernas. Unha diminución característica da sensibilidade vibracional, táctil, da dor e da temperatura, diminución e perda de Aquiles e reflexos do xeonllo. A derrota das extremidades superiores é menos común e correlaciona coa duración da diabetes. Sensacións subxectivas en forma de parestesia e dor nocturna intensa poden preceder a aparición de signos obxectivos de trastornos neurolóxicos.A dor e hiperalgesia graves, agravadas durante a noite, provocan insomnio, depresión, perda de apetito e, en casos graves, unha diminución significativa do peso corporal. En 1974, M. Ellenberg describiu a "cachéxia polineuropática diabética". Esta síndrome desenvólvese principalmente en homes maiores e combínase con dor intensa con anorexia e perda de peso, alcanzando o 60% do peso corporal total. Non se observou correlación coa gravidade e tipo de diabetes. Na literatura doméstica publicouse un caso similar á enfermidade nunha muller anciá con diabetes tipo II. A polineuropatía distal adoita causar trastornos tróficos en forma de hiperhidrose ou anhidrose, adelgazamento da pel, perda de cabelo e úlceras moito menos tróficas, principalmente nos pés (úlceras neurotróficas). O seu trazo característico é a preservación do fluxo sanguíneo arterial nos vasos das extremidades inferiores. As manifestacións clínicas de neuropatía distal somática diabética normalmente invólvense baixo a influencia do tratamento por períodos que van desde varios meses ata un ano.
A neuroartropatía é unha complicación bastante rara da polineuropatía obstructiva e caracterízase por destruír progresivamente unha ou varias articulacións do pé ("pé diabético"). Este síndrome foi descrito por primeira vez en 1868 polo neuropatólogo francés Charcot nun paciente con sífilis terciaria. Esta complicación obsérvase en moitas condicións, pero a maioría das veces en pacientes con diabetes mellitus. A prevalencia de neuropatía é de aproximadamente 1 caso por 680-1000 pacientes. Significativamente máis a miúdo, a síndrome de "pé diabético" desenvólvese ante o fondo da diabetes mellitus a longo prazo (máis de 15 anos) e principalmente nas persoas maiores. O 60% dos pacientes presentan unha lesión das articulacións tarsal e tarsal-metatarsiana, o 30% das articulacións metatarsofalangeas e o 10% dos nocellos. Na maioría dos casos, o proceso é unilateral e só no 20% dos pacientes é bilateral. Aparecen flaqueza, hiperemia da zona das articulacións correspondentes, deformación do pé, articulación do nocello, úlceras tróficas da sola a falta de síndrome de dor practicamente. A identificación do cadro clínico da enfermidade é frecuentemente precedida de lesións, estiramento dos tendóns, formación de cornos con ulceración posterior en 4-6 semanas e unha fractura do terzo inferior da perna con danos nas articulacións do nocello. A destrución ósea masiva con secuestro e resorción de tecido óseo, violación grave de superficies articulares e cambios hipertróficos periarticulares en tecidos brandos, esclerose subcondral, formación de osteófitos, fracturas intraarticulares son reveladas radioloxicamente. A miúdo o proceso destrutivo radiolóxico non está acompañado de síntomas clínicos. Na patoxénese da neuroartropatía nos anciáns, ademais da polineuropatía, intervén o factor de isquemia debido ao dano na microvasculatura e nos principais vasos. Xuntar a infección pode estar acompañado de flemón e osteomielite.
, , , , , , , , , , , ,
Neuropatía diabética

Neuropatía diabética - danos específicos no sistema nervioso periférico debido a procesos dismetabólicos na diabetes mellitus.
A neuropatía diabética maniféstase por unha violación da sensibilidade (parestesia, entumecemento das extremidades), disfunción autonómica (taquicardia, hipotensión, disfagia, diarrea, anhidrose), trastornos xenitourinarios, etc.
Con neuropatía diabética, faise un exame do funcionamento dos sistemas endocrinos, nerviosos, cardíacos, dixestivos e urinarios. O tratamento inclúe insulinoterapia, o uso de medicamentos neurotrópicos, antioxidantes, o nomeamento de terapia sintomática, acupuntura, FTL, terapia de exercicios.
A neuropatía diabética é unha das complicacións máis comúns da diabetes detectada nun 30-50% dos pacientes. Dise que a neuropatía diabética está presente en signos de danos nos nervios periféricos en persoas con diabetes, coa exclusión doutras causas de disfunción do sistema nervioso.
A neuropatía diabética caracterízase por unha condución nerviosa deteriorada, sensibilidade, trastornos do sistema nervioso somático e / ou autónomo.
Debido á multiplicidade das manifestacións clínicas, a neuropatía diabética enfróntase a especialistas no campo da endocrinoloxía, neuroloxía, gastroenteroloxía e podoloxía.
Manifestacións clínicas do pé neuroartropático e isquémico
Boa pulsación dos vasos sanguíneos
Tecido normal do pé
Cornos espremidos
Diminución ou ausente do reflexo de Aquiles
A tendencia ao pé "martelo"
"Caída de pé" (paso de paso)
Quirroartropatía (cheir grega - man)
Atrofia de tecidos brandos
Delgado e seco
Reflexo normal de Aquiles
Blanqueamento dos pés cando se erguen deitados
Outra manifestación da neuroartropatía é a cheuropatía diabética (neuroartropatía), cuxa prevalencia é do 15 ao 20% en pacientes con diabetes mellitus tipo 1 cunha duración de 10 a 20 anos. O primeiro signo da síndrome é un cambio na pel das mans. Faise seco, ceroso, compactado e espesado. Entón faise difícil e imposible estender o dedo pequeno e, posteriormente, outros dedos debido a un dano nas articulacións. A neuroartropatía normalmente precede á aparición de complicacións crónicas da diabetes mellitus (retinopatía, nefropatía). O risco destas complicacións en presenza de neuroartropatías aumenta 4-8 veces.
Amiotrofia - Unha forma rara de neuropatía diabética. A síndrome caracterízase por debilidade e atrofia dos músculos da cintura pélvica, dor muscular, diminución e perda de reflexos no xeonllo, deterioración da sensibilidade na zona do nervio femural, fasciculacións individuais. O proceso comeza asimétricamente e logo faise bilateral e prodúcese con máis frecuencia en homes maiores con diabetes leve. A electromiografía detéctase a patoloxía muscular primaria e o dano nervioso. Unha biopsia muscular pode detectar a atrofia das fibras musculares individuais, a preservación da estriación transversal, a ausencia de cambios inflamatorios e necróticos, a acumulación de núcleos baixo o sarcolemma. Obsérvase un patrón similar de biopsia muscular con miopatía alcohólica. A amiotrofia diabética debe diferenciarse da polimiosite, a esclerose lateral amiotrófica, a miopatía tirotóxica e outras miopatías. O prognóstico da amotrofia diabética é favorable: normalmente despois de 1-2 anos ou antes, prodúcese a recuperación.
O sistema nervioso autónomo regula a actividade dos músculos lisos, glándulas endocrinas, corazón e vasos sanguíneos. A violación da inervación parasimpática e simpática é a base dos cambios na función dos órganos internos e do sistema cardiovascular. No 30-70% dos casos obsérvanse manifestacións clínicas de neuropatía autónoma, dependendo da poboación examinada de pacientes con diabetes mellitus. A patoloxía gastrointestinal inclúe a disfunción do esófago, estómago, duodeno e intestinos. A violación da función do esófago exprésase nunha diminución da súa peristalsis, expansión e diminución do ton do esfínter inferior. Clínicamente, os pacientes presentan disfagia, azia e ocasionalmente - ulceración do esófago. A gastropatía diabética obsérvase en pacientes cunha longa duración da enfermidade e maniféstase por vómitos de alimentos comidos o día anterior. Os raios X detectan unha diminución e paresis de peristalsis, expansión do estómago, retardando o seu baleiro. No 25% dos pacientes, detéctase a expansión e diminución do ton do duodeno e o seu bulbo. A secreción e acidez do zume gástrico é reducido.Nos exemplares de biopsia do estómago detéctanse signos de microangiopatía diabética, que se combinan coa presenza de retino- e neuropatía diabética. A enteropatía diabética maniféstase por un aumento da peristalsis do intestino delgado e unha diarrea que ocorre periodicamente, a miúdo pola noite (a frecuencia dos movementos intestinais chega ás 20-30 veces ao día). A diarrea diabética non adoita ir acompañada de perda de peso. Non hai correlación co tipo de diabetes e a súa gravidade. En exemplares de biopsia da membrana mucosa do intestino delgado non se detectaron cambios inflamatorios e outros. O diagnóstico é difícil debido á necesidade de diferenciarse da enterite de diversas etioloxías, síndromes de malabsorción, etc.
Neuropatía da vexiga (atonía) caracterizada por unha diminución da súa contractilidade en forma de ralentizar a micción, reducíndoa a 1-2 veces ao día, a presenza de ouriños residuais na vexiga, o que contribúe á súa infección. O diagnóstico diferencial inclúe hipertrofia prostática, presenza de tumores na cavidade abdominal, ascites, esclerose múltiple.
Impotencia - Un frecuente signo de neuropatía autónoma e pode ser a súa única manifestación observada no 40-50% dos pacientes con diabetes mellitus. Pode ser temporal, por exemplo, coa descompensación da diabetes, pero despois será permanente. Hai unha diminución da libido, unha reacción inadecuada, un debilitamento do orgasmo. A infertilidade nun home con diabetes pode asociarse a unha exaculación retrógrada, cando a debilidade do esfínter da vexiga leva a que o esperma se lance a ela. En pacientes con diabetes mellitus con impotencia, non hai violacións da función gonadotrópica hipofisaria, o contido de testosterona no plasma é normal.
A patoloxía da sudoración nas etapas iniciais da diabetes exprésase no seu fortalecemento. Con un aumento da duración da enfermidade, obsérvase a súa diminución, ata a anhidrose das extremidades inferiores. Neste caso, a sudoración intensifícase nas partes superiores do corpo (cabeza, pescozo, peito), especialmente pola noite, o que simula a hipoglucemia. Ao estudar a temperatura da pel, revélase unha violación dos patróns e das reaccións orais-caudais e proximal-distais á calor e ao frío. Un tipo peculiar de neuropatía autónoma é a sudoración saborosa, que se caracteriza por unha transpiración profusa na cara, no pescozo, no peito superior varios segundos despois de tomar certos alimentos (queixo, adobo, vinagre, alcohol). É rara. Un aumento local da sudoración débese a unha disfunción do ganglio simpático cervical superior.
Neuropatía cardíaca diabética autónoma (DVKN) caracterízase por hipotensión ortostática, taquicardia persistente, un débil efecto terapéutico nela, unha frecuencia cardíaca fixa, hipersensibilidade ás catecolaminas, infarto de miocardio indolor e, ás veces, morte súbita do paciente. A hipotensión postural (ortostática) é o signo máis rechamante da neuropatía autonómica. Exprésase na aparición en pacientes en posición permanente de mareos, debilidade xeral, escurecemento nos ollos ou deficiencia visual. Este complexo de síntomas adoita considerarse como un estado hipoglucémico, pero en combinación cunha caída postural da presión arterial, a súa orixe non está en dúbida. En 1945, A. Rundles asociaba por primeira vez a hipotensión postural con neuropatía na diabetes. As manifestacións de hipotensión postural poden aumentar despois de tomar fármacos antihipertensivos, diuréticos, antidepresivos tricíclicos, medicamentos de fenotiazina, vasodilatadores, así como nitroglicerina. A administración de insulina tamén pode agravar a hipotensión postural ao diminuír o retorno venoso ou danar a permeabilidade do endotelio capilar cunha diminución do volume plasmático, mentres que o desenvolvemento de insuficiencia cardíaca ou síndrome nefrótico reduce a hipotensión. Crese que a súa aparición explícase pola rotura da reacción da renina plasmática para plantarse debido ao deterioro da innervación simpática do aparello juxtaglomerular, así como por unha diminución dos niveis de noradrenalina plasmática basal e estimulada (de pé) ou dun defecto baroreceptor.
En pacientes con diabetes mellitus complicado por DVKN, en repouso, un aumento da frecuencia cardíaca de ata 90-100, e ás veces ata 130 latidos / min. A taquicardia persistente, que non é susceptible de efectos terapéuticos en pacientes con diabetes mellitus, é causada por unha insuficiencia parasimpática e pode servir de manifestación na etapa inicial dos trastornos cardíacos autónomos. A inervación vagal do corazón é o motivo da perda da capacidade de variación normal da frecuencia cardíaca na cardiopatía diabética e, por regra xeral, precede á deservación simpática. Reducir a variación dos intervalos cardio en repouso pode servir como indicador do grao de trastornos funcionais do sistema nervioso autónomo.
A denervación total do corazón é rara e caracterízase por un ritmo cardíaco frecuente fixo. A dor típica no desenvolvemento de infarto de miocardio é pouco característica para os pacientes que padecen DVKN. Na maioría dos casos, durante os seus pacientes non senten dor ou son atípicos. Suponse que a causa de ataques cardíacos indolor en estes pacientes é o dano aos nervios viscerais, que determinan a sensibilidade á dor do miocardio.
M. McPage e P. J. Watkins reportaron 12 casos de "parada cardiopulmonar" súbita en 8 mozos con diabetes con neuropatía autónoma grave. Non houbo datos clínicos e anatómicos sobre infarto de miocardio, arritmias cardíacas ou estado hipoglucémico. Na maioría dos casos, a causa do ataque foi a inhalación do fármaco con anestesia xeral, o uso doutras drogas ou a broncopneumonía (5 ataques producíronse inmediatamente despois da anestesia). Así, a parada cardiorrespiratoria é un signo específico de neuropatía autonómica e pode ser fatal.
Encefalopatía diabética. Os cambios persistentes no sistema nervioso central nos mozos adoitan asociarse a alteracións metabólicas agudas, e na vellez tamén están determinados pola gravidade do proceso aterosclerótico nos vasos do cerebro. As principais manifestacións clínicas da encefalopatía diabética son trastornos mentais e síntomas cerebrais orgánicos. Na maioría das veces, en pacientes con diabetes, a memoria está prexudicada. Un efecto especialmente pronunciado no desenvolvemento de trastornos mnesticos é exercido por condicións hipoglucémicas. Os trastornos da actividade mental tamén se poden manifestar por unha maior fatiga, irritabilidade, apatía, bágoas, trastornos do sono. Os trastornos mentais graves na diabetes mellitus son raros. Os síntomas neurolóxicos orgánicos poden manifestarse mediante microsimptomáticas difusas, que indican unha lesión difusa do cerebro ou síntomas orgánicos grosos que indican a presenza dunha lesión do cerebro. O desenvolvemento da encefalopatía diabética está determinado polo desenvolvemento de cambios dexenerativos nas neuronas cerebrais, especialmente durante condicións hipoglucemicas, e focos isquémicos asociados á presenza de microangiopatía e aterosclerose.
Patoloxía da pel. Para os pacientes con diabetes mellitus, a dermopatía diabética, a necrobiose lipoide e o xanthoma diabético son máis características, pero ningún deles é absolutamente específico para a diabetes.
Dermopatía ("puntos atróficos") expresada na aparición na superficie dianteira das patas das simples métricas pátulas de cor pardo avermellada cun diámetro de 5-12 mm, que logo se converten en manchas atróficas pigmentadas da pel. A dermopatía é máis frecuentemente detectada en homes con longa duración de diabetes. A patoxénese da dermopatía está asociada a unha microangiopatía diabética.
A necrobiose lipoide é moito máis común en mulleres e no 90% dos casos localízase nunha ou ambas as pernas.Noutros casos, o lugar da derrota é o tronco, os brazos, a cara e a cabeza. A frecuencia da necrobiose lipoide ofrece un 0,1-0,3% en relación a todos os pacientes con diabetes. A enfermidade caracterízase pola aparición de áreas da pel de vermello pardo ou amarelo de tamaño de 0,5 a 25 cm, a miúdo oval. As lesións cutáneas están rodeadas dun bordo eritematoso de vasos dilatados. A deposición de lípidos e caroteno provoca a cor amarela das áreas afectadas da pel. Os signos clínicos da necrobiose lipoide poden estar varios anos antes do desenvolvemento da diabetes mellitus tipo I ou detectarse no seu antecedente. Como resultado do exame de 171 pacientes con necrobiose lipoide, o 90% deles revelaron unha conexión entre esta enfermidade e a diabetes mellitus: nalgúns pacientes, a necrobiose desenvolveuse antes ou contra a diabetes mellitus, outra parte dos pacientes tiña unha predisposición hereditaria a ela. Histoloxicamente, atópanse signos de endarterite obliterante, microangiopatía diabética e cambios necrobióticos secundarios na pel. A destrución de fibras elásticas, elementos da reacción inflamatoria nas áreas de necrose e a aparición de células xigantes observáronse electrónicamente microscopicamente. Unha das razóns para a necrobiose lipoide considérase que se incrementou a agregación plaquetaria baixo a influencia de diversos estímulos, que xunto coa proliferación endotelial provoca trombose de pequenos vasos.
Xanthoma diabético desenvólvese como consecuencia da hiperlipidemia, e o papel principal o xoga un aumento do contido de chilomicronos e triglicéridos no sangue. As placas amarelentas localízanse principalmente nas superficies flexibles das extremidades, peito, pescozo e cara e consisten nunha acumulación de histiocitos e triglicéridos. A diferenza dos xantomas observados na hipercolesterolemia familiar, normalmente están rodeados de bordo eritematoso. A eliminación da hiperlipidemia leva á desaparición do xanthoma diabético.
Vexa diabética refírese a raras lesións na pel na diabetes. Esta patoloxía foi descrita por primeira vez en 1963 por R. P. Rocca e E. Regeuga. As burbullas prodúcense de súpeto, sen vermelhidão, nos dedos e os dedos dos pés, así como no pé. Os seus tamaños varían desde uns poucos milímetros a varios centímetros. A burbulla pode aumentar ao longo de varios días. O fluído da burbulla é transparente, ás veces hemorráxico e sempre estéril. A burbulla diabética desaparece de forma espontánea (sen abrirse) ás 4-6 semanas. Notouse unha aparición máis frecuente da vexiga diabética en pacientes con signos de neuropatía diabética e longa duración de diabetes, así como no fondo da cetoacidosis diabética. O exame histolóxico revelou a localización intradérmica, subepidérmica e subroginal da vexiga. Descoñécese a patoxénese da vexiga diabética. É necesario diferenciala de pemfigus e trastornos metabólicos da porfirina.
Granuloma en forma de anel Daria pode ocorrer en pacientes con diabetes mellitus: os anciáns, máis a miúdo nos homes. As erupcións aparecen no tronco e as extremidades en forma de manchas edemáticas en forma de moeda de cor rosa ou amarelo avermellado, propensas a un rápido crecemento periférico, fusión e formación de aneis e figuras policíclicas estrañas bordeadas por un borde denso e elevado. Non se cambia a cor da zona algo caída central. Os pacientes quéixanse dunha leve sensación de coceira ou picazón. O curso da enfermidade é longo e recorrente. Normalmente, as erupcións xurídicas pasan as 2-3 semanas e as novas aparecen no seu lugar. Histoloxicamente, detéctanse edemas, vasodilatacións, infiltrados perivasculares a partir de neutrófilos, histiocitos e linfocitos. Non se estableceu a patoxénese da enfermidade. As reaccións alérxicas á sulfanilamida e outros fármacos poden servir como factores provocadores.
Vitiligo (áreas de pel simétricas depigmentadas) detéctanse en pacientes con diabetes nun 4,8% dos casos en comparación co 0,7% da poboación xeral e nas mulleres dúas veces máis. O vitiligo adoita combinarse coa diabetes mellitus tipo I, o que confirma a xénese autoinmune de ambas enfermidades.
Máis a miúdo que noutras enfermidades, a diabetes vai acompañada de furúnculos e carbúnculos, que normalmente ocorren nun contexto de descompensación da enfermidade, pero tamén pode ser unha manifestación de diabetes latente ou precedente da tolerancia á glicosa. Unha gran tendencia dos pacientes diabéticos ás enfermidades fúngicas exprésase en manifestacións de epidermofitosis, que se atopan principalmente nos espazos interdigitais dos pés. Máis a miúdo que en individuos con tolerancia á glucosa non perturbada, detéctanse dermatose coceira, eczema e picor na área xenital. A patoxénese desta patoloxía da pel está asociada a unha violación do metabolismo intracelular da glicosa e unha diminución da resistencia á infección.
, , , , , , , , , ,
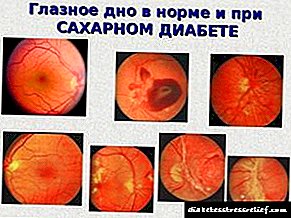
Patoloxía do órgano de visión na diabetes
En pacientes con diabetes mellitus atópanse diversas violacións da función do órgano visual, ata cegue, 25 veces máis que na poboación xeral. Entre os pacientes con cegueira, o 7% son pacientes con diabetes. As violacións da función do órgano da visión poden ser causadas por danos na retina, no iris, na córnea: a lente, o nervio óptico, os músculos extraoculares, o tecido orbital, etc.
A retinopatía diabética é unha das principais causas de deficiencia visual e cegueira en pacientes. Entre o 60 e o 80% dos pacientes atópanse diversas manifestacións (no contexto dunha duración de 20 anos de diabetes mellitus). Entre os pacientes con diabetes tipo I cunha duración de enfermidade superior aos 15 anos, obsérvase esta complicación no 63-65%, dos cales prolifera retinopatía no 18-20% e cegueira completa no 2%. En pacientes con diabetes tipo II, os seus síntomas desenvólvense cunha duración menor da diabetes. Unha deficiencia visual importante afecta o 7,5% dos pacientes e a cegueira completa ocorre na metade deles. O factor de risco para o desenvolvemento e progresión da retinopatía diabética é a duración da diabetes mellitus, xa que existe unha correlación directa entre a frecuencia desta síndrome e a duración da diabetes tipo I. Segundo V. Klein et al., Ao examinar a 995 pacientes, descubriuse que a frecuencia de discapacidade visual aumenta do 17% en pacientes con diabetes que non duran máis de 5 anos ata o 97,5% cunha duración de ata 10-15 anos. Segundo outros autores, os casos de retinopatía oscilan ata o 5% durante os primeiros 5 anos da enfermidade, ata o 80% coa diabetes que dura máis de 25 anos.
Nos nenos, independentemente da duración da enfermidade e do grao da súa compensación, a retinopatía é detectada con moita menos frecuencia e só no período posterior á puberdade. Este feito suxire o papel protector dos factores hormonais (STH, somatomedina "C"). A probabilidade de inchazo do disco óptico tamén aumenta coa duración da diabetes: ata 5 anos - a súa ausencia e despois de 20 anos - o 21% dos casos, en media é do 9,5%. A retinopatía diabética caracterízase pola expansión das venulas, a aparición de microaneurismos, exsudados, hemorragias e retinitis proliferadora. Os microaneurismos dos capilares e, especialmente, das vénulas son cambios específicos da retina na diabetes mellitus. O mecanismo da súa formación está asociado a hipoxia tisular por trastornos metabólicos. Unha tendencia característica é un aumento do número de microaneurismos na rexión premacular. Os microaneurismos de longa existencia poden desaparecer debido á súa rotura (hemorragia) ou trombose e organización debido á deposición de proteínas de material similar a hialina e lípidos neles. Os exudos en forma de turbidez, de cor amarela e de cor branca amarela, localízanse normalmente na área das hemorraxias en varias partes da retina. En aproximadamente o 25% dos pacientes con retinopatía diabética, obsérvanse cambios na forma de retinitis proliferadora.Normalmente, no fondo dos microaneurismos, hemorraxias retinais e exsudados, aparecen hemorragias vítreas, que se acompaña da formación de tecidos conectivos-cordas proliferativas vasculares que penetran dende a retina no vítreo. A engurrada posterior do tecido conxuntivo provoca un desprendemento de retina e cegueira. O proceso de formación de novos vasos tamén se produce na retina, con tendencia a danar o disco óptico, o que provoca unha diminución ou perda completa da visión. A retinite proliferadora ten unha correlación directa coa duración da diabetes. Os seus síntomas adoitan atoparse 15 anos despois da detección de diabetes en pacientes novos e despois de 6-10 anos en adultos. Unha frecuencia significativa desta complicación obsérvase cunha longa duración da enfermidade en pacientes enfermos a idade nova. En moitos pacientes, a retinitis proliferad combínase coas manifestacións clínicas da nefropatía diabética.
Segundo a clasificación moderna (segundo E. Kohner e M. Porta), distínguense tres etapas da retinopatía diabética. Fase I: retinopatía non proliferativa. Caracterízase pola presenza na retina de microaneurismos, hemorraxias, edema da retina, focos exudativos. Etapa II: retinopatía preproliferativa. Caracterízase pola presenza de anomalías venosas (nitidez, tortuosidade, duplicación e / ou flutuacións pronunciadas no calibre dos vasos sanguíneos), un gran número de exudados sólidos e "algodón", anomalías microvasculares intraretinais e moitas grandes hemorraxias retinais. Etapa III: retinopatía proliferativa.
Caracterízase por neovascularización do disco óptico e / ou doutras partes da retina, hemorraxias vítreas coa formación de tecido fibroso na zona das hemorraxias preretinais. A causa da cegueira en pacientes con diabetes é a hemorragia vítrea, a maculopatía, o desprendemento de retina, o glaucoma e a catarata.
A retinopatía diabética (incluída a proliferativa) caracterízase por un curso en forma de onda con tendencia a remisións espontáneas e exacerbación periódica do proceso. A progresión da retinopatía facilítase pola descompensación da diabetes mellitus, a hipertensión arterial, a insuficiencia renal e, en gran medida, o embarazo, así como a hipoglucemia. As enfermidades das pálpebras (blefarite, colazión, cebada) non son específicas para a diabetes mellitus, pero a miúdo combínanse e caracterízanse por un curso recorrente persistente causado por unha violación do metabolismo da glicosa tisular e unha diminución das propiedades inmunobiolóxicas do corpo.
Os cambios nos vasos da conxuntiva en pacientes con diabetes exprésanse en presenza de flebopatía (alongamento e expansión dos extremos venosos dos capilares, microaneurismos) e ás veces exsudados.
Os cambios na córnea exprésanse en queratodistrofia puntual epitelial, queratite fibrosa e uveal, úlceras corneas recorrentes, que normalmente non provocan unha diminución significativa da visión. Con compensación insuficiente para a diabetes mellitus, ás veces obsérvase deposición de material similar ao glicóxeno no epitelio pigmentario da superficie posterior do iris, o que provoca cambios dexenerativos e depigmentación das súas seccións correspondentes. No contexto da retinopatía proliferativa no 4-6% dos pacientes, obsérvase rubeose de iris, expresada no crecemento de vasos de nova formación na súa superficie anterior e cámara anterior do ollo, que pode ser a primeira causa do glaucoma hemorrágico.
As cataratas distinguen entre variedades metabólicas (diabéticas) e senís. O primeiro desenvólvese en pacientes dependentes da insulina mal compensada e está localizado nas capas subcapsulares da lente. O segundo ocorre en persoas maiores, tanto en pacientes con diabetes como en saudables, pero madura moito máis rápido no primeiro, o que explica a necesidade dunha intervención cirúrxica máis frecuente (intervencións.A patoxénese da catarata diabética está asociada ao aumento da conversión de glicosa en sorbitol nos tecidos da lente fronte aos antecedentes de hiperglicemia. A súa excesiva acumulación provoca edema celular, que modifica directa ou indirectamente o metabolismo da mitositite, o que leva ao desenvolvemento de cataratas.
O glaucoma ocorre no 5% dos pacientes con diabetes fronte ao 2% dos sans. Aumento da presión intraocular en máis de 20 mm RT. Art. pode danar a función do nervio óptico e causar discapacidade visual. A diabetes mellitus é frecuentemente combinada con varios tipos de glaucoma (ángulo aberto, ángulo estreito e retinopatía proliferadora asociada). Típico para os pacientes é unha forma de ángulo aberto, caracterizada por unha saída difícil de humidade da cámara debido á eliminación do aparello de drenaxe do ollo. Os cambios na mesma (canle de Schlemm) son similares ás manifestacións de microangiopatía diabética.
A función muscular oculomotora deteriorada (oftalmoplexia) é causada polo dano aos pares III, IV e VI dos nervios oculomotor cranial. Os signos máis característicos son diplopia e ptosis, que son máis comúns en pacientes con diabetes tipo I. Nalgúns casos, a ptose e diplopia poden ser as primeiras manifestacións da diabetes clínica. A causa da oftalmoplexia é a mononeuropatía diabética.
Obsérvase unha deficiencia visual transitoria en pacientes con diabetes mellitus ante os antecedentes do tratamento inicial con insulina debido ás importantes flutuacións da glicemia, así como a un dos signos anteriores ao desenvolvemento de cataratas. O curso non compensado de diabetes con hiperglucemia marcada vén acompañado dun aumento da refracción debido ao aumento do poder refractivo da lente. Por regra xeral, antes do inicio das cataratas, a miopía desenvólvese. Os cambios anteriores na agudeza visual poden deberse en gran medida á acumulación de sorbitol e fluído na lente. Sábese que a hiperglicemia aumenta na lente a conversión de glicosa en sorbitol, que ten unha pronunciada osmolaridade que favorece a retención de fluídos. Isto á súa vez pode provocar cambios na forma da lente e nas súas propiedades refractivas. A redución da glicemia, especialmente durante o tratamento con insulina, contribúe a miúdo ao debilitamento da refracción. Na patoxénese destes trastornos tamén é posible unha diminución da secreción de humidade na cámara anterior, o que contribúe a un cambio na posición da lente.
O dano dos tecidos orbitais é raro e é causado por unha infección bacteriana ou fúngica. Ademais, tanto os tecidos orbitais como os periorbitais están implicados no proceso. Os pacientes presentan proptose do globo ocular, oftalmoplexia (ata fixación central da mirada), discapacidade visual, dor. Un gran perigo para a vida é a implicación do seo cavernoso no proceso. Tratamento conservador: con medicamentos antibacterianos e antifúngicos.
A atrofia dos nervios ópticos non é un resultado directo da diabetes, sen embargo, obsérvase en pacientes cunha longa duración da enfermidade en presenza de retinopatía e glaucoma proliferativos diabéticos.
Para diagnosticar a patoloxía do órgano da visión, é necesario determinar a súa agudeza e campo, empregando biomicroscopia da parte anterior do ollo para identificar cambios vasculares na conxuntiva, limbo, iris e grao de nubrado da lente. A oftalmoscopia e a angiografía por fluorescencia permiten avaliar o estado dos vasos da retina. Os pacientes con diabetes precisan exames repetidos por un oftalmólogo 1-2 veces ao ano.
Enfermidade cardíaca na diabetes
A patoloxía cardiovascular é o principal factor causante de alta mortalidade en pacientes con diabetes mellitus.Un dano ao corazón nunha enfermidade pode deberse a microangiopatía diabética, distrofia miocárdica, neuropatía cardíaca diabética autónoma e tamén a aterosclerose coronaria. Ademais, en pacientes con diabetes mellitus moito máis frecuentemente que en pacientes sen diabetes, hai endocardite bacteriana, abscesos miocárdicos contra sepsis, pericardite en insuficiencia renal crónica e miocardite hipokalémica na cetoacidosis.
A lesión vascular diabética da microvasculatura (microangiopatía diabética) tamén se atopou no músculo cardíaco. Este proceso caracterízase histoloxicamente por un engrosamento da membrana do soto de capilares, venulas e arteriolas, unha proliferación endotelial e a aparición de aneurismas. Depósito excesivo de substancias positivas PAS, envellecemento prematuro de pericitos, acumulación de coláxeno participan na patoxénese do engrosamento da membrana do soto. A microangiopatía diabética, atopada no miocardio, contribúe á violación da súa actividade funcional.
Entre os pacientes con microcardiopatía idiopática, a frecuencia relativa dos pacientes con diabetes aumenta significativamente. Neste caso, detéctanse lesións de pequenos vasos (con grandes arterias coronarias sen cambios), acumulación extravascular de coláxeno, triglicéridos e colesterol entre miofibrilas, que non vai acompañada de hiperlipidemia. Clínicamente, a miocardiopatía caracterízase por un acurtamento do período de exilio do ventrículo esquerdo, un alargamento do período de tensión e un aumento do volume diastólico. Os cambios inherentes á miocardiopatía poden contribuír á frecuente aparición de insuficiencia cardíaca durante o período agudo de infarto de miocardio e alta mortalidade. A patoxénese da distrofia do miocardio diabético débese a trastornos metabólicos ausentes en individuos sans e pacientes ben compensados con diabetes mellitus. A deficiencia absoluta ou relativa de insulina interrompe o transporte de glicosa pola membrana celular, polo que a maior parte do gasto enerxético do miocardio repónse debido ao aumento da utilización de ácidos graxos libres, que se forman durante a aumento da lipólise (en condicións de deficiencia de insulina). A oxidación insuficiente de FFA vai acompañada dunha maior acumulación de triglicéridos. Un aumento dos niveis de tecido de glicosa-6-fosfato e frutosa-6-fosfato provoca a acumulación de glicóxeno e polisacáridos no músculo cardíaco. A compensación da diabetes contribúe á normalización dos procesos metabólicos no miocardio e á mellora da súa función.
A neuropatía cardíaca autónoma diabética é unha das manifestacións clínicas da vexetoneuropatía diabética, que tamén inclúe gastropatía, enteropatía, atonía da vexiga, impotencia e sudoración perturbada. O DVKN caracterízase por varios signos específicos, incluíndo taquicardia constante, frecuencia cardíaca fixa, hipotensión ortostática, hipersensibilidade ás catecolaminas, infarto de miocardio indolor e síndrome de "parada cardiopulmonar". É causada por danos ás partes parasimpáticas e simpáticas do sistema nervioso central. Inicialmente, perturba a inervación parasimpática do corazón, que se manifesta na taquicardia anteriormente mencionada ata 90-100 pulsacións / min, e nalgúns casos ata 130 latidos / min, que é difícil de tratar. O debilitamento da función vago tamén é o motivo da desregulación do ritmo cardíaco, que se manifesta na ausencia de variación respiratoria nos intervalos cardíacos. O dano ás fibras nerviosas sensibles tamén se explica pola aparición relativamente frecuente de infarto de miocardio nestes pacientes cunha clínica atípica, caracterizada pola ausencia ou a débil severidade da síndrome da dor.Cun aumento da duración da diabetes mellitus, os cambios na inervación simpática das fibras musculares lisas dos vasos periféricos únense aos trastornos parasimpáticos, que se expresa na aparición de hipotensión ortostática en pacientes. Neste caso, os pacientes senten mareos, escurecendo nos ollos e parpadeando de "moscas". Esta condición desaparece por conta propia ou o paciente vese obrigado a tomar unha posición inicial. Segundo A. R. Olshan et al., A hipotensión ortostática en pacientes prodúcese debido a unha diminución da sensibilidade dos barorreceptores. N. Oikawa et al. cren que, en resposta á subida, hai unha diminución da adrenalina plasmática.
Outra manifestación bastante rara de fracaso parasimpático é a falla cardiopulmonar, descrita por M. McPage e P. J. Watkins en pacientes con diabetes tipo I, e caracterizada por un cesamento repentino da actividade cardíaca e da respiración. Dos 8 pacientes descritos, 3 faleceron durante esta enfermidade. Na maioría dos casos, a causa da morte é a inhalación dun analgésico estupefaciente durante a analxésia por cirurxía. Na autopsia do falecido non se estableceu a súa causa. O paro cardiopulmonar, segundo os autores, é de orixe pulmonar primaria debido á diminución da sensibilidade do centro respiratorio e da hipoxia en pacientes con neuropatía autónoma, xa que os corpos carotídeos e os quimioceptores están innervados por nervios glosofaringeos e vagos. Como consecuencia da hipoxia, prodúcese hipotensión, diminúe o fluxo sanguíneo cerebral e a detención respiratoria da xénese central é confirmada pola resposta rápida dos pacientes aos estimulantes respiratorios. As mostras que detectan trastornos do sistema parasimpático baséanse nunha diminución da variación de intervalos cardio (unha diminución da arritmia respiratoria) causada polos cambios descritos anteriormente no tecido nervioso. A miúdo, para este propósito, utilízanse probas con rexistro de cambios na frecuencia cardíaca durante a respiración normal e profunda, unha proba de Valsalva modificada, a proba Eving e algúns outros. Detéctanse violacións da inervación simpática do corazón mediante unha proba ortostática e outras probas. Todos estes métodos de diagnóstico distínguense pola relativa sinxeleza de execución, non invasividade e bastante alta informatividade. Pódense recomendar para uso tanto en hospitais como en ambulatorios.
Aterosclerose das arterias coronarias. A localización da aterosclerose coronaria en pacientes con diabetes mellitus é a mesma que en pacientes sen diabetes e maniféstase pola participación predominante das arterias coronarias proximais. A única diferenza é a aparición de aterosclerose coronaria en pacientes novos con diabetes mellitus cunha manifestación máis grave. Ao parecer, a diabetes ten significativamente menos colaterales, xa que os datos de angiografía das principais arterias coronarias en pacientes con esclerose coronaria en presenza e ausencia de diabetes son os mesmos. Segundo estudos experimentais, crese que o papel protagonista na rápida progresión da aterosclerose en pacientes con diabetes é desempeñado pola hiperinsulinemia endóxena ou exóxena: a insulina, ao inhibir a lipólise, aumenta a síntese de colesterol, fosfolípidos e triglicéridos nas paredes dos vasos sanguíneos. A permeabilidade das células endoteliais resistentes á insulina cambia baixo a influencia das catecolaminas (no fondo das flutuacións da glicemia), o que contribúe ao contacto da insulina coas células musculares lisas das paredes arteriais, o que estimula a proliferación destas células e a síntese de tecido conectivo na parede vascular. As lipoproteínas son capturadas por células musculares lisas e penetran no espazo extracelular, onde forman placas ateroscleróticas.Esta hipótese explica a relación limiar entre a glicosa e aterosclerose, así como o feito de que os factores de risco afectan igualmente o desenvolvemento da aterosclerose en pacientes con diabetes e en persoas saudables. Sábese que a enfermidade de tipo II caracterízase por un aumento dos niveis de insulina basal e un aumento da frecuencia de aterosclerose e enfermidades coronarias (CHD). Ao comparar pacientes con diabetes mellitus e enfermidades coronarias con pacientes sen diabetes, atopouse un aumento da resposta á insulina á administración oral de glicosa e un aumento máis acusado da secreción de insulina despois dunha mostra oral con tolbutamida. Na diabetes tipo II, en combinación coa aterosclerose, aumenta a relación insulina / glicosa. Un estudo sobre pacientes con aterosclerose de arterias coronarias, cerebrais e periféricas sen diabetes tamén revelou un aumento da resposta de insulina á carga oral de glicosa. A obesidade vai acompañada de hiperinsulinemia tanto na ausencia como na presenza de diabetes mellitus. O risco de enfermidades coronarias é significativamente maior en presenza de obesidade tipo androide.
Infarto de miocardio. En comparación coa súa prevalencia na poboación de pacientes con diabetes mellitus dunha idade similar, ocorre dúas veces máis veces. A enfermidade coronaria é a principal causa de morte en pacientes con diabetes tipo II. A mortalidade por infarto de miocardio nestes pacientes é extremadamente alta e chega ao 38% nos primeiros días despois do seu inicio, e ao 75% nos próximos 5 anos. O curso clínico dun ataque cardíaco en pacientes con diabetes ten as seguintes características: a aparición de ataques cardíacos extensos, moitas veces observaron complicacións tromboembólicas de insuficiencia cardíaca, a prevalencia de ataques cardíacos recorrentes e un aumento da taxa de mortalidade no período agudo e a miúdo dunha clínica de ataque cardíaco atípico con dor leve e ausente. A frecuencia desta complicación correlaciona directamente coa duración da diabetes (especialmente en pacientes con tipo I), a idade dos pacientes, a presenza de obesidade, hipertensión, hiperlipidemia e en menor medida coa severidade da diabetes e a natureza do seu tratamento. En moitos casos, a diabetes tipo II debuta o seu infarto de miocardio.
As maiores dificultades no seu diagnóstico son manifestacións atípicas. Ao redor do 42% dos pacientes durante un infarto de miocardio non sente dor (en comparación co 6% dos pacientes sen diabetes) ou é atípico e leve. Os signos dun ataque cardíaco en pacientes con diabetes poden ser a aparición súbita de insuficiencia xeral, edema pulmonar, náuseas e vómitos desmotivados, descompensación de diabetes mellitus con aumento da glicemia e cetoacidosis de orixe descoñecida, alteracións do ritmo cardíaco. Estudos de pacientes con diabetes que morreron por infarto de miocardio demostraron que o 30% deles xa sufrira un ataque cardíaco non diagnosticado e o 6,5% mostrou cambios que indicaban 2 ou máis ataques cardíacos indolorais anteriores. Os datos do exame de Framingham indican que un ataque cardíaco detectado por un estudo ECG aleatorio foi observado no 39% dos pacientes con diabetes e no 22% dos pacientes sen ela. A aparición de infarto de miocardio indolor en diabetes mellitus agora está frecuentemente asociada a neuropatía cardíaca autónoma e danos ás fibras sensibles dos nervios aferentes. Esta hipótese confirmouse no estudo de fibras nerviosas en pacientes que morreron durante un ataque cardíaco indolor. No grupo control do falecido (pacientes con ou sen dor, con ou sen diabetes), non se detectaron cambios similares na autopsia.
No período agudo de infarto de miocardio, o 65-100% dos pacientes presentan hiperglicemia basal, o que pode ser o resultado da liberación de catecolaminas e glucocorticoides en resposta a unha situación estresante.O aumento significativo observado na secreción de insulina endóxena non elimina a hiperglicemia, xa que aumenta o contido de ácidos graxos libres no sangue, o que suprime o efecto biolóxico da insulina. A violación da tolerancia aos hidratos de carbono no período agudo do infarto de miocardio adoita ser de natureza transitoria, pero case sempre indica un risco de desenvolver diabete. O exame posterior (despois de 1-5 anos) de pacientes con hiperglucemia transitoria no período agudo de infarto de miocardio indica que o 32-80% deles revelaron posteriormente NTG ou diabetes clínica.
Factores de aparición e síntomas
 Os resultados de moitos estudos patomorfolóxicos demostraron que a amiotrofia diabética se produce no fondo dos danos autoinmunes nos vasos nerviosos (perineuria, epineuria) coa aparición de perivasculite e microvasculite. Estas enfermidades contribúen a danos isquémicos ás raíces e vasos sanguíneos.
Os resultados de moitos estudos patomorfolóxicos demostraron que a amiotrofia diabética se produce no fondo dos danos autoinmunes nos vasos nerviosos (perineuria, epineuria) coa aparición de perivasculite e microvasculite. Estas enfermidades contribúen a danos isquémicos ás raíces e vasos sanguíneos.
Hai evidencias dun sistema de complementos, linfocitos endoteliais, expresión de citocinas inmunoreactivas e exposición a células T citotóxicas. Tamén se rexistraron casos de infiltración por polinucleares venulares (post-capilar). Ao mesmo tempo, descubriuse nas raíces e nervios a destrución e a disfunción de axóns, a acumulación de hemosiderina, o engrosamento da perineuria, a desmielinización local e a neovascularización.
Ademais, a atrofia muscular en diabéticos débese a algúns factores predispoñentes:
- idade - maiores de 40 anos,
- xénero: a miúdo ocorre complicación en homes,
- o abuso de alcol, que agrava o curso da neuropatía,
- crecemento: a enfermidade é máis común entre persoas altas cuxas terminacións nerviosas son máis longas.
A neuropatía proximal motora asimétrica comeza de forma subaguda ou aguda. Os seus síntomas son dor, sensación de arrastre e sensación de ardor na parte dianteira da coxa e na rexión interna da parte inferior da perna.
A aparición de tales signos non está asociada á actividade motora. Na maioría das veces ocorren de noite.
Despois de atrofia e debilidade dos músculos da coxa e da cintura pélvica desenvólvese. Ao mesmo tempo, é difícil para o paciente dobrar a cadeira e a articulación do xeonllo é inestable. Ás veces están implicados no proceso patolóxico aductores da coxa, da capa muscular do glúteo e do grupo peroneal.
A presenza ou reflexión do reflexo do xeonllo cunha lixeira diminución ou conservación de Aquiles indica a presenza de trastornos reflexos. De cando en vez, a atrofia muscular en diabéticos afecta as partes proximais das extremidades superiores e da cintura do ombreiro.
A gravidade dos trastornos sensoriais é mínima. A miúdo, a patoloxía adquire un carácter asimétrico. Neste caso, non hai síntomas de danos nos condutores da medula espiñal.
No caso da neuropatía diabética proximal, a sensibilidade non adoita prexudicarse. Basicamente, os síntomas da dor desaparecen en 2-3 semanas, pero nalgúns casos persisten ata 6-9 meses. A atrofia e a paresis acompañan ao paciente durante máis dun mes.
Ademais, no contexto destas complicacións, pode producirse unha perda de peso non explicada, que é a base para a realización de estudos sobre a presenza de tumores malignos.
Dano renal na diabetes
A nefropatía diabética (síndrome de Kimmelstil-Wilson, glomerulosclerose intercapilar) é unha manifestación da síndrome diabética tardía. Baséase en diversos procesos, incluída a glomerulosclerose nodular e difusa, o engrosamento da membrana do soto dos capilares glomerulares renais, a arterio e a arteriolosclerose, así como a fibrose tubular-intersticial.
Esta complicación é unha das principais causas de morte entre os pacientes con diabetes mellitus, aumentándoa en 17 veces en comparación coa poboación xeral. En aproximadamente a metade de todos os casos, a nefropatía diabética desenvólvese en pacientes con diabetes mellitus antes dos 20 anos.As súas manifestacións clínicas detéctanse despois de 12-20 anos de enfermidade. Non obstante, algúns cambios na función renal e trastornos anatómicos desenvolven moito antes. Entón, mesmo co inicio da diabetes mellitus, obsérvase un aumento do tamaño dos riles, o lumen dos túbulos e a taxa de filtración glomerular. Despois de compensar a diabetes, o tamaño dos riles normalízase, pero a taxa de filtración glomerular permanece elevada incluso despois de 2-5 anos, cando unha biopsia de punción revela un engrosamento da membrana do soto dos capilares glomerulares, o que indica a etapa inicial (histolóxica) da nefropatía diabética. Clínicamente, non se observaron outros cambios durante 12-18 anos en pacientes, a pesar da progresión de trastornos anatómicos.
O primeiro síntoma da nefropatía diabética é a proteinuria transitoria, que se produce, por regra xeral, durante o exercicio ou a ortostase. Entón tórnase constante a velocidade de filtración glomerular normal ou lixeiramente reducida. Un aumento significativo da proteinuria, que supera os 3 g / día e ás veces acada os 3 g / l, vén acompañado de disproteinemia, caracterizada por hipoalbuminemia, unha diminución da IgG, hipergamaglobulinemia e un aumento das alfa2-macroglobulinas. Ao mesmo tempo, entre o 40 e o 50% dos pacientes desenvolven síndrome nefrótico, a hiperlipidemia aparece respectivamente de tipo IV segundo Friedrichsen. Despois de 2-3 anos de proteinuria constante, aparece azotemia, aumentan os niveis de urea e creatinina no sangue e diminúe a filtración glomerular.
A progresión da enfermidade leva outros 2-3 anos ao desenvolvemento da metade dos pacientes con síndrome de insuficiencia renal clínica, especialmente un rápido aumento na oficina obsérvase en pacientes con proteinuria grave en combinación coa síndrome nefrótica. Co desenvolvemento da insuficiencia renal, a taxa de filtración glomerular diminúe drasticamente, detéctanse os niveis de nitróxeno residual (máis do 100 mg%) e creatinina (máis do 10 mg%), anemia hipocromática ou normocromática. No 80-90% dos pacientes nesta etapa da enfermidade, a presión arterial aumenta de xeito significativo. A xénese da hipertensión arterial débese principalmente á retención de sodio e á hipervolemia. A hipertensión arterial grave pódese combinar con insuficiencia cardíaca segundo o tipo ventricular dereito ou complicada por edema pulmonar.
A insuficiencia renal adoita ir acompañada de hiperqualemia, que pode chegar a 6 mmol / L ou máis, o que se manifesta por cambios característicos de ECG. A súa patoxénese pode deberse a mecanismos extrarenais e renales. Os primeiros inclúen unha diminución da insulina, aldosterona, norepinefrina e hiperosmolaridade, acidosis metabólica, beta-bloqueantes. A segunda é unha diminución da filtración glomerular, da nefrite intersticial, do hipoxonosteronismo hiporeninémico, dos inhibidores da prostaglandina (indometacina) e da aldactona.
O curso clínico da nefropatía diabética é complicado por unha infección do tracto urinario, a pielonefrite crónica, que contribúe ao desenvolvemento de nefritis intersticial. A pielonefrite crónica é a miúdo asintomática e maniféstase por un deterioro no curso clínico da nefropatía diabética ou unha descompensación da diabetes mellitus. Este último (segundo datos da sección - 110%) combínase con papilite necrótica, que pode manifestarse de forma severa (1%) cun aumento da temperatura corporal, macrohematuria, cólicas renales e tamén de forma latente, a miúdo non diagnosticada, xa que a súa única manifestación é a microhematuria. . Nalgúns pacientes con síntomas de insuficiencia renal, cambia o curso da diabetes mellitus, que se expresa nunha diminución da necesidade diaria de insulina debido a unha diminución do apetito dos pacientes por náuseas e vómitos, así como debido a unha diminución da degradación da insulina nos riles e un aumento da súa vida media.
O curso clínico e a manifestación de nefropatía diabética en pacientes con diabetes tipo I e II presentan diferenzas significativas. Na diabetes tipo II, a nefropatía progresa moito máis lentamente e non é a principal causa de mortes.
Aparentemente as manifestacións clínicas da nefropatía diabética en varios tipos de diabetes son causadas por un grao de participación diferente na súa patoxénese de cambios reversibles ou irreversibles no tecido renal.
Patoxénese da nefropatía diabética por D'Elia.
- Aumento da filtración glomerular sen aumentar o fluxo de plasma renal.
- Proteinuria con hiperglicemia, deficiencia de insulina, agravada por esforzo físico e ortostase.
- Acumulación na mesangía de inmunoglobulinas, produtos de descomposición de proteínas, hiperplasia de mesanxio.
- Capacidade reducida dos túbulos distais para secretar ións de hidróxeno.
- Aumento da síntese de coláxeno na membrana do soto.
- Esclerose hialina de arteriolas con dano no aparello xuxtaglomerular.
- Aterosclerose das arterias con dano renal.
- Necrose das papilas.
Pola natureza do curso clínico, a nefropatía diabética divídese en formas latentes, manifestadas clínicamente e terminais. Este último caracterízase pola uremia. Cando se subdivide a nefropatía na fase, úsase a clasificación Mogensen (1983), que está baseada en datos de laboratorio e clínicos.
- A etapa de hiperfunción prodúcese ao inicio da diabetes mellitus e caracterízase por hiperfiltración, hiperfusión, hipertrofia renal e normoalbuminuria (
ILive non ofrece consello médico, diagnóstico ou tratamento.
A información publicada no portal está destinada só a fins informativos e non debe usarse sen consultar a un especialista.
Lea atentamente as regras e políticas do sitio. Tamén podes contactar connosco.
Clasificación da neuropatía diabética
Dependendo da topografía, distínguese a neuropatía periférica coa implicación predominante dos nervios espiñales no proceso patolóxico e a neuropatía autónoma en caso de violación da inervación dos órganos internos. Segundo a clasificación sindromica da neuropatía diabética, hai:
I. Síndrome de polineuropatía simétrica xeralizada:
- Cunha lesión predominante dos nervios sensoriais (neuropatía sensorial)
- Con dano predominante nos nervios motores (neuropatía motora)
- Con danos combinados aos nervios sensoriais e motores (neuropatía sensorimotor)
- Neuropatía hiperglicémica.
II. O síndrome da neuropatía diabética autonómica (autónoma):
- Cardiovascular
- Gastrointestinal
- Urogenital
- Respiratorio
- Motor do barco
III. Síndrome de neuropatía diabética focal ou multifocal:
- Neuropatía cranial
- Neuropatía do túnel
- Amiotrofia
- Radiculoneuropatía / Plexopatía
- Polineuropatía desmielinizante inflamatoria crónica (HVDP).
Varios autores distinguen a neuropatía central e as súas seguintes formas: encefalopatía diabética (encefalomielopatía), trastornos cerebrais vasculares agudos (PNMK, ictus), trastornos mentais agudos causados por descompensación metabólica.
Segundo a clasificación clínica, tendo en conta as manifestacións da neuropatía diabética, distínguense varias etapas do proceso:
1. Neuropatía subclínica
2. Neuropatía clínica:
- dor crónica
- dor aguda
- forma indolora en combinación cunha diminución ou perda completa de sensibilidade
3. Etapa de complicacións tardías (deformidade neuropática dos pés, pé diabético, etc.).
A neuropatía diabética refírese a polineuropatías metabólicas. Un papel especial na patoxénese da neuropatía diabética pertence a factores neurovasculares: microangiopatías que interrompen a subministración de sangue aos nervios.
Múltiples trastornos metabólicos que se desenvolven neste contexto conducen en última instancia a edema do tecido nervioso, trastornos metabólicos nas fibras nerviosas, deterioración de impulsos nerviosos, aumento do estrés oxidativo, desenvolvemento de complexos autoinmunes e, en última instancia, a atrofia de fibras nerviosas.
Os factores dun maior risco de desenvolver neuropatía diabética son a idade, a duración da diabetes, a hiperglucemia incontrolada, a hipertensión arterial, a hiperlipidemia, a obesidade, o tabaquismo.
Polineuropatía periférica
A polineuropatía periférica caracterízase polo desenvolvemento dun complexo de trastornos motores e sensoriais, que son máis pronunciados desde as extremidades. A neuropatía diabética maniféstase por queimadura, entumecimiento, formigueo da pel, dor nos dedos dos pés e pés, dedos, calambres musculares a curto prazo.
Pode crearse unha insensibilidade aos estímulos á temperatura, unha maior sensibilidade ao tacto, incluso a outros moi lixeiros. Estes síntomas tenden a empeorar durante a noite.
A neuropatía diabética vén acompañada de debilidade muscular, debilitamento ou perda de reflexos, o que leva a un cambio de marcha e unha deterioración da coordinación dos movementos.
Dolores e parestesia esgotadoras levan consigo insomnio, perda de apetito, perda de peso, depresión do estado mental dos pacientes - depresión.
As complicacións posteriores da neuropatía diabética periférica poden incluír úlceras do pé, deformación dos dedos dos pés como martelo, colapso do arco do pé. A polineuropatía periférica precede con bastante frecuencia a forma neuropática da síndrome do pé diabético.
Que é amiotrofia diabética
A amotrofia (a negación, os músculos musculares, a nutrición trófica) é debilidade muscular. Provoca danos nas raíces da medula espiñal. A forma proximal (máis próxima ao centro) da enfermidade caracterízase por unha diminución da forza dos músculos da coxa. Os nervios lombosacrais e os plexos participan no seu desenvolvemento.
A enfermidade é unha variante rara (1% dos casos) de neuropatía diabética. Esta complicación da diabetes prodúcese debido á diminución da nutrición (isquemia) das fibras nerviosas. A violación da patencia de pequenos vasos que traen sangue ao nervio, leva á destrución da fibra nerviosa. Ademais dos trastornos isquémicos típicos das polineuropatías, tamén se atopou o papel dos complexos autoinmunes.
Debido a cambios na resposta das células inmunes, recoñecen os seus tecidos como estranxeiros e comezan a producir anticorpos. Fórmase un complexo de antíxeno + anticorpo A súa presenza na parede vascular é a causa do proceso inflamatorio. Isto explica a resposta á dor pronunciada e a necesidade de usar medicamentos antiinflamatorios activos para o tratamento da enfermidade.
O curso da patoloxía é progresivo, a miúdo os pacientes quedan discapacitados a falta dunha terapia adecuada.
E aquí hai máis información sobre a neuropatía diabética das extremidades inferiores.
Como distinguir a amiotrofia da polineuropatía
Ambas as enfermidades afectan as fibras nerviosas e causan dor nas extremidades. Na táboa preséntanse importantes diferenzas entre amiotrofia e polineuropatía común.
Signo
Amiotrofia
Polineuropatía
Tipo de diabetes
Primeiro e segundo
Idade
Duración da diabetes
Calquera pasa primeiro
Compensación por enfermidade
Nivel alto de azucre
Inicio da enfermidade
Localización da dor
Sensibilidade
Non se cambiou ao principio
Forza muscular
Hai que ter en conta que os diabéticos teñen un curso combinado destas enfermidades. Neste caso, haberá signos de actividade motora deteriorada de toda a extremidade.
Signos e síntomas da patoloxía
A aparición de amiotrofia diabética é bastante típica:
- dor súbita na parte dianteira da coxa - ardor, disparo, máis forte durante a noite, hai alodinia - dor dun pequeno toque,
- debido á debilidade dos músculos femorais, resulta difícil saír da cama, feces, subir e baixar as escaleiras,
- dor na rexión lumbar ou sacra,
- redución de volume (atrofia muscular) da coxa afectada.
A amotrofia caracterízase principalmente por unha lesión unilateral. A medida que o proceso avanza, o proceso pode converterse en dúas caras e os músculos da perna inferior están implicados nel. Dende o inicio da dor na coxa ata a debilidade muscular, normalmente leva desde unha semana a 1 mes.Se o paciente non ten polineuropatía diabética concomitante, a sensibilidade da pel non cambia. O síndrome da dor dura unhas 3-7 semanas, pero coñécense casos da súa persistencia de 8 a 9 meses.
A debilidade muscular, o movemento prexudicado, a diminución do volume da cadeira permanecen durante moito tempo. Poden estar asociados con malestar xeral grave e perda de peso. Tales manifestacións da enfermidade na maioría dos casos por pacientes e mesmo médicos son consideradas como osteocondrose, e a emaciación provoca sospeita dun proceso de tumor. O tratamento con calmantes convencionais non trae alivio e aumentan a atrofia muscular e a debilidade.
Pero a recuperación pode durar varios anos, moitas veces hai un efecto residual, incluso coa terapia adecuada.
Métodos de diagnóstico
Se o paciente só sofre unha radiografía e tomografía da columna vertebral, a amiotrofia permanece sen detectar. Para esta enfermidade é necesario un exame especial:
- Electromiografía (estudo da función muscular). Hai unha diminución da condutividade do sinal, a contractilidade no grupo femoral.
- Electroneurografía (determinación do estado das fibras nerviosas). Reflicte danos nas raíces da nervios espiñal por un lado ou bilateral con intensidade variada.
- Punción vertebral. Aumento de contido proteico coa composición celular normal.
Para aclarar o diagnóstico, prescríbese resonancia magnética. Amosa a ausencia de cambios na columna vertebral, o proceso do tumor está excluído. Nas análises de sangue, detéctase un aumento da glicosa en xaxún e despois dunha carga de azucre, detéctase unha hemoglobina glicada, característica dun curso leve de diabetes ou de severidade moderada.
Tratamento da amiotrofia diabética proximal
A corrección dos trastornos do metabolismo dos carbohidratos é un requisito previo para un resultado de tratamento sostible. No segundo tipo de enfermidade, pode ser necesario conectar a insulina, xa que as hormonas do grupo glucocorticoides - Prednisolona, Metipred - adoitan entrar no réxime de tratamento. O último medicamento é máis eficaz nos primeiros 3 meses desde o inicio da enfermidade. É administrado por terapia de pulso (altas doses de 3 a 5 inxeccións).
No contexto das inxeccións hormonais, a mellora xeralmente prodúcese rapidamente: a dor diminúe e a forza muscular aumenta. Isto demostra unha vez máis o papel do factor autoinmune no desenvolvemento da amiotrofia. Hai un grupo de pacientes cunha resposta débil ás hormonas. É posible que se recomenda a administración de citostáticos (metotrexato), unha inmunoglobulina intravenosa, así como sesións de purificación de sangue por plasmafereis.
En danos ás fibras nerviosas da diabetes implican moléculas activas de osíxeno (radicais libres). As capacidades de autodefensa do sistema antioxidante en diabéticos son débiles.
Polo tanto, indícase o uso de ácido alfa-lipoico para inhibir a destrución do tecido nervioso. A introdución do seu curso pode ter unha importancia profiláctica para a aparición de neuropatía. Cunha enfermidade xa desenvolvida, úsanse inxeccións intravenosas de dúas semanas de Berlition, Thiogamma, Espa-lipon, seguidas de cambio de comprimidos. O tratamento ten unha duración mínima de 2 meses.
Para aliviar a dor, non se usan medicamentos convencionais (ibuprofeno, nimesulide) do grupo de antiinflamatorios non esteroides. Prescribir medicamentos con acción anticonvulsiva - Gabagamma, Letras, Finlepsin. Combínanse con pequenas doses de antidepresivos: amitriptilina, clofranil.
Masaxes das extremidades inferiores
No período de recuperación é necesario conectar masaxe e ximnasia médica, reflexoloxía, inxestión de vitaminas B (Milgamma, Neurovitan).
A amiotrofia diabética prodúcese por danos nas raíces da medula espiñal. No seu desenvolvemento participa un aumento do nivel de glicosa en combinación coa inflamación autoinmune das paredes vasculares.Como resultado, a nutrición das fibras nerviosas é perturbada. A enfermidade ocorre de súpeto, con dor aguda ao longo da fronte da coxa. Engádelle debilidade muscular, engádese unha diminución do volume da extremidade afectada.
E aquí hai máis información sobre a polineuropatía diabética.
Para o diagnóstico, debes examinar a función dos músculos e das fibras nerviosas. O tratamento inclúe medicamentos antidiabéticos, terapia de pulso hormonal, ácido alfa lipoico. Pode aliviar a dor con anticonvulsivos e antidepresivos. É necesario un longo período de rehabilitación para restaurar a forza muscular.
Vídeo útil
Vexa o vídeo de tratamento da diabetes tipo 1:
Hai neuropatía diabética das extremidades inferiores debido a aumentos prolongados no azucre no sangue. Os principais síntomas son formigueo, adormecemento das pernas, dor. O tratamento inclúe varios tipos de drogas. Podes anestesiar e tamén se recomenda ximnasia e outros métodos.
Unha complicación bastante grave da diabetes é a angiopatía diabética. Existe unha clasificación, que en gran parte está determinada polos síntomas do paciente. Para o tratamento, preséntase inicialmente un diagnóstico para determinar o grao de dano e logo prescríbense medicamentos ou se realiza unha cirurxía.
Realízase o diagnóstico de neuropatía diabética en pacientes con diabetes tipo 1 e tipo 2. Inicialmente, o exame o realiza un endocrinólogo e, a continuación, o neuropatólogo examina a sensibilidade cun kit especial para un procedemento no que hai un monofilamento, unha horquilla e outros dispositivos.
Se se comproba a neuropatía diabética, o tratamento realízase mediante varios métodos: medicamentos e pílulas para aliviar a dor, mellorar o estado das extremidades inferiores, así como masaxes.
Moitas veces, a polineuropatía diabética maniféstase pola dor. Os síntomas adicionais dependen do seu tipo. Pode ser sensorial, sensible, periférico, diabético, autónomo. A patoxénese tamén depende de que tipo de clasificación evolucionou.
Neuropatía autonómica
A neuropatía diabética autónoma pode desenvolverse e continuar en forma cardiovascular, gastrointestinal, urogenital, sudomotora, respiratoria e outras formas caracterizadas por funcións prexudicadas de órganos individuais ou sistemas enteiros.
A forma cardiovascular de neuropatía diabética pode desenvolverse xa nos primeiros 3-5 anos de diabetes mellitus. Maniféstase por taquicardia no repouso, hipotensión ortostática, cambios de ECG (prolongación do intervalo QT), aumento do risco de isquemia miocárdica indolora e ataque cardíaco.
A forma gastrointestinal de neuropatía diabética caracterízase por hipersalivación gustativa, disquinesia esofágica, perturbacións profundas na función motor-evacuación do estómago (gastroparesis), desenvolvemento de refluxo gastroesofágico patolóxico (disfagia, azia, esofagite).
En pacientes con diabetes mellitus, a gastrite hipoácida é frecuente, úlcera péptica asociada a Helicobacter pylori, un aumento do risco de disquinesia da vesícula biliar e enfermidades do cálculo biliar.
Unha lesión intestinal na neuropatía diabética vén acompañada dunha violación da peristalsis co desenvolvemento de disbiose, diarrea acuosa, steatorrea, estreñimiento, incontinencia fecal. Do fígado, a miúdo detéctase unha hepatose graxa.
Coa forma urogenital de neuropatía diabética autónoma, perturba o ton da vexiga e dos uréteres, que pode ir acompañado de retención urinaria ou incontinencia urinaria.
Os pacientes con diabetes son propensos ao desenvolvemento de infeccións urinarias (cistite, pielonefrite).
Os homes poden queixarse de disfunción eréctil, unha violación da dolorosa inervación dos testículos, as mulleres - vaxina seca, anorgasmia.
Os trastornos sudomotores na neuropatía diabética caracterízanse por hipoxes e anhidrose distal (diminución da transpiración dos pés e mans) co desenvolvemento dunha hiperhidrose central compensatoria, especialmente durante as comidas e a noite.
A forma respiratoria de neuropatía diabética ocorre con episodios de apnea, hiperventilación dos pulmóns e unha diminución na produción de tensioactivo.
En neuropatía diabética, diplopia, hemeralopia sintomática, trastornos de termoregulación, hipoglucemia asintomática e “cachéxia diabética” son un esgotamento progresivo.
O algoritmo de diagnóstico depende da forma de neuropatía diabética. Na consulta inicial, analízase con detalle a anamnesis e as queixas polos cambios no sistema cardiovascular, dixestivo, respiratorio, xenitourinario e visual.
En pacientes con neuropatía diabética, é preciso determinar o nivel de glicosa, insulina, péptido C, hemoglobina glicosilada no sangue, estudar as pulsacións nas arterias periféricas, medir a presión sanguínea, examinar as extremidades inferiores de deformidades, lesións de fungos, cornos e cornos.
Dependendo das manifestacións no diagnóstico da neuropatía diabética, ademais do endocrinólogo e o diabetólogo, poden participar outros especialistas: un cardiólogo, gastroenterólogo, neurólogo, oftalmólogo, podólogo.
O exame inicial do sistema cardiovascular consiste en realizar un ECG, probas cardiovasculares (probas de Valsalva, probas ortostáticas, etc.
), Ecocardiografía, determinación do colesterol e lipoproteínas.
Un exame neurolóxico para a neuropatía diabética inclúe estudos electrofisiolóxicos: electromiografía, electroneurografía, potenciais evocados.
Valóranse reflexos e varios tipos de sensibilidade sensorial: táctil usando un monofilamento, vibracións usando unha horquilla, temperatura - ao tocar un obxecto frío ou quente, dor - picando a pel co lado contundente da agulla, propioceptiva - usando un test de estabilidade na posición de Romberg. A biopsia de caviar e biopsias de pel úsanse para formas atípicas de neuropatía diabética.
Un exame gastroenterolóxico para a neuropatía diabética implica unha ecografía dos órganos abdominais, endoscopia, radiografías do estómago, estudos do paso do bario polo intestino delgado e probas de Helicobacter.
En caso de queixas do sistema urinario, examínase unha análise xeral de orina, realízase unha ecografía dos riles, vexiga (incluída
Ultrasonido con determinación de orina residual), cistoscopia, urografía intravenosa, electromiografía dos músculos da vexiga, etc.
Razóns provocadoras
Adicionalmente, o proceso atrófico nos músculos dos diabéticos está determinado por determinadas causas predispoñentes:
- factor de idade maior de corenta anos,
- factor de xénero: os homes son máis frecuentemente afectados,
- a presenza de malos hábitos: abuso de bebidas alcohólicas,
- crecemento: o proceso patolóxico afecta a miúdo a persoas altas, porque teñen unha neuroterminal máis longa.
Tratamento da neuropatía diabética
O tratamento da neuropatía diabética realízase de xeito secuencial e por fases. O tratamento eficaz da neuropatía diabética é imposible sen conseguir unha compensación por diabetes.
Para este fin, prescríbense insulina ou comprimidos antidiabéticos e controlase a glicosa.
Como parte dun enfoque integrado para o tratamento da neuropatía diabética, é necesario desenvolver un réxime de dieta e exercicio óptimo, reducir o exceso de peso corporal e manter un nivel normal de presión arterial.
Durante o prato principal, indícase a inxestión de vitaminas neurotrópicas (grupo B), antioxidantes (ácido alfa-lipoico, vitamina E), oligoelementos (preparados de Mg e Zn). Coa forma dolorosa de neuropatía diabética, é recomendable prescribir analxésicos, anticonvulsivos.
Os métodos fisioterapéuticos de tratamento son útiles: estimulación nerviosa, magnetoterapia, láseroterapia, terapia lixeira, acupuntura, terapia de exercicios.
Na neuropatía diabética requírese especialmente un coidado dos pés: levar calzado cómodo (ortopédico), pedicura médica, baños de pés, hidratación do pé, etc.
O tratamento de formas autónomas de neuropatía diabética realízase tendo en conta a síndrome desenvolvida.
Previsión e prevención da neuropatía diabética
A detección precoz da neuropatía diabética (tanto periférica como autonómica) é a clave para un prognóstico favorable e unha mellora da calidade de vida dos pacientes.
As etapas iniciais da neuropatía diabética pódense reverter conseguindo unha compensación persistente para a diabetes.
A neuropatía diabética complicada é o principal factor de risco de infarto de miocardio sen dor, arritmias cardíacas e amputacións non traumáticas das extremidades inferiores.
Para previr a neuropatía diabética é necesario un seguimento constante dos niveis de azucre no sangue, unha corrección oportuna do tratamento, un control regular por parte dun diabetólogo e outros especialistas.
Síntomas e tratamento da amotrofia diabética

- Razóns provocadoras
- Cadro sintomático
- Diagnóstico
- Terapia
- Previsión de vida
A amiotrofia diabética (neuropatía) é unha combinación de complicacións da diabetes. Nalgunhas versións do sistema muscular fórmanse consecuencias patolóxicas como consecuencia do dano ao nervio. O diagnóstico dunha condición patolóxica é extremadamente difícil, xa que ten un curso asintomático.
Segundo as estatísticas, coa tolerancia á glucosa deteriorada, as complicacións desenvólvense no 10-12% dos casos e, con diabetes tipo II, detéctase amiotrofia diabética en máis do 25% dos pacientes. O perigo desta enfermidade é a formación de case o 75% dos diabéticos no caso de non facer unha terapia adecuada nas extremidades inferiores.
Unha rara opción para a neuropatía diabética é a radiculoplexite lumbosacral. O proceso patolóxico é característico exclusivamente para diabete tipo II, é dicir, para pacientes dependentes da insulina de 40 a 60 anos. Esta condición fórmase debido á microangiopatía diabética por danos axonais.
Os resultados dun gran número de estudos patomorfolóxicos indican a aparición de patoloxía como resultado de danos autoinmunes nos vasos dos feixes nerviosos (perineuria, epineuria) co desenvolvemento de perivasculite ou microvasculite. Estes últimos tamén axudan a desenvolver a destrución isquémica das raíces neuronais e da rede vascular.
Hai evidencias a favor do sistema do complemento, das células do linfocito endotelial, da expresión das inmunocitocinas e do efecto dos linfocitos T citotóxicos.
Existen opcións para a infiltración de pequenos vasos post-capilares por células polinucleares.
Neste contexto, detectouse e destrución de axóns, acumulación de hemosiderina, aumento do grosor da perineuria, desmielinización local e nova vascularización nas raíces neuronais e feixes nerviosas.
Cadro sintomático
A neuropatía proximal motora asimétrica ten un inicio subagudo ou agudo con dor, rastrexo e sensación de ardor na superficie anterior da coxa e no plano medial da perna inferior. A aparición dos síntomas descritos non ten ningunha conexión coa actividade motora. A miúdo aparecen de noite.
Ao cabo dun tempo, fórmase un proceso atrófico e unha diminución da forza muscular da coxa e da cintura pélvica. Neste caso, é difícil para o doente dobrar a cadeira, maniféstase a inestabilidade da articulación do xeonllo. Nalgunhas realizacións, os aductores da rexión femoral, os músculos gluteais e o grupo peroneal únense ao proceso patolóxico.
Un exemplo de trastornos reflexos é a perda ou diminución do reflexo do xeonllo no fondo dunha lixeira diminución ou preservación de Aquiles. Raramente, a atrofia muscular en pacientes diabéticos afecta as partes próximas dos brazos e a cintura do ombreiro.
A intensidade das perturbacións sensoriais é extremadamente baixa. Moitas veces a enfermidade vólvese asimétrica. Non se observan signos de dano nos condutores da columna vertebral.
Con esta patoloxía normalmente presérvase a sensibilidade. A dor desaparece despois de dúas a tres semanas, con todo, ás veces afórranse ata 6-9 meses. O proceso atrófico e a pareza ocorren durante moitos meses.
Os fenómenos parentéticos e o proceso atrófico persisten durante moitos meses, ás veces acompañados dunha diminución imprevisible do peso corporal.
Unha perda de peso tan rápida adoita levar ao paciente a sospeitar do desenvolvemento dun tumor maligno no seu corpo.
O período de recuperación dura varios anos e, nalgúns pacientes, mantense un defecto residual.
Diagnóstico
O diagnóstico só se pode facer despois dun exame minucioso do paciente debido ao curso asintomático.
O diagnóstico faise en polo menos 2 signos de natureza neurolóxica. Para o diagnóstico, prescríbense varios exames de laboratorio:
- exame xeral de orina e sangue,
- probas reumáticas
- avaliación de fluídos sinoviais
- Resonancia magnética da columna vertebral (parte inferior do lombo e sacro),
- estimulación ENMG e agulla EMG.
En CSF obsérvase un aumento do contido de proteínas. Despois da EMG, obsérvase denervación ou fascicación multifocal nos grupos cervicales paraspinais das patas.
As medidas terapéuticas son bastante longas (ata dous ou máis anos). A taxa de recuperación depende directamente de mecanismos compensatorios na enfermidade subxacente.
Os principais principios do tratamento eficaz:
- control constante do azucre no sangue periférico,
- tratamento sintomático en presenza de dor,
- terapia patoxenética.
Na fase inicial do tratamento, a terapia de pulso prescríbese co goteo de metilprednisolona.
Os niveis de azucre no sangue poden estabilizarse transferindo o paciente á insulina.
Para o alivio da dor, móstrase Pregabalina (dúas veces ao día, 150 mg cada unha). Como medicamento adicional, prescríbese Amitriptilina en pequena dose.
O tratamento con glucocorticosteroides só se permite nos primeiros tres meses do transcurso da enfermidade.
Se o tratamento con anticonvulsivos e glucocorticoides é ineficaz, recorren á inmunoglobulina intravenosa.
Nalgunhas realizacións úsanse medicamentos citostáticos e plasmerefese.
Moitas veces o desenvolvemento do proceso patolóxico é axudado polo estrés oxidativo, que se forma no fondo dun exceso de radicais libres e unha diminución da función do sistema antioxidante. Por iso, na terapia, o papel principal tamén se lle outorga aos antioxidantes con fins profilácticos e terapéuticos en caso de complicación tardía da diabetes.
Os medicamentos eficaces tamén poden incluír ácido alfa lipoico, o que reduce a imaxe sintomática neuropática.
Previsión de vida
O pronóstico de vida considérase relativamente favorable, incluso no caso dun curso grave, cando os pacientes durante un determinado período perden a capacidade de moverse de forma independente.
Por certo, tamén pode estar interesado no seguinte GRATIS materiais:
- Libros gratuítos: "TOP 7 exercicios nocivos para exercicios de mañá, que debes evitar" | "6 regras para un estiramento eficaz e seguro"
- Restauración das articulacións do xeonllo e da cadeira con artrosis: unha gravación en vídeo gratuíta do webinar, dirixida polo médico de terapia do exercicio e medicina deportiva - Alexander Bonin
- Clases gratuítas para o tratamento da dor lumbar dun médico certificado en terapia de exercicios. Este médico desenvolveu un sistema único de recuperación para todas as partes da columna vertebral e xa axudou máis de 2000 clientes con varios problemas de costas e pescozo.
- Queres aprender a tratar os pinchos do nervio ciático? Entón mira coidadosamente o vídeo nesta ligazón.
- 10 compoñentes nutricionais esenciais para unha columna vertebral saudable: neste informe descubrirás como debe ser a túa dieta diaria para que vostede e a súa columna vertebral estean sempre cun bo corpo e espírito saudable. Información moi útil!
- Ten osteocondrose? Entón recomendamos estudar métodos eficaces para tratar a osteocondrose lumbar, cervical e torácica sen drogas.
Clasificación e síntomas da neuropatía diabética
Sabendo cal é a neuropatía diabética, cómpre considerar os signos e síntomas que sinalan unha enfermidade.
A sintomatoloxía da patoloxía baséase na parte do sistema nervioso máis afectada. Noutras palabras, os síntomas da enfermidade poden diferir significativamente e todo depende do dano no corpo do paciente.
Cando a rexión periférica está afectada, a sintomatoloxía faise sentir despois de dous meses. Esta circunstancia está asociada a que no corpo humano hai un gran número de terminacións nerviosas e, por primeira vez, nervios viables asumen a funcionalidade dos danados.
A neuropatía periférica diabética caracterízase por que as mans e os pés están inicialmente afectados.
Clasificación da neuropatía diabética:
- Síndrome sintomático de polineuropatía xeneralizada: neuropatía sensorial, neuropatía motora, enfermidade sensorimotora, patoloxía hiperglicémica.
- Neuropatía autónoma diabética: urogenital, respiratorio, sudomotor, cardiovascular.
- Neuropatía focal: túnel, craneal, plexopatía, amotrofia.
A neuropatía sensorial é a derrota da susceptibilidade das terminacións nerviosas a unha distorsión simétrica das sensacións dunha persoa. Por exemplo, unha perna será máis sensible que a outra. Debido a que durante a patoloxía os nervios están afectados, hai unha transmisión inadecuada de sinais desde os receptores da pel ao cerebro.
Obsérvanse os seguintes síntomas:
- Alta susceptibilidade aos irritantes ("golpes de oca" rastreando nas extremidades, sensación de ardor, picazón, dores periódicas afiadas sen motivo).
- Unha reacción negativa ante calquera irritante. Un "irritante leve" pode ser o resultado dunha síndrome de dor grave. Por exemplo, un paciente pode espertar durante a noite debido á dor debido ao toque dunha manta.
- Diminución ou perda absoluta de susceptibilidade. Inicialmente, hai unha perda de sensibilidade das extremidades superiores, entón as extremidades inferiores sofren (ou viceversa).
Nova información: 5 principais signos de diabetes
A neuropatía diabética motor caracterízase por danos nos nervios responsables do movemento, que regula a transmisión de sinais do cerebro aos músculos. Os síntomas desenvólvense bastante lentamente, un signo característico desta condición é un aumento dos síntomas durante o sono e o descanso.
O cadro clínico de tal patoloxía caracterízase por perda de estabilidade ao camiñar, funcionamento deteriorado do sistema músculo-esquelético, limitación da mobilidade articular (edema e deformidade) e debilidade muscular.
A neuropatía diabética autónoma (tamén chamada neuropatía autonómica) é unha consecuencia da funcionalidade deteriorada dos nervios do sistema nervioso autónomo, responsable do traballo dos órganos internos.
Síntomas da neuropatía autónoma na diabetes tipo 2:
- Interrupción do tracto dixestivo (difícil de tragar, dor no estómago, ataques de vómitos).
- Violacións da funcionalidade dos órganos pélvicos.
- Función cardíaca deteriorada.
- Cambio de pel.
- Discapacidade visual.
A neuropatía óptica é unha patoloxía que pode levar á perda da percepción visual de carácter longo ou temporal.
A forma urogenital de neuropatía diabética caracterízase por unha violación do ton da vexiga, así como por danos nos uréteres, que poden ir acompañados de retención urinaria ou incontinencia urinaria.
A neuropatía distal ocorre en case a metade dos pacientes con diabetes. O perigo da patoloxía reside na irreversibilidade dos danos. A neuropatía distal das extremidades inferiores caracterízase pola perda de sensación das pernas, dor e diversas sensacións de malestar - formigueo, ardor, picazón.
Patoloxía Diagnósticos
A neuropatía diabética ten moitas ramas, cada unha delas cunha característica propia. Para diagnosticar a neuropatía diabética, o médico recolle primeiro o historial dun paciente.
Para obter o cadro clínico máis completo, úsase unha escala especial e cuestionarios. Por exemplo, úsase unha escala de signos de natureza neurálxica, unha escala xeral de síntomas e outros.
Durante un exame visual, o médico examina as articulacións, mira a condición do pé, o pé e as palmas, a deformación das cales indica neuropatía. Determina se a vermelhidão, a sequedad e outras manifestacións da enfermidade están presentes na pel.
Un exame obxectivo do paciente revela un síntoma tan importante como o esgotamento e outros síntomas secundarios. A cachexia diabética pode ser extrema cando o paciente non ten depósitos subcutáneos de graxa e graxa na rexión abdominal.
Tras a inspección realízase unha proba de sensibilidade ás vibracións. Mediante un dispositivo vibrador especial, que o médico presenta ao dedo do pé grande ou outras áreas. Tal estudo realízase tres veces. Se o paciente non sente a frecuencia de oscilación de 128 Hz, entón isto indica unha diminución da susceptibilidade.
Novas informacións: diabetes sen compensación: que é?
Para determinar o tipo de patoloxía e para aprender a tratala máis adiante, realízanse as seguintes medidas diagnósticas para determinar a neuropatía diabética:
- Determinase a sensibilidade táctil.
- Determinase a sensibilidade á temperatura.
- A sensibilidade á dor está determinada.
- Valóranse reflexos.
A neuropatía diabética caracterízase por un curso diverso, polo tanto, na gran maioría dos casos, todas as medidas de diagnóstico realízanse sen excepción.
O tratamento da neuropatía é un proceso bastante complicado, laborioso e caro. Pero co inicio oportuno da terapia, o prognóstico é favorable.
Prevención patolóxica
A neuropatía diabética é unha enfermidade complexa, chea de numerosas consecuencias para o paciente. Pero este diagnóstico pode previrse. A regra básica é o control da glicosa no corpo do paciente.
É o alto nivel de glicosa que é un grave factor de risco para a perda de funcionalidades polas células nerviosas e as terminacións. Existen algunhas medidas preventivas que axudarán a evitar complicacións e consecuencias graves no contexto da enfermidade subxacente.
Observando os primeiros signos de patoloxía, é necesario contactar inmediatamente cun médico. É el quen prescribirá un tratamento adecuado. Sábese que calquera enfermidade é máis fácil de tratar con precisión nas fases iniciais do desenvolvemento e as posibilidades de controlar a patoloxía aumentan varias veces.
É necesario controlar o nivel de azucre no sangue, seguir unha dieta baixa en carbohidratos para diabéticos, cos máis pequenos cambios no corpo, informa ao seu médico.
É necesario levar un estilo de vida activo, facer deportes, paseos diarios ao aire libre (polo menos 20 minutos), os exercicios matutinos non son menos importantes. Recoméndase involucrarse en terapia física.
A neuropatía diabética está chea de numerosas complicacións, pero con acceso oportuno a un médico, o éxito na terapia está garantido. Se estabilizas a glicosa no corpo ao nivel requirido e aseguras o mellor funcionamento do sistema nervioso, entón todos os síntomas desaparecerán literalmente despois dos 1-2 meses.
Que opinas disto? Que medidas estás a tomar para evitar complicacións contra a diabetes?
Causas da amotrofia diabética
A principal razón é o longo e esquecido curso da diabetes. Hai tamén factores que causan amiotrofia diabética:
O azucre redúcese ao instante! A diabetes co paso do tempo pode levar a unha serie de enfermidades, como problemas de visión, condicións de pel e cabelo, úlceras, gangrena e incluso tumores cancerosos. A xente ensinou a experiencia amarga para normalizar os niveis de azucre. ler máis.
- idade
- crecemento elevado
- uso frecuente de bebidas alcohólicas,
- fumar
- danos nas fibras nerviosas,
- xénero
- enfermidades crónicas
- enfermidades infecciosas
- patoloxías xenéticas
- o desenvolvemento da amiloidosis,
- patoloxías autoinmunes.
Síntomas da amiotrofia diabética
Con amiotrofia diabética prodúcense os seguintes síntomas:
- mareos e sensación de debilidade,
- dor nos músculos das nádegas e cadeiras,
- debilidade muscular da perna superior e da pelvis,
- custa levantarse, sentarse, subir e baixar as escaleiras,
- violación de camiñar
- dano muscular
- perda de peso cunha diminución do apetito,
- adormecimiento nos brazos e nas pernas,
- aumento da sensibilidade ao tocar,
- falta de sensacións táctiles.
Características de diagnóstico
Cando aparecen os primeiros síntomas da amiotrofia diabética, definitivamente debes consultar a un médico. O especialista recollerá antecedentes médicos e realizará un exame obxectivo. Ao exame, detéctase unha alta sensibilidade ao tocar e a aparición de sensacións dolorosas. Ademais, o médico comprobará a forza dos reflexos e a sensibilidade aos cambios de temperatura. O paciente nota unha sensación de entumecimiento nos brazos e nas pernas e unha falta de sensacións táctiles. Despois, o especialista prescribirá métodos de investigación especiais:
- análise xeral de sangue e orina,
- bioquímica do sangue
- proba de azucre
- exame para probas reumáticas,
- Resonancia magnética da columna vertebral,
- exame de fluído sinovial,
- electromiografía
- electroneuromiografía estimulante.
Tratamento da enfermidade
Se o paciente mostrou os primeiros signos da enfermidade, debe ir con urxencia ao hospital. O autotratamento na casa sen o control dos médicos leva graves consecuencias. Ao seu ingreso, o médico recollerá un historial médico e examinará ao paciente. O médico prescribirá probas para poder facer un diagnóstico preciso. Despois do diagnóstico, seleccionará un réxime de tratamento. A base da terapia é tomar medicación. O médico dará recomendacións sobre cambios de estilo de vida para a eficacia do tratamento.
Fisioterapia
Para o tratamento da enfermidade prescríbense varios fármacos, os principais dos que figuran na táboa: