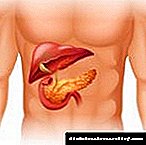
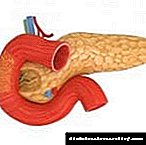
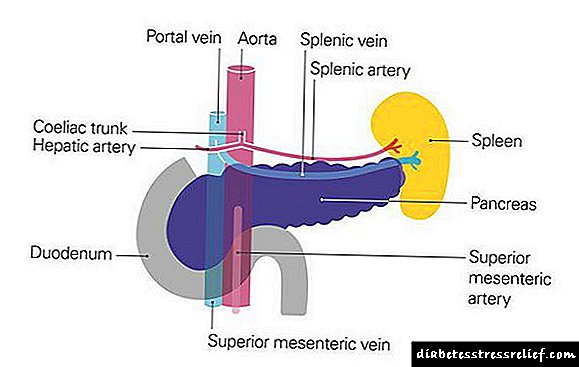
Como usar a droga Fendivia?
| Sistema Terapéutico Transdérmico (TTC) | 1 peza |
| compoñente activo | |
| Fendivia ™ 12,5 μg / h: contido de fentanilo 1,38 mg, parche 4,2 cm 2, velocidade de liberación de fentanil 12,5 μg / h | |
| Fendivia ™ 25 μg / h: contido de fentanil - 2,75 mg, parche de 8,4 cm 2, velocidade de liberación de fentanil - 25 μg / h | |
| Fendivia ™ 50 μg / h: contido de fentanil - 5,5 mg, parche 16,8 cm 2, velocidade de liberación de fentanil - 50 μg / h | |
| Fendivia ™ 75 μg / h: contido de fentanil - 8,25 mg, parche de 25,2 cm 2, velocidade de liberación de fentanil - 75 μg / h | |
| Fendivia ™ 100 μg / h: contido de fentanilo - 11 mg, parche de 33,6 cm 2, velocidade de liberación de fentanil - 100 μg / h | |
| excipientes | |
| película de protección exterior: Película PET | |
| capa de depósito: capa de adhesivo de silicona, dimeticona (E900) | |
| micro encoros que conteñan o compoñente activo: dipropilenglicol, hipolosa (E463) | |
| membrana de liberación: copolímero de etileno e acetato de vinilo | |
| capa adhesiva de pel: capa de adhesivo de silicona, dimeticona (E900) | |
| película extraíble de protección: película de poliéster recuberto de flúor |
Descrición da forma de dosificación
Un parche translúcido rectangular con bordos redondeados sobre unha película protectora transparente extraíble. A película protectora é máis grande que o parche. Unha incisión sinusoidal divide a película protectora extraíble en dúas partes.
As seguintes etiquetas aplícanse ao parche mediante impresión a cor:
1) Fendivia ™ 12,5 μg / h - parche (18 ± 0,5) mm de ancho (24 ± 0,5) mm de largo: "Fentanil 12,5 μg / hora" - selado marrón,
2) Fendivia ™ 25 μg / h - parche (24,6 ± 0,5) mm de ancho, (37 ± 0,5) mm de largo: "Fentanil 25 μg / hora" - impresión vermella,
3) Fendivia ™ 50 μg / h - parche (34 ± 0,5) mm de ancho (51,3 ± 0,5) mm de largo: "Fentanyl 50 μg / hora" - selado verde,
4) Fendivia ™ 75 μg / h - parche (42 ± 0,5) mm de ancho (61,7 ± 0,5) mm de largo: "Fentanyl 75 μg / hora" - impresión azul claro,
5) Fendivia ™ 100 μg / h - parche (49 ± 0,5) mm de ancho, (70 ± 0,5) mm de largo: "Fentanyl 100 μg / hora" - impresión gris.
Indicacións de uso
Inxección: dor de intensidade severa e moderada (angina pectorais, infarto de miocardio, dor en pacientes con cancro, trauma, dor postoperatoria), premedicación para distintos tipos de anestesia xeral en combinación con droperidol, antipsicóticos (incluído durante a cirurxía de órganos tórax e cavidade abdominal, grandes vasos en neurocirurxía, con operacións xinecolóxicas, ortopédicas e outras).
O TTS é un síndrome da dor crónica de severidade moderada: dor causada por cancro, dor de xénese diferente, que require analxésia con analxésicos narcóticos (por exemplo, neuropatía, artrite, infeccións por varicela zoster, etc.).
Contraindicacións
Hipersensibilidade, depresión grave do centro respiratorio.
TTS - dor aguda ou postoperatoria (imposibilidade de seleccionar a dose adecuada durante un curto período de tratamento, que pode levar a hipoventilación grave ou mortal), pel irritada, irradiada ou danada (no sitio de aplicación), diarrea con colite pseudomembranosa causada por cefalosporinas, lincosamidas, penicilinas, dispepsia tóxica, depresión respiratoria aguda, embarazo, lactación, idade menor de 18 anos.
Como usar: dosificación e curso do tratamento
In / in, in / m. Adultos en preparación para a cirurxía 10-15 minutos antes do inicio - iv, 0,05-0,1 mg de fentanilo con 2,5-5 mg de droperidol.
Para anestesia xeral - iv, 0,4-0,6 mg, para manter anestesia - iv, 0,05-0,2 mg cada 20-30 minutos, para alivio da dor despois da cirurxía - iv - 0,05-0,1 mg, se é necesario, repetiu doses despois de 1 ou 2 horas
Para alivio da dor con infarto de miocardio - 0,1 mg xunto con 5 mg de droperidol (durante 3 minutos).
Nenos en preparación para a cirurxía - 2 μg / kg, para anestesia xeral - 10-150 μg / kg iv ou 150-250 μg / kg iv, para o mantemento da anestesia - 1-2 μg / kg iv 2 mcg / kg v / m. A nenos menores de 2 anos non se lles estableceron doses.
O parche aplícase localmente durante 72 horas nunha superficie plana da pel (non irritada, con pelo mínimo, lavada con auga limpa se é necesario, sen o uso de deterxentes e secada completamente) e presionada ben (áreas de aplicación alternativas). A dose selecciónase individualmente. Para os pacientes que non tomaron opiáceos previamente, a dose inicial é de 25 μg / h, con tolerancia aos opiáceos ao cambiar ao tratamento con fentanilo, a dose inicial calcúlase segundo as táboas correspondentes, en función da necesidade diaria de analxésicos, se se usa unha dose superior a 300 μg / h, adicional ou vías alternativas de administración.
Acción farmacolóxica
Agonista do receptor opiaco analxésico (principalmente receptores mu) do sistema nervioso central, da medula espiñal e dos tecidos periféricos. Aumenta a actividade do sistema antinociceptivo, aumenta o limiar de sensibilidade á dor.
Os principais efectos terapéuticos do fármaco son analxésicos e sedativos. Ten un efecto deprimente sobre o centro respiratorio, diminúe o ritmo cardíaco, excita os centros n.vagus e o centro de vómitos, aumenta o ton dos músculos lisos do tracto biliar, os esfínters (incluíndo a uretra, a vexiga e o esfínter de Oddi), mellora a absorción de auga do tracto gastrointestinal. Reduce a presión arterial, a motilidade intestinal e o fluxo sanguíneo renal. No sangue aumenta a concentración de amilase e lipase, reduce a concentración de STH, catecolaminas, ADH, cortisol, prolactina.
Promove a aparición do sono (principalmente en relación coa eliminación da dor). Causa euforia. A taxa de desenvolvemento da dependencia das drogas e a tolerancia aos efectos analxésicos ten diferenzas individuais significativas.
A diferenza doutros analxésicos opioides, raramente provoca reaccións de histamina.
O efecto analxésico máximo con administración de i.v. desenvólvese despois de 3-5 minutos, con i / m - despois de 20-30 minutos, a duración do fármaco cunha única administración de i / v ata 100 mcg é de 0,5-1 h, con administración de i / m. como doses adicionais - 1-2 horas, cando se usa TTS - 72 horas
Efectos secundarios
Do sistema respiratorio: máis frecuentemente - depresión respiratoria, hipoventilación, ata parada respiratoria.
Do sistema nervioso e dos órganos sensoriais: máis a miúdo - dor de cabeza, somnolencia (incluído nos recentemente nados), menos frecuentemente - depresión do sistema nervioso central (incluído despois da cirurxía), axitación paradoxal do sistema nervioso central, delirio, convulsións, menos frecuentemente - percepción visual borrosa, diplopia, soños vivos, perda de memoria, frecuencia non establecida - confusión, euforia, alucinacións, cefalea, hipertensión intracraneal.
Do sistema dixestivo: máis a miúdo - náuseas, vómitos, menos veces - flatulencias, espasmos do esfínter de Oddi, desaceleración do baleiro gástrico, estreñimiento, cólicas biliares (en pacientes con antecedentes).
Do CCC: máis frecuentemente - bradicardia, baixada da presión sanguínea, menos frecuentemente - inhibición da actividade CCC, ata parada cardíaca.
Do sistema urinario: espasmo dos uréteres, retención urinaria.
Reaccións alérxicas - menos frecuentemente - dermatite alérxica, laringospasmo, calafríos, prurito, broncoespasmo.
Reaccións locais (cando se usa o parche): picazón, erupcións cutáneas, lavado da pel (desaparecen dentro das 24 horas despois de eliminar o parche), queima.
Outros: rixidez muscular a curto prazo (incluído o músculo torácico), transpiración aumentada, dependencia das drogas, síndrome de retirada (dor vaga, diarrea, palpitaciones, rinitis, estornudos, golpes de ganso, sudoración, anorexia, náuseas, vómitos, nerviosismo, fatiga irritabilidade, tremor, pupilas dilatadas, debilidade xeral), tolerancia.
Instrucións especiais
A droga debe ser usada só por persoal altamente cualificado nun hospital especializado. No período postoperatorio, o paciente necesita un seguimento coidadoso.
En pacientes con peso corporal reducido durante operacións prolongadas ou no caso de uso repetido frecuente de fentanilo, é posible un aumento da duración da súa acción.
Aumenta a actividade da plasma amilase e lipasa debido ao espasmo do esfínter de Oddi e aumenta a presión no sistema biliar (o estudo destes encimas debe realizarse ou varias horas antes do uso de fentanilo, ou 24 horas despois da súa administración).
Un estudo radionúclido ralentiza a visualización do tracto hepatobiliario debido a un espasmo do esfínter de Oddi.
Se é necesario, a cita do medicamento durante a lactación debería deixar de amamantar.
Non se recomenda o uso do parche para dor aguda ou postoperatoria (debido á imposibilidade de seleccionar unha dose por un curto período de tratamento e ao risco de hipoventilación), en mulleres en idade reprodutiva e require precaución en enfermidades pulmonares crónicas, incluída EPOC (posiblemente depresión do centro respiratorio), conciencia deteriorada, coma, tumores cerebrais, bradyarrhythmias, insuficiencia hepática e renal, na idade e na infancia.
Cando se usa o parche, recoméndase evitar a exposición directa a fontes de calor externas (almofadas de calefacción, saunas, baños de sol, etc.).
Durante o tratamento, non debes realizar actividades potencialmente perigosas que requiran unha maior atención e velocidade das reaccións psicomotrices.
Interacción
O óxido de dinitróxeno aumenta a rixidez muscular, antidepresivos tricíclicos, opiáceos, sedantes e hipnóticos, fenotiazinas, medicamentos ansiolíticos (tranquilizantes), medicamentos para anestesia xeral, relaxantes musculares periféricos, antihistamínicos, que teñen efectos sedativos e outros probol, etanol. Depresión do SNC, hipoventilación, hipotensión arterial, bradicardia, supresión do centro respiratorio, etc.).
Aumenta o efecto dos medicamentos antihipertensivos. Os beta-bloqueantes poden reducir a frecuencia e a gravidade da reacción hipertensiva na cirurxía cardíaca (incluída a esternotomía), pero aumentan o risco de bradicardia.
A buprenorfina, a nalbupina, a pentazocina, a naloxona, a naltrexona reducen o efecto analxésico do fentanilo e eliminan o seu efecto inhibidor no centro respiratorio.
As benzodiazepinas prolongan a liberación de neuroleptanalgesia.
É necesario reducir a dose de fentanilo ao usar insulina, corticoides, medicamentos antihipertensivos.
Os inhibidores da MAO aumentan o risco de complicacións graves.
Os relaxantes musculares evitan ou eliminan a rixidez muscular, os relaxantes musculares con actividade m-anticolinérxica (incluído o bromuro de pancuronium) reducen o risco de bradicardia e hipotensión (especialmente cando se usan beta-bloqueantes e outros vasodilatadores) e poden aumentar o risco de taquicardia, hipertensión miorréica. que non teñen actividade m-anticolinérxica (incluído o suxametonio) non reducen o risco de bradicardia e hipotensión arterial (especialmente no fondo dunha historia cardiolóxica cargada) e aumentan o risco de graves efectos en tempo completo do CCC.
Farmacodinámica
Fendivia ™ é un parche transdérmico que proporciona un subministro sistémico continuo de fentanilo durante 72 horas.O fenanilo é un analxésico opioide con afinidade principalmente para os receptores de opiáceos do sistema nervioso central, a medula espiñal e os tecidos periféricos. Aumenta a actividade do sistema antinociceptivo, aumenta o limiar de sensibilidade á dor. A droga Fendivia ™ ten efectos analxésicos e sedativos. Fentanyl ten un efecto deprimente sobre o centro respiratorio, retarda o ritmo cardíaco, excita os centros n.vagus e o centro de vómitos, aumenta o ton dos músculos lisos do tracto biliar, os esfínters (incluída a uretra, a vexiga e o esfínter de Oddi), mellora a absorción de auga do tracto dixestivo. Reduce a presión arterial, a motilidade intestinal e o fluxo sanguíneo renal. No sangue aumenta a concentración de amilase e lipase, reduce a concentración de STH, catecolaminas, ACTH, cortisol, prolactina. Promove a aparición do sono (principalmente en relación coa eliminación da dor). Causa euforia. A taxa de desenvolvemento da dependencia das drogas e a tolerancia aos efectos analxésicos ten diferenzas individuais significativas. Raramente provoca reaccións de histamina.
Farmacocinética
A concentración analxésica mínima efectiva de fentanilo no soro sanguíneo en pacientes que non utilizaron anteriormente analxésicos opioides é de 0,3–1,5 ng / ml. A frecuencia de efectos indesexables en tales pacientes aumenta cunha concentración de fentanilo no soro sanguíneo por encima de 2 ng / ml. Co desenvolvemento da tolerancia, aumenta tanto a concentración analxésica efectiva mínima de fentanilo como a concentración á que se producen reaccións indesexables.
Aspiración. Despois da primeira aplicación do parche transdérmico, a concentración de fentanilo no soro sanguíneo aumenta gradualmente, normalmente nivelando entre 12 e 24 horas, e permanece relativamente constante durante o resto de 72 horas. Coa segunda aplicación de 72 horas do parche transdérmico, conséguese unha concentración constante de fentanilo no soro sanguíneo, que permanece durante as aplicacións posteriores do parche do mesmo tamaño. A concentración de fentanilo no sangue é proporcional ao tamaño do parche transdérmico. A absorción de fentanilo pode variar lixeiramente segundo o lugar da aplicación. Observouse unha absorción lixeiramente reducida de fentanilo (aproximadamente un 25%) en estudos realizados con voluntarios sans durante a aplicación do parche no peito en comparación coa aplicación no brazo superior e nas costas.
Distribución. O fenanilo únese nun 84% ás proteínas plasmáticas, pasa polo BBB, a placenta e o leite materno.
Metabolismo. O fenanil ten unha cinética lineal de biotransformación e metabolízase principalmente no fígado polas enzimas CYP3A4. O principal metabolito do fentanilo é o norfentanil, que non está activo.
A cría. Despois da eliminación do parche transdérmico, a concentración de fentanilo no soro sanguíneo diminúe gradualmente. T1/2 fentanilo despois da aplicación do parche transdérmico é de 17 horas (13 a 22 horas) nos adultos e 22-25 horas nos nenos. A absorción continuada de fentanilo da superficie da pel leva a unha excreción máis lenta do fármaco do soro sanguíneo en comparación coa administración de iv. Ao redor do 75% do fentanilo excrétase na urina, principalmente en forma de metabolitos, menos do 10% non se modifica, arredor do 9% excrétase nas feces, principalmente en forma de metabolitos.
Grupos especiais de pacientes
A alteración da función hepática ou renal pode causar un aumento da concentración sérica de fentanil. En pacientes anciáns, debilitados ou debilitados, é posible unha diminución da eliminación de fentanilo, o que pode levar a unha T1/2 fentanilo.
Nenos. Dependendo do peso corporal, a limpeza (l / h / kg) é maior un 82% en nenos de 2 a 5 anos e un 25% maior en nenos de 6 a 10 anos en comparación con nenos de 11 a 16 anos que teñen tal a mesma limpeza que nos adultos.
Embarazo e lactación
Non se estableceu a seguridade dos parches transdérmicos con fentanilo durante o embarazo. Estudos en animais estableceron algunha toxicidade reprodutiva.
Fentanyl debe usarse só durante o embarazo se é necesario. O uso prolongado durante o embarazo pode provocar síntomas de abstinencia nos recentemente nados. Moi raramente, houbo síntomas de síntoma de abstinencia en recentemente nados cuxas nais usaron constantemente un parche transdérmico con fentanilo durante o embarazo.
O fentanyl non se debe usar durante o parto e parto (incluída a cesárea), comopasa pola placenta e pode provocar depresión respiratoria no feto ou no recentemente nado.
O fenanil se excreta no leite materno e pode provocar efectos sedantes e depresión respiratoria nun bebé amamantado. Polo tanto, se é necesario, a cita do medicamento Fendivia ™ durante a lactación debería deixar de amamantar (durante todo o tempo de uso e non menos de 72 horas despois do último uso).
Dosificación e administración
O parche transdérmico libera fentanilo dentro de 72 horas.A velocidade de liberación de fentanil é de 12,5, 25, 50, 75 e 100 μg / h, que é aproximadamente 0,3, 0,6, 1,2, 1,8 e 2,4. mg / día, respectivamente.
A dosificación requirida de fentanilo é seleccionada individualmente, tendo en conta o estado do paciente, e debe revisarse regularmente. Débese empregar a dosificación efectiva máis baixa.
Selección de dosis inicial
A dosificación inicial de fentanilo establécese segundo o nivel de inxestión de opioides no período anterior, ademais de ter en conta o posible desenvolvemento de tolerancia, tratamento con drogas concomitantes, saúde xeral e estado médico do paciente, i.e. tamaño corporal, idade e grao de esgotamento, gravidade da enfermidade.
Adultos previamente tratados con opioides
Para trasladar a pacientes que recibiron anteriormente opioides desde a administración oral ou parenteral de opioides a un parche transdérmico, deberase empregar a táboa 1. Se é necesario, a dosificación pode axustarse de 12,5 ou 25 μg / h cara a arriba ou cara arriba para seleccionar. a dose eficaz máis baixa dependendo da resposta do paciente e da necesidade de alivio da dor adicional.
Adultos non tratados previamente con opioides
Por regra xeral, a administración transdérmica non se recomenda para pacientes que non recibiran anteriormente opioides. Débense considerar métodos alternativos de administración (oral, parenteral). Para previr a sobredose en pacientes que non recibiron anteriormente opioides, recoméndase que se prescriban doses baixas de opioides de liberación inmediata (incluíndo morfina, hidromorfono, oxicodona, tramadol e codeína), cuxa dose debe seleccionarse para que coincida co parche transdérmico para o alivio da dor. a unha dosificación de 12,5 ou 25 mcg / h. Despois diso, os pacientes poden cambiar ao uso do medicamento Fendivia ™.
En condicións en que a administración oral de opioides non é posible e se recoñece o uso dun parche transdérmico como o único método de tratamento posible, o uso de Fendivia ™ debe iniciarse cunha dosificación mínima de 12,5 μg / h. Nestes casos, requírese un seguimento especial do paciente.
Existe o risco de depresión respiratoria grave ou que poida prever a vida aínda que se use unha dosificación mínima de 12,5 μg / h de Fendivia ™ en pacientes que non recibiran anteriormente opioides.
Transición de tomar outros opioides
Cando un paciente pasa da administración oral ou parenteral de analxésicos con opioides ao tratamento con fentanilo, a dosificación inicial de Fendivia ™ calcúlase do seguinte xeito.
1) Débese determinar o número de analxésicos de opioides requiridos polo paciente durante as últimas 24 horas (mg / día).
2) A cantidade recibida debe transferirse á dose diaria de morfina oral (mg / día) adecuada usando a táboa 1.
3) A dose adecuada de fentanilo determínase empregando as táboas 2 e 3.
Non se deben empregar as táboas 2 e 3 para cambiar dun parche transdérmico a outros opioides para evitar prescribir unha dose demasiado alta. Isto pode levar a unha sobredose.
Táboa de conversión - coeficientes para converter a dose diaria de opioides empregados anteriormente en dose oral diaria de morfina analxésica equivalente (mg / día do opioide × coeficiente anteriormente usado = dose equivalente analxésica diaria de morfina)
| Opioide usado anteriormente | Forma de solicitude | Coeficiente |
| morfina | por vía oral | 1 a |
| parenteral | 3 | |
| buprenorfina | sublingualmente | 75 |
| parenteral | 100 | |
| codeína | por vía oral | 0,15 |
| parenteral | 0,23 b | |
| diamorfina | por vía oral | 0,5 |
| parenteral | 6 b | |
| fentanilo | por vía oral | — |
| parenteral | 300 | |
| hidromorfono | por vía oral | 4 |
| parenteral | 20 b | |
| cetobemidona | por vía oral | 1 |
| parenteral | 3 | |
| levorfanol | por vía oral | 7,5 |
| parenteral | 15 b | |
| metadona | por vía oral | 1,5 |
| parenteral | 3 b | |
| oxicodona | por vía oral | 1,5 |
| parenteral | 3 | |
| oximorfina | rectalmente | 3 |
| parenteral | 30 b | |
| petidina | por vía oral | — |
| parenteral | 0,4 b | |
| tapentadol | por vía oral | 0,4 |
| parenteral | — | |
| tramadol | por vía oral | 0,25 |
| parenteral | 0,3 |
e A actividade da morfina oral ou intramuscularmente utilizada baséase na experiencia clínica en pacientes con síndrome de dor crónica.
b A partir de estudos cunha única administración de i / m de cada un dos analxésicos opioides enumerados anteriormente, realizados para establecer a súa actividade relativa en comparación coa morfina. As doses para a administración oral son as doses recomendadas ao pasar da vía parenteral á vía oral de administración do medicamento.
A dose inicial recomendada de Fendivia ™ dependendo da dose oral diaria de morfina (para pacientes adultos clinicamente menos estables que requiren substitución de opioides: a proporción da transición da morfina administrada oralmente ao uso transdérmico de fentanilo é de 150: 1)
| Dose diaria de morfina oral, mg / día | A dose do medicamento Fendivia ™, mcg / h |
| e En estudos clínicos, os límites indicados das doses diarias de morfina utilizáronse para calcular a transferencia do paciente a Fendivia ™. |
A dose inicial recomendada de Fendivia ™ dependendo da dose oral diaria de morfina (para pacientes adultos con terapia opioide estable e ben tolerada: a proporción da transición da morfina administrada oralmente ao uso transdérmico de fentanilo é de 100: 1)
| Dose diaria de morfina oral, mg / día | A dose do medicamento Fendivia ™, mcg / h |
| ≤44 | 12,5 |
| 45–89 | 25 |
| 90–149 | 50 |
| 150–209 | 75 |
| 210–269 | 100 |
| 270–329 | 125 |
| 330–389 | 150 |
| 390–449 | 175 |
| 450–509 | 200 |
| 510–569 | 225 |
| 570–629 | 250 |
| 630–689 | 275 |
| 690–749 | 300 |
Unha avaliación inicial do máximo efecto analxésico do medicamento Fendivia ™ pode realizarse non antes de 24 horas despois da aplicación. Esta limitación débese a que gradualmente se produce un aumento da concentración de fentanilo no soro sanguíneo nas primeiras 24 horas despois da aplicación do parche transdérmico. Polo tanto, ao pasar dun medicamento a outro, a terapia analxésica anterior debería ser interrompida gradualmente despois da aplicación da dose inicial de Fendivia ™ ata que se estabilice o seu efecto analxésico.
Selección de dose e terapia de mantemento
O parche transdérmico debe ser substituído por un novo cada 72 horas.
A dose é seleccionada individualmente ata que se consiga a relación óptima do nivel de analxésia e tolerabilidade do medicamento Fendivia ™. Normalmente, á 1 hora, a dose aumenta en 12,5 ou 25 mcg / h. Non obstante, ao axustar a dose, hai que ter en conta o estado do paciente e a necesidade de analxésia adicional (as doses orais de morfina 45 e 90 mg / día equivalen aproximadamente ás doses de 12,5 e 25 μg / h de Fendivia ™, respectivamente). Despois de aumentar a dose, o paciente pode necesitar ata 6 días para lograr unha analxésia estable.
Por iso, despois de aumentar a dose, é necesario empregar un parche transdérmico de dosificación aumentada polo menos 2 veces durante 72. Só despois disto, o seguinte aumento de dose é posible se o alivio da dor é insuficiente.
Para conseguir unha dose superior a 100 mcg / h, pódense usar varios parches transdérmicos simultaneamente. Se se produce dor progresiva, os pacientes poden necesitar ocasionalmente doses adicionais de analxésicos de acción curta. Se a dose de Fendivia ™ supera os 300 mcg / h, debe considerarse o uso de métodos adicionais ou alternativos de alivio da dor ou de vías alternativas de administración de analxésicos opioides.
Só ao comezo da terapia, se despois da aplicación da dose inicial hai unha diminución significativa no efecto analxésico, o parche pode ser substituído despois de 48 horas cun parche da mesma dosificación e despois de 72 horas pode aumentarse a dose.
Se é necesario substituír o parche transdérmico ata 72 horas (por exemplo, se o parche está desconxelado), un parche da mesma dosificación debe estar pegado a outra zona da pel. Unha situación similar pode levar a un aumento da concentración de fentanilo no plasma sanguíneo e, polo tanto, o paciente necesita un seguimento cercano.
Cando se pasa dun tratamento a longo prazo con morfina a un parche transdérmico con fentanilo, pode producirse a síndrome de retirada a pesar dun efecto analxésico adecuado. Cando se producen síntomas de abstinencia, recoméndase que os pacientes reciban morfina de acción curta en doses baixas.
Descontinuación de Fendivia ™
Se é necesario interromper o uso do parche transdérmico, entón calquera outro opioides deberá ser substituído gradualmente, comezando cunha dose baixa e aumentándoa lentamente. Isto débese a que o contido de fentanilo no soro sanguíneo despois da eliminación do parche transdérmico diminúe gradualmente. Necesítanse polo menos 20 horas para reducir o fentanil sérico nun 50%. Existe unha regra xeral: a retirada de analxésia con analxésicos opioides debe levarse a cabo paulatinamente para evitar síntomas de retirada (náuseas, vómitos, diarrea, ansiedade e tremor muscular).
Uso en pacientes anciáns
Os pacientes maiores deben ser examinados e observados con coidado. Se é necesario, a dose de Fendivia ™ debe reducirse (ver "Instrucións especiais"). En pacientes anciáns que non recibiron anteriormente opioides, Fendivia ™ só se debe usar se a prestación supera o risco. Como dosificación inicial, só se debería usar 12,5 mcg / h.
Uso en pacientes con alteración da función hepática e renal
Os pacientes con alteración da función hepática e renal deben ser examinados e controlados con atención para detectar signos dunha sobredose de fentanilo e, se é necesario, a dose de Fendivia ™ debe reducirse (ver "Instrucións especiais").
En pacientes con alteración da función hepática e renal que non recibiran anteriormente opioides, Fendivia ™ debe usarse só se o beneficio supera o risco. Como dosificación inicial, só se debería usar 12,5 mcg / h.
Uso en pacientes con febre / baixo a influencia de fontes de calor externas
Os pacientes con febre poden necesitar un axuste da dose de fentanilo (ver "Instrucións especiais").
Use en nenos a partir de 16 anos
O réxime de dosificación para nenos maiores de 16 anos é similar ao réxime de dosificación para adultos.
Uso en nenos de 2 a 16 anos
O medicamento Fendivia ™ debe usarse só naqueles nenos que xa recibiron oralmente unha cantidade equivalente de morfina nunha dosificación de polo menos 30 mg / día. Ao pasar da administración oral ou parenteral de analxésicos opioides a un parche transdérmico con fentanilo en nenos, a dose inicial calcúlase usando as táboas 1 e 4.
A dose inicial recomendada de Fendivia ™ para nenos de 2 a 16 anos a, dependendo da dose oral diaria de morfina b
| Dosis diaria oral de morfina para nenos, mg / día | A dose de Fendivia ™ para nenos, mcg / h |
| 30–44 | 12,5 |
| 45–134 | 25 |
Un Cambiar a doses de fentanilo superior a 25 mcg / h non é diferente para nenos e adultos (ver táboa 2).
b Nos ensaios clínicos empregáronse os límites indicados para as doses diarias de morfina orais para calcular a transferencia do paciente a Fendivia ™.
En dous estudos realizados en nenos, a dosificación requirida do parche transdérmico calculouse con precaución: de 30 a 44 mg / día de morfina, por vía oral ou unha cantidade equivalente doutros analxésicos opioides, substituíuse por un parche transdérmico a unha dose de 12,5 μg / h. Este esquema de transferencia para nenos úsase só cando se substitúe a morfina oral (ou o seu equivalente) por un parche transdérmico. O réxime non se pode usar para transferir fentanilo a outros analxésicos opioides, xa que neste caso pode producirse unha sobredose.
O efecto analxésico da primeira dose do parche transdérmico con fentanilo non alcanza o nivel óptimo durante as primeiras 24 horas.Por iso, durante as primeiras 12 horas despois de cambiar ao medicamento Fendivia ™, o paciente debe recibir doses previas de analxésicos. Nas próximas 12 horas, os pacientes deberán proporcionar analxésicos en función da necesidade clínica.
Dado que o nivel de fentanilo no sangue alcanza o seu valor máximo despois das 12-24 horas, recoméndase observar aos pacientes por eventos adversos, que poden incluír depresión respiratoria durante polo menos 48 horas despois de comezar a terapia parche transdérmica ou despois de aumentar a dose (ver "Instrucións especiais" )
Terapia de selección e mantemento da dose en nenos de 2 a 16 anos
O parche transdérmico debe ser substituído por un novo cada 72. A dose é seleccionada individualmente ata que se consiga a relación óptima do nivel de analxésia e tolerabilidade do medicamento Fendivia ™. Se o efecto analxésico de Fendivia ™ é insuficiente, deberase prescribir morfina ou outro analxésico de opioide de acción curta. Dependendo da necesidade adicional de anestesia e da gravidade da dor nun neno, é posible un aumento da dose. O axuste da dose debe realizarse gradualmente, con incrementos de 12,5 mcg / h. A dose non debe aumentar máis dunha vez cada 72 horas.
O parche transdérmico debe aplicarse sobre a superficie plana da pel intacta e non irradiada do tronco ou ombreiro. A parte traseira superior é o mellor lugar para aplicar un parche transdérmico en nenos pequenos. Con esta aplicación, a probabilidade de auto-eliminación do parche transdérmico é reducida por nenos.
Para a súa aplicación, recoméndase escoller un lugar cun pelo mínimo (preferiblemente sen pelo). Antes de aplicar o pelo no lugar de aplicación deberase cortar (non afeitarse). Se hai que lavar o sitio de aplicación antes de aplicar o parche transdérmico, debe facerse con auga limpa. Non use xabón, locións, aceites, alcol ou outros medios, como poden provocar irritacións na pel ou cambiar as súas propiedades. Antes da aplicación, a pel debe estar absolutamente seca.
Dado que o parche transdérmico está protexido por unha película de protección exterior impermeable, non se pode eliminar durante unha curta estancia na ducha.
Elimínase o paquete transdérmico do paquete dobrando unha parte entallada preto da punta da frecha e rasgando coidadosamente o material do paquete.
O parche transdérmico debe aplicarse inmediatamente despois da retirada do paquete, sen tocar o seu lado adhesivo. Despois de eliminar a película protectora, o parche transdérmico debe estar presionado firmemente coa palma da man ata o lugar de aplicación durante uns 30 segundos. Asegúrese de que o parche transdérmico estea ben pegado á pel, especialmente arredor dos bordos. Pode ser necesaria unha corrección adicional de parches. A continuación, lave as mans con auga limpa.
O parche debe ser usado continuamente durante 72 horas, despois de que se debe substituír por un novo parche transdérmico. Un novo parche transdérmico debe aplicarse sempre sobre outra zona da pel, sen captar o lugar da aplicación anterior. No mesmo lugar de aplicación, o parche transdérmico pódese aplicar de novo non antes de 7 días.
Inspeccione o parche transdérmico antes do uso.
Non se debe dividir ou cortar o parche transdérmico (ver "Instrucións especiais").
Sobredose
Unha sobredose de fentanilo maniféstase en forma de aumento dos seus efectos farmacolóxicos, o máis grave é a depresión respiratoria.
Síntomas letarxia, coma, depresión do centro respiratorio con respiración e / ou cianose de Cheyne-Stokes. Outros síntomas poden incluír hipotermia, diminución do ton muscular, bradicardia, hipotensión arterial. Os signos de toxicidade inclúen sedación profunda, ataxia, miose, convulsións e depresión respiratoria.
Tratamento: eliminación do parche transdérmico, administración dun antagonista específico - naloxona, efectos físicos ou verbais sobre o paciente, terapia de funcións vitais sintomáticas e de apoio (incluída a administración de relaxantes musculares, ventilación mecánica, con bradicardia - administración de atropina, cunha marcada diminución da presión arterial - reposición de BCC )
A dose inicial recomendada para adultos é de 0,4-2 mg de naloxona iv. Se é necesario, pode dar a mesma dose cada 2-3 minutos ou prescribir unha administración a longo prazo de 2 mg de naloxona disolta en 500 ml de solución de cloruro sódico ao 0,9% ou solución de destrosa ao 5% (0,004 mg / ml). A taxa de administración debe axustarse tendo en conta as infusións anteriores de bolus e a resposta individual do paciente.
Se a administración intravenosa non é posible, entón a naloxona pode administrarse intramuscularmente ou s.c. Despois da administración de i / m ou s / c de naloxona, o inicio da acción será máis lento en comparación coa administración de i / v. A administración intramuscular dá un efecto máis prolongado que a administración intravenosa.
A depresión respiratoria por sobredosis pode persistir máis tempo que o efecto dun antagonista de opioides. Eliminar o efecto analxésico pode orixinar un aumento da dor aguda e a liberación de catecolaminas. Se é necesario, o paciente debe ser atendido na unidade de coidados intensivos.
Forma de dosificación:
sistema terapéutico transdérmico (TTC)
Substancia activa:
Fendivia ™ 12,5 μg / h: Cada TTC contén 1,38 mg de fentanil nun parche de 4,2 cm² e libera fentanilo a unha velocidade de 12,5 μg / h.
Fendivia ™ 25 μg / h: Cada TTC contén 2,75 mg de fentanilo nun parche de 8,4 cm² e libera fentanilo a unha velocidade de 25 μg / h.
Fendivia ™ 50 μg / h: Cada TTC contén 5,50 mg de fentanil nun parche de 16,8 cm² e libera fentanilo a unha velocidade de 50 μg / h.
Fendivia ™ 75 μg / h: Cada TTC contén 8,25 mg de fentanil nun parche de 25,2 cm² e libera fentanilo a unha velocidade de 75 μg / h.
Fendivia ™ 100 μg / h: Cada TTC contén 11,00 mg de fentanil nun parche de 33,6 cm² e libera fentanilo a unha velocidade de 100 μg / h.
Excipientes:
1) Filme protector exterior:
- película de polietileno tereftalato,
2) A capa de depósito:
- capa de adhesivo de silicona,
- dimeticona (E 900),
3) Microreservas que conteñen a substancia activa:
- dipropilenglicol,
- Hipólose (E 463),
4) Membrana de liberación:
- copolímero de etileno e acetato de vinilo,
5) Capa adhesiva da pel:
- capa de adhesivo de silicona,
- dimeticona (E 900),
6) Película extraíble de protección:
- unha película de poliéster con revestimento de polímero con fluor.
Un parche translúcido rectangular con bordos redondeados sobre unha película protectora transparente extraíble. A película protectora é máis grande que o parche. Unha incisión sinusoidal divide a película protectora extraíble en dúas partes.
As seguintes etiquetas aplícanse ao parche mediante impresión a cor:
1) Fendivia ™ 12,5 μg / hora, parche 18 ± 0,5 mm de ancho, 24 ± 0,5 mm de lonxitude:
- "Fentanil 12,5 μg / hora" - impresión marrón,
2) Fendivia ™ 25 μg / h, parche 24,6 ± 0,5 mm de ancho, 37 ± 0,5 mm de largo:
- "Fentanyl 25 μg / hour" - impresión en vermello,
3) Fendivia ™ 50 μg / h, parche de 34 ± 0,5 mm de ancho, 51,3 ± 0,5 mm de largo:
- "Fentanyl 50 μg / hour" - impresión verde,
4) Fendivia ™ 75 mcg / h, parche 42 ± 0,5 mm de ancho, 61,7 ± 0,5 mm de longo:
- "Fentanyl 75 μg / hour" - impresión azul claro,
5) Fendivia ™ 100 μg / hora, parche 49 ± 0,5 mm de ancho, 70 ± 0,5 mm de lonxitude:
- "Fentanyl 100 μg / hora" - impresión gris.
Propiedades farmacolóxicas
Farmacodinámica
Fendivia ™ é un parche transdérmico que proporciona unha inxestión sistémica continua de fentanilo durante 72 horas. O fenanilo é un analxésico de opioides con afinidade principalmente para os receptores de opio μ do sistema nervioso central (SNC), medula espiñal e tecidos periféricos. Aumenta a actividade do sistema antinociceptivo, aumenta o limiar de sensibilidade á dor. A droga Fendivia ™ ten efectos analxésicos e sedativos. O fentanyl ten un efecto deprimente no centro respiratorio, retarda o ritmo cardíaco, excita os centros n. vago e centro de vómitos, aumenta o ton dos músculos lisos do tracto biliar, esfínters (incluída a uretra, a vexiga e o esfínter de Oddi), mellora a absorción de auga do tracto gastrointestinal (GIT). Baixa a presión arterial (BP), a motilidade intestinal e o fluxo sanguíneo renal.
No sangue, aumenta a concentración de amilase e lipase, reduce a concentración de hormona de crecemento, catecolaminas, hormona adrenocorticotrópica, cortisol, prolactina. Promove a aparición do sono (principalmente en relación coa eliminación da dor). Causa euforia. A taxa de desenvolvemento da dependencia das drogas e a tolerancia aos efectos analxésicos ten diferenzas individuais significativas. A diferenza doutros analxésicos opioides, provoca significativamente menos reaccións de histamina.
Farmacocinética
A concentración analxésica efectiva mínima de fentanilo no soro sanguíneo en pacientes que non usaron anteriormente analxésicos opioides é de 0,3-1,5 ng / ml. A frecuencia de efectos indesexables en tales pacientes aumenta cunha concentración de fentanilo no soro sanguíneo por encima de 2 ng / ml. Co desenvolvemento da tolerancia, aumenta tanto a concentración analxésica efectiva mínima de fentanilo como a concentración á que se producen reaccións indesexables.
Aspiración: despois da primeira aplicación do parche transdérmico, a concentración de fentanilo no soro sanguíneo aumenta gradualmente, normalmente nivelando entre 12 e 24 horas, e permanece relativamente constante durante o resto de 72 horas. Coa segunda aplicación de 72 horas do parche transdérmico, conséguese unha concentración constante de fentanilo no soro sanguíneo, que permanece durante as aplicacións posteriores do parche do mesmo tamaño. A concentración de fentanilo no sangue é proporcional ao tamaño do parche transdérmico. A absorción de fentanilo pode variar lixeiramente segundo o lugar da aplicación. Observouse unha absorción lixeiramente reducida de fentanilo (aproximadamente un 25%) en estudos realizados con voluntarios sans durante a aplicación do parche no peito en comparación coa aplicación no brazo superior e na parte traseira.
Distribución: O fentanilo únese nun 84% ás proteínas do plasma, atravesa a barreira hematoencefálica, a placenta e no leite materno.
Metabolismo: O fentanilo ten unha cinética lineal de biotransformación e metabolízase principalmente no fígado mediante enzimas CYP3A4. O principal metabolito do fentanilo é o norfentanil, que non está activo.
Retirada: despois da eliminación do parche transdérmico, a concentración de fentanilo no soro sanguíneo diminúe gradualmente. A semivida de fentanilo despois da aplicación do parche transdérmico é de 17 horas (13-22 horas) nos adultos e 22-25 horas nos nenos. A absorción continuada de fentanilo da superficie da pel provoca unha excreción máis lenta da droga do soro sanguíneo en comparación coa administración intravenosa.
Ao redor do 75% do fentanilo excrétase na urina, principalmente en forma de metabolitos, menos do 10% - sen cambios. Ao redor do 9% excrétase en feces, principalmente en forma de metabolitos.
Grupos especiais de pacientes
A alteración da función hepática ou renal pode causar un aumento da concentración sérica de fentanil. En pacientes anciáns, debilitados ou debilitados, é posible unha diminución da eliminación do fentanilo, o que pode levar a unha vida media máis longa de fentanilo.
Nenos
Dependendo do peso corporal, a limpeza (l / h / kg) é superior ao 82% en nenos de 2 a 5 anos e un 25% maior en nenos de 6 a 10 anos en comparación con nenos de 11 a 10 anos 16 anos que teñen o mesmo despacho que os adultos.
Uso durante o embarazo e durante a lactación
Embarazo
Non se estableceu a seguridade dos parches transdérmicos con fentanilo durante o embarazo. Estudos en animais estableceron algunha toxicidade reprodutiva.
Fentanyl debe usarse só durante o embarazo se é necesario. O uso a longo prazo durante o embarazo pode causar "síndrome de retirada" nos recentemente nados. Moi poucas veces se informou da presenza de síntomas de "síndrome de retirada" en recentemente nados cuxas nais empregaron constantemente un parche transdérmico con fentanilo durante o embarazo.
O fentanyl non se debe usar durante o parto e parto (incluída a cesárea), como pasa pola placenta e pode provocar depresión respiratoria no feto ou no recentemente nado.
A lactación materna
O fenanil se excreta no leite materno e pode provocar efectos sedantes e depresión respiratoria nun bebé amamantado. Polo tanto, se é necesario, a cita do medicamento Fendivia ™ durante a lactación debería deixar de amamantar (durante todo o tempo de uso e polo menos 72 horas despois do último uso).
Efecto secundario
A seguridade dos parches transdérmicos con fentanilo avaliouse en 1565 adultos e 289 nenos que participaron en 11 estudos clínicos sobre o uso do fármaco para o tratamento da dor crónica de xénese oncolóxica e non oncolóxica. Estes pacientes recibiron polo menos unha dose dun parche transdérmico con fentanilo, tras o que se evaluou a seguridade do fármaco. Con base nos datos de seguridade combinados de ensaios clínicos, os acontecementos adversos máis comúns (cunha frecuencia de polo menos o 10%) foron náuseas (35,7%), vómitos (23,2%), estreñimiento (23,1 %), somnolencia (15,0%), mareos (13,1%) e dor de cabeza (11,8%). Proponse un medicamento en forma de solución para inxección (administrada por vía intravenosa e intramuscular). Á venda pode atopar un parche transdérmico. O fenanil actúa como un composto activo. Ofrécense diferentes versións da droga. A dosificación da sustancia activa pode variar (mg): 1,38, 2,75, 5,5, 8,25, 11. A intensidade da liberación de fentanilo tamén varía (μg / h): 12,5, 25, 50, 75, 100. O parche está cuberto cunha película protectora, contén outras substancias na composición: Hai unha serie de restricións relativas ao uso:
As reaccións adversas clasifícanse segundo a frecuencia de aparición:
Moi frecuente (> 1/10)
Frecuente (> 1/100, 1/1000, 1 / 10.000,Formas e composición de liberación
Con coidado
Fabricante
LTS Lohmann Therapy System AG. Lohmannstrasse 2, D-56626, Andernach, Alemaña. LTS Lohmann Therapie-Systeme AG. Lohmannstrasse, 2, D-56626 Andernach, Alemaña.
Titular do certificado de rexistro: Takeda Pharma A / S. Dubendal Alle 10, 2630 Taastrup, Dinamarca. Takeda Pharma A / S. Dybendal Alle 10, 2630 Taastrup, Dinamarca.
As reclamacións dos consumidores deben enviarse a: Takeda Pharmaceuticals LLC. 119048, Moscú, r. Usacheva, 2, p. 1.
Tel .: (495) 933-55-11, fax: (495) 502-16-25.
Como usar Fendivia
A dosificación do compoñente activo determínase individualmente. A cantidade de fentanilo depende da condición do paciente, da presenza / ausencia de experiencia co uso precoz de analxésicos estupefacientes. Cando se usa o parche, limpase e secase o instrumento externo. Non se deben usar deterxentes, a auga limpa é suficiente. A pel non debe deformarse.
A dose inicial é de 12,5 ou 25 mg. A continuación, increméntase con cada parche novo. A cantidade diaria máxima de fentanilo é de 300 mg. Se é necesario aumentar a dose, considere fondos en forma líquida. Para evitar signos de retirada, recoméndase reducir lentamente a cantidade de sustancia activa.
Como cambiar
A duración de uso dun parche é de 72 horas. Despois faise unha substitución. Se o efecto terapéutico é débil, o produto cambia despois de 48 horas. Ademais, o seguinte parche está instalado nun novo lugar. Se non se ten en conta esta recomendación, a concentración de fentanilo aumenta. No proceso de retirar o parche, debe ser dobrado con superficies pegajosas cara ao interior e desfacerse.

Con diabetes, pódese usar a droga, pero segundo o médico.
Tracto gastrointestinal
Náuseas seguidas de vómitos, dor abdominal, alteración das feces, diminución da dixestión, secas mucosas da boca. Poucas veces ocorren síntomas de obstrución intestinal.

Tomar Fendivia pode levar á perda de apetito.
Forma e composición de liberación
A droga prodúcese baixo a forma dun sistema terapéutico transdérmico (TTC): un parche rectangular translúcido con bordes redondeados sobre unha película protectora transparente extraíble, máis grande que o parche, a película protectora está dividida en dúas partes por unha incisión sinusoidal, parches 12.5 / 25/50 / 75/100 μg / h teñen unha lonxitude de 24/37 / 51,3 / 61,7 / 70 mm (± 0,5 mm cada unha) e un ancho de 18 / 24,6 / 34/42/49 mm (± 0,5 mm cada un, respectivamente, as seguintes etiquetas aplícanse aos parches mediante impresión a cor (segundo a velocidade de liberación da sustancia activa): 12,5 μg / h - marrón Fentanilo 12,5 μg / hora, 25 μg / h - Fentanilo 25 μg / hora vermello, 50 μg / h - Fentanilo 50 μg / hora verde, 75 μg / h - Fentanilo 75 μg / hora azul claro , 100 μg / h - gris Fentanyl 100 μg / hora cada TTS é envasado nunha bolsa termosilível de aluminio, papel e poliacrilonitrilo (PAN), nunha caixa de cartón 5 bolsas e instrucións para o uso de Fendivia.
Composición para 1 parche (TTC):
- compoñente activo: fentanilo, cuxo contido en 1 TTC é: 1,38, 2,75, 5,5, 8,25 ou 11 mg nun parche cunha taxa de liberación de 12,5, 25, 50, 75 e 100 μg / h e cunha superficie de contacto de 4,2, 8,4, 16,8, 25,2 e 33,6 cm², respectivamente
- película extraíble de protección: película de poliéster con revestimento de polímero que conteña flúor,
- película de protección exterior: película de polietileno tereftalato (película PET),
- micro tanques, incluído o compoñente activo: hiprolosa (E463), dipropilenglicol,
- capa de depósito / adhesivo para a pel: dimeticona (E900), capa adhesiva de silicona,
- membrana de liberación: un copolímero de acetato de vinilo e etileno.
Uso durante o embarazo e a lactación
A droga está prescrita, pero como último recurso. Úsase por razóns de saúde, cando os beneficios son máis substanciais que o posible dano. Con terapia durante o embarazo, hai o risco de desenvolver a retirada no bebé despois do parto.
Dado que o medicamento entra no leite materno e a través da placenta, o risco de desenvolver síntomas negativos no neno é bastante alto.
Uso na vellez
Durante o tratamento, o proceso de eliminación do fentanil ralentízase. Isto leva a un aumento gradual da súa concentración. Por este motivo, a dose debe revisarse. A droga está aprobada para o seu uso só se o beneficio supera o dano. O tratamento debe comezar cunha dose de 12,5 mg.

Na vellez, o medicamento está aprobado para o seu uso só se a prestación supera o dano.
Comentarios sobre Fendivia
A avaliación de consumidores e especialistas permitirá facer unha opinión máis completa sobre o medicamento.
Danilov I.I., oncólogo, 49 anos, Vladivostok
A ferramenta cumpre a súa función: elimina a dor. As desvantaxes inclúen a baixa velocidade de acción, xa que o fentonil se libera gradualmente: primeiro penetra na estrutura do integumento exterior e só despois no sangue. A pesar da súa forma, este remedio pode ser perigoso debido a trastornos do sistema inmunitario (desenvólvense reaccións anafilactoides).
Verilova A.A., cirurxiá, de 53 anos, San Petersburgo
Eu uso a droga raramente debido á forma inconveniente. Actúa lentamente. Ademais, o custo é elevado. Se consideramos as súas propiedades principais, a eficacia desta ferramenta non é inferior aos análogos noutras formas.
Fentanyl parches en vez de pastillas
Eugenio, 33 anos, Penza
A droga é bastante perigosa, como a maioría dos opiáceos. Algún tempo despois do inicio da terapia, deixou de axudar. Lin sobre o posible desenvolvemento da tolerancia á sustancia activa, pero non penso que un analgésico estupefaciente puidese deixar de cumprir tan rápido a súa función. Tiven que cambiar a un analóxico.
Veronika, 39 anos, Moscova
Con oncoloxía, axuda mal. O efecto é de curta duración, despois do que é necesario cambiar o parche un pouco antes, o que é un problema, porque non se pode aplicar máis de 1 vez dentro de 48 horas. Por este motivo, o médico prescribiu outro medicamento.
Fendivia, instrucións de uso: método e dosificación
O parche de Fendivia úsase de forma transdérmica.
O fenanil libérase a unha velocidade de 12,5, 25, 50, 75 ou 100 μg / h, que é aproximadamente 0,3, 0,6, 1,2, 1,8 ou 2,4 mg por día, respectivamente.
A dosificación determínase individualmente, dependendo da condición do paciente, e débese avaliar regularmente despois de cada uso. É necesario aplicar a dose mínima efectiva.
Recoméndase aplicar un parche que conteña fentanilo sobre a superficie plana e non danada da pel do ombreiro ou do tronco. Os nenos pequenos deberían pegalo na parte superior das costas para reducir o risco de auto-eliminación.
O sitio para a aplicación debe ser elixido cunha liña mínima de pelo. Antes de aplicar TTS, o pelo no sitio de solicitude debe ser cortado (sen afeitar). Se é necesario lavar o lugar de aplicación antes de pegar o parche, debe facerse con auga limpa. Non se recomenda o uso de locións, xabón, alcohol, aceites ou outros produtos, porque poden provocar irritacións na pel ou un cambio nas súas propiedades. Antes do procedemento, a pel debe estar absolutamente seca. Dado que o parche está cuberto cunha película de protección impermeable, non a pode eliminar cunha ducha curta.
Inmediatamente despois de retirar o parche da bolsa impermeable e eliminar a película protectora, aplícaa na pel sen tocar o lado pegajoso e presione firmemente contra o lugar de aplicación coa palma durante aproximadamente 30 segundos. O TTS debe axustarse perfectamente á pel, especialmente arredor dos bordos, se é necesario, fixalo adicionalmente e despois lavar as mans con auga limpa.
Fendivia está deseñado para uso continuo durante 72 horas. Sempre é necesario aplicar un parche novo a outra zona da pel sen usar o lugar da aplicación anterior. Pegar o parche no mesmo sitio pode repetirse antes de 7 días.
A dose inicial establécese tendo en conta o nivel de inxestión de opioides no período anterior á terapia con Fendivia, o risco de desenvolver a tolerancia, o tratamento concomitante con outros fármacos, a saúde xeral do paciente e o seu estado médico, é dicir, a idade, o peso corporal, o grao de esgotamento e a gravidade da lesión.
Os pacientes que non foron tratados previamente con opioides non se lles recomenda un método transdérmico do seu uso, neste caso, debe recorrer á administración oral e parenteral de fármacos. Para previr a sobredose, deben empregar doses iniciais baixas de opioides de liberación inmediata (incluíndo tramadol, oxicodona, hidromorfono, morfina e codeína). A dose destes fármacos para adultos é necesaria para titularse de xeito que, segundo a efectividade do efecto analxésico, corresponda a 12,5 / 25 μg / h de Fendivia. No futuro, os pacientes poderán facer a transición ao uso dun parche transdérmico.
No caso de que a administración oral de opioides estea contraindicada ou inaceptable e se recoñeza o uso de TTC como único método posible de terapia, é necesario comezar o tratamento coa dose máis baixa - 12,5 μg / h.
Ao cambiar a un parche transdérmico, para un paciente que utilizou opioides oral / parenteral no período anterior, é necesario establecer a cantidade de analxésicos opioides recibidos anteriormente, que precisou nas últimas 24 horas (mg / día). A dose resultante debe converterse á dose diaria oral equivalente de morfina (mg / día) usando o coeficiente adecuado.
A dose equivalente de morfina establécese multiplicando a dose de analxésicos de opioides polos seguintes factores (opioide anteriormente usado en coeficiente mg / día ×) usado para recalcular a dose diaria para administración oral / parenteral:
- morfina - 1 a / 3,
- fentanilo - - / 300,
- codeína - 0,15 / 0,23 b,
- diamorfina - 0,5 / 6 b,
- cetobemidona - 1/3,
- hidromorfono - 4/20 b,
- levorfanol - 7,5 / 15 b,
- oxicodona: 1,5 / 3,
- petidina - - / 0,4 b,
- tramadol - 0,25 / 0,3,
- tapentadol - 0,4 / -,
- metadona - 1,5 / 3 b.
a - actividade de morfina obtida por vía oral ou intramuscular (IM) en función da experiencia clínica en pacientes con síndrome de dor crónica.
b - segundo os resultados de estudos obtidos cunha única inxección intramuscular de cada un destes fármacos para determinar a súa actividade relativa en comparación coa morfina, as doses orais son as doses recomendadas ao pasar de vía parenteral a vía de administración oral.
Establécese a dose inicial adecuada de fentanilo dependendo da dose diaria oral de morfina.
Para pacientes adultos clínicamente menos estables que necesitan substitución de opioides, recoméndase a seguinte transición dunha dose diaria de morfina oral a unha dose de fentanilo transdérmico cunha relación de transición de 150 ÷ 1 morfina (mg / día) - fentanilo (μg / h):
- menos de 90 a 12,5,
- 90–134 – 25,
- 135–224 – 50,
- 225–314 – 75,
- 315–404 – 100,
- 405–494 – 125,
- 495–584 – 150,
- 585–674 – 175,
- 675–764 – 200,
- 765–854 – 225,
- 855–944 – 250,
- 945–1034 – 275,
- 1035–1124 – 300.
Para pacientes adultos que toman un tratamento estable ben tolerado con opioides, recoméndase a seguinte transición da dose diaria de morfina oral á dose de fentanilo transdérmico cunha proporción de transición de 100 ÷ 1 morfina (mg / día) - fentanil (μg / h):
- menos de 44 - 12,5,
- 45–89 – 25,
- 90–149 – 50,
- 150–209 – 75,
- 210–269 – 100,
- 270–329 – 125,
- 330–389 – 150,
- 390–449 – 175,
- 450–509 – 200,
- 510–569 – 225,
- 570–629 – 250,
- 630–689 – 275,
- 690–749 – 300.
A avaliación inicial do máximo efecto analxésico de Fendivia debe realizarse non antes de 24 horas despois da aplicación. O motivo desta limitación é un aumento gradual da concentración de fentanilo no soro sanguíneo nas primeiras 24 horas despois de aplicar o parche. Como resultado, durante a transición dun medicamento analxésico a outro, a terapia anterior debería deterse paulatinamente, despois da aplicación da dose inicial de fentanilo e ata a estabilización do seu efecto analxésico.
O TTC debe substituírse por un novo cada 72 horas. A valoración da dose de mantemento realízase individualmente ata que se consiga un nivel adecuado de analxésia, tendo en conta a tolerabilidade do fármaco. Por regra xeral, a dose pode aumentarse cada vez en 12,5 ou 25 μg / h, dependendo da condición do paciente e da necesidade de analxésia adicional (morfina oral a doses de 45 e 90 mg / día é aproximadamente equivalente a Fendivia a doses de 12,5 e 25 μg / h, respectivamente). A analxésia estable pode ocorrer 6 días despois de aumentar a dose. Polo tanto, despois de axustar a dose, requírese usar un parche de dosificación polo menos 2 veces durante 72 horas, e só entón, se é necesario, aumentar o seu seguinte aumento.
Para conseguir unha dose superior a 100 μg / h, permítese o uso simultáneo de varios yesos. Cando aparece dor de avance, pode ser necesario prescribir doses adicionais de analxésicos de acción curta. Cando se usa Fendivia nunha dose superior a 300 μg / h, hai que considerar a posibilidade de usar analxésicos adicionais / alternativos ou métodos de administración de analxésicos opioides.
Ao comezo do curso da terapia, no caso dunha diminución significativa do efecto analxésico despois da aplicación da dose inicial, despois de 48 horas o parche pódese substituír por outro similar e despois de 72 horas pódese aumentar a dose.
Se o parche se descolocou ou hai que substituílo por outro motivo antes de que pasasen as 72 horas, pódese pegar un parche cunha dose similar a outra zona da pel. Neste caso, a condición do paciente debe controlarse coidadosamente debido ao risco de aumento da concentración plasmática do medicamento.
No contexto da transición da terapia prolongada con morfina ao tratamento cun parche transdérmico, pode producirse a síndrome de retirada, incluso cun efecto analxésico adecuado. Se se produce este trastorno, recoméndase seguir administrando morfina de acción curta en doses baixas.
Se é necesario interromper a terapia cun parche transdérmico, debe substituírse por outros opioides gradualmente, comezando cunha dose baixa, debido á lenta diminución do fentanil sérico despois de eliminar o parche e a ameaza de retirada. Para reducir a concentración de fentanilo no sangue nun 50%, necesítanse polo menos 17 horas.
En nenos e adolescentes de 2 a 16 anos, Fendivia pódese usar só nos casos en que os pacientes xa tomaron oralmente morfina en cantidades equivalentes (a unha dose de polo menos 30 mg / día). Ao pasar do uso oral / parenteral de analxésicos opioides a un parche con fentanilo, a dose inicial en nenos calcúlase dependendo da dose oral diaria de morfina. Fendivia a unha dose de 12,5 e 25 μg / h é equivalente á morfina a unha dose oral de 30-44 e 45-134 mg / día, respectivamente. A transición en nenos ao uso de fentanilo en doses superiores a 25 μg / h non difire da que en pacientes adultos.
Cun único parche transdérmico de 12,5 μg / h, só se pode substituír morfina cando se toma por vía oral a unha dose de 30-44 mg / día ou outros analxésicos opioides nunha cantidade equivalente. Este esquema non se pode usar para transferir aos nenos do uso de fentanilo a outros analxésicos opioides debido á posible aparición dunha sobredose.
Dado que o efecto analxésico da dose inicial do parche durante as primeiras 24 horas non chega a un nivel adecuado, despois de pasar ao tratamento con Fendivia, os nenos deberían recibir analxésicos previos na cantidade habitual. Durante as próximas 12 horas, pódense utilizar analxésicos utilizados anteriormente cando sexa clínicamente necesario. A dose establécese individualmente, despois do inicio do tratamento, o parche debe ser substituído por un novo cada 72 horas. Se precisa aumentar a dose, a súa corrección en nenos realízase gradualmente, en incrementos de 12,5 μg / h, sen aumentar con máis frecuencia que 1 vez en 72 horas. En caso de insuficiencia de acción analxésica, é posible o uso adicional de morfina ou doutro analxésico opioide de acción curta.
Embarazo e lactación
Non hai datos que confirmen a seguridade de Fendivia durante o embarazo. No curso do estudo sobre animais, revelouse unha certa toxicidade reprodutiva. O uso prolongado de parches transdérmicos con fentanilo durante o embarazo pode provocar a aparición da síndrome de retirada en recentemente nados. Rexistráronse informes separados sobre os síntomas existentes deste síndrome en recentemente nados cuxas nais usaron constantemente TTC durante o embarazo.
O uso de fentanilo durante o embarazo só se permite en caso de emerxencia. Fendivia non se recomenda para o seu uso durante o parto e o parto (incluso a través dunha cesárea), xa que o medicamento penetra na placenta e pode provocar depresión respiratoria no feto / recentemente nado.
A droga detéctase no leite materno e pode causar depresión respiratoria e sedación nun bebé amamantado. A este respecto, se é necesario empregar Fendivia durante a lactación, é necesario interromper a lactación (durante todo o período de uso, así como durante un período de 72 horas despois da última aplicación).
Uso na infancia
O uso de TTC en nenos menores de 2 anos está contraindicado, xa que non hai datos que confirmen a seguridade e eficacia da terapia. Recoméndase aos adolescentes maiores de 16 anos un réxime de dosificación similar ao dos pacientes adultos.
Non se debe administrar Fendivia a nenos maiores de 2 anos que non recibiran previamente tratamento con analxésicos opioides. O uso do medicamento só é posible se os nenos teñen tolerancia aos opioides. Teña en conta que existe a ameaza potencial de depresión respiratoria grave ou con risco de vida independentemente da dose recibida. Recoméndase supervisar aos pacientes para o desenvolvemento de eventos adversos durante polo menos 48 horas despois do inicio do tratamento ou despois de aumentar as doses.
Ao escoller o sitio de aplicación, deberase ter coidado e vixiar coidadosamente como se pega o parche para evitar que o neno deglome accidentalmente.
Con alteración da función hepática
Dado que a transformación metabólica do fentanilo ocorre no fígado, en presenza de alteración da función hepática, é posible unha diminución da taxa da súa excreción.
Debido ao risco de sobredose potencial con trastornos funcionais existentes do fígado, os pacientes deben ser monitorados durante a terapia. Se é necesario, pode ser necesaria unha redución da dose de fentanilo.
A dose inicial de Fendivia non debe superar os 12,5 mcg / h.
Interacción farmacolóxica
- derivados do ácido barbitúrico: o risco de depresión respiratoria agrávase, esta combinación está contraindicada,
- inhibidores do citocromo P450 3A4 (CYP3A4) - nefazodona, nelfinavir, eritromicina, voriconazol, fluconazol, claritromicina, cetoconazol, ritonavir, itraconazol, cimetidina, verapamil, amiodarona, aumenta a concentración de sangue ou aumenta a concentración de sangue ou aumenta a concentración de plasma ou pode acción, e tamén aumenta a probabilidade de reaccións adversas, incluída a depresión respiratoria grave. É necesario vixiar o paciente e, se é necesario, reducir a dose de fentanilo ou deixar o seu uso e, a falta de un control minucioso, evite esta combinación de fármacos. O intervalo entre o cesamento da terapia con inhibidores de CYP3A4 e a primeira aplicación do parche debe ser de polo menos 48 horas,
- Indutores de CYP3A4 - fenobarbital, carbamazepina, rifampicina, fenitoína: a concentración de fentanilo no plasma diminúe e o seu efecto terapéutico se debilita, como resultado do que se pode facer un axuste da dose. Esta combinación require coidados especiais. Se o tratamento concomitante cun indutor de CYP3A4 é cancelado, pode ser necesario reducir a dose de fentanilo e controlar o paciente,
- Supresores do SNC - anestésicos xerais, outros opioides, hipnóticos e sedantes, derivados de fenotiazina, relaxantes musculares, tranquilizantes, alcohol, antihistamínicos con efecto calmante: poden producirse efectos sedativos aditivos, pode producirse hipotensión, hipoventilación, sedación profunda / coma, coidado. observación da afección
- fármacos serotonérxicos - inhibidores selectivos da recaptación de serotonina (ISRS), inhibidores selectivos da recaptación de serotonina e noradrenalina (ISRS), inhibidores da MAO: esta combinación non se recomenda debido á ameaza de desenvolver o síndrome da serotonina. Cando se combina con MAO, tamén é posible aumentar o efecto dos analxésicos narcóticos,
- nalbuphine, buprenorfina, pentazocina: o efecto analxésico se debilita, pode aparecer síndrome de retirada en pacientes con dependencia de opioides, non se recomenda a combinación,
- relaxantes musculares con actividade vagolítica (incluído o bromuro de pancuronio): o risco de hipotensión arterial e bradicardia é reducido (especialmente cando se usa beta-bloqueantes e outros vasodilatadores) e a ameaza de hipertensión arterial e taquicardia agrávase,
- relaxantes musculares que non presentan actividade vagolítica (succinilcolina): o risco de trastornos graves do CCC agrávase, o risco de bradicardia e hipotensión arterial (especialmente con un historial cardiolóxico debilitado) non diminúe.
Os análogos de Fendivia son: Lunaldin, Durogezik Matrix, Fentanyl, Dolforin, Fentadol Reservoir, Fentadol Matrix, Fentanyl M Sandoz.
O prezo de Fendivia nas farmacias
O prezo de Fendivia por un paquete que conteña 5 xeso (TTS) pode ser:
- dose de 12,5 mcg / h - 1700 rub.,
- dose de 25 mcg / h - 2100 rublos.,
- dose de 50 mcg / h - 3100 rublos.,
- dose de 75 mcg / h - 3800 rub.,
- dose de 100 mcg / h - 4500 rublos.

Educación: Primeira Universidade Médica Estatal de Moscova chamada I.M. Sechenov, especialidade "Medicina Xeral".
A información sobre o medicamento está xeneralizada, proporcionada con fins informativos e non substitúe as instrucións oficiais. A auto-medicación é perigosa para a saúde!
Segundo as estatísticas, o luns o risco de lesións nas costas aumenta un 25% e o risco de ataque cardíaco - un 33%. Teña coidado.
Nun esforzo para sacar o paciente, os médicos adoitan ir demasiado lonxe. Así, por exemplo, un tal Charles Jensen no período comprendido entre 1954 e 1994. sobreviviron a máis de 900 operacións de eliminación de neoplasia.
Científicos estadounidenses realizaron experimentos con ratos e concluíron que o zume de sandía impide o desenvolvemento de aterosclerose dos vasos sanguíneos. Un grupo de ratos bebía auga simple e o segundo un zume de sandía. Como resultado, os vasos do segundo grupo estaban libres de placas de colesterol.
Se o fígado deixase de funcionar, a morte ocorrería dentro dun día.
Pásanse máis de 500 millóns de dólares ao ano en medicamentos contra a alerxia só nos Estados Unidos. ¿Aínda crees que se atopará unha forma de derrotar as alerxias?
Durante a operación, o noso cerebro gasta unha cantidade de enerxía igual a unha lámpada de 10 vatios. Así que a imaxe dunha lámpada encima da túa cabeza no momento da aparición dun pensamento interesante non está tan lonxe da verdade.
Se sorrí só dúas veces ao día, podes baixar a presión arterial e reducir o risco de ataques cardíacos e golpes.
O coñecido medicamento "Viagra" foi desenvolvido orixinalmente para o tratamento da hipertensión arterial.
Durante os estornudos, o noso corpo deixa de funcionar completamente. Ata o corazón se detén.
Se caes dun burro, é máis probable que lle rodes o pescozo que se caes dun cabalo. Simplemente non intente refutar esta afirmación.
Con visitas regulares á cama de bronceado, a posibilidade de padecer cancro de pel aumenta nun 60%.
Dentistas apareceron relativamente recentemente. No século XIX era obriga dun perruqueiro común sacar os dentes enfermos.
No 5% dos pacientes, o antidepresivo clomipramina provoca un orgasmo.
As persoas acostumadas a almorzar regularmente son moito menos propensas a ser obesas.
James Harrison, residente australiano de 74 anos, converteuse nun doador de sangue preto de 1.000 veces. Ten un tipo de sangue raro, cuxos anticorpos axudan a sobrevivir aos recentemente nados con anemia grave. Así, o australiano salvou preto de dous millóns de nenos.
A falta parcial de dentes ou incluso a adentia completa pode ser o resultado de lesións, cariñas ou enfermidades das encías. Non obstante, os dentes perdidos pódense substituír por próteses.