Pankreatite crónica e diabetes
| Título | Medicina |
| Ver | abstracto |
| Lingua | Ruso |
| Data engadida | 19.06.2015 |
Facultade de Formación Continuada e Formación Profesional de Especialistas
Departamento de Terapia, Endocrinoloxía e Medicina de Emerxencias
“Diabetes mellitus por pancreatite aguda ou crónica”
diabetes de pancreatite
1. O lugar da diabetes pancreatogénica en varias clasificacións da diabetes
2. A patoxénese da diabetes por pancreatite aguda ou crónica
3. A prevalencia de diabetes por pancreatite aguda ou crónica
4. Manifestacións clínicas de diabetes por pancreatite aguda ou crónica
4.1 Complicacións crónicas da diabetes mellit pancreatogénica
5. Diagnóstico da diabetes con pancreatite crónica
6. Aspectos terapéuticos da diabetes mellit pancreatogénica
A diabetes mellitus, secundaria a enfermidades da parte exocrina do páncreas, ou a diabetes pancreatogénica, é un estado de hiperglicemia persistente, que se produce como consecuencia dunha enfermidade pancreática adquirida, na que se produce unha violación de funcións pancreáticas tanto exocrinas como endocrinas. Os pacientes adoitan desenvolver síntomas asociados a hiperglicemia, pero mostran claramente un maior risco de hipoglucemia e inestabilidade glicémica.
A diabetes secundaria en relación ás enfermidades do páncreas foi descrita por primeira vez en 1788 por Sir Thomas Cowley, que relatou o caso dun home "de 34 anos, forte, san e obeso", "afectado pola diabetes" e "gradualmente esgotado e, a pesar do tratamento, finalmente faleceu ". Na autopsia, "o páncreas estaba cheo de pedras que estaban firmemente incrustadas na súa substancia. Tiñan varios tamaños. A súa superficie era desigual como a das pedras de morera. O extremo dereito do páncreas era moi duro e parecía compactado."
Máis de 100 anos despois, en 1889, Minkowski demostrou que a resección experimental do páncreas en cans causaba diabete, e en 1940, Schumaker determinou que polo menos o 2% de todos os casos de pancreatite aguda levaron a unha diabetes clínicamente grave. A pesar de aceptar o feito de que a pancreatite aguda raramente culminou cunha diabetes excesiva, os médicos comezaron a recoñecer a pancreatite crónica ou a pancreatite aguda recorrente como unha causa común de tolerancia á glicosa deteriorada.
A diabetes mellitus é unha das enfermidades máis comúns no mundo. Esta é a sétima principal causa de morte nos Estados Unidos e, en xeral, o risco de morte entre as persoas con diabetes é aproximadamente o dobre que o das persoas sen diabetes. As persoas con diabetes teñen un maior risco de desenvolver enfermidades coronarias, vertedura, insuficiencia renal en fase final, isquemia de extremidades inferiores, así como deficiencia visual e cegueira. Desde o punto de vista da economía sanitaria, as persoas con diabetes necesitan polo menos 2-3 veces máis recursos sanitarios en comparación coas persoas sen ela. Por estes motivos e debido á combinación con outros factores de risco cardiovascular coñecidos, incluída a hipertensión, a dislipidemia e a obesidade, a prevención e o diagnóstico oportuno de prediabetes e diabetes mellitus teñen consecuencias importantes.
A pancreatite aguda é un proceso inflamatorio no páncreas, que implica tecidos peripancreáticos e insuficiencia de sistemas e órganos. A incidencia anual de agudos varía con pancreatite de 13 a 45/100000 persoas. A pancreatite aguda é a enfermidade pancreática máis común, e a hiperglucemia é un signo precoz común que se usa nos modelos prognósticos. Esta hiperglicemia, por regra xeral, considérase como un fenómeno transitorio, que se resolve completamente en case todos os pacientes. Isto explica que a homeostase con glicosa é a miúdo controlada de xeito intermitente despois de ser dada de alta do hospital. Os datos sobre a prevalencia de prediabetes e diabetes recentemente diagnosticados tras a pancreatite aguda son contradictorios. Algúns informes demostran que a homeostase con glicosa está completamente restaurada e, segundo outros, os seus trastornos persisten nunha parte significativa dos pacientes. Un estudo recente demostrou tamén que os pacientes con hiperglucemia transitoria en enfermidades agudas teñen un maior risco de desenvolver diabete. Ademais, a probabilidade de prediabetes e diabetes despois dun episodio de pancreatite aguda segue sen estar clara, do mesmo xeito que a etioloxía e a gravidade da pancreatite aguda. Aproximadamente a cuarta parte dos casos de pancreatite aguda progresa e leva a enfermidades crónicas.
A pancreatite crónica é un proceso inflamatorio e caracterízase por unha lesión progresiva e reversible principalmente do exocrino e, nunha fase posterior, do parénquima endocrino do páncreas, seguido da súa substitución por tecido fibroso. A incidencia anual de crónicas varía entre 5 e 12/100000 persoas con pancreatite, ea súa prevalencia é de aproximadamente 50/100000 persoas. A afectación do tecido pancreático endócrino prodúcese nun estadio tardío da enfermidade. Segundo as pautas clínicas para o diagnóstico e tratamento da pancreatite crónica da Asociación Gastroenterolóxica Rusa en 2013, os signos de insuficiencia pancreática endocrina e endocrina aparecen na terceira etapa da pancreatite crónica e a diabetes mellitus desenvólvese na fase IV, caracterizada pola atrofia do páncreas.
Os pacientes adoitan desenvolver síntomas asociados á hiperglicemia, pero teñen un risco claramente maior de desenvolver hipoglucemia e inestabilidade glicémica. A hipoglicemia asociada a medicamentos coa insulina ou a sulfonilurea é máis común e tende a ser máis grave e durar máis tempo. A hipoglicemia é o resultado dunha violación da contraregulación e restauración da glicosa debido á secreción insuficiente de glucagón, a unha reacción debilitada de catecolamina e á posterior activación deteriorada da produción de glicosa polo fígado. Desde o punto de vista do enfoque terapéutico, pode ser necesario manter os niveis de glucosa no plasma lixeiramente por encima do rango normal para evitar reaccións hipoglicémicas frecuentes e mellorar a calidade de vida.
Un diagnóstico incorrecto de diabetes mellitus debido a unha pancreatite aguda ou crónica leva a un tratamento médico inadecuado a estes pacientes, xunto con condicións concomitantes (dixestivo, absorción, etc.) que afectan o estado nutricional do paciente. Ademais, o uso máis común de resección de páncreas e a maior supervivencia de pacientes con fibrosis quística e, o máis importante, a crecente propagación da pancreatite crónica, suxire que a diabetes mellitus debido á pancreatite aguda ou crónica requirirá máis atención de diabetólogos e gastroenterólogos.
1. Coloque a diabetes pancreatogénica en varias clasificacións da diabetes
Segundo os requisitos para a formulación do diagnóstico de diabetes mellitus na 5ª edición dos algoritmos de atención médica especializada para pacientes con diabetes mellitus, o diagnóstico de esta diabetes debería soar como "Diabetes mellitus debido (indique a razón)".
Segundo a clasificación da American Diabetes Association, a diabetes pancreatogénica é a diabetes tipo 3 (T3cDM). Nas recomendacións para a diabetes, prediabetes e enfermidades cardiovasculares EASD / ESC, a diabetes pancreatogénica clasifícase como "Outros tipos específicos de diabetes: diabetes secundario despois de varias enfermidades (pancreatite, trauma ou cirurxía pancreática)"
Clasificación das causas da diabetes mellitus secundaria a enfermidades do páncreas exocrino (T3cDM, American Diabetic Association, 2013)
1. Pancreatite
2. Lesión / resección do páncreas
3. Neoplasia
4. Fibrosis quística
5. Hemocromatosis
6. Pankreatopatía fibrocálculo
7. Outros.
2. Patoxénese da diabetes mellitus por pancreatite aguda ou crónica
Aínda non hai unha idea clara dos mecanismos patoxenéticos da disfunción pancreática hormonal na pancreatite aguda, non hai algoritmos comúns para a súa corrección. As estreitas conexións anatómicas e funcionais entre funcións exo- e endocrinas do páncreas levan inevitablemente unha influencia mutua nas enfermidades deste órgano.
O dano ao páncreas para o desenvolvemento da diabetes debe ser extenso, coa excepción do cancro, que ademais de reducir a masa de células beta, outros mecanismos patolóxicos. A experiencia co uso de resección total de páncreas demostra que para o inicio da diabetes hai que eliminar máis do 80-90% do tecido pancreático. Para provocar un metabolismo deteriorado da glicosa, a resección parcial do páncreas no ser humano debería superar o 50% do volume, mentres que a resección pancreática total causa inevitablemente a diabetes. En persoas saudables, a hemipancreatectomía vai acompañada dunha tolerancia á glicosa deteriorada nun 25% dos casos e, por regra xeral, non se precisa máis do 20-25% do páncreas residual para asegurar a homeostase normal á glicosa.
En 1896, Chiari propuxo a dixestión automática do páncreas como resultado da activación prematura de encimas do páncreas como mecanismo de pancreatite aguda. Máis tarde quedou claro que polo menos a metade das células acinares poden ser danadas independentemente da activación do tripsinóxeno. Ata o de agora, a patoxénese exacta da pancreatite aguda non foi completamente estudada, aínda que claramente é moi dependente e / ou mediada por unha resposta inflamatoria sistémica. Unha reacción inflamatoria sistémica que conduce a necrose pancreática instantánea e fallo múltiple de órganos cunha mortalidade do 7-15% pode observarse nun 20% dos pacientes. A resposta inflamatoria sistémica mantense e controla a activación da fervenza inflamatoria mediada por citocinas, inmunocitos e sistema complementario. Ao mesmo tempo, actívase unha reacción antiinflamatoria mediada por citocinas antiinflamatorias e inhibidores de citocinas. Esta reacción antiinflamatoria pode inhibir a resposta inmune, o que pon ao hóspede en risco de infeccións sistémicas. Curiosamente, as células beta pancreáticas expresan estes sensores de dano internos, que tamén están implicados na patoxénese da diabetes tipo 2.
A hiperglucemia en pancreatite aguda débese á deterioración da secreción de insulina, unha diminución da utilización periférica de glicosa e aumento da produción de hormonas contra-hormonais. A hiperglucemia grave está asociada a pancreatite máis grave e é un factor prognóstico desfavorable. A hiperglucemia transitoria e a glicosuria ocorren en aproximadamente o 50% dos pacientes con pancreatite aguda. O grao de tolerancia á glucosa deteriorada é un indicador da gravidade da pancreatite. O alcol causa danos no páncreas máis graves e a pancreatite con alcohol é máis frecuentemente complicada pola tolerancia á glicosa deteriorada. A hiperglucemia que acompaña a un ataque de pancreatite é o resultado de danos no páncreas e estado de estrés concomitante. Tanto a gravidade como a duración dos trastornos metabólicos nos hidratos de carbono están relacionados co grao de dano ao tecido pancreático. Un estudo da fase inicial da pancreatitis aguda necrótica experimental en ratas (a 5 horas do inicio da enfermidade) mostrou edema, hemorraxia, necrose graxa, destrución de acinar e infiltración de leucocitos na parte exocrina do páncreas, mentres que os illotes endocrinos conservaban unha estrutura normal e as células b contiñan unha cantidade suficiente de insuficiencia. . Non obstante, a capacidade de segregar insulina en resposta á estimulación da glicosa viuse claramente deteriorada (P> 0,05). A arquitectura dos illotes do páncreas mantívose intacta con claros cambios inflamatorios nas rexións exocrinas veciñas. O transportador específico de glicosa das illas illotas (GLUT 2) no experimento tivo unha baixa concentración, polo tanto, unha secreción de insulina deteriorada na pancreatite aguda pode asociarse con dificultade para transportar a glicosa ás células b.
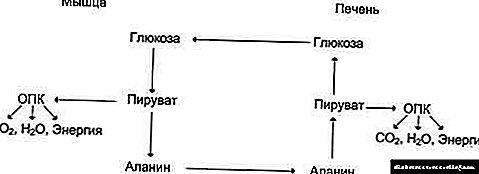
En pacientes con pancreatitis aguda, os niveis de insulina no plasma son menores que en individuos sans. A secreción de insulina en resposta a glicosa ou glucagón está deteriorada, mentres que as infusións de alanina conducen a un aumento normal dos niveis de insulina no plasma. Cunha diminución da intensidade do proceso agudo, a produción normal de insulina tende a restaurarse. A concentración de glucagón plasmático aumenta e normalmente permanece alta durante polo menos 1 semana. A combinación de hiperglucagonemia e hipoinsulinemia é suficiente para explicar o desenvolvemento da cetoacidosis e a rara aparición de coma diabético.
Ademais de aumentar os niveis de glicosa plasmática, nunha minoría de pacientes con pancreatite aguda e falta de historia de hiperlipidemia, pode aumentar a concentración de lípidos séricos. Os triglicéridos séricos> 1000-2000 mg / dl en pacientes con hiperlipidemia tipo I, IV ou V (clasificación Fredrickson) son un factor de risco de pancreatite aguda. As concentracións plasmáticas de ácidos graxos libres aumentan despois da pancreatite aguda, como consecuencia da deterioración da secreción de insulina e un aumento concomitante da secreción de glucagón e cortisol. A pesar de que os cambios no ambiente hormonal na pancreatite aguda poden contribuír ao desenvolvemento da cetoacidosis, este é un feito raro, debido á conservación da secreción residual de insulina endóxena, suficiente para inhibir a lipólise e a cetoxénese e debido á secreción insuficiente de glucagón.
A secuencia exacta de eventos que conducen á pancreatite crónica non foi completamente determinada. Estudos experimentais demostraron que os estímulos nocivos provocan un brote de especies reactivas de osíxeno, a liberación de citocinas e o posterior esgotamento de antioxidantes, o que conduce á pancreatostasis, é dicir. prevención da exocitosis apical por células acinar pancreáticas. Estas células secretan rápidamente enzimas sintetizadas nos vasos sanguíneos e linfáticos, provocando unha reacción inflamatoria. Recentemente informouse de que a ciclooxixenase 2, o regulador dominante da produción de prostaglandina, xoga un papel importante na patoxénese do dano ás partes exocrinas e endocrinas na pancreatite crónica.
Os illotes de Langerhans, en realidade, están relativamente ben conservados, en comparación co grao de destrución das células acinares. Ás veces o páncreas pode adoptar unha natureza adenomatosa debido á perda completa de tecido exocrino en combinación coa preservación do seu compoñente endocrino.Nos illotes restantes, a reordenación da parte endocrina da poboación celular prodúcese cunha perda de células beta proporcionalmente maior que as células alfa, o que leva a un cambio na relación normal de 2: o número de células delta, por regra xeral, segue sendo normal, e hai un lixeiro aumento no número de células PP. As illas rodeadas de tecido acinoso normal, por regra xeral, teñen unha composición citolóxica normal, o que indica o efecto trófico do páncreas exocrino. A mala absorción que se produce na pancreatite crónica tamén pode levar á secreción de incretinas alterada, o que, á súa vez, pode contribuír á disfunción das illas e á tolerancia á glicosa.
Obsérvase un nivel moi elevado de diabetes con pancreatite fibrocalculosa nos trópicos, cun cadro clínico ben recoñecido. Esta forma de pancreatite calcificante crónica obsérvase principalmente en nenos e adultos mozos rurais en países en desenvolvemento tropical. Afirmouse que o 60-70% de todos os casos de pancreatite crónica en India e China están relacionados con pancreatite tropical. A súa prevalencia en pacientes con diabetes é moi variable, do 0,5 ao 16% na India e chega ao 80% entre os pacientes novos que toman insulina en Nixeria.
A diabetes é unha complicación tardía case universal da pancreatite calcifiante crónica e normalmente desenvólvese dentro dos dez anos posteriores ao inicio da pancreatite, pero correlaciona aínda máis claramente coa idade do paciente. A maioría dos pacientes presentan grandes pedras intraductais durante o exame, cuxa etioloxía inclúe deficiencia proteica e calórica, o uso de varias toxinas exóxenas, anormalidades ductais do páncreas e, posiblemente, unha predisposición xenética. A diabetes neste caso, por regra xeral, é grave e é necesaria a insulinoterapia, aínda que estudos patohistolóxicos e inmunohistoquímicos indican a preservación parcial de células insulinopositivas no páncreas de pacientes con pancreatite fibrocalcule. A secreción de insulina residual explica, moi probablemente, o raro desenvolvemento da cetoacidosis en pacientes con pancreatite fibrocalculosa.
Os desencadenantes etiolóxicos específicos para enfermidades do páncreas poden contribuír á intolerancia aos carbohidratos. A hipertrigliceridemia, por exemplo, está asociada á resistencia á insulina e normalmente leva a unha diabetes mellit clínicamente grave. O alcohol debilita os efectos da insulina e leva a unha tolerancia á glicosa deteriorada por exposición directa ao fígado. Con pancreatite hereditaria, unha rara enfermidade autosómica dominante, a diabetes pode desenvolverse nunha fase tardía e poden producirse complicacións diabéticas a longo prazo.
Un historial familiar positivo de diabetes mellitus pode predispoñer a pacientes con pancreatite crónica ao desenvolvemento da diabetes a unha idade nova. A prevalencia de diabetes sen ningunha conexión coa pancreatite é efectivamente maior nas familias dos pacientes que desenvolveron diabetes. Non obstante, demostrouse un marcado aumento da incidencia de HLA tipos B8, DR3, DR4 e DR3 / DR4 en pacientes con diabetes mellitus despois da pancreatite crónica. Suxeriuse que a autoinmunidade pode contribuír ao desenvolvemento da diabetes secundaria á pancreatite crónica, xa que algúns anticorpos contra as células dos illotes atopáronse nalgúns pacientes antes de comezar a diabetes. Non obstante, isto segue sendo un punto de referencia. A pancreatite crónica autoinmune caracterízase por un inchazo difuso e ten un grave grao de fibrose asociado coa infiltración do páncreas exocrino do páncreas por células mononucleares. O trastorno pode causar edema pancreático grave ou a formación dun tumor, con malabsorción e colestase, e ás veces diagnostícase erróneamente cancro ou linfoma de páncreas.
As mutacións xenéticas poden causar unha insuficiencia pancreática endócrina e exocrina; a rexeneración das células beta pancreáticas é deteriorada, determinando unha diminución da masa celular beta, como se observa na pancreatite crónica.
O proceso fibroso na pancreatite crónica conduce a unha diminución da masa de células beta e pode cambiar a circulación capilar do páncreas, o que conduce a unha diminución da perfusión dos illotes, un deterioro do envío de secretagogos ás células beta, así como unha diminución da saída de hormonas pancreáticas. A perda de células beta en funcionamento explica a diminución da secreción de insulina: canto maior sexa a perda de tecido endocrino pancreático, maior será o deterioro da secreción de insulina e o grao de tolerancia á glicosa. En pacientes con diabetes mellitus secundarios a pancreatite crónica con hiperglucemia en xaxún leve ou moderada, a concentración basal de insulina no plasma pode ser normal ou moderadamente elevada. Non obstante, a secreción de insulina prexudicada está case sempre presente. Unha diminución do potencial máximo de secreción de insulina nestes pacientes é obvia e indica unha diminución do subministro de insulina. Cando os niveis de glicosa no plasma superan os 10 mmol / L (180 mg / dl), a miúdo non se detectan concentracións de insulina plasmática e péptido C.
A resposta das células beta aos aminoácidos tamén diminúe dependendo do grao de morte das células beta e da gravidade da tolerancia á glucosa deteriorada.
A secreción estimulada pola arginina do péptido C pode ser normal en pacientes con pancreatite crónica e tolerancia á glicosa, pero sempre reducida en pacientes con hiperglucemia en xaxún.
As funcións exocrinas e endocrinas correlacionan entre si, o que indica unha relación causal directa entre o proceso inflamatorio no tecido pancreático exocrino e o desenvolvemento da diabetes. Atopouse unha correspondencia exacta entre a resposta de insulina á inxestión oral de glicosa e a concentración de enzimas pancreáticas no zume duodenal despois da administración intravenosa de colecistokinina-pancreosimina (CCK-PZ). Os pacientes con steatorrea presentan unha menor secreción de péptido C que en pacientes con menor deterioro da función exocrina.
En individuos sans, a inxestión de glucosa provoca unha secreción máis intensa de insulina que a infusión intravenosa dunha cantidade equivalente de glicosa, como resultado da activación do sistema de incretina. Na pancreatite crónica, a secreción de factores de incretina: colecistokinina, gastrina, enteroglucagón, péptido insulinotrópico dependente de glicosa (PBI) e polipéptido intestinal vasoactivo empeora. Por outra banda, estudos recentes reportaron un aumento da liberación de péptido-1 similar ao glucagón (GLP-1), en resposta á administración de glicosa oral en pacientes con diabetes secundarios á pancreatite en comparación con pacientes con tolerancia normal ou prexudicada a glicosa. En pacientes con diabetes mellitus secundarios á pancreatite crónica, a resposta á insulina á colecistokinina é proporcional ao grao de hiperglicemia. En contraste, redúcese a secreción de insulina en resposta ao PIB. Non obstante, a infusión de GLP-1 en pacientes con diabetes mellitus secundario á pancreatite crónica vén acompañada dunha diminución da glicosa no sangue e un aumento da concentración plasmática de péptido C, esta reacción non difire da observada en persoas saudables. Na diabetes mellitus, secundaria á pancreatite crónica, aínda non está claro se existe un eixe deseñado de incretina desequilibrada ou a secreción de hormonas intestinais e pancreáticas cambia simultaneamente. As concentracións do PIB plasmático aumentan en pacientes con diabetes mellitus con pancreatite crónica, especialmente despois da retirada de insulina. Por outra banda, o grao de aumento da colecistokinina relacionada co plasma é reducido en comparación con suxeitos sen diabetes ou con non diabéticos con pancreatite crónica.
En pacientes con pancreatite crónica, normalmente mantense unha concentración de glicosa en xaxún normal ata que se perde o 20-40% da masa de células beta. Non obstante, este grao de perda de masa das células beta vén acompañado dun importante deterioro da liberación de insulina mediada por glicosa, aínda que a resposta á colecistoquinina e a arginina segue sendo normal. Un cambio na resposta aos factores de incretina e aminoácidos faise evidente cando a masa das células beta diminúe nun 40-60%. Finalmente, cando a masa das células beta diminúe en máis do 80-90%, a hiperglucemia en xaxún e a secreción de insulina prexudicada desenvólvense como resposta a todos os secretagogos. A secreción de glágono nestes pacientes é heteroxénea e recoñécense dúas condicións principais. Mentres que algúns pacientes presentan un defecto de combinación na secreción de insulina e glucagón, outros poden mostrar severa hipoinsulinemia e altas concentracións de glucagón no plasma. Ademais, a resposta do glucagón á estimulación con arginina ou alanina só se esmorece no 50% dos pacientes con tolerancia á glicosa. Coa progresión da enfermidade pancreática, a capacidade das células alfa para responder á hipoglucemia inducida pola insulina. Non obstante, a carga oral de glicosa pode ir acompañada dun aumento paradoxal dos niveis de glucagón plasmático, mentres que a resposta do glucagón á secretina e á colecistoquinina é normal ou aumentada.
Hai controversia sobre a natureza molecular e a fonte de glucagón circulante en pacientes con diabetes como consecuencia da pancreatite crónica. Determináronse polo menos catro variedades de glucagón inmunoreactivo (pesos moleculares de máis de 50.000, 9.000, 3.500 e 2.000) no plasma de individuos sans. O glágono cun peso molecular de 3500 é de orixe páncreas e ten actividade biolóxica completa. Esta é a única forma que responde á estimulación con arginina e supresión da somatostatina. Estudos funcionais e análises cromatográficas apoian a hipótese da orixe pancreática de glucagón circulante na pancreatite crónica, pero tamén é probable unha contribución significativa do glucagón enteropancreático á concentración plasmática medida por radioinmunoensayo. Así, a concentración basal de glucagón gastrointestinal aumenta en pacientes con diabetes mellitus.
3. A prevalencia de diabetes por pancreatite aguda ou crónica
Os datos sobre a prevalencia da diabetes secundaria en relación ás enfermidades do páncreas seguen a ser escasos, pero a incidencia desta enfermidade é probablemente maior do que se cre comunmente. Segundo estudos antigos, a diabetes pancreatogénica representa o 0,5-1,7% de todos os casos de diabetes. Nun informe máis recente, a prevalencia da diabetes secundaria estímase nun 9,2% dos casos nunha cohorte de 1868 pacientes con diabete alemán para os que se documentou insuficiencia pancreática exocrina e imaxe anormal do páncreas. Noutra cohorte de 1922 pacientes negativos con autoanticorpos con insuficiencia pancreática exocrina e endócrina e alteracións morfolóxicas típicas do pancreas, só o 8% dos casos foron diagnosticados con diabetes mellitus, mentres que no 80% dos casos se detectou diabetes tipo 2 e no 12% dos pacientes - diabetes tipo 1 De feito, neste grupo de poboación, o 76% dos pacientes presentaban pancreatitis crónica, o 8% tiña hemocromatosis, o 9% tiña cancro de páncreas, o 4% tiña fibrosis quística e a resección do páncreas realizouse no 3% dos casos.
A incidencia de pancreatite crónica é maior en poboacións con consumo excesivo de alcol e en países tropicais, onde a prevalencia de diabetes secundaria a pancreatite fibrocalcule pode chegar ao 90%, que é ata un 15-20% de todos os pacientes con diabetes. Así, a prevalencia da diabetes inducida pola pancreatite é probablemente subestimada, a miúdo esquécese o diagnóstico da diabetes pancreatogénica e os pacientes normalmente son mal clasificados.
En 24 ensaios clínicos potenciais participaron 1102 pacientes con pancreatite aguda, prediabetes e / ou diabetes en 37% dos casos. A prevalencia global de prediabetes, diabetes mellitus e tratamento coa insulina despois da pancreatite aguda foi do 16%, 23% e 15%, respectivamente. A diabetes mellitus recentemente diagnosticada desenvolveuse nun 15% das persoas dentro dos 12 meses posteriores ao primeiro episodio de pancreatite aguda.
e o risco aumentou significativamente en 5 anos (risco relativo 2,7). Observouse unha tendencia similar con respecto ao tratamento coa insulina.
Os pacientes con pancreatitis aguda adoitan desenvolver prediabetes e / ou diabetes despois de ser dados de alta do hospital e o risco de desenvolver diabete duplícase nos próximos 5 anos.
A prediabetes e / ou a diabetes observáronse en case o 40% dos pacientes despois da pancreatite aguda, e a diabetes desenvolveuse en case o 25% dos pacientes tras a pancreatite aguda, o 70% dos cales requiren unha insulina constante. Ademais, a gravidade da pancreatite aguda parece ter pouco efecto no desenvolvemento de prediabetes ou diabetes despois de pancreatite aguda. Os pacientes que presentaban unha pancreatite aguda grave tiveron só unha prevalencia lixeiramente maioritaria tanto de prediabetes (20%) como de diabetes mellitus (30%). Unha análise de meta-regresión tamén demostrou que o risco de desenvolver prediabetes ou diabetes despois da pancreatite aguda é independente da etioloxía, así como da idade e do xénero. O desenvolvemento tanto de prediabetes como de diabetes é máis común nos primeiros tempos despois da pancreatite aguda. A prevalencia de prediabetes e diabetes dentro dos 12 meses posteriores ao primeiro episodio de pancreatite aguda foi do 19% e do 15%, respectivamente. Por desgraza, só hai un estudo que examinou a pacientes con prediabetes que tiveron pancreatite aguda para determinar se desenvolveron diabete, pero, segundo a literatura sobre diabetes, os pacientes con prediabetes teñen máis probabilidades de desenvolver diabete.
A pancreatite aguda é unha causa recoñecida da diabetes. Aínda que a perda de células do páncreas debido á necrose (con ou sen intervención cirúrxica) considérase a principal causa da diabetes despois da pancreatite aguda, en máis do 70% dos pacientes, a extensión da necrose non superou o 30% e o 78% dos pacientes foron conservadores. Ademais, aparentemente non houbo efectos da gravidade da enfermidade no risco de desenvolver diabete. Isto suxire que a diabetes despois da pancreatite aguda pode desenvolverse debido a mecanismos diferentes á necrose.
Os anticorpos contra a descarboxilase do ácido glutámico (IA2) atopáronse en pacientes con diabetes mellitus autoinmune latente e diabetes mellitus tipo 1. É posible que a pancreatite aguda cause unha reacción en individuos predispostos xeneticamente xa con risco de desenvolver diabetes mellitus. Ademais, recentemente suxeriuse que certos factores metabólicos, como a obesidade e a hipertrigliceridemia, poñen aos pacientes cun maior risco de desenvolver pancreatite aguda chamada pancreatite metabólica aguda, e estes factores tamén poden aumentar o risco de desenvolver diabete despois da pancreatite aguda.Dado que non había datos dispoñibles sobre indicadores metabólicos antes do primeiro ataque de pancreatite aguda, os futuros estudos terán que responder a preguntas sobre a presenza de autoanticorpos preexistentes, cambios estruturais ou funcionais predispostos ao desenvolvemento de hiperglicemia e diabetes mellitus despois da pancreatite aguda.
É importante salientar que a presenza de diabetes mellitus preexistente considérase en si mesmo un factor de risco para a pancreatite aguda, que destaca a base complexa de cambios metabólicos asociados á pancreatite aguda.
Ao analizar a tendencia da enfermidade ao longo do tempo, resulta que a prevalencia de prediabetes e diabetes en xeral e de diabetes mellitus en particular aumentou notablemente co paso do tempo. Debe recoñecerse que a prevalencia da diabetes mellitus aumenta exponencialmente despois de 45 anos, e o efecto do envellecemento na función celular e o aumento da resistencia á insulina causada pola obesidade poden explicar parcialmente esta tendencia, sen embargo, a análise de metaregresión demostrou que a idade non é tan importante. entre pacientes despois de pancreatite aguda. Outro mecanismo posible é que algunhas persoas puidesen sufrir ataques reiterados de pancreatite aguda antes de ser examinados despois de 5 anos. Isto foi informado nalgúns estudos, pero isto non se tivo en conta na maioría das obras incluídas. Isto significa que o efecto de ataques repetidos de pancreatite aguda sobre o risco de prediabetes e diabetes pode aumentar a súa prevalencia co tempo de seguimento. Non se sabe se os ataques reiterados de pancreatite aguda poden contribuír á perda de células pancreáticas, actuando como posible mecanismo para o desenvolvemento de diabetes mellitus e afeccións relacionadas.
4. Manifestacións clínicas de diabetes por pancreatite aguda ou crónica
Os pacientes con formas secundarias de diabetes presentan síntomas típicos asociados á hiperglucemia, pero un risco claramente aumentado de hipoglucemia. Os episodios de hipoglucemia asociados a terapia con insulina ou fármacos con sulfonilurea son máis comúns e normalmente son máis graves e prolongados, moitas veces leva á hospitalización e pon a pacientes cun maior risco de morte. A hipoglicemia é especialmente común despois da pancreatectomía, causando a morte no 20-50% dos pacientes. Un panorama tan dramático é consecuencia dunha violación da contrarregulación e restauración da glicosa. A incapacidade do corpo para responder rapidamente a unha diminución da concentración de glucosa no plasma débese á secreción insuficiente de glucagón, a unha reacción de catecolamina reducida e á posterior activación deteriorada da produción de glicosa no fígado. Un aumento da incidencia de episodios hipoglucémicos está asociado á inestabilidade glicémica.
O abuso continuado de etanol despois do tratamento farmacéutico ou quirúrgico da pancreatite pode afectar o equilibrio metabólico dos pacientes con diabetes, xa que o alcol inhibe a gluconeoxénese, afecta a secreción hipotalámico-hipofisaria da hormona adrenocorticotrópica e da hormona de crecemento e induce a resistencia á insulina. A hipoglicemia pode ser especialmente perigosa se se reduce a inxestión de nutrientes e se esgotan as tendas de glicóxeno hepático.
O abuso de alcol despois da pancreatectomía é un factor importante no desenvolvemento da hipoglucemia e da morte. Nestes pacientes, a mala adhesión á administración de insulina contribúe a miúdo á inestabilidade metabólica.
Por outra banda, o desenvolvemento de cetoacidosis e coma diabético na diabetes mellit pancreatogénica é raro incluso en pacientes sen secreción residual do péptido C. Cando isto sucede, case sempre están asociados a condicións estresantes como a infección ou a cirurxía. No pico da secreción de insulina residual, o esgotamento das reservas de graxa e a baixa taxa de lipólise concomitante contribúen pouco ao risco de cetose. Unha resistencia similar á cetose obsérvase na diabetes mellitus tropical, onde a desnutrición e o consumo moi baixo de graxas insaturadas contribúen a unha diminución da síntese de corpos cetonas. O papel da deficiencia de glucagón na protección dos pacientes con diabete pancreático contra a cetoacidosis é controvertido. Non obstante, é posible que, a pesar de que o glucagón poida ser necesario para o desenvolvemento da cetose, a súa deficiencia poida retrasar ou retardar a progresión da cetoacidosis diabética.
As dificultades para manter un control metabólico satisfactorio estable en pacientes con diabetes mellitus debido a pancreatite aguda ou crónica provocaron a inclusión deste grupo de enfermidades na categoría de "diabetes fráxil".
A insuficiencia pancreática exocrina con malabsorción pode contribuír á inestabilidade do control da glicosa. A estatorrea pode causar malabsorción de glicosa, contribuíndo así a reaccións hipoglucémicas posprandiais, así como un cambio na secreción de insulina. O desenvolvemento da diabetes en pacientes con enfermidade do páncreas pode asociarse a unha perda de peso importante, difícil de corrixir incluso con unha insulina terapéutica adecuada. Ademais, a perda de peso por si só pode cambiar notablemente a sensibilidade á insulina.
4.1 Complicacións crónicas da diabetes mellit pancreatogénica
Desde finais dos anos 50, xeralmente entendeuse que a diabetes despois dunha pancreatite crónica non está asociada a complicacións vasculares. Para explicar esta crenza, declaráronse varios factores, entre eles unha predisposición xenética ausente ou reducida, insuficiencia pancreática exocrina, colesterol sérico baixo, inxestión de poucas calorías, etc. Non obstante, debido á esperanza de vida prolongada dos pacientes, recolléronse máis casos de angiopatía diabética.
A prevalencia de retinopatía diabética en pacientes con diabetes mellitus tras pancreatite crónica ou pancreatectomía difire significativamente da reportada inicialmente. Máis recentemente, unha avaliación máis precisa da retinopatía diabética revelou unha incidencia do 30-40%, unha cifra similar á atopada en pacientes con diabetes tipo 1. A incidencia de retinopatía correlaciona coa duración da hiperglicemia. Non hai un patrón obvio entre a presenza de retinopatía e un historial familiar positivo de diabetes, a frecuencia de detección de antíxenos HLA, a presenza de anticorpos ás células illotísticas ou os niveis plasmáticos de péptido C.
Continúan as controversias sobre a incidencia da nefropatía diabética na diabetes secundaria. Algúns autores informaron de que "non foron capaces de atopar a ninguén que soubese dun caso confirmado por autopsia de glomerulosclerose intracappilar combinada con hemocromatosis ou pancreatite. Non obstante, cada vez son máis os casos de glomerulosclerose nodular en pacientes con diabetes debido a Pancreatitis aguda ou crónica. Algúns casos de glomerulopatía diabética reportáronse en pacientes con pancreatectomía total, pero hai que considerar unha duración máis curta Isto explica por que pode ser difícil detectar estadios tardíos do dano renal diabético, mentres que os cambios funcionais tempranos pódense atopar varios anos antes do inicio da albuminuria. Nunha serie de 86 pacientes con diabetes debido a pancreatite aguda ou crónica, a excreción de albúmina urinaria Determinouse máis de 40 mg / 24 h no 23% dos pacientes, e a albuminuria asociouse coa duración da diabetes e da presión arterial, pero non con antecedentes familiares de diabetes, antíxenos HLA ou niveis de péptido C no plasma. A incidencia de retinopatía foi case dúas veces maior en pacientes con MAU, o que suxire que a asociación "oculorenal" descrita en pacientes con diabete tipo 1 tamén se produce en diabetes pancreatogénico. A hiperfiltración glomerular, outro signo precoz da disfunción renal, pódese detectar con diabetes pancreatogénico do mesmo xeito que coa diabetes tipo 1. A pesar do dano renal diabético, os niveis de excreción de albúmina superiores a 0,5 g / día ou insuficiencia renal excesiva non son atípicos.
A neuropatía é unha queixa común na diabetes pancreatogénica. Detéctase entre un 10 e un 20% dos casos de polineuropatía distal ou mononeuropatía e os signos electrofisiolóxicos de velocidade de condución deteriorada atópanse en máis do 80% dos pacientes con diabetes mellitus secundarios a enfermidades pancreáticas. Verificouse que a sensibilidade ás vibracións se perturba aproximadamente do mesmo xeito que coa diabetes tipo 1.
A diferenza tanto da retinopatía como da nefropatía, non existe ningunha relación entre a neuropatía e a duración da diabetes. Isto pode deberse ao efecto de factores concomitantes distintos da hiperglicemia (tabaquismo, alcol e malabsorción).
Tamén hai cambios no sistema nervioso autónomo. O 8% dos pacientes con diabetes mellitus atopáronse trastornos dos reflexos cardiovasculares tras a pancreatite crónica, mentres que un 13% adicional destes pacientes detectouse un defecto na liña límite. Non obstante, debe observarse certa precaución ao correlacionar a hiperglicemia con neuropatía somática e autonómica diabética, porque o consumo de alcol é común nestes individuos. Así, o verdadeiro mecanismo patoxenético da neuropatía en pacientes con diabetes mellitus con enfermidades pancreáticas, moi probablemente, inclúe moitos factores.
As macroangiopatías, especialmente o infarto de miocardio, son raras na diabetes pancreatogénica. Nun informe, atopáronse complicacións vasculares no 25% dos pacientes con diabetes mellitus despois da pancreatite crónica, e algúns necesitaron amputacións ou derivaron a cirurxía vascular. A relativamente curta duración da diabetes mellitus e a enfermidade pancreática subxacente dificultan a valoración da prevalencia de complicacións macrovasculares nestes pacientes. Segundo unha observación dispoñible a longo prazo, a frecuencia de mortes cardiovasculares en pacientes con pancreatite crónica é do 16%, que é inferior á da diabetes clásica.
5. Diagnóstico da diabetes con pancreatite crónica
Non sempre é fácil diagnosticar e clasificar correctamente a un paciente con diabetes mellitus debido a unha pancreatite aguda ou crónica. A existencia a longo prazo dos tipos 1 e 2 de diabetes mellitus vén acompañada da insuficiencia da parte exocrina do páncreas e os pacientes con diabetes teñen un maior risco de desenvolver pancreatite aguda e / ou crónica en todo caso.
Os pacientes con antecedentes de pancreatite poden desenvolver diabetes tipo 1 ou tipo 2, independentemente do estado da función pancreática exocrina. Para clasificar adecuadamente a pacientes con diabetes por pancreatite aguda ou crónica, deberían establecerse criterios de diagnóstico aceptados que actualmente non están dispoñibles. N. Ewald et al suxiren usar os seguintes criterios:
Principais criterios (deben estar presentes):
- Insuficiencia pancreática exocrina (proba monoclonal de elastase fecal-1 ou probas funcionais directas)
- Patoloxía do páncreas durante a imaxe (ecografía endoscópica, MRI, CT)
- Falta de diabetes tipo 1 asociada a marcadores autoinmunes
- Non hai secreción pancreática do polipéptido
- Secreción de incretina prexudicada (por exemplo, GLP-1)
- Sen resistencia á insulina (por exemplo, índice de resistencia á insulina HOMA-IR)
- Función deteriorada das células beta (por exemplo, HOMA-B, relación de péptido C / glicosa)
- Baixos niveis de vitaminas solubles en graxa sérica (A, D, E e K)
En calquera caso, as novas manifestacións da diabetes deberían empregar realmente os criterios definidos pola Asociación Europea para o Estudo da Diabetes (EASD) e a American Diabetes Association (ADA) e comprobar a diabetes pancreatogénica. Polo menos, se o paciente mostra un cadro clínico atípico e se queixa de síntomas do tracto gastrointestinal, o médico debe ser consciente da existencia de diabetes pancreatogénico e iniciar o diagnóstico posterior.
Por suposto, calquera paciente con pancreatite crónica debe ser controlado para o desenvolvemento de diabetes mellit pancreatogénico. Unha avaliación inicial dos pacientes con pancreatite crónica debería incluír unha avaliación da glicemia en xaxún e HbA1c. Estes estudos deberían repetirse polo menos anualmente. Os achados patolóxicos con calquera deles requiren un diagnóstico adicional. Se os resultados da proba suxiren unha tolerancia á glicosa deteriorada, recoméndase unha proba oral de tolerancia á glucosa. Unha análise concomitante dos niveis de insulina e / ou péptido C pode ser útil para distinguir entre diabetes mellitus tipo 2 e diabetes mellitus debido a pancreatite aguda ou crónica.
A avaliación da resposta do polipéptido pancreático ante unha hipoglucemia inducida pola insulina, unha infusión de secreción ou unha mestura de nutrientes pode ser de interese diagnóstico adicional. A falta de resposta do polipéptido pancreático permite distinguir a diabetes mellit pancreatogénica do tipo 1, e tamén pode distinguir a diabetes debido á pancreatite aguda ou crónica do tipo 2 con niveis elevados de polipéptido pancreático. Non obstante a determinación regular da secreción pancreática de incretina e a resposta do polipéptido pancreático na práctica cotiá non son posibles.
6. Aspectos terapéuticos da diabetes mellit pancreatogénica
Os principais obxectivos do tratamento da diabetes mellitus, independentemente do seu tipo, inclúen: eliminar os síntomas subxectivos e obxectivos da enfermidade, previr o coma diabético, previr e retardar a progresión das complicacións tardías da diabetes mellitus (nefropatía e retinopatía diabética, neuropatía, etc.). A solución das tarefas, segundo ideas modernas, é posible ao alcanzar e manter o nivel de glicemia o máis preto posible de persoas saudables, eliminando os síntomas subxectivos e obxectivos da enfermidade.
A dieta para a diabetes mellit pancreatogénica corresponde á de diabetes mellitus tipo 1, coa excepción da necesidade de corrixir malabsorción, deficiencia de vitaminas e oligoelementos, o nomeamento de nutrición fraccionada proporciona a prevención da hipoglucemia.
A pancreatite aguda está acompañada de hiperglucemia importante no 50% dos pacientes, e ás veces tamén pode desenvolverse cetose ou coma diabético. En caso de hiperglucemia importante, cetose ou coma, é necesario un control minucioso da concentración de glicosa plasmática, electrólitos, cetonas e outros parámetros metabólicos, xunto coa administración de líquidos intravenosos e infusións de insulina de acordo cos principios clásicos do tratamento da cetoacidosis diabética.
A hiperglucemia considérase o principal obstáculo para un apoio nutricional adecuado, incluso en pacientes sen diabetes. Así, é necesario un suministro adecuado de insulina durante a nutrición artificial, empregando a administración parenteral ou subcutánea de análogos de insulina de longa acción.Recoméndase que os pacientes con pancreatite aguda grave sexan xestionados por un equipo multidisciplinar de médicos da unidade de coidados intensivos.
Para os pacientes con pancreatite fulminante aguda, debe recomendarse a terapia conservadora, máis que a resección pancreática, xa que esta última vén acompañada dunha maior incidencia de diabetes. En todos os casos, a tolerancia á glicosa debe valorarse 3-6 meses despois dun episodio de pancreatite aguda.
En pacientes con pancreatite crónica ou pancreatectomia parcial, pódense prescribir axentes hipoglucemicos orais a aqueles individuos que aínda manteñen unha resposta satisfactoria de péptidos C ao glucagón ou á inxestión de alimentos. Prefírense as sulfonilureas de corta duración que as de longa duración para minimizar o risco de hipoglucemia grave. Non obstante, débese ter precaución ao usar medicamentos por vía oral en pacientes con cambios nas mostras de fígado funcionais. Máis recentemente, suxeriuse a posibilidade de usar inhibidores da GLP-1 e da dipeptidil peptidase 4, porque o seu efecto de redución da glicosa no plasma non semella aumentar o risco de hipoglucemia. Non obstante, hai algúns problemas porque aínda non está claro se existe un maior risco de desenvolver pancreatite, presuntamente asociada ao uso de terapia con incretina.
A insulinoterapia é necesaria despois da pancreatectomía total, aínda que a necesidade de insulina é menor que en pacientes con diabetes tipo 1, especialmente durante a noite. En contraste, a necesidade de insulina posprandial pode ser maior. Isto é especialmente certo en pacientes con pancreatectomía total, mentres que os pacientes dependentes da insulina con pancreatite crónica ou pancreatectomia parcial adoitan ter requerimentos de insulina similares aos da diabetes tipo 1. Para controlar a hiperglicemia durante a noite e sobre o estómago baleiro debe empregarse unha dose nocturna de acción prolongada durante a noite. Os análogos de acción longa reducen o risco de hipoglucemia nocturna en comparación coa insulina NPH, polo que se debería preferir o primeiro. Así, pode ser apropiado un réxime clásico de bolo basal con análogos de insulina de corta e longa acción. En pacientes altamente motivados e educados, o tratamento coa insulina por infusión continua subcutánea úsase con éxito para lograr un control metabólico coidadoso, evitando á vez a hipoglucemia e a cetose.
Independentemente do tratamento escollido, a hipoglucemia segue sendo o principal perigo. Un aumento da frecuencia e gravidade dos eventos hipoglucémicos é consecuencia probable dunha combinación de varios factores, incluído o exceso de insulina, sensibilidade á insulina, contraregulación deteriorada, dieta inadecuada ou absorción de nutrientes, consumo de alcol e enfermidades hepáticas. O risco de hipoglucemia fatal é especialmente elevado en pacientes con pancreatectomía total, e isto impulsou a busca de métodos cirúrxicos e farmacéuticos máis seguros. Así, a preservación do duodeno e do píloro parece garantir un control metabólico máis estable e unha redución de episodios de hipoglucemia. Se se producen reaccións hipoglicémicas, deben ser tratadas de xeito agresivo e as súas causas e mecanismos deben ser avaliados e explicados aos pacientes. Os pacientes deben formarse para previr a aparición de hipoglucemia grave, debendo prestar atención a rexeitar o alcol, a aumentar a actividade física, a alimentación fraccionada e a adhesión á terapia de substitución de enzimas. Máis recentemente, propúxose un autotrasplante de illote para previr a dependencia da insulina. O autotrasplante de illote asegura un funcionamento estable das células beta e un bo control glicémico ata 13 anos despois de realizar a pancreatectomía total para o tratamento da pancreatite crónica.
Debido á extrema "fraxilidade" da diabetes en pacientes con enfermidades do páncreas, a educación dos pacientes e o autocontrol dos niveis de glicosa no sangue son extremadamente importantes. O control estricto da glicosa no fogar e a administración repetida de pequenas doses de insulina, xunto con programas educativos intensivos, poden levar a un bo control metabólico estable e estable nestes pacientes. Non obstante, deberán ir acompañados de pasos específicos, incluída a corrección do estado nutricional e a retirada de alcol do paciente. O consumo excesivo de alcol tamén leva a producir un dano hepático progresivo, que só pode prexudicar o control metabólico.
A absorción deteriorada coa steatorrea aumenta o risco de hipoglucemia e deteriora a secreción de insulina por trastornos do sistema de incretina. En pacientes con diabetes mellit pancreatogénico, a terapia enzimática con fármacos resistentes aos ácidos debe prever a liberación de graxa con feces inferiores a 20 g / día. Recoméndase un tratamento simultáneo con antagonistas do receptor H2 porque unha redución da secreción de ácido gástrico reduce a degradación dos encimas pancreáticos. Recoméndase unha dieta rica en calor (máis de 2500 kcal / día) rica en hidratos de carbono complexos e baixa en graxa. En pacientes con pancreatite crónica, a inxestión de graxa pode aumentar a frecuencia e intensidade da dor abdominal. Así, a inxestión de graxa non debe superar o 20-25% da inxestión calorífica total. As porcións deben ser pequenas e as comidas frecuentes, con 3 comidas principais e 2 ou 3 lanches intermedios. Se é necesario, a dieta debe complementarse con electrólitos, calcio, vitamina D e potasio. O síndrome acelerado do tránsito intestinal e do dumping despois da gastrectomía tamén pode contribuír á malabsorción e ao control metabólico inestable. Finalmente, nalgúns pacientes con diabetes mellitus secundarios á enfermidade pancreática adquirida, pode ser difícil conseguir un control metabólico óptimo debido ao alto risco de hipoglucemia. O mantemento dos niveis de glicosa no plasma lixeiramente por encima do normal pode ser necesario para evitar reaccións hipoglucémicas frecuentes e mellorar a calidade de vida. Cómpre lembrar que moitos destes pacientes teñen unha esperanza de vida reducida e menor risco de desenvolver complicacións diabéticas. Aínda que a cetoacidosis raramente se produce, de súpeto pode desenvolverse baixo estrés (infección, cirurxía, etc.) e require un axuste adecuado das doses de insulina.
Tipos de pancreatite
A enfermidade ocorre en formas agudas e crónicas.
En forma aguda, debido á inflamación, o zume do páncreas non pasa no lumen do duodeno, senón que dixerir os tecidos do propio páncreas. Este proceso provoca cambios necróticos nas células do órgano enfermo e, en casos especialmente graves, a morte completa de toda a glándula.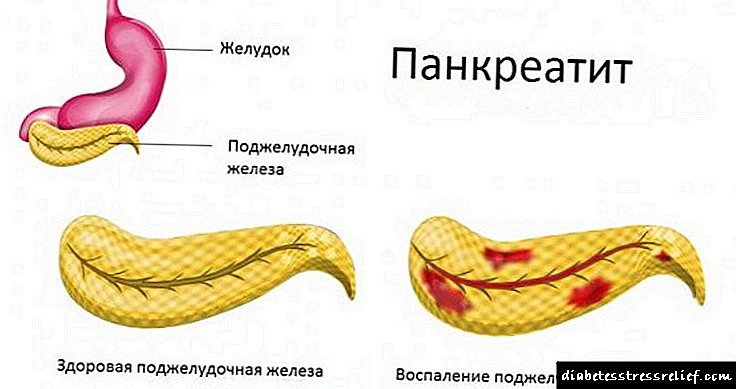
A pancreatite crónica, segundo a causa, clasifícase do seguinte xeito:
- Primaria - orixinalmente xurdida no páncreas por algún motivo.
- Secundario - é consecuencia de enfermidades doutros órganos: colecistite, úlceras, enterocolite.
- Postraumático: consecuencia da exposición mecánica ou da cirurxía. O mecanismo da diabetes
A diabetes mellitus tipo 1, con pancreatite, aparece debido a que os condutos pancreáticos inflamados non pasan enzimas dixestivas ao lumen do duodeno 12 e comeza a autoxestión, a dexeneración do tecido celular en morte gorda, conectiva ou completa de fragmentos de órganos. O corpo experimenta unha deficiencia absoluta de insulina e aumenta o nivel de glicosa no sangue, que afecta destrutivamente a todos os sistemas do corpo.
A diabetes tipo 2 ocorre cunha produción de insulina suficiente. Pero debido a unha violación dos mecanismos metabólicos, non cumpre a súa función principal, creando unha insuficiencia relativa.
Os cambios patolóxicos acumulan co paso do tempo e divídense en catro etapas:
- Na primeira fase, as exacerbacións a curto prazo están intercaladas con calmas longas. Na glándula fórmase unha inflamación crónica, que flúe principalmente con síndromes de dor rara. Este período pode durar ata 10-15 anos.
- A segunda fase caracterízase por unha disfunción máis pronunciada do sistema dixestivo. A inflamación provoca unha liberación incontrolada de insulina no sangue, o que pode levar incluso a unha hipoglucemia temporal. A condición xeral complícase coa deterioración de feces, náuseas, diminución do apetito, formación de gases en todas as seccións do tracto gastrointestinal.
- A funcionalidade do páncreas redúcese de xeito crítico. E, se no estómago baleiro, as probas non revelan desviacións, entón despois de comer, a glicosa no plasma sanguíneo determínase moito máis alá do intervalo de tempo normal.
- E na última etapa, prodúcese diabete secundario, que afecta a un terzo dos pacientes con pancreatite crónica.
Características do curso da diabetes na pancreatite crónica
Sería lóxico concluír que dúas enfermidades son moito máis difíciles de tratar que unha. Pero a práctica demostra o fracaso de tal conclusión. O proceso secundario ten unha serie de características, grazas ás cales pódese curar ben:
- Case sen cetoacitosis,
- O tratamento con insulina adoita levar á hipoglucemia,
- Bo para dietas baixas en carbohidratos,
- Na primeira etapa, os medicamentos orais para a diabetes curan bastante eficaz Prevención e tratamento da diabetes mellitus pancreática
Non todas as pancreatitis crónicas provocan necesariamente o desenvolvemento da diabetes. Cun tratamento adecuado e unha dieta estrita, non só podes mellorar o páncreas, senón tamén evitar a aparición de diabetes.
O médico endocrinólogo selecciona o tratamento individual en cada caso. Dependendo dos indicadores da produción de enzimas dixestivas pola glándula, un especialista competente prescribe unha terapia de substitución baseada en enzimas farmacéuticas dunha acción similar. Así como inxeccións de insulina se é necesario.
Nutrición para pancreatite e diabetes

Debe saber que o tratamento adecuado e a estricta adhesión á dieta poden levar á curación completa destas doenzas graves. Coma a miúdo e en pequenas porcións: 250-300 gramos por comida. Dea preferencia aos produtos que conteñen proteínas: soia, clara de ovo, carne, peixe, noces.
Elimina da dieta alimentos ácidos que provocan unha secreción rápida de zume gástrico: ácidos, picantes, fumados, fritos, que conteñan alcohol, demasiado quentes ou fríos. Nunha palabra, todos os pratos. o que pode causar estrés adicional na secreción pancreática.
A comida prefírese ao vapor e consúmase en quente, en vez de quente ou fría.
Se é difícil elixir de xeito independente a dieta correcta, pode aplicar recomendacións dietéticas especialmente deseñadas recollidas baixo os nomes: táboa nº 5 para pacientes con pancreatite e táboa nº 9 para diabéticos. Pero antes de escoller esta ou esa dieta, é necesario consultar co seu médico.
Só tendo en conta todas as características do curso da enfermidade e as condicións xerais do paciente, o médico dá as recomendacións máis precisas sobre nutrición.
Selección de produtos
En diferentes períodos da enfermidade, a dieta pode variar lixeiramente. Así, por exemplo, as froitas doces e azedo ou os pratos a base de arroz, fariña de avea e sêmola son bastante aceptables durante períodos de remisións prolongadas, están completamente excluídos cando a enfermidade empeora.
Os produtos axeitados deben seleccionarse individualmente para cada paciente, tendo en conta:
- Preferencias persoais
- Captación de glucosa
- Intolerancia a calquera sustancia
- Corrección da absorción parcial de nutrientes.

No período agudo, está estrictamente prohibido comer pratos cun alto contido en azucre, alimentos graxos e afumados, pastelería, fritos, cereais: arroz, fariña de avena, sêmola, froitas e verduras cruas, pan branco.
En canto aos aceites vexetais, é mellor usar, nunha cantidade razoable, linaza e oliva do primeiro prensado en frío, que teñen propiedades curativas. Tamén danará o leite cun baixo contido de graxa. O leite enriquece o corpo con vitaminas, minerais e axuda a aliviar os procesos inflamatorios no tracto dixestivo.
Por desgraza, a xente está tan disposta que, entendendo todo o valor da saúde, aínda "cava a súa tumba cunha culler". Pero a mesma sabedoría popular hai moito tempo atopou unha solución sinxela aos problemas co páncreas: fame, frío e paz.
Seguindo esta sinxela regra e seguindo unha terapia especialmente seleccionada, a maioría dos pacientes poderían superar moitas enfermidades e volver a un estado saudable e completo.