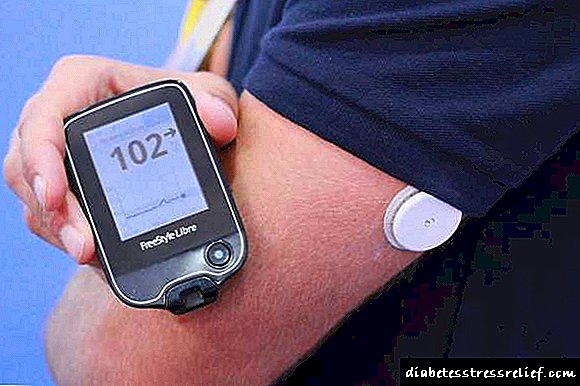
Como usar a suspensión Penfill de NovoMix 30
Nome internacional - novomix 30 penfill
Composición e forma de lanzamento.
Suspensión por administración de SC branco, homoxéneo (sen grumos, poden aparecer flocos na mostra), cando se estratifica, se estratifica, formando un precipitado branco e un sobrenadante incoloro ou case incoloro, cunha mestura coidadosa do precipitado debería formarse unha suspensión homoxénea. 1 ml contén insulina bifásica aspart - 100 UI (3,5 mg), insulina aspart soluble - 30%, proteína insulina aspart protamina - 70%.
Excipientes: glicerol - 16 mg, fenol - 1,5 mg, metacresol - 1,72 mg, cloruro de cinc - 19,6 μg, cloruro sódico - 0,877 mg, fosfato sódico dihidrato - 1,25 mg, sulfato de protamina
0,33 mg de hidróxido sódico
2,2 mg, ácido clorhídrico
1,7 mg, auga d / i - ata 1 ml.
Suspensión d / p / á introdución de 100 pezas / 1 ml: cartuchos 3 ml 5 unidades.
3 ml (300 Pezas) - cartuchos (5) - ampollas (1) - paquetes de cartón.
Acción farmacolóxica.
NovoMix 30 Penfill é unha suspensión bifásica constituída por unha mestura de análogos de insulina: insulina soluble aspart (análogo de insulina de acción curta do 30%) e cristais de insulina aspart protamina (70% análoga de insulina de acción media).
A sustancia activa NovoMix 30 Penfill é insulina aspart, producida polo método de biotecnoloxía do ADN recombinante empregando a cepa Saccharomyces cerevisiae.
Insulin aspart é unha insulina humana soluble equipotencial baseada en índices de molaridade.
Unha diminución da glicosa no sangue prodúcese debido ao aumento do seu transporte intracelular despois da unión de insulina aspart aos receptores de insulina do músculo e dos tecidos graxos e a inhibición simultánea da produción de glicosa polo fígado.
Despois da administración subcutánea de NovoMix 30 Penfill, o efecto desenvólvese dentro de 10-20 minutos. Máximo
o efecto obsérvase no intervalo de 1 a 4 horas despois da inxección. A duración do medicamento chega ás 24 horas.
Nun ensaio clínico comparativo de tres meses en que participaron pacientes con diabetes tipo 1 e tipo 2 que recibiron NovoMix 30 Penfill e insulina humana bifásica 30 dúas veces ao día antes do almorzo e a cea, NovoMix 30 Penfill reduciuse con máis forza a glicosa no sangue postprandial (despois almorzo e cea).
Metaanálise de datos de nove ensaios clínicos con pacientes diabéticos
Os tipos 1 e 2 demostraron que NovoMix 30 Penfill, cando se administra antes do almorzo e a cea, proporciona un mellor control dos niveis de glicosa en sangue posprandina (aumento medio dos niveis de glicosa prandial despois do almorzo, xantar e cea), en comparación coa insulina bifásica 30 humana.
Aínda que a glicosa en xaxún foi maior en pacientes que usaban NovoMix 30 Penfill, en xeral, NovoMix 30 Penfill ten o mesmo efecto na concentración de hemoglobina glicosilada (HbA)1c), como a insulina bifásica humana 30.
Nun estudo clínico que implicou a 341 pacientes con diabetes tipo 2, os pacientes foron randomizados aos grupos de tratamento só NovoMix 30 Penfill, NovoMix 30 Penfill en combinación con metformina e metformina en combinación con un derivado da sulfonilurea.
Concentración de HbA1c despois de 16 semanas de tratamento non difiren en pacientes que recibían NovoMix 30 Penfill en combinación con metformina e en pacientes que recibiron metformina en combinación con un derivado de sulfonilurea. Neste estudo, o 57% dos pacientes presentaban unha concentración de HbA basal1c foi superior ao 9%, nestes pacientes a terapia con NovoMix 30 Penfill en combinación con metformina provocou unha diminución máis significativa da concentración
Hba1cque en pacientes que reciben metformina en combinación cun derivado da sulfonilurea.
Noutro estudo, os pacientes con diabetes mellitus tipo 2 con control glicémico deficiente que tomaron medicamentos hipoglicémicos orais foron aleatorizados nos seguintes grupos: recibir NovoMix 30 dúas veces ao día (117 pacientes) e recibir insulina glargina unha vez ao día (116 pacientes). Despois de 28 semanas de consumo de drogas, a diminución media da concentración de HbA1c no grupo NovoMix, 30 Penfill ascenderon ao 2,8% (o valor medio inicial foi do 9,7%). No 66% e 42% dos pacientes que empregan NovoMix 30 Penfill ao final do estudo, o valor de HbA1c estaban por baixo do 1% e do 6,5%, respectivamente. A glicosa media en plasma de xexún diminuíu en aproximadamente 7 mmol / L (de 14,0 mmol / L no inicio do estudo a 7,1 mmol / L).
Os resultados dunha metaanálise de datos obtidos durante ensaios clínicos con pacientes con diabetes mellitus tipo 2 mostraron unha diminución do número total de episodios de hipoglucemia nocturna e hipoglucemia grave con NovoMix 30 Penfill en comparación coa insulina bifásica humana 30. Ao mesmo tempo, hai un risco xeral de día. A hipoglicemia en pacientes que recibían NovoMix 30 Penfill foi maior.
Nenos e adolescentes. Realizouse un estudo clínico de 16 semanas que comparou a glicosa no sangue despois das comidas con NovoMix 30 (antes das comidas), insulina humana / insulina bifásica humana 30 (antes das comidas) e isofan-insulina (administrada antes de durmir). O estudo participou a 167 pacientes de 10 a 18 anos. Medias de HbA1c en ambos os grupos mantívose preto dos valores iniciais ao longo do estudo. Ademais, ao usar NovoMix 30 Penfill ou insulina bifásica humana 30, non houbo diferenzas na incidencia da hipoglucemia.
Tamén se realizou un estudo transversal de dobre cego nunha poboación de pacientes de 6 a 12 anos (un total de 54 pacientes, 12 semanas para cada tipo de tratamento). A incidencia da hipoglucemia e un aumento da glicosa despois dunha comida no grupo de pacientes que utilizan NovoMix 30 Penfill foron significativamente máis baixos en comparación cos valores do grupo de pacientes que usaban insulina bifásica humana. 30 valores de HbA1c ao final do estudo, no grupo de insulina bifásica humana 30 foron significativamente inferiores que no grupo de pacientes que utilizaban NovoMix 30 Penfill.
Pacientes anciáns. Farmacodinámica NovoMix 30 Penfill en pacientes anciáns e senís non se estudou. Non obstante, nun estudo de sección transversal aleatoria de dobre cego realizado en 19 pacientes con diabetes mellitus tipo 2 con idades comprendidas entre 65 e 83 anos (idade media de 70 anos), comparáronse a farmacodinámica e a farmacocinética de insulina aspart e insulina humana soluble. Diferencias relativas na farmacodinámica (taxa máxima de infusión de glicosa - GIRmáx e a zona baixo a curva da súa velocidade de infusión durante 120 min despois da administración de preparados de insulina - AUCGIR, 0-120 min) entre insulina aspart e insulina humana en pacientes anciáns foi similar á de voluntarios sans e en pacientes máis novos con diabetes mellitus.
Farmacocinética
En insulina aspart, a substitución do aminoácido prolino na posición B28 por ácido aspartico reduce a tendencia das moléculas a formar hexámeros na fracción soluble de NovoMix 30 Penfill, que se observa na insulina humana soluble. Neste sentido, a insulina aspart (30%) é absorbida da graxa subcutánea máis rápido que a insulina soluble contida na insulina bifásica humana. O 70% restante recae na forma cristalina, protamina-insulina aspart, cuxa taxa de absorción é a mesma que a da insulina humana NPH.
A concentración máxima de insulina no soro sanguíneo despois da administración de NovoMix 30 Penfill é un 50% superior á da insulina bifásica humana 30, e o tempo que leva para conseguilo é o dobre do que a insulina bifásica humana 30.
En voluntarios sans, despois da administración de NovoMix 30 a razón de 0,20 U / kg de peso corporal, a concentración máxima de insulina aspart no soro sanguíneo alcanzouse aos 60 minutos e ascendeu a 140 ± 32 pmol / L. Duración T1/2NovoMix 30, que reflicte a taxa de absorción da fracción asociada á protamina, foi de 8 a 9 horas. Os niveis de insulina sérica volveron á liña base 15-18 horas despois da administración subcutánea do medicamento. En pacientes con diabetes mellitus tipo 2, a concentración máxima alcanzouse 95 minutos despois da administración e mantívose por encima da liña base durante polo menos 14 horas.
Pacientes anciáns e senís. Non se realizou un estudo sobre a farmacocinética de NovoMix 30 en pacientes anciáns e senís. Non obstante, as diferenzas relativas na farmacocinética entre insulina aspart e insulina soluble humana en pacientes anciáns con diabetes tipo 2 (entre 65 e 83 anos, idade media - 70 anos) foron similares ás de voluntarios sans e en pacientes máis novos con diabetes mellitus. En pacientes anciáns, observouse unha diminución da taxa de absorción, o que provocou unha desaceleración da Tmáx (82 minutos (rango interquartil: 60-120 minutos)), mentres que a concentración máxima media (Cmáx) foi semellante á observada en pacientes máis novos con diabetes tipo 2 e algo menos que en pacientes con diabetes tipo 1.
Pacientes con insuficiencia renal e hepática. Non se realizou un estudo da farmacocinética de NovoMix 30 Penfill en pacientes con insuficiencia renal e hepática. Non obstante, cun aumento da dose do medicamento en pacientes con distintos graos de alteración da función renal e hepática, non houbo ningún cambio na farmacocinética da insulina aspart soluble.
Nenos e adolescentes. Non se estudaron as propiedades farmacocinéticas de NovoMix 30 Penfill en nenos e adolescentes. Non obstante
Estudáronse as propiedades farmacocinéticas e farmacodinámicas da insulina aspart soluble en nenos (de 6 a 12 anos) e adolescentes (de 13 a 17 anos) con diabetes tipo 1.
En pacientes de ambos os grupos de idade, a insulina aspart caracterizouse por unha rápida absorción e valores de Tmáxsemellantes ás dos adultos. Non obstante, os valores de Cmáx en dous grupos de idade foron diferentes, o que indica a importancia da selección individual de doses de insulina aspart.
Seguridade suburbana preclínica. No curso de estudos preclínicos, non había perigo para os humanos, baseados en datos xeralmente aceptados.
estudos de seguridade farmacolóxica, reutilización de toxicidade, xenotoxicidade e toxicidade reprodutiva.
En ensaios in vitro, que incluíron a unión a receptores de insulina e IGF-1 e o efecto no crecemento celular, demostrouse que as propiedades da insulina aspart son similares ás da insulina humana. Os estudos demostraron tamén que a disociación da unión de insulina aspart aos receptores de insulina é equivalente á da insulina humana.
Diabetes mellitus tipo 1. Diabetes mellitus tipo 2 (no caso de resistencia a axentes hipoglucemicos orais, resistencia parcial a estes fármacos durante a terapia combinada, enfermidades intercurrentes).
Réxime de dosificación e método de aplicación da nova mestura 30 penfill.
NovoMix 30 Penfill está pensado para a administración subcutánea. Non pode ingresar NovoMix 30 Penfill por vía intravenosa, xa que isto pode levar a unha hipoglucemia grave. NovoMix 30. Tamén se debe evitar intramuscular NovoMix 30 Non se pode usar Penfill para infusión de insulina subcutánea (PPII) nas bombas de insulina. A dose de NovoMix 30 Penfill é determinada polo médico individualmente en cada caso, de acordo coas necesidades do paciente. Para alcanzar o nivel óptimo de glicemia, recoméndase controlar a concentración de glicosa no sangue e axustar a dose do medicamento.
Os pacientes con diabetes tipo 2, NovoMix 30 Penfill, poden prescribirse tanto como monoterapia como en combinación con fármacos hipoglicémicos orais nos casos en que o nivel de glicosa no sangue está insuficientemente regulado só por medicamentos hipoglicémicos orais.
O comezo da terapia. Para os pacientes con diabetes tipo 2 que reciben primeiro insulina, a dose inicial recomendada de NovoMix 30 Penfill é de 6 unidades antes do almorzo e 6 unidades antes da cea. Tamén está permitida a introdución de 12 unidades de NovoMix 30 Penfill unha vez ao día pola noite (antes da cea).
Transferir o paciente doutras preparacións de insulina. Ao transferir un paciente de insulina humana bifásica a NovoMix 30 Penfill debería comezar coa mesma
dose e modo de administración. A continuación, axuste a dose de acordo coas necesidades individuais do paciente (ver as seguintes recomendacións para a valoración da dose do medicamento). Como sempre, ao transferir un paciente a un novo tipo de insulina é necesaria unha supervisión médica estrita durante a transferencia do paciente e nas primeiras semanas de usar o novo medicamento.
Intensificación da terapia. É posible reforzar a NovoMix 30 Penfill terapia pasando dunha única dose diaria a unha dobre. Recoméndase que tras alcanzar unha dose de 30 unidades do medicamento cambie ao uso de NovoMix 30 Penfill dúas veces ao día, dividindo a dose en dúas partes iguais - mañá e noite (antes do almorzo e a cea). A transición ao uso de NovoMix 30 Penfill tres veces ao día é posible dividindo a dose da mañá en dúas partes iguais e introducindo estas dúas partes pola mañá e ao xantar (tres veces ao día).
Axuste da dose. Para axustar a dose de NovoMix 30 Penfill, úsase a menor concentración de glucosa en xaxún obtida nos últimos tres días. Para avaliar a adecuación da dose anterior, use o valor da concentración de glicosa no sangue antes da seguinte comida. O axuste da dose pódese facer unha vez á semana ata que se alcance o valor HbA obxectivo.1c. Non aumente a dose do medicamento se se observou hipoglucemia durante este período. O axuste da dose pode ser necesario cando aumente a actividade física do paciente, cambie a súa dieta normal ou teña unha condor. Para axustar a dose de NovoMix 30 Penfill, recoméndase empregar as seguintes recomendacións para a valoración da dose:
| Concentración de glicosa no sangue antes das comidas | NovoMkks 30 corrección do foso | |
| 10 mmol / l | > 180 mg / dl | + 6 unidades |
Grupos especiais de pacientes. Como sempre, cando se empregan preparados de insulina, en pacientes de grupos especiais, a concentración de glicosa en sangue debe controlarse con máis coidado e axustar a dose de aspart aspart individualmente.
Pacientes anciáns e senís. NovoMix 30 Penfill pódese usar en pacientes anciáns. Non obstante, a experiencia co seu uso en combinación con fármacos hipoglicémicos orais en pacientes maiores de 75 anos é limitada.
Pacientes con insuficiencia renal e hepática. En pacientes con insuficiencia renal ou hepática, pódese reducir a necesidade de insulina.
Nenos e adolescentes. NovoMix 30 Penfill pódese usar para tratar nenos e adolescentes maiores de 10 anos nos casos nos que se prefire o uso de insulina pre-mesturada. Hai datos clínicos limitados para nenos de 6 a 9 anos (ver sección Propiedades farmacodinámicas).
NovoMix 30 Penfill debe administrarse de forma subcutánea na coxa ou na parede abdominal anterior. Se o desexa, a droga pódese administrar ao ombreiro ou ás nádegas.
É necesario cambiar o sitio da inxección dentro da rexión anatómica para evitar o desenvolvemento de lipodistrofia.
Como en calquera outra preparación de insulina, a duración da acción de NovoMix 30 Penfill depende da dose, lugar de administración, intensidade do fluxo sanguíneo, temperatura e nivel de actividade física.
En comparación coa insulina humana bifásica, NovoMix 30 Penfill comeza a actuar con máis rapidez, polo que debe administrarse inmediatamente antes das comidas. Se é necesario, pode administrarse NovoMix 30 Penfill pouco despois dunha comida.
Instrucións para pacientes sobre o uso de NovoMix 30 Penfill.
Non podes empregar NovoMix 30 Penfill:
Se é alérxico (hipersensible) á insulina aspart ou a algún dos compoñentes que compoñen NovoMix 30 Penfill.
Se sente que se achega a hipoglucemia (baixo contido de azucre no sangue).
Para infusión de insulina subcutánea (PPII) en bombas de isisulina.
Se se caen os cartuchos ou dispositivos de inserción co cartucho instalado ou o cartucho está danado ou esmagado.
Se se violaron as condicións de almacenamento da droga ou se conxelou.
Se a insulina non se torna uniformemente branca e turbia despois da mestura.
Se quedan grumos brancos na preparación despois da mestura ou se as partículas brancas se pegan ao fondo ou ás paredes do cartucho.
Antes de usar NovoMix 30 Penfill:
Comprobe a etiqueta para asegurarse de que se seleccionou o tipo correcto de insulina.
Verifique sempre o cartucho, incluído o pistón de goma. Non use o cartucho se ten danos visibles ou se existe un espazo entre o pistón e a franxa branca do cartucho. Para obter máis información, consulte as instrucións para usar o sistema para a administración de insulina.
Use sempre unha nova agulla para cada inxección para evitar a infección.
NovoMix 30 Penfill e agullas están pensadas só para uso individual.
NovoMix 30 é para inxección subcutánea. Nunca administre esta insulina por vía intravenosa ou intramuscular.
Cada vez, cambie o sitio da inxección dentro da rexión anatómica. Isto axudará a reducir o risco de selos e ulceraciones no lugar da inxección. Os mellores lugares para a inxección son a parede abdominal anterior, as nádegas, a coxa anterior ou o ombreiro. A insulina actuará máis rápido se se introduce na parede abdominal anterior. Supervisa regularmente a concentración de glicosa no sangue.
O procedemento para a mestura de insulina.
Antes de colocar o cartucho no sistema de inxección para administrar insulina, manteña a temperatura ambiente e logo mestúrao como se describe a continuación:
Cando use NovoMix 30 Penfill por primeira vez, enrolle o cartucho coas palmas das 10 veces. É importante que o cartucho estea en posición horizontal. A continuación, levante e baixe o cartucho 10 veces cara arriba e abaixo para que a bola de vidro dentro do cartucho se mova dun extremo do cartucho ao outro. Repita estas manipulacións ata que
ata que o líquido quede uniformemente branco e turbio. O procedemento de mestura será máis doado se a estas alturas a insulina chegou á temperatura ambiente. Inxectar inmediatamente.
Antes de cada inxección posterior, axite o dispositivo de inxección co cartucho nel ata que o líquido quede uniformemente branco e turbio, pero polo menos 10 veces. Inxectar inmediatamente.
Asegúrese de que polo menos 12 unidades de insulina queden no cartucho para garantir unha mestura uniforme. Se quedan menos de 12 unidades, use o novo NovoMix 30 Penfill.
Como administrar insulina.
A insulina debe inxectarse baixo a pel. Use a técnica de inxección recomendada polo seu médico ou enfermeira, siga as instrucións para administrar insulina como se describe nas instrucións do seu dispositivo para administrar insulina.
Manteña a agulla debaixo da pel durante polo menos 6 segundos. Manteña o gatillo presionado ata que a agulla se saque de debaixo da pel. Isto asegurará que se manteña unha dose completa de insulina e evitará que o sangue entre na agulla ou no cartucho de insulina.
Despois de cada inxección, asegúrese de eliminar e descartar a agulla, nunca garde NovoMix 30 Penfill coa agulla pegada. Se non, o líquido pode filtrarse, o que pode provocar unha dose incorrecta de insulina.
Non reencher o cartucho con insulina.
NovoMix 30 Penfill está deseñado para o seu uso con sistemas de inxección de insulina Novo Nordisk e agullas NovoFine ou NovoTvist.
Se NovoMix 30 Penfill e a outra insulina do cartucho Penfill se usan ao mesmo tempo para o tratamento, é necesario empregar dous sistemas separados para a administración da insulina, un para cada tipo de insulina.
Por precaución, leve sempre un reposto para a entrega de insulina no caso de que perdas ou danas o teu NovoMix 30 Penfill.
Precaucións para o uso nova mestura 30 penfilla.
NovoMix 30 Penfill e agullas son para uso persoal. Non encher o cartucho Penfill. NovoMix 30 Penfill non se pode usar se despois da mestura non se volve uniformemente branco e turbo. Cómpre salientar ao paciente a necesidade de mesturar a suspensión NovoMix 30 Penfill inmediatamente antes do uso. Non podes usar NovoMix 30 Penfill se estivo conxelado. Os pacientes deben ser avisados para que descarten a agulla despois de cada inxección.
Efecto secundario.
As reaccións adversas observadas en pacientes que utilizan NovoMix 30 débense principalmente ao efecto farmacolóxico da insulina. O acontecemento adverso máis común coa insulina é a hipoglucemia. A incidencia de efectos secundarios asociados ao uso de NovoMix 30 varía segundo a poboación do paciente, o réxime de dosificación do fármaco e o control glicémico.
Na fase inicial da insulinoterapia, poden producirse erros de refracción, edema e reaccións no lugar da inxección
droga (incluíndo dor, vermelhidão, urticaria, inflamación, hematoma, inchazo e picazón no lugar da inxección). Estes síntomas adoitan ser temporais. Unha rápida mellora do control glicémico pode levar a un estado de "neuropatía de dor aguda", que normalmente é reversible. A intensificación da insulinoterapia cunha forte mellora do control do metabolismo dos carbohidratos pode levar a un deterioro temporal do estado da retinopatía diabética, mentres que unha mellora a longo prazo do control glicémico reduce o risco de progresión da retinopatía diabética. A lista de efectos secundarios preséntase na táboa.
Todos os efectos secundarios que se presentan a continuación, baseados en datos de ensaios clínicos, agrúpanse segundo a frecuencia de desenvolvemento segundo MedDRA e os sistemas de órganos. A incidencia de efectos secundarios defínese como: moi a miúdo (≥1 / 10), a miúdo (≥ 1/100 a drogas, retardando a absorción de alimentos).
As enfermidades concomitantes, especialmente infecciosas e acompañadas de febre, adoitan aumentar a necesidade do corpo de insulina. O axuste da dose tamén pode ser necesario se o paciente ten enfermidades concomitantes dos riles, fígado, alteración da función suprarenal, hipófise ou glándula tiroides.
Ao transferir un paciente a outro tipo de insulina, os primeiros síntomas dos precursores da hipoglucemia poden cambiar ou facerse menos pronunciados en comparación cos que usan o tipo anterior de insulina.
Traslado do paciente doutros preparados de insulina. A transferencia do paciente a un novo tipo de insulina ou a unha preparación de insulina doutro fabricante debe realizarse baixo estricta supervisión médica. Se cambia a concentración, tipo, fabricante e tipo (insulina humana, un análogo da insulina humana) dos preparados de insulina e / ou o método de produción, pode ser necesario un cambio de dose. Os pacientes que pasan doutras preparacións de insulina ao tratamento con NovoMix 30 Penfill poden ter que aumentar a frecuencia das inxeccións ou cambiar a dose en comparación coas doses dos preparados de insulina utilizados anteriormente. Se é necesario, axuste de dose, pódese facer xa na primeira inxección do medicamento ou durante as primeiras semanas ou meses de tratamento.
Reaccións no lugar da inxección. Como ocorre con outros tratamentos coa insulina, as reaccións poden desenvolverse no lugar da inxección, que se manifesta por dor, vermelhidão, colmeas, inflamación, hematomas, inchazo e picazón. O cambio regular do sitio da inxección na mesma rexión anatómica pode reducir os síntomas ou evitar o desenvolvemento destas reaccións. As reaccións normalmente desaparecen dentro duns días a varias semanas. En poucos casos, NovoMix 30 Penfill pode ser necesario cancelar debido ás reaccións no lugar da inxección.
O uso simultáneo de fármacos do grupo tiazolidinione e preparados de insulina.Informáronse casos de desenvolvemento de insuficiencia cardíaca crónica no tratamento de pacientes con tiazolidinediones en combinación con preparados de insulina, especialmente se tales pacientes teñen factores de risco para o desenvolvemento de insuficiencia cardíaca crónica. Este feito debe terse en conta á hora de prescribir a terapia combinada con tiazolidinediones e preparados de insulina a pacientes. Co nomeamento de tal terapia combinada, é necesario realizar exames médicos dos pacientes para identificar signos e síntomas de insuficiencia cardíaca crónica, aumento de peso e presenza de edema. Se os síntomas de insuficiencia cardíaca empeoran en pacientes, o tratamento con tiazolidinediones debe deixarse.
Influencia na capacidade para conducir vehículos e traballar con mecanismos.A capacidade dos pacientes para concentrarse e a velocidade de reacción pode verse alterada durante a hipoglucemia, o que pode ser perigoso en situacións nas que estas habilidades son especialmente necesarias (por exemplo, cando conducen vehículos ou traballan con máquinas e mecanismos).
Debe aconsellar aos pacientes que adopten medidas para evitar o desenvolvemento de hipoglucemia mentres conducen. Isto é especialmente importante para pacientes sen síntomas diminuídos de precursores de desenvolver hipoglucemia ou que padecen episodios frecuentes de hipoglucemia. Nestes casos, debe considerarse a adecuación da condución e a realización deste traballo.
Sobredose.
Non se estableceu unha dose específica requirida para unha sobredose de insulina, pero a hipoglucemia pode desenvolverse gradualmente se se administran doses demasiado altas de insulina en relación ás necesidades do paciente.
O paciente pode eliminar unha hipoglucemia leve tomando glicosa ou alimentos que conteñan azucre. Por iso, recoméndase a pacientes con diabetes levar constantemente produtos que conteñen azucre.
En caso de hipoglucemia grave, cando o paciente está inconsciente, debe administrarse 0,5 mg a 1 mg de glucágono intramuscular ou subcutáneamente (unha persoa adestrada pode administrar) ou unha solución de glicosa intravenosa (dextrosa) (só un médico médico pode administrar). Tamén é necesario administrar dextrosa por vía intravenosa se o paciente non recupera a consciencia 10-15 minutos despois da administración de glucagón. Despois de recuperar a conciencia, aconséllase que o paciente tome alimentos ricos en carbohidratos para evitar a recorrencia da hipoglucemia.
Interaccións con outras drogas.
efecto hipoglicémico da insulina aumentar os fármacos hipoglicémicos orais, inhibidores de man, inhibidores de ACE, inhibidores de anhidrase carbónica, bloqueadores beta non selectivos, bromocriptina, octreótido, sulfonamidas, esteroides Anabolica, tetraciclinas, clofibrato, o cetoconazol, o mebendazol, piridoxina, teofilina, ciclofosfamida, fenfluramina, drogas Li +, etanol e medicamentos que conteñen etanol. Os anticonceptivos orais, corticosteroides, hormonas tiroideas, diuréticos tiazídicos, heparina, antidepresivos tricíclicos, simpatomiméticos, danazol, clonidina, BMKK, diazoxido, morfina, fenitoína, nicotina debilitan o efecto hipoglucémico da insulina. Baixo a influencia de reserpina e salicilados, é posible tanto un debilitamento coma un aumento da acción do medicamento.
Condicións de vacacións das farmacias.
Termos e condicións de almacenamento.
Almacenar a unha temperatura de 2 ° C a 8 ° C (na neveira), pero non preto do conxelador. Non conxele. Para cartuchos abertos: Non garde na neveira. Almacenar a unha temperatura non superior a 30 ºC. Use dentro de 4 semanas.
Almacene os cartuchos nunha caixa de cartón para protexer da luz.
NovoMix 30 Penfill debe protexerse contra calor e luz excesiva. Manter fóra do alcance dos nenos.
A vida útil é de 2 anos.
O uso do medicamento Novomix 30 penfill só segundo o prescrito polo médico, as instrucións danse como referencia!
Forma de solicitude de NovoMix 30 Penfill en suspensión
NovoMix® 30 Penfill® está destinado á administración subcutánea. Non administre NovoMix® 30 Penfill® por vía intravenosa, xa que isto pode levar a unha hipoglucemia grave. Tamén se debe evitar a administración intramuscular de NovoMix® 30 Penfill®. Non use NovoMix® 30 Penfill® para infusión de insulina subcutánea (PPII) en bombas de insulina.
A dose de NovoMix® 30 Penfill® é determinada polo médico individualmente en cada caso, de acordo coas necesidades do paciente. Para alcanzar o nivel óptimo de glicemia, recoméndase controlar a concentración de glicosa no sangue e axustar a dose do medicamento.
Os pacientes con diabetes tipo 2, NovoMix® 30 Penfill® poden prescribirse tanto como monoterapia como en combinación con fármacos hipoglicémicos orais nos casos en que o nivel de glicosa no sangue está insuficientemente regulado só por medicamentos hipoglucemicos orais.
Para os pacientes con diabetes tipo 2 que reciben primeiro insulina, a dose inicial recomendada de NovoMix® 30 Penfill® é de 6 unidades antes do almorzo e 6 unidades antes da cea. Tamén está permitida a introdución de 12 unidades de NovoMix® 30 Penfill® unha vez ao día pola noite (antes da cea).
Traslado dun paciente doutros preparados de insulina
Ao transferir un paciente de insulina humana bifásica a NovoMix® 30, Penfill® debe comezar coa mesma dose e modo de administración. A continuación, axuste a dose de acordo coas necesidades individuais do paciente (ver as seguintes recomendacións para a valoración da dose do medicamento). Como sempre cando se traslada un paciente a un novo tipo de insulina, requírese unha supervisión médica estrita durante a transferencia do paciente e nas primeiras semanas de usar o novo medicamento.
É posible reforzar a terapia con NovoMix® 30 Penfill® pasando dunha única dose diaria a unha dobre. Recoméndase que despois de alcanzar unha dose de 30 unidades do medicamento cambie ao uso de NovoMix® 30 Penfill® dúas veces ao día, dividir a dose en dúas partes iguais - mañá e noite (antes do almorzo e a cea). A transición ao uso de NovoMix® 30 Penfill® tres veces ao día é posible dividindo a dose da mañá en dúas partes iguais e introducindo estas dúas partes pola mañá e ao xantar (tres veces ao día).
Para axustar a dose de NovoMix® 30 Penfill®, úsase a menor concentración de glicosa en sangue obtida nos últimos tres días.
Para avaliar a adecuación da dose anterior, use o valor da concentración de glicosa no sangue antes da seguinte comida.
O axuste da dose pódese realizar unha vez á semana ata alcanzar o valor obxectivo de HbA1c.
Non aumente a dose do medicamento se se observou hipoglucemia durante este período.
O axuste da dose pode ser necesario cando aumente a actividade física do paciente, cambie a súa dieta normal ou teña unha condor.
Para axustar a dose de NovoMix® 30 Penfill®, recoméndase empregar as seguintes recomendacións para a valoración da dose:
Concentración de glicosa no sangue antes das comidas
Grupos especiais de pacientes
Como sempre, cando se empregan preparados de insulina, en pacientes de grupos especiais, a concentración de glicosa en sangue debe controlarse con máis coidado e axustar a dose de aspart aspart individualmente.
Pacientes anciáns e senís
NovoMix® 30 Penfill® pode usarse en pacientes anciáns. Non obstante, a experiencia co seu uso en combinación con fármacos hipoglicémicos orais en pacientes maiores de 75 anos é limitada.
Pacientes con insuficiencia renal e hepática:
En pacientes con insuficiencia renal ou hepática, pódese reducir a necesidade de insulina.
Nenos e adolescentes:
NovoMix® 30 Penfill® pode usarse para tratar nenos e adolescentes maiores de 10 anos nos casos nos que se prefire o uso de insulina pre-mesturada. Hai datos clínicos limitados para nenos de 6 a 9 anos (ver sección Propiedades farmacodinámicas).
NovoMix® 30 Penfill® debe administrarse de forma subcutánea na coxa ou na parede abdominal anterior. Se o desexa, a droga pódese administrar ao ombreiro ou ás nádegas.
É necesario cambiar o sitio da inxección dentro da rexión anatómica para evitar o desenvolvemento de lipodistrofia. Como en calquera outra preparación de insulina, a duración da acción de NovoMix® 30 Penfill® depende da dose, lugar de administración, intensidade do fluxo sanguíneo, temperatura e nivel de actividade física.
En comparación coa insulina bifásica humana, NovoMix® 30 Penfill® actúa máis rapidamente, polo que debe administrarse inmediatamente antes das comidas. Se é necesario, pode administrarse NovoMix® 30 Penfill® pouco despois dunha comida.
Como usar: dosificación e curso do tratamento
S / c na coxa ou parede abdominal anterior. Se é necesario, na zona do ombreiro ou das nádegas. É necesario cambiar o sitio da inxección dentro da rexión anatómica para evitar o desenvolvemento de lipodistrofia. A droga adminístrase inmediatamente antes dunha comida, se é necesario, inmediatamente despois dunha comida. A temperatura da insulina administrada debe estar a temperatura ambiente.
A dose do medicamento é determinada polo médico individualmente en cada caso, en función da concentración de glicosa no sangue. A media, a dose diaria de NovoMix 30 Penfill é de 0,5-1 U / kg de peso corporal. En pacientes con resistencia á insulina (incluída a obesidade), a necesidade diaria de insulina pode aumentar e en pacientes con secreción endóxena residual de insulina pode reducirse.
Insulina NovoMiks: dose do medicamento para a súa administración, revisións
A insulina NovoMiks é un medicamento composto por análogos da hormona que reduce o azucre humano. É administrado no tratamento da diabetes mellitus, tanto de tipo insulinodependente coma non insulino-dependente. No momento do melón, a enfermidade esténdese por todos os recunchos do planeta, mentres que o 90% dos diabéticos sofre a segunda forma da enfermidade, o 10% restante desde a primeira forma.
| Vídeo (fai clic para reproducir). |
As inxeccións de insulina son vitais, cunha administración insuficiente, ocorren efectos irreversibles no corpo e incluso a morte. Por iso, cada persoa cun diagnóstico de diabetes mellitus, a súa familia e amigos debe estar "armada" co coñecemento sobre medicamentos hipoglucémicos e insulina, así como sobre o seu uso adecuado.
A insulina está dispoñible en Dinamarca en forma de suspensión, que se atopa nun cartucho de 3 ml (NovoMix 30 Penfill) ou nunha xiringa de 3 ml (NovoMix 30 FlexPen). A suspensión é de cor branca, ás veces é posible a formación de flocos. Coa formación dun precipitado branco e un líquido translúcido por riba del, só precisa axitalo, como se indica nas instrucións adxuntas.
As substancias activas do medicamento son insulina aspart soluble (30%) e cristais, así como insulina aspart protamina (70%). Ademais destes compoñentes, o medicamento contén unha pequena cantidade de glicerol, metacresol, hidróxido fosfato sódico dihidrato, cloruro de cinc e outras substancias.
| Vídeo (fai clic para reproducir). |
10-20 minutos despois da introdución do medicamento baixo a pel, comeza o seu efecto hipoglucémico. A insulina aspart únese aos receptores hormonais, polo que a glicosa é absorbida polas células periféricas e inhibe a súa produción do fígado. O maior efecto da administración de insulina obsérvase despois de 1-4 horas, e o seu efecto dura 24 horas.
Os estudos farmacolóxicos ao combinar insulina con fármacos que reducen o azucre do segundo tipo de diabéticos demostraron que NovoMix 30 en combinación con metformina ten un efecto hipoglucemico maior que a combinación de sulfonilurea e derivados da metformina.
Non obstante, os científicos non probaron o efecto da droga en nenos pequenos, persoas de avanzada idade e que padecen patoloxías do fígado ou dos riles.
Só o médico ten dereito a prescribir a dosificación correcta de insulina, tendo en conta o nivel de glicosa no sangue do paciente. Cómpre lembrar que o fármaco se administra tanto co primeiro tipo de enfermidade como cunha terapia ineficaz do segundo tipo.
Dado que a hormona bifásica actúa moito máis rápido que a hormona humana, adoita administrarse antes de comer alimentos, aínda que tamén é posible administralo pouco despois de estar saturado con alimentos.
O indicador medio da necesidade dun diabético nunha hormona, segundo o seu peso (en quilogramos), é de 0,5-1 unidades de acción ao día. A dosificación diaria do medicamento pode aumentar con pacientes insensibles á hormona (por exemplo, con obesidade) ou diminuír cando o paciente ten algunhas reservas de insulina producida. É mellor inxectar na zona da coxa, pero tamén é posible na rexión abdominal das nádegas ou do ombreiro. Non é desexable coitelo no mesmo lugar, incluso dentro da mesma zona.
Insulin NovoMix 30 FlexPen e NovoMix 30 Penfill pódense usar como ferramenta principal ou en combinación con outros fármacos hipoglucemicos. Cando se combina coa metformina, a primeira dose de hormona é de 0,2 unidades de acción por quilogramo e día. O médico poderá calcular a dose destes dous fármacos a partir de indicadores de glicosa no sangue e as características do paciente. Cómpre destacar que as disfuncións renales ou hepáticas poden provocar unha diminución da necesidade dun diabético en insulina.
NovoMix só se administra de forma subcutánea (máis sobre o algoritmo para administrar insulina de forma subcutánea), está prohibido facer inxeccións no músculo ou por vía intravenosa. Para evitar a formación de infiltrados, moitas veces é necesario cambiar a área de inxección. As inxeccións pódense facer en todos os lugares indicados anteriormente, pero o efecto da droga prodúcese moito antes cando se introduce na zona da cintura.
A droga almacénase durante o espírito dos anos desde a data de liberación. Unha nova solución non empregada nun cartucho ou unha xeringa almacénase na neveira de 2 a 8 graos e úsase a temperatura ambiente durante menos de 30 días.
Para evitar a entrada da luz solar, hai que levar un tapón de protección na xeringa.
NovoMix non ten practicamente contraindicacións salvo unha rápida diminución do nivel de azucre ou unha maior susceptibilidade a calquera sustancia contida.
Nótese que durante o parto do neno non se atoparon efectos secundarios na nai e no fillo expectantes.
Cando se amamanta, pódese administrar insulina, xa que non se transmite ao bebé con leite. Pero aínda así, antes de usar NovoMix 30, a muller necesita consultar un médico que prescribirá doses seguras.
En canto ao dano potencial da droga, está principalmente relacionado co tamaño da dosificación. Por iso, é moi importante administrar o medicamento prescrito, seguindo todas as recomendacións do médico. Os efectos secundarios posibles poden incluír:
- O estado de hipoglucemia (máis sobre o que é a hipoglucemia na diabetes mellitus), que vai acompañado de perda de coñecemento e convulsións.
- Erupción na pel, urticaria, picazón, sudoración, reaccións anafilácticas, angioedema, aumento da frecuencia cardíaca e diminución da presión arterial.
- Cambio na refracción, ás veces - desenvolvemento da retinopatía (disfunción dos vasos da retina).
- Distrofia de lípidos no lugar da inxección, así como vermelhidão e inchazo no lugar da inxección.
En casos excepcionais, por descoido do paciente, pode producirse unha sobredose, cuxos síntomas varían, segundo a gravidade da afección. Os signos de hipoglucemia son somnolencia, confusión, náuseas, vómitos, taquicardia.
Cunha sobredose leve, o paciente necesita comer un produto que conteña gran cantidade de azucre. Pode ser galletas, doces, zume doce, é recomendable ter algo nesta lista. Unha sobredose grave require administración inmediata de glucagón subcutáneamente. Se o corpo do paciente non responde á inxección de glucagón, o provedor debe administrar glucosa.
Despois de normalizar a condición, o paciente necesita consumir hidratos de carbono facilmente dixeribles para evitar unha hipoglicemia repetida.
Ao administrar NovoMix 30 inxeccións de insulina, débese dar importancia a que algúns fármacos teñan un efecto sobre o seu efecto hipoglicémico.
O alcol aumenta principalmente o efecto de redución do azucre da insulina e os bloqueadores beta-adrenérxicos enmascaran signos dun estado hipoglucémico.
Dependendo dos medicamentos empregados en combinación coa insulina, a súa actividade pode aumentar e diminuír.
Obsérvase unha diminución da demanda de hormonas ao usar os seguintes medicamentos:
- fármacos hipoglicémicos internos,
- inhibidores da monoamina oxidasa (MAO),
- inhibidores da encima convertedora de angiotensina (ACE),
- bloqueadores beta-adrenérxicos non selectivos,
- octreótido
- esteroides anabolizantes
- salicilados,
- sulfonamidas,
- bebidas alcohólicas
Algúns medicamentos reducen a actividade da insulina e aumentan a necesidade do paciente para ela. Tal proceso prodúcese cando se usa:
- hormonas tiroideas
- glucocorticoides,
- simpatomiméticos
- danazol e tiazidas,
- anticonceptivos que toman internamente.
Algúns medicamentos xeralmente non son compatibles coa insulina NovoMix. Trátase, en primeiro lugar, de produtos que conteñen tioles e sulfitos. Tamén está prohibido engadir á medicina a solución de infusión. O uso de insulina con estes axentes pode producir consecuencias extremadamente graves.
Dado que a droga se produce no exterior, o seu prezo é bastante alto. Pódese mercar con receita médica nunha farmacia ou pedirse en liña no sitio web do vendedor. O custo do medicamento depende de se a solución está no cartucho ou a xeringa e no envase. O prezo varía para NovoMix 30 Penfill (5 cartuchos por paquete) - de 1670 a 1800 rublos rusos, e NovoMix 30 FlexPen (5 xeringas por paquete) ten un custo no rango de 1630 a 2000 rublos rusos.
As críticas sobre a maioría dos diabéticos que inxectaron hormona bifásica son positivas. Algúns din que cambiaron a NovoMix 30 despois de usar outras insulinas sintéticas. Neste sentido, é posible destacar tales vantaxes do fármaco como a facilidade de uso e unha diminución da probabilidade de padecer unha hipoglicemia.
Ademais, aínda que o medicamento ten unha lista considerable de posibles reaccións negativas, poucas veces se producen. Polo tanto, NovoMix pode considerarse unha droga completamente exitosa.
Por suposto, houbo críticas que nalgunhas situacións non cabía. Pero cada fármaco ten contra-indicacións.
Nos casos en que o remedio non sexa adecuado para o paciente ou cause efectos secundarios, o médico que o atende pode cambiar o réxime de tratamento. Para iso, axusta a dose do medicamento ou incluso cancela o seu uso. Por iso, é necesario empregar un medicamento cun efecto hipoglucémico similar.
Cómpre salientar que os preparados NovoMix 30 FlexPen e NovoMix 30 Penfill non teñen análogos no compoñente activo: insulina aspart. O médico pode prescribir un medicamento que teña un efecto similar.
Estes medicamentos véndense por receita médica. Polo tanto, se é necesario, con insulina terapia, o paciente debe consultar a un médico.
Os medicamentos que teñen un efecto similar son:
- Humalog Mix 25 é un análogo sintético da hormona producida polo corpo humano. O compoñente principal é a insulina lispro. O medicamento tamén ten un efecto curto regulando os niveis de glicosa e o seu metabolismo. Trátase dunha suspensión branca, que se libera nunhas plumas de xeringa chamadas Quick Pen. O custo medio dun medicamento (5 plumas de xiringa de 3 ml cada unha) é de 1860 rublos.
- A Himulina M3 é unha insulina de acción media que se libera en suspensión. O país de fabricación do medicamento é Francia. A sustancia activa do fármaco é a insulina biosintética humana. Reduce efectivamente a concentración de glicosa no sangue sen provocar a aparición de hipoglucemia. No mercado farmacéutico ruso pódense mercar varias formas de medicación, como Humulin M3, Humulin Regular ou Humulin NPH. O prezo medio da droga (5 plumas de xiringa de 3 ml) é igual a 1200 rublos.
A medicina moderna avanzou, agora as inxeccións de insulina só hai que facer algunhas veces ao día. As plumas convencionais de xeringa facilitan este procedemento moitas veces. O mercado farmacolóxico ofrece unha ampla selección de diversas insulinas sintéticas. Un dos fármacos máis coñecidos é NovoMix, que reduce os niveis de azucre a valores normais e non conduce a hipoglucemia. O seu uso adecuado, así como a dieta e a actividade física asegurarán unha longa e indolora vida para os diabéticos.
- Kit de primeiros auxilios
- Tenda en liña
- Sobre empresa
- Datos de contacto
- Contactar coa editorial:
- +7 (495) 258-97-03
- +7 (495) 258-97-06
- Correo electrónico: protexido por correo electrónico
- Enderezo: Rusia, 123007, Moscova, ul. 5º Tronco, d.12.
O sitio web oficial do grupo de empresas de radar ®. A principal enciclopedia de drogas e bens do surtido de farmacias de Internet ruso. O catálogo de medicamentos Rlsnet.ru ofrece aos usuarios acceso a instrucións, prezos e descricións de medicamentos, suplementos dietéticos, dispositivos médicos, dispositivos médicos e outros produtos. A guía farmacolóxica inclúe información sobre a composición e forma de liberación, acción farmacolóxica, indicacións para o seu uso, contraindicacións, efectos secundarios, interaccións medicamentosas, método de uso de fármacos, compañías farmacéuticas. O directorio de medicamentos contén prezos para medicamentos e produtos farmacéuticos en Moscova e outras cidades rusas.
Está prohibido transmitir, copiar, difundir información sen o permiso de RLS-Patent LLC.
Ao citar materiais de información publicados nas páxinas do sitio www.rlsnet.ru, requírese unha ligazón á fonte de información.
Estamos en redes sociais:
Todos os dereitos reservados.
Non está permitido o uso comercial de materiais.
A información está destinada a profesionais sanitarios.
INSULINUM ASPARTUM A10A D05
COMPOSICIÓN E FORMA DE EMISIÓN:
suspender d / dentro. 100 cartuchos 100 UI / ml 3 ml. na pluma de xeringa, nº 1, nº 5
Nº UA / 4862/01/01 do 15/02/2010 ao 15/02/2015
hipoglucemia, hipersensibilidade á insulina aspart ou calquera ingrediente do medicamento.
As reaccións adversas observadas en pacientes que usan NovoMix 30 FlexPen están asociadas principalmente á magnitude da dose administrada do medicamento e son unha manifestación da acción farmacolóxica da insulina. O efecto secundario máis común da terapia con insulina é a hipoglucemia. Pode producirse se a dose supera significativamente a necesidade de insulina do paciente. A hipoglucemia grave pode causar perda de consciencia e / ou convulsións, seguida de deterioración temporal ou permanente da función cerebral e incluso a morte. Segundo os resultados de estudos clínicos, así como os datos rexistrados despois do lanzamento do medicamento no mercado, a incidencia de hipoglucemia grave varía en diferentes grupos de pacientes e con diferentes réximes de dosificación, a incidencia de hipoglucemia grave en pacientes que reciben insulina aspart é a mesma que en persoas que reciben insulina humana. insulina
A continuación móstrase a frecuencia das reaccións adversas que, segundo estudos clínicos, poden asociarse coa introdución do medicamento NovoMix 30 Flexpen.
Segundo a frecuencia de aparición, estas reaccións divídense en ás veces (>1/1000, 1/10 000,
- Etiquetas: Novo Nordisk, NOVOMIX 30 FLEXPEN, NOVOMIX 30 FLEXPEN
Acción farmacolóxica
Axente hipoglicémico, un análogo da insulina humana de duración media.
Interacciona cun receptor específico da membrana exterior das células e forma un complexo receptor insulina que estimula procesos intracelulares, incluído síntese de varios encimas clave (hexokinase, piruvato quinase, glicóxeno sintasa). A diminución da concentración de glicosa no sangue débese a un aumento do seu transporte intracelular, aumento da absorción por tecidos, estimulación de lipoxénese, glicogenoxénese e diminución da taxa de produción de glicosa polo fígado.
Ten a mesma actividade que a insulina humana en equivalente molar. A substitución da aminoácido prolina na posición B28 con ácido aspartico reduce a tendencia das moléculas a formar hexámeros na fracción soluble do medicamento, que se observa na insulina humana soluble. Neste sentido, a insulina aspart absorbe a graxa subcutánea máis rápido que a insulina soluble contida na insulina bifásica humana. A insulina aspart protamina é absorbida máis tempo.
Despois da administración de s / c de NovoMix 30 Penfill, o efecto desenvólvese despois de 10-20 minutos, o efecto máximo - en 1-4 horas.A duración da acción de NovoMix 30 Penfill alcanza as 24 horas (dependendo da dose, lugar de administración, intensidade do fluxo sanguíneo, temperatura corporal e nivel de actividade física )
Clasificación nosolóxica (ICD-10)
| Suspensión por administración subcutánea | 1 ml |
| substancia activa: | |
| insulina aspart: insulina soluble aspart (30%) e cristais de insulina aspart protamina (70%) | 100 Pezas (3,5 mg) |
| excipientes: glicerol - 16 mg, fenol - 1,5 mg, metacresol - 1,72 mg, cloruro de cinc - 19,6 mg, cloruro sódico - 0,877 mg, dihidrato de fosfato sódico - 1,25 mg, sulfato de proteína - aproximadamente 0,33 mg hidróxido de sodio - aproximadamente 2,2 mg, ácido clorhídrico - aproximadamente 1,7 mg, auga para inxección - ata 1 ml | |
| Un cartucho (3 ml) contén 300 unidades |
NOVOMIKS 30 Flexpen: formulario, composición e embalaxe de liberación
Suspensión por administración de SC de cor branca, homoxénea (sen grumos, poden aparecer flocos na mostra), cando se estratifica, se estratifica, formando un precipitado branco e debería formarse un sobrenadante incoloro ou case incoloro, axitando con coidado unha suspensión homoxénea.
Glicerol PRING, fenol, metacresol, cloruro de cinc, cloruro de sodio, hidróxido de fosfato sódico dihidrato, sulfato de protamina, hidróxido de sodio, ácido clorhídrico, auga d / i.
* 1 unidade corresponde a 35 μg (ou 6 nmol) de insulina anhidra aspart.
3 ml (300 pezas) - cartuchos de vidro (1) - plumas de xeringa multidosexibles para múltiples inxeccións (5) - paquetes de cartón.
Un análogo da insulina humana de duración media cun inicio rápido de acción.
NovoMix 30 Flexpen é unha suspensión bifásica constituída por insulina soluble aspart (análoga de insulina de acción curta do 30%) e cristais de insulina aspart protamina (70% análoga de insulina de acción media).
Insulina aspart obtida por biotecnoloxía recombinante do ADN empregando unha cepa de Saccharomyces cerevisiae.
Insulin aspart é unha insulina humana soluble equipotencial baseada en índices de molaridade.
Unha diminución da concentración de glicosa no sangue prodúcese debido ao aumento do seu transporte intracelular despois da unión de insulina aspart aos receptores de insulina do músculo e dos tecidos graxos e a inhibición da produción de glicosa polo fígado.
Despois de s / c administración do medicamento NovoMix 30 Flexpen, o efecto desenvólvese despois de 10-20 minutos. O efecto máximo obsérvase 1-4 horas despois da inxección.A duración do medicamento chega ás 24 horas.
Nun ensaio clínico comparativo de tres meses no que participaron pacientes con diabetes tipo 1 e tipo 2 que recibiron NovoMix 30 Flex Pen e insulina humana bifásica 30 2 veces / día antes do almorzo e a cea, NovoMix 30 FlexPen demostrou que diminúe a concentración postgrandial de glicosa en sangue máis. (despois do almorzo e a cea).
Unha metaanálise dos datos obtidos en 9 ensaios clínicos con pacientes con diabetes tipo 1 e tipo 2 demostrou que NovoMix 30 FlexPen, cando se administra antes do almorzo e da cea, proporciona un mellor control da concentración posprandial de glicosa no sangue (aumento medio da concentración de glicosa prandial despois almorzo, xantar e cea), en comparación coa insulina bifásica humana 30. Aínda que a concentración de glicosa en xaxún en pacientes que reciben Novo Mix 30 FlexPen foi maior, en xeral NovoMix 30 FlexPen exerce o mesmo ystvie a concentración de hemoglobina glicosilada (HBA1C), como a insulina bifásica humana 30.
Nun estudo clínico que implicou pacientes con diabetes mellitus tipo 2 (n = 341), os pacientes foron aleatorizados aos grupos de tratamento só con NovoMix 30 FlexPen, NovoMix 30 FlexPen en combinación con metformina e metformina combinados cun derivado da sulfonilurea. Concentración de HbA1C despois de 16 semanas de tratamento non difiren en pacientes que recibían NovoMix 30 Flexpen en combinación con metformina e en pacientes que recibiron metformina en combinación con un derivado de sulfonilurea. Neste estudo, o 57% dos pacientes presentaban unha concentración de HbA basal1C foi superior ao 9%, nestes pacientes a terapia con NovoMix 30 FlexPen en combinación con metformina provocou unha diminución máis significativa da concentración de HbA1Cque en pacientes que reciben metformina en combinación cun derivado da sulfonilurea.
Noutro estudo, os pacientes con diabetes mellitus tipo 2 con control glicémico deficiente que tomaron medicamentos hipoglicémicos orais foron aleatorizados aos seguintes grupos: NovoMix 30 FlexPen 2 veces / día (117 pacientes) e insulina glargine 1 vez / día (116 pacientes). Despois de 28 semanas de consumo de drogas, a diminución media do HbA1C no grupo de aplicacións NovoMix, o 30 Flexpen foi do 2,8% (o valor medio inicial foi do 9,7%). O 66% e o 42% dos pacientes que utilizaban NovoMix 30 FlexPen caracterizáronse por valores de HbA ao finalizar o estudo1C por debaixo do 7% e do 6,5% respectivamente. A glicosa media en plasma de xexún diminuíu en aproximadamente 7 mmol / L (de 14 mmol / L no inicio do estudo a 7,1 mmol / L).
Os resultados dunha metaanálise de datos obtidos de ensaios clínicos con pacientes con diabetes mellitus tipo 2 mostraron unha diminución do número total de episodios de hipoglucemia nocturna e hipoglucemia grave con NovoMix 30 FlexPen en comparación coa insulina bifásica humana 30. Ao mesmo tempo, hai un risco xeral de día. a hipoglucemia en pacientes que recibían NovoMix 30 Flexpen foi maior.
Realizouse un estudo clínico de 16 semanas en nenos e adolescentes que comparou a glicosa en sangue despois das comidas con NovoMix 30 FlexPen (antes das comidas), insulina humana / insulina bifásica 30 30 (antes das comidas) e insulina isófana (administrada antes durmir). O estudo participou a 167 pacientes de 10 a 18 anos. Medias de HbA1C en ambos os grupos mantívose preto dos valores iniciais ao longo do estudo. Ademais, ao usar NovoMix 30 Flexpen ou insulina bifásica humana 30, non houbo diferenzas na incidencia da hipoglucemia. Tamén se realizou un estudo transversal de dobre cego nunha poboación de pacientes de 6 a 12 anos (un total de 54 pacientes, 12 semanas para cada tipo de tratamento).A incidencia da hipoglucemia e un aumento da glicosa despois de comer no grupo tratado con NovoMix 30 FlexPen foron significativamente inferiores en comparación cos valores do grupo utilizando insulina bifásica humana. 30 valores de HbA1C ao final do estudo, no grupo de insulina bifásica humana 30 foron significativamente máis baixos que no grupo de NovoMix 30 FlexPen.
Non se estudou a farmacodinámica de NovoMix 30 FlexPen en pacientes anciáns e senís. Non obstante, nun estudo de sección transversal aleatoria de dobre cego realizado en 19 pacientes con diabetes mellitus tipo 2 con idades comprendidas entre 65 e 83 anos (idade media de 70 anos), comparáronse a farmacodinámica e a farmacocinética de insulina aspart e insulina humana soluble. Diferencias relativas na farmacodinámica (taxa máxima de infusión de glicosa - GIRmáx e a zona baixo a curva da súa velocidade de infusión durante 120 min despois da administración de preparados de insulina - AUCGIR, 0-120 min) entre insulina aspart e insulina humana en pacientes anciáns foi similar á de voluntarios sans e en pacientes máis novos con diabetes mellitus.
En insulina aspart, a substitución de aminoácido prolino na posición B28 por ácido aspartico reduce a tendencia das moléculas a formar hexámeros na fracción soluble NovoMix ® 30 FlexPen ®, que se observa na insulina humana soluble. Neste sentido, a insulina aspart (30%) é absorbida da graxa subcutánea máis rápido que a insulina soluble contida na insulina bifásica humana. O 70% restante recae na forma cristalina de protamina-ipsulina aspart, cuxa taxa de absorción é a mesma que a da insulina humana NPH.
Ao aplicar NovoMix ® 30 FlexPen ® Cmáx A insulina sérica é, en media, un 50% maior que cando se usa insulina bifásica humana 30, mentres que o tempo para alcanzar a Cmáx 2 veces menos de media. Cando s / c administración do medicamento a voluntarios saudables a unha dose de 0,2 U / kg de peso corporal C mediamáx insulina aspart foi de 140 ± 32 pmol / L e conseguiuse aos 60 minutos.
En pacientes con diabetes mellitus tipo 2máx conseguido 95 minutos despois da administración e permanece por encima do orixinal durante polo menos 14 horas
A concentración sérica de insulina volve ao seu nivel inicial despois das 15-18 horas despois da inxección de sc.
T1/2reflectindo a taxa de absorción da fracción asociada á protamina é de 8-9 horas
Farmacocinética en casos clínicos especiais
Non se realizou un estudo da farmacocinética de NovoMix ® 30 FlexPen ® en pacientes anciáns. Non obstante, as diferenzas relativas na farmacocinética entre insulina aspart e insulina soluble humana en pacientes anciáns con diabetes mellitus tipo 2 (entre 65 e 83 anos, idade media - 70 anos) foron similares ás de voluntarios sans e en pacientes máis novos con diabetes mellitus. En pacientes anciáns, observouse unha diminución da taxa de absorción, o que provocou unha desaceleración da Tmáx (82 min (rango interquartil: 60-120 min)), mentres que a media Cmáx foi semellante á observada en pacientes máis novos con diabetes tipo 2 e algo menos que en pacientes con diabetes tipo 1.
Non se realizou un estudo da farmacocinética de NovoMix ® 30 FlexPen ® en pacientes con insuficiencia renal e hepática. Non obstante, cun aumento da dose do medicamento en pacientes con distintos graos de alteración da función renal e hepática, non houbo ningún cambio na farmacocinética da insulina aspart soluble.
Non se estudaron as propiedades farmacocinéticas de NovoMix ® 30 FlexPen ® en nenos e adolescentes. Non obstante, as propiedades farmacocinéticas e farmacodinámicas da insulina aspart soluble estudáronse en nenos (de 6 a 12 anos) e adolescentes (de 13 a 17 anos) con diabetes tipo 1.En pacientes de ambos os grupos de idade, a insulina aspart caracterizouse por unha rápida absorción e valores de Tmáxsemellantes ás dos adultos. Non obstante, os valores de Cmáx en dous grupos de idade foron diferentes, o que indica a importancia da selección individual de doses de insulina aspart.
NovoMix30 FlexPen está destinado á administración de sc. Non se pode administrar o medicamento iv. isto pode levar a unha hipoglucemia grave. Tamén é necesario evitar a administración intramuscular de NovoMix30 FlexPen. Non use NovoMix 30 FlexPen para infusión de insulina subcutánea en bombas de insulina.
A dose de NovoMix 30 FlexPen é determinada polo médico individualmente e en cada caso, de acordo coas necesidades do paciente. Para alcanzar niveis óptimos de glicemia, recoméndase controlar a concentración de glicosa no sangue e axustar a dose do medicamento.
Os pacientes con diabetes mellitus tipo 2 NovoMix 30 FlexPen poden prescribirse tanto como monoterapia como en combinación con medicamentos hipoglicémicos orais e naqueles casos en que o nivel de glicosa no sangue non está suficientemente regulado só por medicamentos hipoglucemicos orais.
Por pacientes con diabetes tipo 2 que reciben primeiro insulina, a dose inicial recomendada de NovoMix 30 FlexPen é de 6 unidades antes do almorzo e 6 unidades antes da cea. A introdución de 12 unidades de NovoMix 30 Flexpen tamén se permite 1 vez / día pola noite (antes de cear).
Traslado dun paciente doutros preparados de insulina
At transferindo un paciente de insulina humana bifásica a NovoMix 30 Flexpen debería comezar coa mesma dose e modo de administración. A continuación, axuste a dose de acordo coas necesidades individuais do paciente (ver a táboa para as recomendacións sobre a titulación da dose do medicamento). Como sempre cando se traslada a un novo tipo de insulina, é necesaria unha supervisión médica estrita durante a transferencia do paciente e nas primeiras semanas do uso do novo medicamento.
O fortalecemento da terapia de NovoMix 30 FlexPen é posible pasando dunha única dose diaria a unha dobre. Recoméndase que despois de alcanzar unha dose de 30 unidades de fármaco para o uso de NovoMix 30 Flexpen 2 veces / día, dividir a dose en 2 partes iguais - mañá e noite (antes do almorzo e a cea).
A transición ao uso de NovoMix 30 Flexpen 3 veces / día é posible dividindo a dose da mañá en 2 partes iguais e administrando estas dúas partes pola mañá e ao xantar (tres veces ao día).
Para o axuste da dose, NovoMix 30 FlexPen usa a menor concentración de glucosa en xaxún obtida nos últimos 3 días.
Para avaliar a adecuación da dose anterior, use o valor da concentración de glicosa no sangue antes da seguinte comida.
O axuste da dose pódese realizar unha vez á semana ata alcanzar o valor HbA obxectivo.1C.
Non aumente a dose do medicamento se se observou hipoglucemia durante este período.
O axuste da dose pode ser necesario cando aumente a actividade física do paciente, cambie a súa dieta normal ou teña unha condor.
Para axustar a dose de NovoMix 30 FlexPen, recoméndase empregar as recomendacións de valoración da dose que figuran na táboa:
Suspensión subcutánea, Novo Nordisk
NovoMix® 30 Penfill®
Suspensión para a administración subcutánea de 1 ml de sustancia activa: insulina aspart - insulina aspart soluble (30%) e cristais de insulina aspart protamina (70%) 100 UI (3,5 mg) excipientes: glicerol - 16 mg, fenol - 1,5 mg , metacresol - 1,72 mg, cinc (en forma de cloruro de cinc) - 19,6 μg, cloruro de sodio - 0,877 mg, hidróxido de fosfato sódico dihidrato - 1,25 mg, sulfato de protamina - aproximadamente 0,32 mg, hidróxido de sodio - aproximadamente 2 , 2 mg, ácido clorhídrico - aproximadamente 1,7 mg, auga para inxección - ata 1 ml 1 cartucho (3 ml) contén 300 pezas
NovoMix® 30 FlexPen®
Suspensión para a administración subcutánea de 1 ml de sustancia activa: insulina aspart - insulina aspart soluble (30%) e cristais de insulina aspart protamina (70%) 100 UI (3,5 mg) excipientes: glicerol - 16 mg, fenol - 1,5 mg , metacresol - 1,72 mg, cinc (en forma de cloruro de cinc) - 19,6 μg, cloruro de sodio - 0,877 mg, hidróxido de fosfato sódico dihidrato - 1,25 mg, sulfato de protamina - aproximadamente 0,32 mg, hidróxido de sodio - aproximadamente 2 , 2 mg, ácido clorhídrico - aproximadamente 1,7 mg,auga para a inxección - ata 1 ml 1 xeringa pre-chea (3 ml) contén 300 pezas
Suspensión homoxénea sen bulbo branco. Na mostra poden aparecer flocos.
Ao estar de pé, a suspensión se delamina, formando un precipitado branco e un sobrenadante incoloro ou case incoloro.
Ao mesturar o precipitado segundo o procedemento descrito nas instrucións de uso médico, deberá formarse unha suspensión homoxénea.
En insulina aspart, a substitución da aminoácido prolina na posición B28 polo ácido aspartico reduce a tendencia das moléculas a formar hexámeros na fracción soluble de NovoMix® 30 Penfill® / FlexPen®, que se observa na insulina humana soluble. Neste sentido, a insulina aspart (30%) é absorbida da graxa subcutánea máis rápido que a insulina soluble contida na insulina bifásica humana. O 70% restante recae na forma cristalina de protamina-insulina aspart, cuxa taxa de absorción é a mesma que a da insulina humana NPH.
O Cmax sérico de insulina despois da administración de NovoMix® 30 Penfill® / FlexPen® é un 50% superior ao da insulina bifásica humana 30 e Tmax é o dobre do que a insulina bifásica humana 30.
En voluntarios sans, despois da administración de NovoMix® 30 a razón de 0,2 U / kg de peso corporal Cmax de insulina aspart no soro foi obtida despois de 60 minutos e ascendeu a (140 ± 32) pmol / L. A duración do T1 / 2 de NovoMix® 30, que reflicte a taxa de absorción da fracción unida á proteína, foi de 8 a 9. O nivel de insulina no soro sanguíneo volveu ao nivel inicial 15-18 horas despois da administración da droga. En pacientes con diabetes mellitus tipo 2, Cmax alcanzouse a 95 minutos despois da administración e mantívose por encima do valor inicial durante polo menos 14 horas.
Pacientes anciáns e senís. Non se realizou un estudo da farmacocinética de NovoMix® 30 en pacientes anciáns e senís. Non obstante, as diferenzas relativas na farmacocinética entre insulina aspart e insulina soluble humana en pacientes anciáns con diabetes mellitus tipo 2 (65-83 anos, idade media de 70 anos) foron similares ás de voluntarios sans e pacientes máis novos con diabetes mellitus. En pacientes anciáns observouse unha diminución da taxa de absorción, o que provocou unha desaceleración do T1 / 2 (rango interquartil de 82 minutos - 60–120 min), mentres que a media de Cmax foi similar á observada en pacientes máis novos con diabetes mellitus tipo 2, e lixeiramente menos que en Pacientes con diabetes tipo 1.
Pacientes con insuficiencia renal e hepática. Non se estudaron farmacocinética de NovoMix® 30 Penfill® / FlexPen® en pacientes con insuficiencia renal e hepática. Non obstante, cun aumento da dose do medicamento en pacientes con distintos graos de alteración da función renal e hepática, non houbo ningún cambio na farmacocinética da insulina aspart soluble.
Nenos e adolescentes. As propiedades farmacocinéticas de NovoMix® 30 Penfill® / FlexPen® non se estudaron en nenos e adolescentes. Non obstante, as propiedades farmacocinéticas e farmacodinámicas da insulina aspart soluble estudáronse en nenos (de 6 a 12 anos) e adolescentes (de 13 a 17 anos) con diabetes mellitus tipo 1. En pacientes de ambos os grupos de idade, insulina aspart caracterizouse por unha absorción rápida e valores de Tmax similares a aqueles. en adultos. Non obstante, os valores de Cmax nos dous grupos de idade foron diferentes, o que indica a importancia da selección individual das doses de insulina aspart.
NovoMix® 30 Penfill® / FlexPen® é unha suspensión bifásica constituída por insulina aspart soluble (análogo de insulina de acción curta do 30%) e cristais de insulina aspart protamina (70% análoga de insulina de acción media). A sustancia activa NovoMix® 30 Penfill® / FlexPen® é insulin aspart, producida polo método de biotecnoloxía do ADN recombinante empregando a cepa Saccharomyces cerevisiae.
Insulin aspart é insulina humana soluble equipotencial baseada na súa molaridade.
Unha diminución da glicosa no sangue prodúcese debido ao aumento do seu transporte intracelular despois da unión de insulina aspart aos receptores de insulina do músculo e dos tecidos graxos e a inhibición simultánea da produción de glicosa polo fígado. Despois da administración SC de NovoMix® 30 Penfill® / FlexPen®, o efecto desenvólvese nun prazo de 10 a 20 minutos. O efecto máximo obsérvase no intervalo de 1 a 4 horas despois da inxección. A duración do medicamento chega ás 24 horas.
Nun ensaio clínico comparativo de tres meses no que participaron pacientes con diabetes tipo 1 e tipo 2 que recibiron NovoMix® 30 Penfill® / FlexPen® e insulina humana bifásica 30, 2 veces ao día, antes do almorzo e a cea, mostrouse NovoMix® 30 Penfill. ® / FlexPen® reduce con máis forza os niveis de glicosa no sangue postprandial (despois do almorzo e a cea).
Unha metaanálise dos datos obtidos en 9 estudos clínicos en pacientes con diabetes tipo 1 e tipo 2 demostrou que NovoMix® 30 Penfill® / FlexPen® cando se administra antes do almorzo e da cea proporciona un mellor control dos niveis de glicosa no sangue postprandial (aumento medio Os niveis de glicosa prandiais despois do almorzo, o xantar e a cea) en comparación coa insulina bifásica humana 30. Aínda que os niveis de glicosa en xaxún en pacientes que utilizan NovoMix® 30 Penfill® / FlexPen® foron maiores, o NovoMix® 30 Penfill® / FlexPen® foi maior. É o mesmo efecto sobre a concentración de hemoglobina glicosilada (HbA1c), así como a insulina humana bifásica 30.
Nun estudo clínico que implicou a 341 pacientes con diabetes tipo 2, os pacientes foron aleatorizados a grupos de tratamento só NovoMix® 30 Penfill® / FlexPen®, NovoMix® 30 Penfill® / FlexPen® en combinación con metformina e metformina en combinación cun derivado da sulfonilurea. A concentración de HbA1c despois de 16 semanas de tratamento non foi diferente nos pacientes que recibiron NovoMix® 30 Penfill® / FlexPen® en combinación con metformina e nos pacientes que recibiron metformina en combinación cun derivado da sulfonilurea. Neste estudo, no 57% dos pacientes, a concentración base de HbA1c foi superior ao 9%; nestes pacientes, o tratamento con NovoMix® 30 Penfill® / FlexPen® en combinación con metformina resultou nunha diminución máis significativa da concentración de HbA1c que en pacientes tratados con metformina en combinación cun derivado. sulfonilureas.
Noutro estudo, os pacientes con diabetes mellitus tipo 2 con control glicémico deficiente que tomaron medicamentos hipoglicémicos orais foron aleatorizados nos seguintes grupos: recibir NovoMix® 30 dúas veces ao día (117 pacientes) e recibir insulina glargina 1 vez ao día (116 pacientes). Tras 28 semanas de administración de fármacos, a diminución media da concentración de HbA1c no grupo NovoMix® 30 Penfill® / FlexPen® foi do 2,8% (o valor medio inicial foi do 9,7%). No 66% e 42% dos pacientes que usaban NovoMix® 30 Penfill® / FlexPen®, ao final do estudo, os valores de HbA1c estaban por baixo dos 7 e 6,5%, respectivamente. A glicosa media en plasma de xexún diminuíu en aproximadamente 7 mmol / L (de 14 mmol / L no inicio do estudo a 7,1 mmol / L).
Os resultados dunha metaanálise de datos obtidos de ensaios clínicos con pacientes con diabetes mellitus tipo 2 mostraron unha diminución do número total de episodios de hipoglucemia nocturna e hipoglucemia grave con NovoMix® 30 Penfill® / FlexPen® en comparación coa insulina bifásica humana 30. o risco global de hipoglucemia diurna en pacientes que recibían NovoMix® 30 Penfill® / FlexPen® foi maior.
Nenos e adolescentes. Realizouse un ensaio clínico de 16 semanas comparando a glicosa no sangue despois das comidas con NovoMix® 30 (antes das comidas), insulina humana / insulina bifásica humana 30 (antes das comidas) e isofan-insulina (administrada antes de durmir). O estudo participou a 167 pacientes de 10 a 18 anos. Os valores medios de HbA1c nos dous grupos mantivéronse preto dos valores iniciais ao longo do estudo. Ademais, ao usar NovoMix® 30 Penfill® / FlexPen® ou insulina humana bifásica 30, non houbo diferenzas na incidencia da hipoglucemia.
Tamén se realizou un estudo transversal de dobre cego nunha poboación de pacientes de 6 a 12 anos (54 pacientes en total, 12 semanas por cada tipo de tratamento). A incidencia da hipoglucemia e un aumento da glicosa despois das comidas no grupo de pacientes que utilizan NovoMix® 30 Penfill® / FlexPen® foron significativamente máis baixas en comparación cos valores do grupo de pacientes que usaban insulina bifásica 30. Os valores de HbA1c ao final do estudo no grupo bifásico. A insulina humana 30 foi significativamente menor que no grupo de pacientes que utilizaban NovoMix® 30 Penfill® / FlexPen®.
Pacientes anciáns. Non se investigou a farmacodinámica de NovoMix® 30 Penfill® / FlexPen® en pacientes anciáns. Non obstante, nun estudo de sección transversal aleatoria de dobre cego realizado en 19 pacientes con diabetes mellitus tipo 2 de 65 a 83 anos (idade media de 70 anos), comparáronse a farmacodinámica e a farmacocinética de insulina aspart e insulina humana soluble. As diferenzas relativas nos valores dos parámetros farmacodinámicos (a velocidade máxima de infusión de glicosa - GIRmax e a área baixo a curva da súa taxa de perfusión durante 120 minutos despois da administración de preparados de insulina - AUCGIR, 0-120 min) entre insulina aspart e insulina humana en pacientes anciáns foi similar á de pacientes sans. voluntarios e en pacientes máis novos con diabetes.
Datos preclínicos de seguridade
Os estudos preclínicos non revelaron ningún perigo para os humanos, a partir de datos de estudos xeralmente aceptados de seguridade farmacolóxica, toxicidade de uso repetido, xenotoxicidade e toxicidade reprodutiva.
En ensaios in vitro, que incluíron a unión a receptores de insulina e IGF-1 e o efecto no crecemento celular, demostrouse que as propiedades da insulina aspart son similares ás da insulina humana. Os estudos demostraron tamén que a disociación da unión de insulina aspart aos receptores de insulina é equivalente á da insulina humana.
Síndrome de Itsenko-Cushing: monografía. . - M .: Medicina, 1988 .-- 224 páx.
Dobrov, A. Diabetes: non é un problema / A. Dobrov. - M.: Book House (Minsk), 2010 .-- 166 p.
Efimov A.S. Anxiopatía diabética Moscova, editorial "Medicina", 1989, 288 pp.- Melnichenko G. A., Peterkova V. A., Tyulpakov A. N., Maksimova N. V. Síndromes homónimos en endocrinoloxía, Práctica - M., 2013. - 172 p.
- Balabolkin M.I., Klebanova E.M., Kreminskaya V. M. Tiroidoloxía fundamental e clínica, Medicina - M., 2013. - 816 p.

Déixeme presentarme. Chámome Elena. Levo máis de 10 anos traballando como endocrinólogo. Creo que actualmente son un profesional no meu campo e quero axudar a todos os visitantes do sitio a resolver tarefas complexas e non así. Recóllense e procesan coidadosamente todos os materiais do sitio para transmitir o máximo posible toda a información necesaria. Antes de aplicar o descrito no sitio web, é sempre necesaria unha consulta obrigatoria con especialistas.
Descrición da forma de dosificación
Suspensión homoxénea sen bulbo branco. Na mostra poden aparecer flocos.
Ao estar de pé, a suspensión se delamina, formando un precipitado branco e un sobrenadante incoloro ou case incoloro.
Ao mesturar o precipitado segundo o procedemento descrito nas Instrucións de uso médico, deberá formarse unha suspensión homoxénea.
Farmacodinámica
NovoMix ® 30 Penfill ® é unha suspensión bifásica constituída por insulina soluble aspart (análoga de insulina de acción curta do 30%) e cristais de protamina insulina aspart (análoga de insulina de acción media do 70%). A sustancia activa NovoMix ® 30 Penfill ® é insulina aspart, producida polo método de biotecnoloxía recombinante do ADN mediante unha cepa Saccharomyces cerevisiae.
Insulin aspart é insulina humana soluble equipotencial baseada na súa molaridade.
Unha diminución da glicosa no sangue prodúcese debido ao aumento do seu transporte intracelular despois da unión de insulina aspart aos receptores de insulina do músculo e dos tecidos graxos e a inhibición simultánea da produción de glicosa polo fígado. Despois da administración subcutánea de NovoMix ® 30 Penfill ®, o efecto desenvólvese dentro de 10-20 minutos. O efecto máximo obsérvase no intervalo de 1 a 4 horas despois da inxección. A duración do medicamento chega ás 24 horas.
Nun estudo clínico comparativo de tres meses no que participaron pacientes con diabetes tipo 1 e tipo 2 que recibiron NovoMix ® 30 Penfill ® e insulina humana bifásica 30 2 veces ao día antes do almorzo e a cea, demostrouse que NovoMix ® 30 Penfill ® reduce os niveis postprandiais máis. glicosa (despois do almorzo e da cea).
Unha metaanálise de datos de 9 ensaios clínicos con pacientes con diabetes tipo 1 e tipo 2 demostrou que NovoMix® 30 Penfill®, administrado antes do almorzo e a cea, proporciona un mellor control dos niveis de glicosa postprandial (aumento medio dos niveis de glicosa prandial). despois do almorzo, xantar e cea), en comparación coa insulina bifásica humana 30. Aínda que o nivel de glicosa en xaxún en pacientes que utilizan NovoMix ® 30 Penfill ® foi maior, en xeral, NovoMix ® 30 Penfill ® ten o mesmo efecto sobre concentración de hemoglobina glicosilada (HbA) 1c ), como a insulina bifásica humana 30.
Nun estudo clínico que implicou a 341 pacientes con diabetes tipo 2, os pacientes foron randomizados aos grupos de tratamento só NovoMix ® 30 Penfill ®, NovoMix ® 30 Penfill ® en combinación con metformina e metformina en combinación cun derivado da sulfonilurea. Concentración de HbA 1c despois de 16 semanas de tratamento non difiren en pacientes que recibían NovoMix ® 30 Penfill ® en combinación con metformina e en pacientes que recibiron metformina en combinación con un derivado de sulfonilurea. Neste estudo, o 57% dos pacientes presentaban unha concentración de HbA basal 1c foi superior ao 9%, nestes pacientes a terapia con NovoMix ® 30 Penfill ® en combinación con metformina provocou unha diminución máis significativa da concentración de HLA 1s que en pacientes que reciben metformina en combinación cun derivado da sulfonilurea.
Noutro estudo, os pacientes con diabetes mellitus tipo 2 con control glicémico deficiente que tomaron medicamentos hipoglicémicos orais foron aleatorizados nos seguintes grupos: recibir NovoMix ® 30 dúas veces ao día (117 pacientes) e recibir insulina glargina 1 vez ao día (116 pacientes). Despois de 28 semanas de consumo de drogas, a diminución media da concentración de HbA 1c no grupo NovoMix ® 30, Penfill ® foi do 2,8% (o valor medio inicial foi do 9,7%). No 66% e 42% dos pacientes que utilizan NovoMix ® 30 Penfill ®, ao finalizar o estudo, os valores de HbA 1c estiveron por baixo do 7 e do 6,5%, respectivamente. A glicosa media en plasma de xexún diminuíu en aproximadamente 7 mmol / L (de 14 mmol / L no inicio do estudo a 7,1 mmol / L).
Os resultados dunha metaanálise de datos obtidos de ensaios clínicos con pacientes con diabetes mellitus tipo 2 mostraron unha diminución do número total de episodios de hipoglucemia nocturna e hipoglucemia grave con NovoMix ® 30 Penfill ® en comparación coa insulina bifásica humana 30. Ao mesmo tempo, hai un risco xeral. a aparición de hipoglucemia diurna en pacientes que recibían NovoMix ® 30 Penfill ® foi maior.
Nenos e adolescentes. Realizouse un ensaio clínico de 16 semanas comparando a glicosa no sangue despois das comidas con NovoMix® 30 (antes das comidas), insulina humana / insulina bifásica humana 30 (antes das comidas) e isofan-insulina (administrada antes de durmir).O estudo participou a 167 pacientes de 10 a 18 anos. Medias HLA 1s en ambos os grupos mantívose preto dos valores iniciais ao longo do estudo. Ademais, ao usar NovoMix ® 30 Penfill ® ou insulina bifásica humana 30, non houbo diferenzas na incidencia da hipoglucemia.
Tamén se realizou un estudo transversal de dobre cego nunha poboación de pacientes de 6 a 12 anos (un total de 54 pacientes, 12 semanas para cada tipo de tratamento). A incidencia da hipoglucemia e un aumento da glicosa despois dunha comida no grupo de pacientes que utilizan NovoMix ® 30 Penfill ® foron significativamente máis baixos en comparación cos valores do grupo de pacientes que usaban insulina humana bifásica 30. Valores de HbA 1c ao final do estudo, no grupo de insulina bifásica humana 30 foron significativamente inferiores que no grupo de pacientes que utilizaban NovoMix ® 30 Penfill ®.
Pacientes anciáns. Farmacodinámica NovoMix ® 30 Penfill ® en pacientes anciáns non foi investigado. Non obstante, nun estudo aleatorio de dobre cego, realizado en 19 pacientes con diabetes mellitus tipo 2 con idades comprendidas entre 65 e 83 anos (idade media de 70 anos), comparáronse a farmacodinámica e a farmacocinética de insulina aspart e insulina humana soluble. Diferencias relativas na farmacodinámica (taxa máxima de infusión de glicosa - GIR máx e a zona baixo a curva da velocidade da súa infusión durante 120 min despois da administración de preparados de insulina - AUC GIR, 0-120 min ) entre insulina aspart e insulina humana en pacientes anciáns foi similar á de voluntarios sans e en pacientes máis novos con diabetes mellitus.
Datos preclínicos pero de seguridade
Os estudos preclínicos non revelaron ningún perigo para os humanos, a partir de datos de estudos xeralmente aceptados de seguridade farmacolóxica, toxicidade de uso repetido, xenotoxicidade e toxicidade reprodutiva.
En probas in vitro Incluíndo a unión a receptores de insulina e IGF-1 e o efecto sobre o crecemento celular, demostrouse que as propiedades da insulina aspart son similares ás da insulina humana. Os estudos demostraron tamén que a disociación da unión de insulina aspart aos receptores de insulina é equivalente á da insulina humana.
Farmacocinética
En insulina aspart, a substitución de aminoácido prolina na posición B28 por ácido aspartico reduce a tendencia das moléculas a formar hexámeros na fracción soluble de NovoMix® 30 Penfill®, que se observa na insulina humana soluble. Neste sentido, a insulina aspart (30%) é absorbida da graxa subcutánea máis rápido que a insulina soluble contida na insulina bifásica humana. O 70% restante é a forma cristalina de protamina-insulina aspart, cuxa taxa de absorción é a mesma que a da insulina humana NPH.
C máx A insulina sérica despois da administración de NovoMix ® 30 Penfill ® é un 50% superior á da insulina bifásica humana 30. a T máx 2 veces máis curto en comparación coa insulina bifásica humana 30.
En voluntarios saudables despois da administración subcutánea do medicamento NovoMix ® 30 a razón de 0,2 Pezas / kg C máx A insulina aspart no soro conseguiuse despois de 60 minutos e foi (140 ± 32) pmol / L. Duración T 1/2 NovoMix ® 30, que reflicte a taxa de absorción da fracción unida a proteína, foi de 8 a 9. O nivel de insulina no soro sanguíneo volveu ás 15-18 horas orixinais despois da administración subcutánea do medicamento. En pacientes con diabetes mellitus tipo 2 máx alcanzou 95 min despois da administración e mantívose por encima da liña base durante polo menos 14 horas
Pacientes anciáns e senís. Non se realizou un estudo sobre a farmacocinética de NovoMix ® 30 en pacientes anciáns e senís. Non obstante, as diferenzas relativas na farmacocinética entre insulina aspart e insulina soluble humana en pacientes anciáns con diabetes mellitus tipo 2 (entre 65 e 83 anos, idade media - 70 anos) foron similares ás de voluntarios sans e en pacientes máis novos con diabetes mellitus.En pacientes anciáns, observouse unha diminución da taxa de absorción, o que provocou unha desaceleración da T 1/2 (82 min (rango interquartil - 60-120 min), mentres que a media C máx foi semellante á observada en pacientes máis novos con diabetes tipo 2 e algo menos que en pacientes con diabetes tipo 1.
Pacientes con insuficiencia renal e hepática. Non se realizou un estudo da farmacocinética de NovoMix ® 30 Penfill ® en pacientes con insuficiencia renal e hepática. Non obstante, cun aumento da dose do medicamento en pacientes con distintos graos de alteración da función renal e hepática, non houbo ningún cambio na farmacocinética da insulina aspart soluble.
Nenos e adolescentes. Non se estudaron as propiedades farmacocinéticas de NovoMix ® 30 Penfill ® en nenos e adolescentes. Non obstante, as propiedades farmacocinéticas e farmacodinámicas da insulina aspart soluble estudáronse en nenos (de 6 a 12 anos) e adolescentes (de 13 a 17 anos) con diabetes mellitus tipo 1. En pacientes de ambos os grupos de idade, insulina aspart caracterizouse por unha absorción rápida e valores de T máx semellantes ás dos adultos. Non obstante, os valores de C máx en dous grupos de idade foron diferentes, o que indica a importancia da selección individual de doses de insulina aspart.
Embarazo e lactación
A experiencia clínica co uso de NovoMix ® 30 Penfill ® durante o embarazo é limitada.
Non obstante, os datos de dous ensaios clínicos aleatorios controlados (respectivamente de 157 e 14 mulleres embarazadas que recibiron insulina aspart nun réxime básico de bolo) non revelaron efectos adversos da insulina aspart sobre o embarazo ou a saúde fetal / recentemente nado en comparación coa insulina humana soluble. Ademais, nun ensaio clínico aleatorio no que participaron 27 mulleres con diabetes gestacional que recibiron insulina aspart e insulina humana soluble (insulin aspart recibiu 14 mulleres, insulina humana 13), demostráronse perfís de seguridade similares para os dous tipos de insulina.
Durante o período do posible inicio do embarazo e durante todo o seu período, é necesario controlar coidadosamente o estado dos pacientes con diabetes mellitus e controlar a concentración de glicosa no sangue. A necesidade de insulina, por regra xeral, diminúe no primeiro trimestre e aumenta gradualmente no segundo e terceiro trimestre do embarazo. Pouco despois do nacemento, a necesidade de insulina volve axiña ao nivel que estaba antes do embarazo.
Durante o período de lactación, NovoMix ® 30 Penfill ® pode usarse sen restricións. A administración de insulina a unha nai lactante non é unha ameaza para o bebé. Non obstante, pode ser necesario axustar a dose de NovoMix ® 30 Penfill ®.
Efectos secundarios
Reaccións adversas observadas en pacientes que utilizan o medicamento NovoMiks ® 30, debido principalmente ao efecto farmacolóxico da insulina. O acontecemento adverso máis común coa insulina é a hipoglucemia. A frecuencia dos efectos secundarios asociados ao uso de NovoMix ® 30 varía segundo a poboación do paciente, o réxime de dosificación do fármaco e o control glicémico.
Na fase inicial da insulinoterapia, poden producirse erros de refracción, edema e reaccións no lugar da inxección (incluíndo dor, vermelhidão, urticaria, inflamación, hematomas, inchazo e picazón no lugar da inxección). Estes síntomas adoitan ser temporais. Unha rápida mellora do control glicémico pode levar a un estado de neuropatía aguda da dor, que normalmente é reversible. A intensificación da insulinoterapia cunha forte mellora do control do metabolismo dos carbohidratos pode levar a un deterioro temporal do estado da retinopatía diabética, mentres que unha mellora a longo prazo do control glicémico reduce o risco de progresión da retinopatía diabética.
A lista de reaccións adversas preséntase na táboa.
Todas as reaccións adversas descritas a continuación, baseadas en datos de ensaios clínicos, agrúpanse segundo a frecuencia de desenvolvemento segundo MedDRA e os sistemas de órganos. A incidencia de reaccións adversas defínese do seguinte xeito: moi a miúdo (≥1 / 10), a miúdo (≥1 / 100, ® 30 Penfill ® non se debe mesturar con outras drogas.
Dosificación e administración
NovoMix ® 30 Penfill ® está destinado a s / c introdución. Non administre NovoMix ® 30 Penfill ® iv, como isto pode levar a unha hipoglucemia grave. Tamén se debe evitar a administración intramuscular de NovoMix ® 30 Penfill ®. Non use NovoMix ® 30 Penfill ® para infusión de sc / insulina (PPII) en bombas de insulina.
A dose de NovoMix ® 30 Penfill ® é determinada polo médico individualmente en cada caso, de acordo coas necesidades do paciente. Para alcanzar o nivel óptimo de glicemia, recoméndase controlar a concentración de glicosa no sangue e axustar a dose do medicamento.
NovoMix ® 30 Penfill ® pode prescribirse a pacientes con diabetes mellitus tipo 2 tanto como monoterapia como en combinación con fármacos hipoglicémicos orais nos casos en que o nivel de glicosa no sangue está insuficientemente regulado só por medicamentos hipoglicémicos orais.
Para os pacientes con diabetes tipo 2 que reciben primeiro insulina, a dose inicial recomendada de NovoMix ® 30 Penfill ® é de 6 unidades antes do almorzo e 6 unidades antes da cea. Tamén está permitida a introdución de 12 unidades de NovoMix ® 30 Penfill ® unha vez ao día pola noite (antes da cea).
Traslado dun paciente doutros preparados de insulina
Ao transferir un paciente de insulina humana bifásica a NovoMix ® 30 Penfill ®, débese comezar coa mesma dose e modo de administración. A continuación, axuste a dose de acordo coas necesidades individuais do paciente (ver as seguintes recomendacións para a valoración da dose do medicamento). Como sempre, ao transferir un paciente a un novo tipo de insulina é necesaria unha supervisión médica estrita durante a transferencia do paciente e nas primeiras semanas de usar o novo medicamento.
É posible reforzar a terapia de NovoMix ® 30 Penfill ®, pasando dunha única dose diaria a unha dobre. Recoméndase que despois de alcanzar unha dose de 30 unidades de fármaco para o uso de NovoMix ® 30 Penfill ® 2 veces ao día, dividise a dose en dúas partes iguais: mañá e noite (antes do almorzo e a cea).
A transición ao uso de NovoMix ® 30 Penfill ® 3 veces ao día é posible dividindo a dose da mañá en dúas partes iguais e introducindo estas dúas partes pola mañá e ao xantar (tres veces ao día).
Para axustar a dose de NovoMix ® 30 Penfill ®, úsase a menor concentración de glicosa en xaxún obtida nos últimos tres días.
Para avaliar a adecuación da dose anterior, use o valor da concentración de glicosa no sangue antes da seguinte comida.
O axuste da dose pódese realizar unha vez á semana ata alcanzar o valor HbA obxectivo. 1c . Non aumente a dose do medicamento se se observou hipoglucemia durante este período.
O axuste da dose pode ser necesario cando aumente a actividade física do paciente, cambie a súa dieta normal ou teña unha condor.
Para axustar a dose de NovoMix ® 30 Penfill ®, a continuación móstranse recomendacións para a súa titulación (ver táboa).
| Concentración de glicosa no sangue antes das comidas | Axuste da dose de NovoMix ® 30 Penfill ®, UNIT |
| 10 mmol / L (> 180 mg / dL) | +6 |
Grupos especiais de pacientes
Como sempre, cando se empregan preparados de insulina, en pacientes de grupos especiais, a concentración de glicosa en sangue debe controlarse con máis coidado e axustar a dose de aspart aspart individualmente.
Pacientes anciáns e senís. NovoMix ® 30 Penfill ® pode usarse en pacientes anciáns. Non obstante, a experiencia co seu uso en combinación con fármacos hipoglicémicos orais en pacientes maiores de 75 anos é limitada.
Pacientes con función deteriorada das noites e fígado. En pacientes con insuficiencia renal ou hepática, pódese reducir a necesidade de insulina.
Nenos e adolescentes. NovoMix ® 30 Penfill ® pode usarse para tratar nenos e adolescentes maiores de 10 anos nos casos nos que se prefire o uso de insulina pre-mesturada. Hai datos clínicos limitados para nenos de 6 a 9 anos (ver Farmacodinámica).
NovoMix ® 30 Penfill ® debe administrarse de forma subcutánea na coxa ou na parede abdominal anterior. Se o desexa, a droga pódese administrar ao ombreiro ou ás nádegas.
É necesario cambiar o sitio da inxección dentro da rexión anatómica para evitar o desenvolvemento de lipodistrofia.
Como en calquera outra preparación de insulina, a duración da acción de NovoMix ® 30 Penfill ® depende da dose, lugar de administración, intensidade do fluxo sanguíneo, temperatura e nivel de actividade física.
En comparación coa insulina humana bifásica, NovoMix ® 30 Penfill ® comeza a actuar con máis rapidez, polo que debe administrarse inmediatamente antes de tomar o esmoleiro. Se é necesario, pódese administrar NovoMix ® 30 Penfill ® pouco despois de tomar o esmoleiro.
Sobredose
Síntomas Non obstante non se estableceu unha dose específica requirida para unha sobredose de insulina hipoglucemia pode desenvolverse gradualmente se as doses son demasiado altas en relación ás necesidades do paciente.
Tratamento. O paciente pode eliminar unha hipoglucemia leve tomando glicosa ou alimentos que conteñan azucre. Por iso, recoméndase a pacientes con diabetes levar constantemente produtos que conteñen azucre.
En caso de hipoglucemia grave, cando o paciente está inconsciente, debe ingresar de 0,5 mg a 1 mg de glucágono en / m ou s / c (pode ser administrado por unha persoa adestrada), ou nunha solución de glicosa (dextrosa) (só pode entrar un profesional médico). Tamén é necesario administrar dextrose iv no caso de que o paciente non recupere a consciencia 10-15 minutos despois da administración do glucagón. Despois de recuperar a conciencia, aconséllase que o paciente tome alimentos ricos en carbohidratos para evitar a recorrencia da hipoglucemia.
Precaucións de seguridade
NovoMix ® 30 Penfill ® e agullas son para uso persoal. Non encher o cartucho Penfill ®.
NovoMix ® 30 Penfill ® non se pode usar se despois da mestura non se volve uniformemente branco e turbo.
Débese resaltar ao paciente a necesidade de mesturar NovoMix® 30 suspensión Penfill® inmediatamente antes do uso.
Non use NovoMix ® 30 Penfill ® se foi conxelado. Os pacientes deben ser avisados para que descarten a agulla despois de cada inxección.
Instrucións especiais
Antes dunha longa viaxe que supón un cambio de fuso horario, o paciente debe consultar co seu médico, xa que cambiar o fuso horario significa que o paciente debe comer e administrar insulina nun momento diferente.
Hiperglicemia. Unha dose insuficiente ou interrupción do tratamento, especialmente con diabetes mellitus tipo 1, pode levar ao desenvolvemento de hiperglicemia e cetoacidosis diabética. Os síntomas da hiperglicemia adoitan aparecer gradualmente ao longo de varias horas ou días. Os síntomas da hiperglucemia son unha sensación de sede, un aumento da cantidade de ouriña liberada, náuseas, vómitos, somnolencia, vermelhidão e sequedad da pel, boca seca, perda de apetito e aparición dun cheiro a acetona no aire exhalado.Sen un tratamento adecuado, a hiperglucemia en pacientes con diabetes tipo 1 pode levar a cetoacidosis diabética, unha condición que pode ser fatal.
Hipoglicemia. Saltar comidas ou unha actividade física intensa non planificada pode levar á hipoglucemia. A hipoglicemia tamén pode desenvolverse se a dose de insulina é demasiado alta en relación ás necesidades do paciente (ver "Efectos secundarios", "Sobredose").
En comparación coa insulina bifásica humana, a administración de NovoMix ® 30 Penfill ® ten un efecto hipoglicémico máis pronunciado dentro das 6 horas despois da administración. Neste sentido, nalgúns casos, pode ser necesario axustar a dose de insulina e / ou a natureza da dieta. Despois de compensar o metabolismo dos hidratos de carbono, por exemplo, cunha terapia con insulina intensificada, os pacientes poden experimentar síntomas típicos dos precursores da hipoglucemia, sobre os que se debe informar aos pacientes. Os sinais de aviso habituais poden desaparecer cun longo curso de diabetes. Un control máis estrito da glicemia en pacientes pode aumentar o risco de hipoglucemia, polo tanto, un incremento da dose de NovoMix ® 30 Penfill ® debe realizarse baixo estricta supervisión médica (ver "Dosificación e administración").
Dado que NovoMix ® 30 Penfill ® debe usarse en conexión directa coa inxestión de alimentos, débese ter en conta a alta velocidade de aparición do efecto do medicamento no tratamento de pacientes con enfermidades concomitantes ou tomar medicamentos que retardan a absorción de alimentos.
As enfermidades concomitantes, especialmente infecciosas e acompañadas de febre, adoitan aumentar a necesidade do corpo de insulina. O axuste da dose tamén pode ser necesario se o paciente ten enfermidades concomitantes dos riles, fígado, alteración da función suprarenal, hipófise ou glándula tiroides.
Ao transferir un paciente a outro tipo de insulina, os primeiros síntomas dos precursores da hipoglucemia poden cambiar ou facerse menos pronunciados en comparación cos que usan o tipo anterior de insulina.
Traslado do paciente doutros preparados de insulina. A transferencia do paciente a un novo tipo de insulina ou a unha preparación de insulina doutro fabricante debe realizarse baixo estricta supervisión médica. Se cambia a concentración, tipo, fabricante e tipo (insulina humana, un análogo da insulina humana) dos preparados de insulina e / ou o método de produción, pode ser necesario un cambio de dose. Os pacientes que pasan doutras preparacións de insulina ao tratamento con NovoMix ® 30 Penfill ® poden necesitar aumentar a frecuencia das inxeccións ou cambiar a dose en comparación coas doses dos preparados de insulina usados anteriormente. Se é necesario, axuste de dose, pódese facer xa na primeira inxección do medicamento ou durante as primeiras semanas ou meses de tratamento.
Reaccións no lugar da inxección. Como ocorre con outros tratamentos coa insulina, as reaccións poden desenvolverse no lugar da inxección, que se manifesta por dor, vermelhidão, colmeas, inflamación, hematomas, inchazo e picazón. O cambio regular do sitio da inxección na mesma rexión anatómica pode reducir os síntomas ou evitar o desenvolvemento destas reaccións. As reaccións normalmente desaparecen dentro duns días a varias semanas. En poucos casos, NovoMix ® 30 Penfill ® pode ser necesario cancelar debido ás reaccións no lugar da inxección.
O uso simultáneo de fármacos do grupo tiazolidinione e preparados de insulina. Informáronse casos de desenvolvemento de insuficiencia cardíaca crónica no tratamento de pacientes con tiazolidinediones en combinación con preparados de insulina, especialmente se tales pacientes teñen factores de risco para o desenvolvemento de insuficiencia cardíaca crónica.Este feito debe terse en conta á hora de prescribir a terapia combinada con tiazolidinediones e preparados de insulina a pacientes. Co nomeamento de tal terapia combinada, é necesario realizar exames médicos dos pacientes para identificar signos e síntomas de insuficiencia cardíaca crónica, aumento de peso e presenza de edema. Se os síntomas de insuficiencia cardíaca empeoran en pacientes, o tratamento con tiazolidinediones debe deixarse.
Influencia na capacidade para conducir vehículos e traballar con mecanismos. A capacidade dos pacientes para concentrarse e a velocidade de reacción pode verse alterada durante a hipoglucemia, o que pode ser perigoso en situacións nas que estas habilidades son especialmente necesarias (por exemplo, cando conducen vehículos ou traballan con máquinas e mecanismos).
Debe aconsellar aos pacientes que adopten medidas para evitar o desenvolvemento de hipoglucemia mentres conducen. Isto é especialmente importante para pacientes sen síntomas diminuídos de precursores de desenvolver hipoglucemia ou que padecen episodios frecuentes de hipoglucemia. Nestes casos, debe considerarse a adecuación da condución e a realización deste traballo.
Formulario de lanzamento
Suspensión para administración subcutánea, 100 pezas / ml. Nos cartuchos de vidro da clase hidrolítica 1, selados con discos de goma por un lado e pistóns de goma polo outro, de 3 ml cada un, colócase unha bola de vidro no cartucho para facilitar a mestura da suspensión, nun paquete de cinco cartuchos, nunha bolsa de cartón 1 ampolla.
Efecto secundario de Novomix 30 penfill:
Efectos secundarios asociados ao efecto sobre o metabolismo dos carbohidratos: hipoglucemia (aumento da sudoración, palidez da pel, nerviosismo ou tremor, ansiedade, cansazo ou debilidade inusual, desorientación, perda de concentración, mareos, fame grave, deficiencia visual temporal, dor de cabeza , náuseas, taquicardia). A hipoglucemia grave pode provocar perda de consciencia e / ou cambras, interrupción temporal ou irreversible do cerebro e morte.
Reaccións alérxicas: posibles - urticaria, erupción cutánea, raramente - reaccións anafilácticas. As reaccións alérxicas xeneralizadas poden incluír erupcións cutáneas, picazón na pel, aumento da transpiración, trastornos gastrointestinais, angioedema, dificultade para respirar, taquicardia e diminución da presión arterial.
Reaccións locais: reaccións alérxicas (vermelhidão, inchazo, picazón da pel no lugar da inxección), normalmente temporais e pasando a medida que continúa o tratamento, é posible a lipodistrofia.
Outro: ao principio da terapia raramente - edema, posiblemente unha violación de refracción.
Uso durante o embarazo e a lactación.
A experiencia clínica con insulina aspart no embarazo é moi limitada.
En estudos experimentais con animais non se atoparon diferenzas entre a embriotoxicidade e a teratoxenicidade da insulina aspart e da insulina humana. Durante o período do posible inicio do embarazo e durante todo o seu período, é necesario un coidadoso seguimento do estado dos pacientes con diabetes mellitus e un control dos niveis de glicosa no sangue. A necesidade de insulina, por regra xeral, diminúe no primeiro trimestre e aumenta gradualmente no segundo e terceiro trimestre do embarazo. Durante o nacemento e inmediatamente despois, os requirimentos de insulina poden caer drasticamente. Pouco despois do nacemento, a necesidade de insulina volve axiña ao nivel que estaba antes do embarazo.
Pódese usar insulina asprat durante a lactación (lactación) e pode ser necesario un axuste da dose da insulina.
Instrucións especiais para o uso Novomix 30 penfill.
Unha dose insuficiente de insulina ou a interrupción do tratamento, especialmente coa diabetes mellitus tipo 1, pode levar ao desenvolvemento de hiperglicemia ou cetoacidosis diabética. Os síntomas da hiperglicemia adoitan aparecer gradualmente ao longo de varias horas ou días. Os síntomas da hiperglicemia son náuseas, vómitos, somnolencia, vermelhidão e sequedad da pel, boca seca, aumento da produción de urina, sede e perda de apetito, así como a aparición dun cheiro a acetona no aire exhalado. Sen un tratamento adecuado, a hiperglicemia pode levar á morte. Despois de compensar o metabolismo dos carbohidratos, por exemplo, cunha terapia intensiva con insulina, os pacientes poden experimentar síntomas típicos de precursores da hipoglucemia.
En pacientes con diabetes cun control metabólico óptimo, as complicacións tardías da diabetes desenvólvense máis tarde e avanzan máis lentamente. Neste sentido, recoméndase realizar actividades dirixidas a optimizar o control metabólico, incluído o control do nivel de glicosa no sangue.
Unha consecuencia das características farmacodinámicas dos análogos de insulina de acción curta é que o desenvolvemento da hipoglucemia cando se usan comeza antes que co uso de insulina humana soluble.
Debe ter en conta a alta taxa de desenvolvemento do efecto hipoglucémico no tratamento de pacientes con enfermidades concomitantes ou tomar medicamentos que ralentizan a absorción de alimentos. En presenza de enfermidades concomitantes, especialmente de orixe infecciosa, a necesidade de insulina, por regra xeral, aumenta. A deterioración da función renal ou hepática pode levar a unha diminución dos requirimentos de insulina.
Ao transferir un paciente a outro tipo de insulina, os primeiros síntomas dos precursores da hipoglucemia poden cambiar ou facerse menos pronunciados en comparación cos que usan o tipo anterior de insulina.
A transferencia do paciente a un novo tipo de insulina ou a unha preparación de insulina doutro fabricante debe realizarse baixo estricta supervisión médica. Se cambia a concentración, tipo, fabricante e tipo (insulina humana, insulina animal, análogo da insulina humana) dos preparados de insulina e / ou o método de fabricación, pode ser necesario un cambio de dose.
Pode ser necesario un cambio na dose de insulina cun cambio na dieta e cun maior esforzo físico. O exercicio inmediato despois de comer pode aumentar o risco de hipoglucemia. Saltar comidas ou exercicio non previsto pode levar ao desenvolvemento de hipoglucemia.
Unha mellora significativa no estado de compensación do metabolismo dos carbohidratos pode levar a un estado de neuropatía de dor aguda, que normalmente é reversible.
A mellora a longo prazo do control glicémico reduce o risco de progresión da retinopatía diabética. Non obstante, a intensificación da insulinoterapia cunha forte mellora do control glicémico pode ir acompañada dunha deterioración temporal da retinopatía diabética.
Non se recomenda para o seu uso en nenos menores de 6 anos.
Influencia na capacidade para conducir vehículos e mecanismos de control
A capacidade dos pacientes para concentrarse e a velocidade de reacción pode verse alterada durante a hipoglucemia e a hiperglicemia, o que pode ser perigoso en situacións nas que estas habilidades son especialmente necesarias (por exemplo, cando conducen un coche ou traballan con máquinas e mecanismos). Debe aconsellar aos pacientes que adopten medidas para evitar o desenvolvemento de hipoglucemia e hiperglicemia cando conducen un coche e traballan con mecanismos. Isto é especialmente importante para pacientes sen síntomas diminuídos de precursores de desenvolver hipoglucemia ou que padecen episodios frecuentes de hipoglucemia. Nestes casos, débese considerar a viabilidade deste traballo.
Interacción de Novomix 30 penfill con outras drogas.
efecto hipoglicémico da insulina mellorar drogas orais hipoglicémicos, inhibidores da MAO, inhibidores de ACE, inhibidores de anhidrase carbónica, bloqueadores beta selectivos, bromocriptina, octreótido, sulfonamidas, esteroides Anabolica, tetraciclinas, clofibrato, cetoconazol, mebendazol, piridoxina, teofilina, ciclofosfamida, fenfluramina, preparacións de litio preparados que conteñen etanol.
Os anticonceptivos orais, GCS, hormonas tiroideas, diuréticos tiazídicos, heparina, antidepresivos tricíclicos, simpatomiméticos, danazol, clonidina, bloqueadores de canles de calcio, diazoxido, morfina, fenitoína, nicotina debilitan o efecto hipoglucémico da insulina.
Baixo a influencia de reserpina e salicilados, é posible tanto un debilitamento coma un aumento da acción do medicamento.
Os medicamentos que conteñen tiol ou sulfito, cando se engaden á insulina, provocan a súa destrución.
Preguntas, respostas, críticas sobre o medicamento NovoMix 30 Penfill
A información facilitada está destinada a profesionais médicos e farmacéuticos. A información máis precisa sobre o medicamento está contida nas instrucións que o fabricante adxunta aos envases. Ningunha información publicada nesta ou calquera outra páxina do noso sitio pode servir como substituto dun chamamento persoal a un especialista.