Produción de insulina enxeñaría xenética
Insulina: unha hormona pancreática que regula | metabolismo de carbohidratos e mantemento dun nivel normal de cazdpano sangue. A falta desta hormona no corpo leva.) A unha das enfermidades máis graves: a diabetes, que como causa da morte, está no terceiro lugar despois de enfermidades cardiovasculares e cancro. A insulina é un globo pequeno | proteína que contén 51 residuos de aminoácidos e consistente en dúas cadeas polipéptidas unidas entre si por dúas pontes disulfuro. Está sintetizado baixo a forma dun precursor fetal dunha única cadea, a preproinsulina, que contén koi un péptido de sinal central (23 residuos de aminoácidos) e un péptido de conexión de 35 enlaces (péptido C). Cando se elimina o péptido sinal, fórmase proinsulina de 86 residuos de aminoácidos na célula, na que están conectadas as cadeas de insulina A e BC-neiun tweed, que lles proporciona a orientación necesaria a 3 dólares no enlace disulfuro. Despois do desprendemento proteolítico do péptido C, fórmase insulina.
Coñécense varias formas de diabetes. A forma máis grave, para o tratamento da que o paciente necesita insulina (unha forma dependente da insulina da enfermidade), é causada pola morte selectiva de células que sintetizan esta hormona (células dos illotes de Langerhans no páncreas). É máis común unha forma de diabetes mellitus, para a que non se precisa un tratamento con insulina, pódese xestionar coa axuda de dietas adecuadas e re:> ma. Normalmente, o páncreas de vacún e vaca non se usa na industria cárnica e conserveira e colócase en vagóns refrixerados para empresas farmacéuticas onde se realiza a extracción de hormonas. Para obter 100 g de cr! A insulina talica require 800-1000 kg de materia prima
A síntese de ambas cadeas e a conexión dos seus enlaces disudfid para obter insulina leváronse a cabo en 1963 e 1965. tres equipos de investigación dos EUA, China e Alemaña. En 1980, a compañía danesa Novo Industri desenvolveu un método para converter a insulina porcina en insulina humana substituíndo o 30º residuo de alanina na cadea B por un residuo de treonina. Tanto a insulina non difería en actividade e duración da acción.
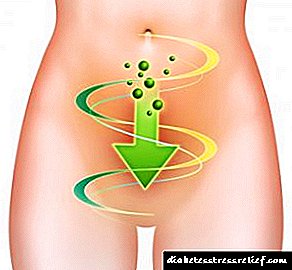
O traballo na enxeñaría xenética da insulina comezou hai uns 20 anos. En 1978, apareceu unha mensaxe sobre a produción dunha cepa de Escherichia coli que produce proinsulina de rata (EUA). No mesmo ano, as cadeas individuais de insulina humana foron sintetizadas mediante a expresión dos seus xenes sintéticos nas células.E.coli(Fig. 5.11). Cada un dos xenes sintetizados foi axustado ao extremo 3 'do xen da enzima (3-galactosidasa e introducido no plásmido vectorial(pBR322).CelasE.coliTransformados con tales plásmidos recombinantes, producíronse proteínas híbridas (quiméricas) consistentes nun fragmento de p-galactosidasa e un péptido de insulina A ou B unido a ela a través dun residuo de metionina. Ao procesar unha proteína quimérica con bromuro de cianóxeno, liberase o péptido. Non obstante, o peche de pontes disulfuro entre as cadeas de insulina formadas foi difícil.
En 1981, sintetizouse un análogo pro-insulina, mini-C-pro-insulina, no que o péptido C de 35 unidades foi substituído por un segmento de seis aminoácidos: arg-arg-gly-ser-lys-arg e a súa expresión mostrouse enE.coli
En 1980, W. Gilbert e os seus colegas illaron o ARNm de insulina dun tumor de células P pancreáticas de rata e obtiveron ADNc del mediante a transcriptasa inversa. O ADNc resultante insertouse no plásmidopBR322E.colina parte media do xene da penicilinase. O plásmido recombinante contiña información sobre a estrutura da proinsulina.Como resultado da tradución do ARNm, sintetizouse unha proteína híbrida nas células que conteñen secuencias de penicilinase e proinsulina, que foron dixeridas con trypsina de tal proteína.
En 1978, empregados do Instituto de Química Bioorgánica baixo a supervisión de Acad. Yu. A. Ovchinnikov, sintetizáronse dous xenes estruturais que codificaban a síntese de neuropéptidos:leucina: encefalina e bradiquinina.O xen encephalin de leucina sintetizado tiña dous extremos "pegajosos":
O xene sintético resultante foi inserido xunto cun fragmento de ADN natural que contén o promotor e a parte proximal do xene da proteína P-galactosidasa de E. coli.E.coliao plásmido
Obtención de insulina, métodos de enxeñaría xenética, Biotecnoloxía - Cursos

1. A estrutura e as funcións da insulina 5
1.1. A estrutura da molécula de insulina 5
1.2. A importancia biolóxica da insulina 7
1.3. Biosíntese de insulina 8
2. Enxeñería xenética síntese de insulina 10
2.1. Uso de métodos de enxeñaría xenética para a síntese de fármacos 10
2.2. Métodos de Enxeñaría Xenética 11
2.3. Produción de insulina enxeñaría xenética 14
Extracto do texto
Ademais, ambos estes compoñentes poden estar presentes á vez na composición da proteína híbrida. Ademais, ao crear proteínas híbridas, pódese usar o principio de multidimensionalidade: a presenza de varias copias do polipéptido diana na proteína híbrida, o que pode aumentar significativamente o rendemento do produto obxectivo.
No Reino Unido, as dúas vertentes de insulina humana sintetizáronse mediante E. coli, conectadas a unha molécula de hormona bioloxicamente activa. Para que un organismo unicelular sintetice moléculas de insulina nos seus ribosomas é necesario subministralo co programa necesario, é dicir, introducirlle o xen hormonal.
A insulina recombinante obtívose no Instituto da Academia Rusa de Ciencias utilizando cepas de E. coli xeneticamente deseñadas. Unha proteína precursora híbrida exprésase a partir da biomasa cultivada, expresada en cantidades
40. da proteína celular total que contén preproinsulina.
A súa conversión a insulina in vitro realízase na mesma secuencia que in vivo - o polipéptido principal é escindido, a preproinsulina convértese en insulina a través das etapas da sulfitólise oxidativa, seguida do peche reductor de tres enlaces disulfuro e o illamento enzimático do péptido C de unión. Despois dunha serie de purificacións cromatográficas de intercambio iónico, xel e HPLC, obtense insulina humana de alta pureza e actividade natural.
Para obter insulina, úsase unha cepa cunha secuencia de nucleótidos inserida no plásmido que expresa unha proteína híbrida consistente nunha proinsulina lineal e un fragmento da proteína A de Staphylococcus aureus unida ao seu terminal N mediante un residuo de metionina 8,9, 10.
O cultivo de biomasa saturada de células da cepa recombinante proporciona o comezo da produción dunha proteína híbrida, o illamento e transformación secuencial da que en tubo leva á insulina.
Outro xeito tamén é posible: obter no sistema bacteriano de expresión dunha proteína recombinante constituída por proinsulina humana e cola de polihistidina unidas a ela a través de residuos de metionina. Está illado mediante cromatografía de quelatos en columnas con escisión de Ni-agarosa e bromo.
A proteína illada é sulfonada con S. Cartografía e análise espectrométrica de masas da proinsulina obtida purificada por cromatografía de intercambio iónico sobre resina de intercambio de anión e cromatografía líquida de alto rendemento RP (fase inversa) mostran a presenza de pontes disulfuro que corresponden ás pontes disulfuro da proinsulina humana nativa.
Recentemente, prestouse moita atención á simplificación do procedemento para producir insulina recombinante mediante enxeñaría xenética.Así, por exemplo, pode obter unha proteína composta por proinsulina unida ao terminal N mediante o residuo de lisina do péptido líder interleucina
2. A proteína exprésase e localízase efectivamente en corpos de inclusión. Despois do illamento, a proteína para producir insulina e péptido C é cortada con trypsina 5, 8, 10.
A insulina resultante e o péptido C purifícanse mediante RP-HPLC. Moi significativa á hora de crear estruturas fundidas é a relación de masa da proteína portadora e do polipéptido diana.
Os péptidos C coa axuda de espaciadores de aminoácidos que levan o sitio de restrición Sfi I e dous residuos de arginina ao principio e ao final do espaciador para a dixestión posterior de tripsina de proteínas están conectados segundo o principio da cabeza da cola.
O HPLC dos produtos de escisión demostra que a división do péptido C procede cuantitativamente e isto permite o uso de xenes sintéticos multiméricos para producir polipéptidos diana a escala industrial.
Conclusión
A radical, e na maioría dos casos, a única forma de manter a vida e a capacidade de traballo dos pacientes con diabetes mellorable é a data, a insulina.
Antes de recibir e introducir a insulina na práctica clínica, esperábase un resultado fatal durante un ou dous anos desde o inicio da enfermidade de pacientes con diabetes tipo I, a pesar do uso de dietas máis debilitantes.
Os pacientes con diabetes tipo I necesitan unha terapia de reemplazo permanente con preparados de insulina. O cesamento da administración regular de insulina por un motivo ou outro leva ao rápido desenvolvemento de complicacións e á morte rápida do paciente.
Actualmente, a prevalencia da diabetes sitúase no terceiro lugar tras enfermidades do sistema cardiovascular e tumores malignos. A prevalencia da diabetes entre os adultos, segundo a Organización Mundial da Saúde, na maioría das rexións do mundo é do 2-5% e tende a aumentar cada
1. O número de pacientes case se duplicou. O número de pacientes dependentes da insulina, a pesar do evidente progreso no campo da asistencia sanitaria, vai aumentando cada ano, e actualmente en Rusia só hai uns 2 millóns de persoas.
Os métodos máis prometedores para producir insulina son os métodos de enxeñaría xenética. A insulina deseñada xeneticamente obtense producindo por separado as cadeas A e B empregando diferentes cepas de produtores e o posterior dobramento da molécula, seguida da separación das isoformas, e da síntese de proinsulina en células de E. Coli coa súa escisión con trypsina e carboxipeptidasa e a produción de insulina nativa.
A creación de fármacos de insulina humana doméstica xeneticamente deseñada abre novas posibilidades para resolver moitos problemas de diabetoloxía rusa co fin de salvar a vida de millóns de persoas con diabetes.
Literatura
Balabolkin M.I., Klebanova E.M., Kreminskaya V.M. Diabetes mellitus: aspectos modernos do diagnóstico e tratamento / Doctor, ed. G. L. Vyshkovsky.-2005.- M .: RLS-2005, 2004.- 960 p.
Gavrikov, A.V. Optimización da produción biotecnolóxica de substancias de interferóns humanos recombinantes: dis. ... cand. biol. Ciencias - M, 2003
Insulina humana xeneticamente deseñada. Aumento da eficiencia da separación cromatográfica mediante o principio de bifuncionalidade. / Romanchikov A.B., Yakimov S.A., Klyushnichenko V.E., Arutunyan A.M., Wulfson A.N. // Química Bioorganica, 1997 - 23, nº 2
Glick B., Parsnip J. Control do uso de métodos biotecnolóxicos // B. Glick, J. Parsnip / Molecular Biotechnology = Molecular Biotechnology. - M.: Mir, 2002 .-- S. 517-532. - 589 páx.
Glick B., Pasternak J. Biotecnoloxía molecular. Principios e aplicación. M .: Mir, 2002.
Davis R., Botstein D, Roth J. Métodos de enxeñaría xenética. A xenética das bacterias // R. Davis, D. Botstein, J. Roth / Per. do inglés.-M.: Mir. - 1984.- 176 p.
Ermishin A.P.Organismos modificados xeneticamente: mitos e realidade / A. P. Ermishin // Mn .: Tekhnalogaliya.- 2004. - 118 p.
Fundamentos da Biotecnoloxía Farmacéutica: Libro de texto / TP Prischep, V.S. Chuchalin, K.L. Zaykov, L.K. Mikhaleva. - Rostov-on-Don .: Phoenix, Tomsk: NTL Publishing, 2006.
Patrushev L.I. Sistemas xenéticos artificiais. // L.I. Patrushev / M .: Nauka.- 2004.
Romanchikov, A.B. Insulina humana xeneticamente deseñada. Aumento da eficiencia da separación cromatográfica mediante o principio de bifuncionalidade. / A.B. Romanchikov e outros.
// Química Bioorganica. 1997. Nº 2. páx. 23
Fundamentos de Rybchin V.N. da Enxeñaría Xenética // V. N. Rybchin / 2ª ed., Revisada. e engade .: Libro de texto para universidades. SPb .: Editorial de SPbSTU. - 2002 .-- 522 s.
Schelkunov S. N. Enxeñaría xenética // Schelkunov S. N. / Novosibirsk: Sib. univ. Editorial.2008.
Schelkunov, S.N. Enxeñaría xenética: libro de texto. bonificación. - 2ª, ed., Rev. e engade. - Novosibirsk: Sib. univ. Editorial, 2004 .-- 496 p.
1. A localización de enlaces disulfuro na molécula de insulina.
2. A disposición de residuos de aminoácidos na molécula de insulina
O efecto da insulina sobre encimas metabólicas clave
Músculo do fígado Activación do tecido adiposo 1. Fosfodiesterasa 1. Fosfodiesterasa 1. LP-lipase
4. Complexo de piruvato deshidroxenase
4. Complexo de piruvato deshidroxenase
5. Fosfatase glicóxeno sintasa e glicóxeno fosforilase
5. Glicóxeno sintase fosfatase b. Indución da acetil-CoA-carboxilase 1. Glucokinase 1. Gliceraldehido fosfato deshidroxenase
6. Represión da glicosa-6-fosfato deshidroxenase. Fosfenolpiruvato carboxinase
Fig. 3 Esquema de biosíntese de insulina en células β de illotes de Langerhans. ER - retículo endoplasmático. 1 - formación dun péptido sinal, 2 - síntese de preproinsulina, 3 - escisión do péptido sinal, 4 - transporte de proinsulina ao aparato Golgi, 5 - conversión de proinsulina a insulina e péptido C e inclusión de insulina e péptido C en gránulos secretores, 6 - secreción de insulina e péptido C.
4. Réxime xeral para a síntese de insulina dos seus predecesores
Fig. 5 Síntese da insulina mediante a formación de dúas cadeas separadas
O método de obtención de insulina humana deseñada xeneticamente

A invención está relacionada co campo da biotecnoloxía, en particular coa produción de insulina humana deseñada xeneticamente para a fabricación de medicamentos empregados no tratamento da diabetes mellitus.
O método realízase cultivando unha cepa produtora dunha proteína híbrida que contén proinsulina humana, Escherichia coli BL21 / pPINS07 (BL07) ou Escherichia coli JM109 / pPINS07, destruíndo as células mediante a desintegración, separando os corpos de inclusión que conteñen a proteína híbrida.
A continuación realízase un lavado previo de corpos de inclusión, disolución simultánea da proteína e restauración de enlaces disulfuro nun tampón con ditiotreitol de 5-10 mM e EDTA de 1 mM, renaturación e purificación da proteína de fusión renaturada mediante cromatografía de intercambio iónico.
A escisión da proteína híbrida lévase a cabo mediante a hidrólise conxunta da trypsina e da carboxipeptidasa B a unha proporción de peso da proteína híbrida, trypsina e carboxipeptidasa B 4000: 0,6: 0,9.
A purificación da insulina realízase mediante cromatografía hidrofóbica ou cromatografía líquida de alto rendemento en fase inversa seguida de filtración en xel e o illamento da insulina por cristalización en presenza de sales de cinc. A invención permite reducir o proceso de obtención de insulina humana deseñada xeneticamente e aumentar a súa produción.
A invención está relacionada co campo da biotecnoloxía, e en particular coa produción de insulina humana deseñada xeneticamente para a fabricación de medicamentos empregados no tratamento da diabetes mellitus.
Tendo en conta os principais logros da diabetoloxía moderna e as recomendacións da Organización Mundial da Saúde, os países europeos para 2001 completaron a transición ao uso da insulina humana. Neste sentido, o desenvolvemento de métodos para producir insulina usando os métodos da tecnoloxía recombinante do ADN é unha tarefa urxente.
Un método coñecido para producir insulina humana deseñada xeneticamente, que consiste en cultivar unha cepa produtora E. Coli producindo proinsulina, que contén unha secuencia de dous dominios de unión de IgG sintéticos da proteína A estafilocócica.
O método consiste en destruír células bacterianas, obter inclusión de Taurus que contén proinsulina, disolución en disolución Tauro, sulfitólise oxidativa da proinsulina, a súa renaturación, purificación da proteína renaturada mediante cromatografía de afinidade, división de proinsulina con enzimas proteolíticas (trypsina e carboxipeptidasa B) e purificación final de insulina con purificación de fase de alta eficiencia cromatografía (Nilson J., Jonasson P., Samuelsson E., Stahl S., Uhlen M. "Produción integrada de insulina humana e o seu péptido C", Journal of biotechnology, 1996, v. 48, p. 241-250) .
As desvantaxes deste método son o elevado custo do produto e o uso na produción de deterxente de insulina, que pode estar presente no produto obxectivo.
Un coñecido método de producir insulina humana deseñada xeneticamente, que consiste en cultivar células da cepa E.
A coli DN5 a / pVK100, destrúe as células bacterianas por desintegración por ultrasóns, separa os corpos de inclusión que conteñen a proteína híbrida das impurezas hidrosolubles por centrifugación, disolve os corpos de inclusión nun tampón que contén 8 M urea, 1 mM ditiotreitol, 0,1 M Tris-HCl, pH 8,0, durante 12-16 horas.
As impurezas insolubles elimínanse por centrifugación, despois da cal a concentración de ditiotreitol aumenta a 10 mM e restablecen os enlaces disulfuro a 37 ° C durante 1 hora. A solución foi diluída 5 veces con auga fría, axustada a pH 4,5 e incubada durante 2 horas a 4 ° C para formar un precipitado.
O precipitado que contiña a proteína híbrida foi separado por centrifugación e renaturado, disolto rapidamente en auga fría a un pH de 10-12, despois de que se diluíu con tampón de glicina de 10 mM, pH 10,8 e mantívose a 4 ° C durante a noite. Tras a ultrafiltración, a solución foi sometida a filtración en xel nunha columna Sephadex G-50 e eluído con tampón de glicina de 10 mM.
As fraccións que conteñen a proteína de fusión recóllense, ultrafiltranse e se líquense conxeladas. A proteína de fusión resultante disólvese en tampón Tris-HCl de 0,08 M, pH 7,5, a unha concentración de 10 mg / ml e fílase simultaneamente con trypsina e carboxipeptidasa B (relación de carboxipeptidasa B: trypsina: proteína de fusión 0,3: 1: 10) a 37. ° C durante 30 minutos.
Despois engade isopropanol ao 40%. A mestura cromatógrafa nunha columna DEAE-Sephadex A-25 e eluído con tampón Tris-HCl 0,05 M, pH 7,5 cun isopropanol ao 40% cun gradiente lineal de cloruro sódico de 0 a 0,1 m. Despois da eliminación do isopropanol, a concentración de cloruro de sodio aumentar ata o 25%, cambiar o pH a 2,0 e recoller o precipitado de insulina.
(Chen J.-Q., Zhang H.-T., Hu M.-N., Tang J.-G., "Produción de insulina humana nun sistema E. Coli con pro-insulina met-lys-humana como o expresado precursor "Bioquímica aplicada e Biotecnoloxía, 1995, v. 55, p. 5-15).
As desvantaxes deste método inclúen o uso de filtración en xel nas etapas iniciais, que require cantidades significativas de sorbente e un gran número de enzimas empregadas na escisión da proteína híbrida.
Un método coñecido para producir insulina humana deseñada xeneticamente, que consiste en cultivar unha cepa produtora de Escherichia coli JM109 / pPINS07, destruír células bacterianas por desintegración, separar corpos de inclusión que conteñen unha proteína híbrida, disolvelos nun tampón que contén urea e ditiotreitol, renaturación e purificación da proteína hibridada renaturada precipitación de compostos de impureza nun isopropanol ao 40% seguido de cromatografía en KM-sefaro, a súa escisión secuencial con trypsina e carboxipeptidasa B, mentres que os produtos A tripsinólise é cromatografiada en SP-Sefarosa, equilibrada con 0,03-0,1 M tampón de acetato de amonio pH 5,0-6,0 que contén urea de 6 M, con elución de proteínas cun gradiente lineal de cloruro sódico de 0 a 0,5 M no inicio O tampón e a fracción de insulina obtida despois da clivaxe con carboxipeptidasa B purificáronse mediante cromatografía líquida de alto rendemento en fase inversa (RP HPLC) seguida de filtración en xel (Pat. RF nº 2141531, MKI C12P 21/02, publ. 1999)
As desvantaxes do método inclúen o uso de cantidades significativas de urea e disolventes orgánicos na fase de purificación da proteína híbrida.
Experto en diabetes

Antes do uso de insulina, a esperanza de vida dun paciente con diabetes mellitus non superaba os 10 anos. A invención deste medicamento salvou a millóns de pacientes. A insulina enxeñaría xenética humana é o último avance da ciencia.
Froito de moitos anos de duro traballo
Antes da invención da preparación de enxeñería xenética (recombinante), a insulina estaba illada do páncreas do gando vacún e dos porcos.
A diferenza entre a insulina porcina e a humana é só un aminoácido
As desvantaxes deste método para obter a droga:
- a complexidade do almacenamento e transporte de materias primas biolóxicas,
- falta de gando
- dificultades asociadas coa asignación e purificación da hormona pancreática,
- alto risco de reaccións alérxicas.
Coa síntese de insulina humana natural no bioreactor en 1982, comezou unha nova era biotecnolóxica. Se nos albores da insulinoterapia o obxectivo dos científicos era só a supervivencia do paciente, no noso tempo o desenvolvemento de novos fármacos está dirixido a conseguir unha compensación sostible para a enfermidade. O obxectivo principal da investigación científica é mellorar a calidade de vida dun paciente con diabetes.
Tecnoloxía moderna
Tipos de medicamentos, segundo o método de preparación:
| Enxeñaría Xenética Recombinante | Para a produción utilízase un E. coli xeneticamente modificado.
| O favorito dos xenetistas é E. coli |
| Modificada xeneticamente | O material de partida é a insulina porcina. Modifícase mediante método de enxeñaría xenética. | Estrutura hormonal |
| Sintético | Un medicamento sintetizado artificialmente, na súa composición, é completamente idéntico á insulina humana. | Fabricación de drogas |
Que pasa no corpo despois da administración de drogas?
Conectando co receptor da membrana celular, a insulina forma un complexo que implementa os seguintes procesos:
- Mellora o transporte intracelular de glicosa e facilita a súa absorción.
- Promove a liberación de encimas que están implicadas no procesamento da glicosa.
- Reduce a taxa de formación de glicóxeno no fígado.
- Estimula o metabolismo de graxas e proteínas.
No caso da administración subcutánea, a insulina comeza a actuar en 20-25 minutos. A duración do medicamento de 5 a 8 horas. A enzima insulinase é escindida e excretada na urina. A droga non atravesa a placenta e non pasa ao leite materno.
Cando se prescribe a insulina deseñada xeneticamente?
Se é preciso axuda urxente
A insulina humana deseñada xeneticamente úsase nos seguintes casos:
- Diabetes tipo 1 ou tipo 2. Úsase como tratamento independente ou en combinación con outras drogas.
- Con resistencia a axentes hipoglucémicos orais.
- Con diabetes en mulleres embarazadas.
- En caso de complicacións dos riles e fígado.
- Ao cambiar a insulina de acción prolongada.
- No período preoperatorio.
- No caso de condicións mortais (coma hiperosmolar ou cetoacidótico).
- En situacións de emerxencia (antes do parto, con feridas).
- Se hai lesións na pel distróficas (úlceras, furunculose).
- Tratamento da diabetes nos antecedentes de infección.
A insulina de enxeñería xenética humana está ben tolerada e non causa reaccións alérxicas, xa que é completamente idéntica á hormona natural.
O control constante é importante!
Está prohibido prescribir medicamentos en caso de:
- baixar o azucre no sangue
- hipersensibilidade ao medicamento.
Nos primeiros días despois do nomeamento do medicamento, é necesario un coidadoso control do paciente.
Efectos secundarios
Perigo de urticaria! Edema de Quincke!
En casos raros, cando se usa insulina, son posibles as seguintes complicacións:
- reaccións alérxicas (urticaria, edema de Quincke, coceira da pel),
- unha forte diminución do azucre no sangue (desenvólvese debido ao rexeitamento da droga por parte do organismo ou en caso de conflito inmunolóxico),
- conciencia prexudicada
- En casos graves, o desenvolvemento de coma hipoglucémico é posible,
- sede, boca seca, letarxia, perda de apetito,
- hiperglicemia (cando se usa o medicamento nun fondo de infección ou febre),
- vermelhidão facial
- reaccións locais na área de administración (queima, picazón, atrofia ou proliferación de graxa subcutánea).
Ás veces, a adaptación ao fármaco vén acompañada de trastornos como o inchazo e a discapacidade visual. Estas manifestacións normalmente desaparecen ao cabo dunhas semanas.
Como atopar insulina xeneticamente deseñada nunha farmacia?
O medicamento está dispoñible en forma de solución para a administración parenteral:
| "Biosulina" | Duración media da acción |
| Actrapid | Insulina de acción curta |
| Gensulina | Preparación básica (combinación de insulinas de curta e media duración) |
| Rinsulina | Efecto rápido |
| Humalog | Para administrar o medicamento úsase unha pluma de xeringa. |
Non é difícil elixir unha preparación de insulina tendo en conta as características individuais do paciente.
Condicións de uso
A administración subcutánea de insulina é máis común.
En casos urxentes, o medicamento adminístrase por vía intravenosa.
En estado grave do paciente
Incluso un diabético con experiencia pode cometer un erro ao usar a droga.
Para evitar complicacións, é necesario:
- Antes do uso, verifique a data de caducidade do medicamento.
- Observe as recomendacións de almacenamento: os envases de reposición deben gardarse na neveira. O frasco desenvolvido pódese almacenar a temperatura ambiente nun lugar escuro.
- Asegúrese de recordar a dosificación correcta: lea de novo a receita do médico.
- Antes da inxección, é imprescindible liberar o aire da xeringa.
- A pel debe estar limpa, pero é indesexable usar alcol para o seu procesamento, xa que reduce a eficacia da droga.
- Elixe o mellor lugar para a inxección. Cando se introduce baixo a pel do abdome, o medicamento actuará máis rápido. Máis lenta absorción de insulina cando se introduce no pliegue gluteal ou no ombreiro.
- Use toda a superficie (prevención de complicacións locais). A distancia entre as inxeccións debe ser como mínimo de 2 cm.
- Agarre a pel na engrenaxe para reducir o risco de meterse no músculo.
- Inxecta a xeringa baixo a pel nun ángulo para que o medicamento non se escape.
- Cando se inxecta no estómago, adminístrase insulina de acción curta 20 minutos antes da comida. En caso de escoller un ombreiro ou nádegas - trinta minutos antes da comida.
Combinación con outras drogas
A miúdo con diabetes, o paciente toma varios medicamentos. A combinación con outros fármacos pode afectar o efecto terapéutico da insulina deseñada xeneticamente.
Para evitar complicacións, debes saber:
| Aumente o efecto da insulina deseñada xeneticamente baixando o azucre no sangue |
| Un medicamento popular usado no tratamento de infeccións do tracto urinario Doxiciclina |
| Reduce a acción da insulina |
| Preste atención! Diurético |
Sobredose
Nalgúns casos, a administración de insulina leva a unha diminución brusca do azucre no sangue. O problema adoita xurdir debido a unha selección incorrecta da dose.
Síntomas iniciais da hipoglucemia:
- debilidade
- palidez da pel
- estado de ansiedade
- mareos
- desorientación
- adormecimiento dos brazos, pernas, lingua e beizos,
- extremidades tremendo
- suor fría
- unha forte sensación de fame
- dores de cabeza.
Tremor; deterioración repentina do benestar
Se notas estes síntomas, debes comer rapidamente algo que conteña hidratos de carbono facilmente digeribles. Pode ser galletas, doces, un anaco de azucre ou pan branco. O té doce axuda en tales situacións.
Se o estado empeora, debes chamar a unha ambulancia. A hipoglicemia pode producir coma ou morte do paciente.
¿É perigosa a insulina recombinante?
Ola A insulina recombinante non é diferente da natural. Para obtela utilízanse bacterias modificadas xeneticamente.
Usando tecnoloxías de enxeñería xenética, un ADN recombinante que contén o xen da insulina é implantado na célula de E. coli. Os organismos modificados xeneticamente multiplícanse e producen unha hormona. A droga é moi eficaz e ten un alto grao de purificación.
Insulina Parte II Produción de insulina microbiolóxica

compoñente de afinidade - facilitando significativamente o illamento da proteína híbrida.
Ademais, ambos estes compoñentes poden estar presentes á vez na composición da proteína híbrida.
Ademais, ao crear proteínas híbridas, pódese usar o principio de multidimensionalidade (é dicir, varias copias do polipéptido obxectivo están presentes na proteína híbrida), o que pode aumentar significativamente o rendemento do produto obxectivo.
2 Expresión da proinsulina en células de E. coli ..
No traballo, os autores usaron a cepa JM 109 N1864 cunha secuencia de nucleótidos inserida no plásmido que expresa unha proteína híbrida, que consta de proinsulina lineal e un fragmento de proteína A de Staphylococcus aureus unido ao seu terminal N mediante o residuo de metionina.
O cultivo de biomasa saturada de células da cepa recombinante proporciona o comezo da produción dunha proteína híbrida, o illamento e transformación secuencial da que en tubo leva á insulina.
Outro grupo de investigadores recibiu unha proteína recombinante no sistema de expresión bacteriana dunha fusión composta por proinsulina humana e unha cola de polihistidina unida a ela a través dun residuo de metionina. Illouse mediante cromatografía de quelatos en columnas de Ni-agarosa de corpos de inclusión e dixerido con bromuro de cianóxeno.
Cartografía e análise espectrometrica de masas da proinsulina obtida purificada por cromatografía de intercambio iónico sobre resina de intercambio aniónico e RP (fase inversa) HPLC (cromatografía líquida de alto rendemento) mostrou a presenza de pontes disulfuro correspondentes ás pontes disulfuro da proinsulina humana nativa. O artigo informa sobre o desenvolvemento dun novo método mellorado para producir insulina humana mediante enxeñaría xenética en células procariotas. Os autores descubriron que a insulina resultante na súa estrutura e actividade biolóxica é idéntica á hormona illada do páncreas.
Recentemente, prestouse moita atención á simplificación do procedemento para producir insulina recombinante mediante enxeñaría xenética. Así, os autores obtiveron unha proteína de fusión constituída polo péptido líder da interleucina 2 unido ao extremo N da proinsulina a través do residuo de lisina.
A proteína foi expresada e localizada de forma eficiente en corpos de inclusión. Despois do illamento, a proteína foi dixerida con tripsina para producir insulina e péptido C. Outro grupo de investigadores actuou dun xeito similar.
Unha proteína de fusión composta por proinsulina e dous dominios sintéticos do estafilococo Localizouse unha proteína que unía a IgG nos corpos de inclusión, pero tiña un nivel de expresión máis elevado. A proteína foi illada por cromatografía de afinidade mediante IgG e procesada con trypsina e carboxipeptidasa B.
A insulina resultante e o péptido C purificáronse mediante HPP RP. Ao crear estruturas fundidas, a relación de masa da proteína portadora e do polipéptido diana é moi significativa.
Así, o traballo describe a construción de estruturas de fusión, onde se usou unha albumina sérica humana que se unía ás proteínas como polipéptido portador. Un, tres e sete péptidos C uníronse a ela.
Os péptidos C conectáronse nunha base de rabo de cabeza usando espaciadores de aminoácidos que transportaban o sitio de restrición Sfi I e dous residuos de arginina ao principio e ao final do espaciador para a posterior división de proteínas con tripsina. A HPLC dos produtos de escisión demostrou que a escisión do péptido C é cuantitativa e isto permite o uso de xenes sintéticos multiméricos para obter polipéptidos diana a escala industrial.
O traballo describe a preparación do mutante proinsulina, que contiña a substitución de Arg32Tyr. Cando esta proteína foi co-escindida coa tripsina e a carboxipeptidasa B, formouse a insulina nativa e un péptido C que contén o residuo de tirosina. Este último, despois do etiquetado 125I, úsase activamente en radioinmunoensayo. 3 Purificación da insulina.
A insulina destinada á fabricación de medicamentos debe ser de alta pureza. Polo tanto, é necesario un control altamente eficaz da pureza dos produtos obtidos en cada fase de produción. Previamente, RP e IO (intercambio iónico) HPLC utilizáronse para caracterizar a proinsulina-S-sulfonato, proinsulina, cadeas individuais A e B, e os seus sulfonatos S.
Tamén se presta especial atención ao derivado de insulina fluorescente. No traballo, os autores investigaron a aplicabilidade e a información dos métodos cromatográficos na análise de produtos en todas as fases da produción de insulina humana e elaboraron un calendario de operacións cromatográficas para separar e caracterizar eficazmente os produtos resultantes.
Ademais, estanse a desenvolver enfoques para automatizar e acelerar os procesos para determinar a pureza e cantidade de insulina.
O artigo informa sobre estudos sobre a posibilidade de usar cromatografía de líquido RP con detección electroquímica para a determinación de insulina, e unha metodoloxía para a determinación de insulina illada do illote de Langerhans mediante cromatografía de inmunoaffinidade con detección espectrometrica foi desenvolvida.
No traballo investigouse a posibilidade de empregar unha microdeterminación rápida de insulina mediante electroforese capilar con detección de fluorescencia láser. A análise realízase engadindo á mostra unha cantidade coñecida de insulina marcada con fenilisotiocianato (FITC) e un fragmento Fab de anticorpos de insulina monoclonal. As insulinas etiquetadas e regulares reaccionan competitivamente co complexo Fab. A insulina marcada con FITZ eo seu complexo con Fab sepáranse en 30 segundos.
Recentemente dedicáronse un gran número de traballos á mellora dos métodos para producir insulina, así como á creación de formas de dosificación baseadas nela.
Por exemplo, nos Estados Unidos, patentan os análogos da insulina hepatospecífica, estruturalmente diferentes da hormona natural debido á introdución de diferentes residuos de aminoácidos nas posicións 13-15 e 19 da cadea A e na posición 16 da cadea B.
Os análogos obtidos utilízanse como parte de varias formas parentélicas (intravenosa, intramuscular, subcutánea), dosificación intranasal ou implantación en forma de cápsulas especiais no tratamento da diabetes mellitus. De especial relevancia é a creación de formas de dosificación administradas sen inxección.
O artigo informa sobre a creación dun sistema macromolecular para administración oral, que é a insulina inmobilizada no volume dun polímero hidrogel modificado con inhibidores da enzima proteolítica. A eficacia deste medicamento é do 70-80% da eficacia da insulina nativa introducida subcutaneamente.
Noutro traballo, un fármaco obtense mediante unha incubación dun paso de insulina con glóbulos vermellos, tomada nunha proporción de 1-4: 100, en presenza dun axente ligante.Os autores denuncian a recepción dun medicamento cunha actividade de 1000 unidades / g, conservación completa da actividade despois da administración oral e almacenamento durante varios anos de forma liofilizada.
Ademais de crear novos fármacos e formas de dosificación baseadas na insulina, estanse a desenvolver novos enfoques para resolver o problema da diabetes.
Así, os autores transfectaron a ADNc proteína transportadora de glucosa GLUT2 previamente transfectada de xeito estable con ADNc de insulina de tamaño completo das células insulares HEP G2.
Nos clones de Insgl HEP G2 obtidos, a glicosa estimula preto da secreción normal de insulina e potencia a resposta secretora a outros estimulantes de secreción.
A microscopía inmunoelectrónica revelou gránulos que conteñen insulina morfológicamente similares aos gránulos nas células b dos illotes de Langerhans. Na actualidade estase a debater a posibilidade de usar "células b artificiais" obtidas por métodos de enxeñaría xenética para o tratamento da diabetes mellitus tipo 1.
Xunto coa resolución de problemas prácticos, estudan os mecanismos de acción da insulina, así como as relacións estruturais e funcionais na molécula. Un dos métodos de investigación é a creación de diversos derivados da insulina e o estudo das súas propiedades fisicoquímicas e inmunolóxicas 23, 24.
Como se mencionou anteriormente, varios métodos para a produción de insulina baséanse na obtención desta hormona en forma de precursor (proinsulina), seguido da clivaxe enzimática á insulina e ao péptido C. Na actualidade demostrouse a presenza de actividade biolóxica para o péptido C, o que fai posible o seu uso con fins terapéuticos xunto coa insulina.
Nos seguintes artigos desta serie consideraranse as propiedades fisicoquímicas e biolóxicas do péptido C, así como métodos para a súa preparación.
Biotecnoloxía na fabricación de fármacos
Son de interese os desenvolvementos para a obtención dunha versión 20G de STGh. Unha tarefa prometedora é obter e estudar non só varias formas de STH, senón tamén STH inmobilizada para obter a acción prolongada da hormona. Desenvolveuse un método orixinal para obter STHch inmobilizado cunha acción prolongada.
Paralelamente á produción de STH, creouse unha tecnoloxía integrada orixinal para a produción de hormonas de adenohipófise, incluídas todas as especies específicas e algunhas das súas modificacións a partir da GST. De gran importancia é a implementación dun programa dirixido para crear un medicamento terapéutico STH (somatogeno), obtido por enxeñaría xenética.
A experiencia clínica demostrou que, optimizando o tratamento do atropelo, é recomendable ter no arsenal varias preparacións farmacéuticas similares obtidas por diversas tecnoloxías ou incluso métodos (MF, Ausomatina, Somatogen).
O tratamento a longo prazo (durante anos) cunha preparación de STHh provoca unha diminución da sensibilidade no corpo.
En parte, isto pode ser o resultado da formación de anticorpos, pero hai que buscar a principal razón a nivel de receptores e procesamento da hormona.
O traballo con GST, así como estudos exhaustivos sobre as hormonas secretadas e as súas diversas formas permiten estudar os sistemas creados pola natureza e comprendelos mellor. A existencia de diversas formas nativas de STH no corpo indica a súa viabilidade e posible uso, por exemplo, nunha clínica.
Á hora de crear novos preparativos de STHch, cómpre primeiro enfocarnos nas formas naturais nativas da hormona e, se é o caso, escalalas mediante enxeñaría xenética, como se fai co monómero STHch.
Na produción de preparados STHch a partir de GST, implementouse con éxito unha tecnoloxía industrial completa para a produción doutras hormonas da adenohipófise (LGH, FSHch, TTGch e outros). É necesario optimizar a produción introducindo novos métodos avanzados (cromatografía de afinidade, etc.
), recibe hormonas altamente puras mediante tecnoloxía integrada.
É necesario ampliar a produción e o uso de conxuntos de inmunomicroanálise das hormonas da adenohipófise para diagnóstico e biotecnoloxía, para levar a cabo a produción regulada de anticorpos normalizados de varias escalas, para crear novos preparados STHch, incluídos os inmobilizados.
O feito de que o STH afecte ao metabolismo de proteínas, graxas e minerais, actúe a nivel celular sen un órgano diana e é anabólico, dá grandes perspectivas para o seu uso para estimular procesos de reparación e tratar varias enfermidades. Un estudo máis amplo destes temas, así como a posibilidade de utilizar varias formas e variantes modificadas de STGch, é unha tarefa urxente e prometedora.
Obtención de insulina na biotecnoloxía
A insulina, a hormona péptida dos illotes de Langerhans do páncreas, é o principal tratamento para a diabetes. Esta enfermidade é causada pola deficiencia de insulina e maniféstase por un aumento da glicosa no sangue. Ata hai pouco, a insulina obtíñase do páncreas dun touro e dun porco.
O fármaco difería da insulina humana por 1-3 substitucións de aminoácidos, polo que había unha ameaza de reaccións alérxicas, especialmente nos nenos. O uso terapéutico xeneralizado da insulina viuse limitado polo seu elevado custo e os seus recursos limitados.
Por modificación química, a insulina dos animais fíxose indistinguible do ser humano, pero isto supuxo un aumento adicional do prezo do produto.
Desde 1982, EliLilly está producindo insulina deseñada xeneticamente a partir da síntese separada de cadeas de E. coli A e B. O custo do produto diminuíu significativamente, a insulina resultante é idéntica á humana. Desde 1980, na prensa apareceron informes sobre a clonación do xen proinsulina, un precursor hormonal que se transforma nunha forma madura con proteólise limitada.
A tecnoloxía de encapsulamento tamén se aplica ao tratamento da diabetes: as células do páncreas nunha cápsula, introducidas unha vez no corpo do paciente, producen insulina durante o ano.
Integrated Genetics lanzou hormonas estimulantes dos folículos e luteinizantes. Estes péptidos están compostos por dúas subunidades. Na orde do día está a síntese industrial de hormonas oligopéptidas do sistema nervioso - encefalinas, construídas a partir de 5 residuos de aminoácidos, e endorfinas, análogos da morfina.
Cando se usan racionalmente, estes péptidos alivian a dor, crean un bo estado de ánimo, aumentan a eficiencia, centran a atención, melloran a memoria e poñen en orde o sono e o espertar.
Un exemplo da aplicación exitosa de métodos de enxeñería xenética é a síntese de p-endorfina empregando a tecnoloxía de proteínas híbridas descrita anteriormente para outra hormona péptida, a somatostatina.
Métodos para producir insulina humana:
Históricamente, o primeiro xeito de obter insulina con fins terapéuticos é o illamento de análogos desta hormona de fontes naturais (illotes do páncreas de bovinos e porcos).
Nos anos 20 do século pasado, descubriuse que as insulinas bovinas e porcinas (que están máis próximas á insulina humana en estrutura e secuencia de aminoácidos) presentan actividade no corpo humano comparable á insulina humana. Despois, utilizouse insulina de touro ou de porco para o tratamento de pacientes con diabetes tipo I.
Non obstante, ao cabo dun tempo demostrouse que nalgúns casos os anticorpos contra a insulina bovina e porcina comezan a acumularse no corpo humano, negando así o seu efecto.
Por outra banda, unha das vantaxes deste método para obter insulina é a dispoñibilidade de materias primas (a insulina bovina e porcina pódese obter facilmente en grandes cantidades), que xogou un papel decisivo no desenvolvemento do primeiro método para producir insulina humana.Este método chámase semi-sintético.
Neste método de produción de insulina humana, usouse insulina de porco como materia prima. O octapeptido C-terminal da cadea B foi escindido da insulina porcina purificada, tras o que se sintetizou o octapeptido C-terminal da insulina humana.
Despois uníase químicamente, retiráronse os grupos protectores e purificouse a insulina resultante. Ao probar este método para obter insulina, mostrouse a identidade completa da hormona obtida coa insulina humana.
A principal desvantaxe deste método é o elevado custo da insulina resultante (aínda agora, a síntese química do octapeptido é un pracer caro, especialmente a escala industrial).
Actualmente, a insulina humana obtense principalmente de dúas formas: por modificación da insulina porcina polo método sintético-enzimático e polo método de enxeñaría xenética.
No primeiro caso, o método baséase en que a insulina porcina difire da insulina humana nunha substitución no extremo C da cadea Ala30Thr B.
A substitución da alanina pola treonina realízase por un corte de alanina catalizado por enzima e a adición dun residuo de treonina protexido polo grupo carboxi en vez diso, que está presente nun gran exceso na mestura de reacción. Despois da ruptura do grupo protector O-terc-butilo obtense insulina humana.
A insulina foi a primeira proteína obtida con fins comerciais empregando a tecnoloxía de ADN recombinante. Existen dous enfoques principais para producir insulina humana deseñada xeneticamente.
No primeiro caso, obtéñense separacións (diferentes cepas produtoras) para ambas cadeas seguidas do dobrado da molécula (formación de pontes disulfuro) e separación de isoformas.
No segundo, a produción en forma de precursor (proinsulina) seguida dunha dixestión enzimática con trypsina e carboxipeptidasa B ata a forma activa da hormona.
Na actualidade, é máis preferible obter insulina en forma de precursor, o que asegura o correcto peche das pontes disulfuro (no caso de preparación separada de cadeas, realízanse sucesivos ciclos de desnaturalización, separación de isoformas e renaturación).
Con ambos os enfoques, é posible obter individualmente os compoñentes de partida (cadeas A- e B ou proinsulina), e como parte de proteínas híbridas. Ademais das cadeas A e B ou proinsulina, as proteínas híbridas poden conter:
1) proteína portadora: proporciona o transporte dunha proteína híbrida ao espazo periplásmico dunha célula ou medio de cultivo,
2) compoñente de afinidade - facilitando significativamente o illamento da proteína híbrida.
Ademais, ambos estes compoñentes poden estar presentes á vez na composición da proteína híbrida. Ademais, ao crear proteínas híbridas, pódese usar o principio de multidimensionalidade (é dicir, varias copias do polipéptido obxectivo están presentes na proteína híbrida), o que pode aumentar significativamente o rendemento do produto obxectivo.
Expresión da proinsulina en células de E. coli ..
O estribo JM 109 N1864 cunha secuencia de nucleótidos que expresa unha proteína de fusión, que consiste nunha proinsulina lineal e unha proteína Staphylococcus aureus Un traballo unido ao seu N-terminal a través do residuo de metionina.
O cultivo de biomasa saturada de células da cepa recombinante proporciona o comezo da produción dunha proteína híbrida, o illamento e transformación secuencial da que en tubo leva á insulina.
Outro grupo de investigadores recibiu unha proteína recombinante no sistema de expresión bacteriana dunha fusión composta por proinsulina humana e unha cola de polihistidina unida a ela a través dun residuo de metionina. Illouse mediante cromatografía de quelatos en columnas de Ni-agarosa de corpos de inclusión e dixerido con bromuro de cianóxeno.
Cartografía e análise espectrometrica de masas da proinsulina obtida purificada por cromatografía de intercambio iónico sobre resina de intercambio aniónico e RP (fase inversa) HPLC (cromatografía líquida de alto rendemento) mostrou a presenza de pontes disulfuro correspondentes ás pontes disulfuro da proinsulina humana nativa. Tamén se informa sobre o desenvolvemento dun novo método mellorado para producir insulina humana mediante enxeñería xenética en células procariotas. Os autores descubriron que a insulina resultante na súa estrutura e actividade biolóxica é idéntica á hormona illada do páncreas.
Recentemente, prestouse moita atención á simplificación do procedemento para producir insulina recombinante mediante enxeñaría xenética. Así, obtívose unha proteína de fusión consistente no péptido líder de interleucina unido ao extremo N da proinsulina a través do residuo de lisina. A proteína foi expresada e localizada de forma eficiente en corpos de inclusión.
Despois do illamento, a proteína foi dixerida con tripsina para producir insulina e péptido C. Outro grupo de investigadores actuou dun xeito similar. Unha proteína de fusión composta por proinsulina e dous dominios sintéticos do estafilococo Localizouse unha proteína que unía a IgG nos corpos de inclusión, pero tiña un nivel de expresión máis elevado.
A proteína foi illada por cromatografía por afinidade de IgG e dixerida con tripsina e carboxipeptidasa B. A insulina resultante e o péptido C purificáronse mediante HPLC RP. Ao crear estruturas fundidas, a relación de masa da proteína portadora e do polipéptido diana é moi significativa.
Descríbese a construción de construcións de fusión onde se usa unha proteína de unión á albumina en ser humano como polipéptido portador. Un, tres e sete péptidos C uníronse a ela.
Os péptidos C conectáronse nunha base de rabo de cabeza usando espaciadores de aminoácidos que transportaban o sitio de restrición Sfi I e dous residuos de arginina ao principio e ao final do espaciador para a posterior división de proteínas con tripsina. A HPLC dos produtos de escisión demostrou que a escisión do péptido C é cuantitativa e isto permite o uso de xenes sintéticos multiméricos para obter polipéptidos diana a escala industrial.
Obtención dunha proinsulina mutante, que contiña a substitución de Arg32Tyr. Cando esta proteína foi co-escindida coa tripsina e a carboxipeptidasa B, formouse a insulina nativa e un péptido C que contén o residuo de tirosina. Este último, despois do etiquetado 125I, úsase activamente en radioinmunoensayo.
A insulina destinada á fabricación de medicamentos debe ser de alta pureza. Polo tanto, é necesario un control altamente eficaz da pureza dos produtos obtidos en cada fase de produción. Previamente, RP e IO (intercambio iónico) HPLC utilizáronse para caracterizar a proinsulina-S-sulfonato, proinsulina, cadeas individuais A e B, e os seus sulfonatos S.
Tamén se presta especial atención ao derivado de insulina fluorescente. No traballo, os autores investigaron a aplicabilidade e a información dos métodos cromatográficos na análise de produtos en todas as fases da produción de insulina humana e elaboraron un calendario de operacións cromatográficas para separar e caracterizar eficazmente os produtos resultantes.
Ademais, estanse a desenvolver enfoques para automatizar e acelerar os procesos para determinar a pureza e cantidade de insulina.
Informáronse sobre estudos sobre a posibilidade de usar cromatografía líquida RP con detección electroquímica para determinar a insulina e elaborouse unha metodoloxía para determinar a insulina illada do illote de Langerhans mediante cromatografía de inmunoaffinidade con detección espectrometrica.
No traballo investigouse a posibilidade de empregar unha microdeterminación rápida de insulina mediante electroforese capilar con detección de fluorescencia láser.A análise realízase engadindo á mostra unha cantidade coñecida de insulina marcada con fenilisotiocianato (FITC) e un fragmento Fab de anticorpos de insulina monoclonal. As insulinas etiquetadas e regulares reaccionan competitivamente co complexo Fab. A insulina marcada con FITZ eo seu complexo con Fab sepáranse en 30 segundos.
Insulina de enxeñería xenética

A cuestión de que se fai a insulina é de interese non só para os médicos e farmacéuticos, senón tamén para os pacientes con diabetes mellitus, así como os seus familiares e amigos.
Hoxe, esta hormona única e tan importante para a saúde humana pódese obter de diversas materias primas mediante tecnoloxías especialmente desenvolvidas e probadas con coidado. Dependendo do método de preparación, distínguense os seguintes tipos de insulina:
- O porco ou bovino, tamén chamado produto animal
- Porco biosintético modificado
- Proxectado xeneticamente ou recombinante
- Modificada xeneticamente
- Sintético
A insulina de porco foi a que máis se usa para a diabetes. A súa aplicación comezou nos anos 20 do século pasado.
Cómpre salientar que a carne de porco ou animal foi a única droga ata os anos 80 do século pasado. Para conseguilo utilízase tecido de páncreas animal.
Non obstante, este método dificilmente se pode chamar óptimo ou sinxelo: traballar con materias primas biolóxicas non sempre é conveniente, e a materia prima en si non é suficiente.
Ademais, a composición da insulina porcina non coincide completamente coa composición da hormona producida por unha persoa sa: varios residuos de aminoácidos están presentes na súa estrutura. Cómpre salientar que as hormonas producidas polo páncreas do gando teñen un número aínda maior de diferenzas, que non se pode chamar un fenómeno positivo.
En tal preparación, ademais da sustancia multicomponente pura, está sempre presente a chamada proinsulina, unha sustancia que non se pode separar mediante métodos modernos de purificación. É el quen adoita converterse nunha fonte de reaccións alérxicas, especialmente perigoso para nenos e anciáns.
As farmacias volven ingresar aos diabéticos. Hai unha droga moderna e sensata europea, pero calan ao respecto. Iso.
Por este motivo, científicos de todo o mundo están interesados en levar a composición da hormona producida polos animais en pleno cumprimento das hormonas pancreáticas dunha persoa sa. Un verdadeiro avance na farmacoloxía e tratamento da diabetes foi a produción dun fármaco semisintético obtido substituíndo o aminoácido alanina nun medicamento de orixe animal por treonina.
Ao mesmo tempo, un método semisintético para producir a hormona baséase no uso de preparados animais. Noutras palabras, simplemente sofren modificacións e convértense en idénticas ás hormonas producidas polos humanos. Entre as súas vantaxes está a compatibilidade co corpo humano ea ausencia de reaccións alérxicas.
As desvantaxes deste método inclúen a escaseza de materias primas e a dificultade de traballar con materiais biolóxicos, así como o elevado custo tanto da propia tecnoloxía como da droga resultante.
Neste sentido, o mellor medicamento para o tratamento da diabetes é a insulina recombinante obtida pola enxeñaría xenética.
Por certo, a miúdo chámase insulina deseñada xeneticamente, indicando así o método para obtela, e o produto resultante chámase insulina humana, destacando así a súa identidade absoluta coas hormonas producidas polo páncreas dunha persoa sa.
Entre as vantaxes da insulina de enxeñería xenética, cabe destacar tamén o seu alto grao de pureza e falta de proinsulina, así como o feito de que non causa reaccións alérxicas e non ten contraindicacións.
A pregunta frecuente é comprensible: en que consiste exactamente a insulina recombinante? Resulta que esta hormona é producida por cepas de levadura, así como Escherichia coli, colocadas nun medio especial de nutrientes. Ademais, a cantidade da sustancia obtida é tan grande que é posible abandonar completamente o uso de drogas obtidas de órganos animais.
Por suposto, non se trata de E. coli simple, senón de xenes modificados e capaces de producir insulina humana xeneticamente deseñada xeneticamente, cuxa composición e propiedades son exactamente as mesmas que a hormona producida polas células do páncreas dunha persoa sa.
As vantaxes da insulina de enxeñería xenética non só son a súa absoluta semellanza coa hormona humana, senón tamén a facilidade de preparación, unha cantidade suficiente de materias primas e un custo accesible.
Científicos de todo o mundo chaman á produción de insulina recombinante un avance real no tratamento da diabetes. A importancia deste descubrimento é tan grande e importante que é difícil sobrevaloralo.
É moi sinxelo notar que hoxe en día case o 95% da necesidade desta hormona se responde coa axuda de insulina deseñada xeneticamente.
Ao mesmo tempo, miles de persoas que antes tiñan alerxia ás drogas recibiron unha oportunidade para unha vida normal.
Tiven diabete durante 31 anos. Agora está san. Pero, estas cápsulas son inaccesibles para a xente común, non queren vender farmacias, non lles resulta rendible.
Como funciona a insulina da enxeñería humana
No tratamento da diabetes mellitus tipo 1 utilízase insulina enxeñería xenética en dúas fases. Nas farmacias véndese en forma de solución e leva a marca "Encantado". O segundo tipo de enfermidade tamén se pode tratar con tal fármaco se os medicamentos prescritos non son adecuados para un diabético.
A insulina deseñada xeneticamente tamén se usa se unha persoa ten coma diabético. Os médicos adoitan prescribir inxeccións a mulleres embarazadas diagnosticadas de diabetes mellitus cando as pastillas para reducir o azucre e unha dieta terapéutica non axudan.
En xeral, úsanse insulinas ou transxénicos xenéticamente durante o parto, cando están sometidos a unha cirurxía, ou se o diabético está ferido grave. O medicamento permítelle cambiar con seguridade as hormonas de acción rápida.
- Antes de empregar a enxeñería xenética humana bifásica de insulina, é necesario facer unha proba e descubrir se este medicamento é adecuado para o paciente. Se un diabético revela hipoglucemia, non se recomenda o uso do medicamento.
- O esquema de acción da solución é que a insulina deseñada xeneticamente interactúe coas células, o que leva á formación de complexos. Cando as células entran nestes complexos, estimúlanse e comezan a traballar máis activamente. Como resultado, prodúcense máis encimas.
- No proceso, a glicosa é absorbida máis rápido, os carbohidratos que entran no corpo son procesados activamente. Así, o fígado produce glicosa máis tempo e as proteínas pódense absorber moito máis rápido.
O principio de acción do medicamento depende da dosificación, tipo de insulina, elección do lugar de inxección. Calquera procedemento debe facerse só logo de acordo co médico asistente. As primeiras inxeccións fanse baixo supervisión médica.
Recomendacións para o uso do medicamento
A enxeñería xenética humana bifásica ou como a insulina ten nomes comerciais diferentes. Ademais, as hormonas poden variar na duración da acción, o método de preparación da solución. Os produtos denomínanse en función do tipo de insulina.
As insulinas xeneticamente deseñadas forman parte de tales medicamentos como Humudar, Vozulim, Actrapid. Insuran, Gensulina. Esta non é unha lista completa de tales drogas, o seu número é bastante grande.
Todos os medicamentos anteriores varían en termos de exposición ao corpo.Os transxénicos poden durar varias horas ou estar activos durante días enteiros.
Os medicamentos combinados en dúas fases inclúen medicamentos que inclúen certos compoñentes que cambian o período de exposición ao medicamento.
- Tales medicamentos véndense en forma de mesturas, incluídas as hormonas obtidas xeneticamente.
- Estes fondos inclúen Mikstard, Insuman, Gansulin, Gensulin.
- As drogas úsanse dúas veces ao día, media hora antes da comida. A este sistema deberase cumprir estrictamente, xa que a hormona está directamente relacionada co período de inxestión de alimentos.
Por produción xénica de insulina humana obtense unha preparación que ten un tempo medio de exposición.
- A solución ten efecto dentro de 60 minutos, pero o momento da maior actividade obsérvase seis a sete horas despois da inxección.
- O medicamento elimínase completamente do corpo despois de 12 horas.
- Estes medicamentos inclúen Insuran, Insuman, Protafan, Rinsulina, Biosulina.
Tamén hai transxénicos cun curto período de exposición ao corpo. Estes inclúen medicamentos insulina Actrapid, Gansulina, Humulina, Insuran, Rinsulina, Bioinsulina. Tales insulinas teñen unha fase activa despois de dúas a tres horas, e os primeiros signos da acción do medicamento pódense ver dentro da media hora despois da inxección.
Antes da administración da insulina, hai que examinar os transxénicos para ver a transparencia e a ausencia de substancias estrañas no líquido. Se no medicamento aparecen substancias estranxeiras, turbidez ou precipitación, hai que descartar o frasco. A medicina non é adecuada para o seu uso.
A insulina empregada debe estar a temperatura ambiente. A dosificación da hormona debe axustarse se o diabético ten unha enfermidade infecciosa, unha disfunción da tiroides, a enfermidade de Addison, o hipopituitarismo e unha enfermidade renal crónica.
Os ataques de hipoglucemia son posibles cunha sobredose do medicamento, no caso dunha transición cara a un novo tipo de insulina, debido a saltarse comidas ou exceso de tensión física. Tamén a culpa pode ser as enfermidades que reducen a necesidade dunha hormona: un grave grao de enfermidade renal, enfermidade do fígado, diminución da glándula tiroide, córtex suprarrenal e glándula pituitaria.
- É posible unha forte diminución do azucre no sangue cun cambio na área de inxección. Polo tanto, é necesario cambiar dun tipo de insulina razoadamente e só logo de acordo co médico que o atende.
- Se un diabético usa insulina de acción curta, ás veces o volume de tecido graxo diminúe no lugar da inxección ou, pola contra, aumenta. Para evitar isto, a inxección debe facerse en diferentes lugares.
As mulleres embarazadas deben ser conscientes de que os requisitos de insulina poden variar durante diferentes trimestres do embarazo. Para iso, cómpre realizar unha proba diaria de azucre no glucómetro cun glucómetro.
A acción da insulina sobre o corpo humano descríbese en detalle no vídeo neste artigo.
1. A estrutura e as funcións da insulina 5
1.1. A estrutura da molécula de insulina 5
1.2. A importancia biolóxica da insulina 7
1.3. Biosíntese de insulina 8
2. Enxeñería xenética síntese de insulina 10
2.1. Uso de métodos de enxeñaría xenética para a síntese de fármacos 10
2.2. Métodos de Enxeñaría Xenética 11
2.3. Produción de insulina enxeñaría xenética 14

Conclusión 18
Síntomas de sobredosis
Ao usar insulina, é importante seguir as recomendacións do médico e observar a dosificación exacta do medicamento prescrito.
En caso de incumprimento das normas e unha sobredosis, o diabético comeza a ter dores de cabeza graves, calambres, fame, sudoración, frecuencia cardíaca, a persoa queda sobrecargada, irritada. Tamén se poden observar frialdes en todo o corpo e tremores.
Tales síntomas son moi similares aos signos dunha diminución da glicosa no sangue.Cunha etapa leve de síntomas, o diabético pode resolver de forma independente o problema e mellorar a condición. Para iso, come doces ou calquera outro produto doce que conteña azucre.
- Se ocorre un coma diabético, empregan unha solución de dextrosa, o medicamento adminístrase por vía intravenosa ata que a persoa está consciente. Nos primeiros sinais sospeitosos é necesario chamar a unha ambulancia, que poderá dar vida á paciente mediante métodos de emerxencia.
- Como efectos secundarios despois do uso de transxénicos, unha persoa ten erupcións na pel en forma de urticaria, partes do corpo se inchan, a presión arterial cae bruscamente, pode producirse picazón e falta de respiración. Esta é unha reacción alérxica a un fármaco, que ao cabo dun tempo pode desaparecer por conta propia sen intervención médica. Se a situación continúa, debes consultar ao teu médico.
- Nos primeiros días de tomar unha preparación de insulina, os diabéticos adoitan deshidratar o corpo, unha persoa experimenta unha falta de líquido, o apetito empeora, inchazo nos brazos e nas pernas e constátase unha somnolencia. Tales síntomas xeralmente desaparecen rapidamente e non se repiten.
Comentarios e comentarios
Teño diabete tipo 2 non dependente da insulina. Un amigo aconsellou baixar o azucre no sangue con DiabeNot. Pedín por internet. Comezou a recepción.
Sigo unha dieta non estrita, cada mañá comecei a percorrer 2-3 quilómetros a pé. Nas dúas últimas semanas, noto unha diminución suave do azucre no contador pola mañá antes do almorzo de 9,3 a 7,1, e ata as 6 de onte.
1! Continúo o curso preventivo. Cancelarei a subscrición sobre os éxitos.
Margarita Pavlovna, agora tamén estou sentada no Diabenot. SD 2. Realmente non teño tempo para facer unha dieta e camiñar, pero non abuso de doces e carbohidratos, creo que XE, pero debido á idade, o azucre segue sendo alto.
Os resultados non son tan bos como os teus, pero por 7,0 o azucre non sae unha semana. Con que glucómetro mides azucre? ¿Amósalle plasma ou sangue integral? Quero comparar os resultados de tomar a droga.
Moitas grazas por unha publicación tan divulgativa.
Produción de insulina enxeñaría xenética

Para que unha persoa se sinta, cómpre supervisar o nivel de insulina no corpo. Esta hormona debería ser suficiente para que a glicosa non se acumule no sangue. Se non, en caso de trastornos metabólicos, o médico diagnostica diabete.
A terapia para o estadio avanzado de diabetes mellorar é repoñer a concentración de insulina que falta, que non pode ser producida de forma natural polo corpo. Para iso, úsase insulina soluble, que é semellante á humana deseñada xeneticamente. O páncreas é o responsable da produción de tal hormona.
Para a produción de insulina, non só se usa a tecnoloxía para producir hormonas naturais, os fabricantes tamén usan insulina modificada obtida artificialmente. O medicamento marcado como "solubilis" indícase como soluble.
Tipos de drogas
A enxeñería xenética humana bifásica ou como a insulina ten nomes comerciais diferentes. Ademais, as hormonas poden variar na duración da acción, o método de preparación da solución. Os produtos denomínanse en función do tipo de insulina.
As insulinas xeneticamente deseñadas forman parte de tales medicamentos como Humudar, Vozulim, Actrapid. Insuran, Gensulina. Esta non é unha lista completa de tales drogas, o seu número é bastante grande.
Todos os medicamentos anteriores varían en termos de exposición ao corpo. Os transxénicos poden durar varias horas ou estar activos durante días enteiros.
Os medicamentos combinados en dúas fases inclúen medicamentos que inclúen certos compoñentes que cambian o período de exposición ao medicamento.
- Tales medicamentos véndense en forma de mesturas, incluídas as hormonas obtidas xeneticamente.
- Estes fondos inclúen Mikstard, Insuman, Gansulin, Gensulin.
- As drogas úsanse dúas veces ao día, media hora antes da comida. A este sistema deberase cumprir estrictamente, xa que a hormona está directamente relacionada co período de inxestión de alimentos.
Por produción xénica de insulina humana obtense unha preparación que ten un tempo medio de exposición.
- A solución ten efecto dentro de 60 minutos, pero o momento da maior actividade obsérvase seis a sete horas despois da inxección.
- O medicamento elimínase completamente do corpo despois de 12 horas.
- Estes medicamentos inclúen Insuran, Insuman, Protafan, Rinsulina, Biosulina.
Tamén hai transxénicos cun curto período de exposición ao corpo. Estes inclúen medicamentos insulina Actrapid, Gansulina, Humulina, Insuran, Rinsulina, Bioinsulina. Tales insulinas teñen unha fase activa despois de dúas a tres horas, e os primeiros signos da acción do medicamento pódense ver dentro da media hora despois da inxección.
Tales drogas elimínanse completamente do corpo despois de seis horas.
Uso de humanos solubles en insulina deseñados xeneticamente para a diabetes

A insulina humana deseñada xeneticamente é un substituto hormonal común da insulina que produce o páncreas. Non só se usa a hormona humana modificada xeneticamente para a síntese, senón tamén a sustancia creada sinteticamente. Outra das opcións coñecidas para crear a droga é o uso de insulina porcina modificada, porque na súa composición e funcións, é o máis próximo ao humano. Programa de produción de insulina de enxeñería xenética. A insulina deseñada xeneticamente pode usarse tanto para a diabetes mellitus tipo 1 como para a diabetes tipo 2, cando se observa unha reacción constante aos fármacos orais con natureza hipoglucemica. Pódese usar cando o paciente está en determinados tipos de coma. Se unha muller embarazada está empezando a padecer diabete, entón está permitido o uso de insulina de enxeñaría, pero só se a dieta non axuda a niveis de glicosa. Recoméndase o seu uso en casos de infección con infeccións nas que se poida observar hipertermia. Os preparados xénicos teñen éxito no seu uso durante o parto, operacións, lesións, trastornos metabólicos e no caso dunha transición gradual á insulina cunha acción longa. Está prohibido usar preparados xénicos que substitúan a hormona por hipersensibilidade a certos elementos do fármaco e por hipoglucemia. Drogas deste tipo reaccionan con certos receptores das membranas celulares, formando complexos con eles. Cando entra nas células, o complexo do fármaco afecta ao traballo, estimulándoo a ser máis activo e a producir encimas adicionais. O nivel de glicosa baixa debido a que é procesado máis rápido polas células. Despois diso, o proceso de lipoxénese, a produción de proteínas acelérase e a velocidade do fígado na formación de glicosa redúcese. A duración do medicamento dependerá do sitio de inxección, tipo de fármaco, dosificación e resposta individual do corpo humano. Só un médico pode establecer doses e prescribir certos medicamentos neste grupo. No período inicial de tomar fármacos, o paciente é acompañado polos médicos para saber se o medicamento é rexeitado. A insulina humana deseñada xeneticamente está contida en fármacos tan coñecidos como Insuran, Insuman, Vozulim, Penfill, Biosulin, Gensulin, Actrapid, Rinsulin, Humulin, Humudar, Rosinsulin e algúns outros. Existen varios tipos de insulina.Unha das clasificacións está relacionada coa duración do medicamento. Segundo ela, a insulina soluble pode ter unha acción curta e longa. Hai fármacos combinados (insulina bifásica), que conteñen unha sustancia de acción rápida e prolongada. A este tipo de medicamentos chámaselle mestura. Entre eles están os que se crean cun cambio na hormona humana. A insulina bifásica é Mikstard, Gansulin, Insuman, Humulin e Gensulin. Deben usarse dúas veces ao día, media hora antes das comidas. Isto débese a que a insulina bifásica ten unha sustancia de acción curta, cuxa inxestión depende da dieta. Un análogo de enxeñería de hormona humana está entre as drogas cun grao medio de duración. Esta insulina soluble comeza a actuar ao cabo dunha hora, e o pico da súa actividade prodúcese despois das 7 horas. Despois de 12 horas, móstrase. O medicamento xeneticamente humano deste grupo é Insuman, Protafan, Humulin, Rinsulina, Biosulina, Gensulina, Gansulina, Insuran. Hai un medicamento humano xeneticamente deseñado entre o grupo cunha acción curta. Por exemplo, estes inclúen Gansulin, Insuran, Humulin, Rinsulin, Gensulin, Bioinsulina e Actrapid. Tal insulina soluble comeza a actuar en media hora e a súa actividade alcanza o seu nivel máximo nun par de horas. Tales fármacos son excretados durante 6 horas. En caso de sobredose de medicamentos con insulina xeneticamente deseñada, poden producirse debilidade, somnolencia, fatiga, irritabilidade, calafríos, aumento da excreción de suor fría, tremor, palidez, palpitacións, dores de cabeza, calambres e fame. Todos estes son síntomas de hipoglucemia. Se esta enfermidade acaba de desenvolverse e está nos seus estadios máis fáciles, pode eliminar todos os síntomas. Para iso, cómpre comer alimentos con azucre e ricos en hidratos de carbono, que se poden dixerir facilmente. Glucagón e solución de dextrosa pódense introducir no corpo. Se unha persoa caeu en coma, entón inxecta unha solución de dextrosa modificada ata que a situación mellore. Algunhas persoas poden desenvolver reaccións alérxicas ao uso de medicamentos modificados xeneticamente con insulina. Os síntomas poden incluír colmeas, inchazo, perda de forza, baixa presión arterial, falta de respiración, erupcións cutáneas, febre e coceira. Nalgúns casos prodúcense hipoglucemia e coma. Pode ocorrer problemas coa conciencia humana e incluso un coma. Se un paciente perdeu medicación, pode desenvolver hiperglicemia. Aparece debido a doses baixas preliminares, co desenvolvemento de fenómenos infecciosos no corpo, e tamén se non se axusta ás regras da dieta. Nalgúns casos, o paciente pode desenvolver lipodistrofia nos lugares onde se administra o fármaco. Ao comezo do uso da droga, pode producirse inflamación, falta de auga, somnolencia e estragar o apetito. Pero estes fenómenos son temporais. O uso dun substituto para a insulina natural, como unha sustancia deseñada xeneticamente, é un excelente complemento para o tratamento da diabetes. Contribúe a reducir o nivel de azucre debido ao feito de que a glicosa é máis absorbida polas células e os procesos do seu transporte cambian. Pero estes medicamentos deben usarse estrictamente segundo a prescrición do médico, porque poden provocar efectos para a saúde non desexados. A insulina é o principal medicamento para o tratamento da diabetes tipo 1. Ás veces tamén se usa para estabilizar o estado do paciente e mellorar o seu benestar no segundo tipo de enfermidade. Esta sustancia pola súa natureza é unha hormona que é capaz de afectar o metabolismo dos carbohidratos en pequenas doses. Normalmente, o páncreas produce bastante insulina, que axuda a manter o nivel fisiolóxico de azucre no sangue. Pero con trastornos endocrinos graves, a única oportunidade para axudar ao paciente adoita ser precisamente as inxeccións de insulina. Por desgraza, é imposible tomala por vía oral (en forma de comprimidos), xa que se destrúe completamente no tracto dixestivo e perde o seu valor biolóxico. A obtención desta hormona do páncreas de porcos e bovinos é unha vella tecnoloxía que raramente se usa na actualidade. Isto débese á baixa calidade do medicamento recibido, á súa tendencia a provocar reaccións alérxicas e a un grao insuficiente de purificación. O feito é que, xa que a hormona é unha sustancia proteica, consiste nun conxunto específico de aminoácidos. A insulina producida no corpo do porco difire na composición de aminoácidos da insulina humana por 1 aminoácido e pola insulina bovina por 3. A principios e mediados do século XX, cando non existían medicamentos similares, incluso esa insulina supuxo un gran avance na medicina e permitiu levar o tratamento de diabéticos a un novo nivel. As hormonas obtidas por este método reducían o azucre no sangue, con todo, a miúdo causaron efectos secundarios e alerxias. As diferenzas na composición de aminoácidos e impurezas no medicamento afectaron á condición dos pacientes, especialmente nas categorías máis vulnerables de pacientes (nenos e anciáns). Outro motivo para a mala tolerancia de tal insulina é a presenza do seu precursor inactivo na droga (proinsulina), do que era imposible desfacerse desta variación do medicamento. Hoxe en día, hai insulinas avanzadas de porco carentes destas carencias. Obtense do páncreas dun porco, pero despois son sometidos a procesamento e purificación adicional. Son multicomponentes e conteñen excipientes. A insulina porcina modificada practicamente non é diferente da hormona humana, polo que aínda se usa na práctica Tales medicamentos son tolerados por pacientes moito mellor e practicamente non provocan reaccións adversas, non inhiben o sistema inmunitario e reducen de xeito eficaz o azucre no sangue. A insulina bovina non se usa na medicina hoxe en día, xa que debido á súa estrutura estranxeira afecta negativamente á inmunidade e a outros sistemas do corpo humano. A insulina humana, que se usa para diabéticos, a escala industrial obtense de dúas formas: Condicións de almacenamento da insulinaIndicacións e contraindicacións
Acción farmacolóxica das drogas
Exemplos de medicamentos para a insulina humana enxeñados xeneticamente
De que consiste a insulina?

Preparativos obtidos de materias primas de orixe animal
Enxeñaría Xenética
Cun cambio fisicoquímico, as moléculas de insulina porcina baixo a acción de encimas especiais fanse idénticas á insulina humana. A composición de aminoácidos da preparación resultante non é diferente da composición da hormona natural que se produce no corpo humano.
Durante o proceso de fabricación, o medicamento sofre unha alta purificación, polo tanto non causa reaccións alérxicas nin outras manifestacións indesexables.
Pero a maioría das veces, a insulina obtense empregando microorganismos modificados (xeneticamente). Usando métodos biotecnolóxicos, as bacterias ou a levadura modifícanse de xeito que eles mesmos poidan producir insulina.
Ademais da propia produción de insulina, a súa purificación xoga un papel importante. Para que o fármaco non produza reaccións alérxicas e inflamatorias, en cada etapa é necesario controlar a pureza das cepas de microorganismos e de todas as solucións, así como dos ingredientes empregados.
Existen 2 métodos para tal produción de insulina. O primeiro deles baséase no uso de dúas cepas (especies) diferentes dun único microorganismo.
Cada unha delas sintetiza só unha cadea da molécula de ADN hormonal (só hai dúas delas e están en espiral retorcidas entre si).
Entón estas cadeas están conectadas, e na solución resultante xa é posible separar as formas activas de insulina das que non teñen significado biolóxico.
A segunda forma de obter o medicamento usando Escherichia coli ou levadura baséase en que o microbio produce por primeira vez insulina inactiva (é dicir, o seu predecesor, a proinsulina). A continuación, usando un tratamento enzimático, esta forma actívase e úsase na medicina.
O persoal que teña acceso a determinadas instalacións de produción deberá ir sempre vestido cun traxe de protección estéril, excluíndo o contacto cos fluídos do corpo humano.
Todos estes procesos normalmente son automatizados, o aire e todas as superficies en contacto con ampolas e frascos son estériles e as liñas cos equipos están herméticamente seladas.
Os métodos de biotecnoloxía permiten aos científicos pensar sobre solucións alternativas á diabetes.
Por exemplo, ata a data, estanse a realizar estudos preclínicos da produción de células beta pancreáticas artificiais, que se poden obter mediante métodos de enxeñaría xenética.
Quizais no futuro sirvan para mellorar o funcionamento deste órgano nunha persoa enferma.
A produción de preparados modernos de insulina é un complexo proceso tecnolóxico que implica automatización e unha mínima intervención humana
Compoñentes adicionais
A produción de insulina sen excipientes no mundo moderno é case imposible de imaxinar, porque poden mellorar as súas propiedades químicas, ampliar o tempo de acción e acadar un alto grao de pureza.
Polas súas propiedades, todos os ingredientes adicionais pódense dividir nas seguintes clases:
- prolongadores (substancias que se usan para proporcionar unha duración de acción máis longa do medicamento),
- compoñentes desinfectantes
- estabilizadores, debido aos cales se mantén unha acidez óptima na solución farmacéutica.
Aditivos prolongadores
Existen insulinas de longa acción cuxa actividade biolóxica dura de 8 a 42 horas (dependendo do grupo do medicamento). Este efecto conséguese debido á adición de substancias especiais - prolongadores á solución de inxección. A maioría das veces, un dos seguintes compostos úsase para este propósito:
As proteínas que prolongan a acción do fármaco sofren unha purificación detallada e son baixo alerxénicas (por exemplo, protamina). As sales de cinc tampouco afectan negativamente á actividade da insulina nin ao benestar humano.
Os desinfectantes na composición da insulina son necesarios para que a flora microbiana non se multiplique durante o almacenamento e o uso nela. Estas substancias son conservantes e aseguran a preservación da actividade biolóxica do medicamento.
Ademais, se o paciente administra a hormona dun frasco só a si mesmo, entón o medicamento pode durar varios días.
Debido a compoñentes antibacterianos de alta calidade, non terá a necesidade de tirar un medicamento que non se use debido á posibilidade teórica de reprodución nunha solución de microbios.
Como desinfectantes pódense utilizar as seguintes substancias na produción de insulina:
Se a solución contén ións de cinc, tamén actúan como un conservante adicional debido ás súas propiedades antimicrobianas
Para a produción de cada tipo de insulina son adecuados certos compoñentes desinfectantes. A súa interacción coa hormona debe investigarse na fase de ensaios preclínicos, xa que o conservante non debe perturbar a actividade biolóxica da insulina ou afectar negativamente as súas propiedades.
O uso de conservantes na maioría dos casos permite que a hormona poida administrarse baixo a pel sen un tratamento previo con alcol ou outros antisépticos (o fabricante adoita referirse a isto nas instrucións).
Isto simplifica a administración do fármaco e reduce o número de manipulacións preparatorias antes da propia inxección.
Pero esta recomendación só funciona se a solución se administra mediante unha xeringa de insulina individual cunha agulla delgada.
Estabilizadores
Os estabilizadores son necesarios para que o pH da solución se manteña nun determinado nivel. A conservación do fármaco, a súa actividade e a estabilidade das propiedades químicas dependen do nivel de acidez. Na fabricación de hormona de inxección para pacientes con diabetes, os fosfatos normalmente úsanse para este propósito.
Para a insulina con cinc, non sempre son necesarios estabilizadores de solución, xa que os ións metálicos axudan a manter o equilibrio necesario.
De todos os xeitos, úsanse outros compostos químicos en vez de fosfatos, xa que unha combinación destas substancias leva á precipitación e á inadecuación da droga.
Unha propiedade importante mostrada a todos os estabilizadores é a seguridade e a incapacidade de entrar en reaccións coa insulina.
Un endocrinólogo competente debe tratar coa selección de medicamentos inxectables para a diabetes para cada paciente.
A tarefa da insulina non é só manter un nivel normal de azucre no sangue, senón tamén non prexudicar a outros órganos e sistemas. A droga debe ser químicamente neutral, baixo alérxeno e preferentemente asequible.
Tamén é bastante cómodo se se pode mesturar a insulina seleccionada coas súas outras versións segundo a duración da acción.
Obtención de insulina, métodos de enxeñería xenética, Biotecnoloxía - Cursos

1. A estrutura e as funcións da insulina 5
1.1. A estrutura da molécula de insulina 5
1.2. A importancia biolóxica da insulina 7
1.3. Biosíntese de insulina 8
2. Enxeñería xenética síntese de insulina 10
2.1. Uso de métodos de enxeñaría xenética para a síntese de fármacos 10
2.2. Métodos de Enxeñaría Xenética 11
2.3. Produción de insulina enxeñaría xenética 14