Diabetes mellitus informe
No artigo, consideramos as instrucións de uso, prezo e análogos de Sitagliptin.
Prodúcese como fosfato monohidrato. A súa forma de liberación son comprimidos recubertos con película.
O fármaco ten diferenzas significativas na acción farmacolóxica e na estrutura química dos análogos, así como derivados dos inhibidores da alfa-glicosidasa, biguanidas e sulfonilureas.

A inhibición do DPP 4 mediante "Sitagliptin" provoca un aumento da concentración das hormonas HIP e GLP-1. Estas hormonas están entre as incretinas. A súa secreción faise nos intestinos.
Como resultado de comer, a concentración de tales hormonas aumenta. As incretinas forman parte do sistema fisiolóxico que regula a homeostase do azucre no corpo humano. Os análogos de Sitagliptin deben ser seleccionados por un médico.
Características da farmacocinética
O medicamento é absorbido a un ritmo elevado despois do seu uso polo paciente. Esta ferramenta ten unha perfecta biodisponibilidade do 87%. A inxestión de alimentos graxos non afecta significativamente á cinética farmacolóxica do medicamento.
A droga é excretada como parte da orina sen cambios. Tras a parada da recepción, excrétase na urina durante a semana con ouriños (87%) e feces (13%).
Isto é confirmado polas instrucións de uso con Sitagliptin. Os análogos da droga son de interese para moitos.
Indicacións de uso da droga
O medicamento úsase na implementación da monoterapia, se o paciente está diagnosticado con diabetes mellitus tipo 2. Esta droga está aprobada para o seu uso independentemente da inxestión de alimentos. A combinación de Sitagliptin e Metformin pode usarse como tratamento complexo en presenza de diabetes mellitus tipo II.

En conxunto con Metformin, a dosificación recomendada do medicamento é de 100 mg unha vez ao día.
Se perdeu o momento da súa administración, debe beber Sitagliptin o antes posible. Isto débese a que non está permitido o uso dunha dobre dosificación da droga.
Está prohibido beber un medicamento con máis frecuencia do recomendado nas instrucións.
A droga fai posible controlar o nivel de azucres no corpo. Non obstante, esta droga non cura a diabetes.
O uso do medicamento debe realizarse cando o paciente está ben, deixar o tratamento só despois da recomendación e consulta do médico que o atende.
A Citagliptin ten análogos? Sobre iso a continuación.
Instrucións para o uso da droga
A sitagliptina é un medicamento que é tolerado bastante ben cando é tomado por un paciente, non só como monoterapia, senón como parte dun tratamento integral con outros axentes con propiedades hipoglucémicas.
A dose principal do medicamento é excretada polos riles. Este método de eliminación do compoñente activo do corpo humano require un especialista para supervisar a saúde deste corpo se o paciente tiña insuficiencia renal antes de usar o medicamento. Se é necesario, axústase a dose tomada. Se hai unha forma leve de insuficiencia renal, o axuste da dose do medicamento non se realiza.
Se un paciente ten insuficiencia renal moderada, a dosificación do medicamento non debe ser superior a 50 miligramos por día.O medicamento pódese usar en calquera momento, independentemente do procedemento, como a diálise.
Cando se usa este medicamento como parte dun tratamento complexo, para evitar a aparición de hipoglucemia inducida por sulfon no corpo do paciente, debe reducirse a cantidade de derivados de sulfonilurea.

A dosificación dos medicamentos utilizados é determinada polo médico que asiste logo que se realice un exame completo do corpo do paciente que sofre o segundo tipo de diabetes.
Se hai sospeita do desenvolvemento de pancreatite no corpo do paciente, é necesario parar o uso de Sitagliptin e outros medicamentos que poidan causar unha agravación da patoloxía.
Antes de usar o medicamento, un especialista debe informar ao paciente sobre os primeiros signos específicos de pancreatite.
Así se di nas instrucións de uso para "Sitagliptin". Prezo, críticas e análogos que se presentan a continuación.
Contraindicacións
O uso deste medicamento pode causar unha inflamación grave do páncreas no corpo humano.
Se o medicamento non se usa correctamente, pode causar moitos efectos secundarios no corpo. Se ocorren os primeiros síntomas de violacións, debes consultar inmediatamente a un especialista.
Use o medicamento en rigor estricto coas instrucións e na cantidade correcta prescrita polo médico asistente.
Cando se usa un medicamento, hai que ter en conta que hai toda unha serie de contraindicacións:
- a presenza do primeiro tipo de diabetes,
- hipersensibilidade
- tempo que leva o bebé,
- cetoacidosis diabética,
- lactación materna
- a idade do paciente é inferior a dezaoito anos.
O prezo e os análogos non se indican nas instrucións de uso con Sitagliptin.

Efectos secundarios factibles
Durante o uso do medicamento en humanos, poden producirse bastantes efectos secundarios. Entre eles destacan:
- angioedema,
- coceira
- anafilaxis,
- dor nas extremidades
- erupción cutánea
- dor nas costas
- vasculite na pel
- artralxia
- urticaria
- mialxia
- enfermidades exfoliativas da pel, síndrome de Stevens-Johnson,
- dor de cabeza
- pancreatite aguda,
- insuficiencia da actividade renal, insuficiencia deste órgano en forma aguda, que necesita diálise,
- estreñimiento
- nasofaringitis,
- vómitos
- infeccións do sistema respiratorio.
Ao usar a droga, é necesario seguir estrictamente as recomendacións nas instrucións, non pode tomala se ten polo menos unha das contraindicacións. Se se produce unha intoxicación ou unha sobredose como consecuencia do uso da droga, debería chamar de inmediato a unha ambulancia, xa que estes fenómenos negativos poden causar problemas de saúde importantes que incluso poden levar á morte.
Principios e métodos para a detección de diabetes
Para o tratamento de articulacións, os nosos lectores usaron con éxito DiabeNot. Vendo a popularidade deste produto, decidimos ofrecelo á súa atención.
O diagnóstico da diabetes mellitus consiste en realizar un exame completo, superando as probas necesarias e un exame por parte dun médico por un endocrinólogo. Normalmente non é difícil facer un diagnóstico, xa que moitos pacientes acoden xa á clínica cunha enfermidade corrente.
Pero os métodos modernos de investigación poden recoñecer non só as etapas iniciais e ocultas da diabetes, senón tamén a condición que precede a esta enfermidade, que se chama prediabetes ou unha violación da tolerancia aos hidratos de carbono.
Métodos de diagnóstico clínico
O médico recolle unha anamnesis, identifica factores de risco, herdanza, escoita queixas, examina o paciente, determina o seu peso.

Síntomas que se teñen en conta á hora de diagnosticar a diabetes:
- forte sede constante - polidipsia,
- formación excesiva de urina - poliuria,
- perda de peso con aumento do apetito - típico para diabetes tipo 1,
- aumento rápido de peso rápido, típico para a diabetes tipo 2,
- sudar, especialmente despois de comer,
- debilidade xeral, fatiga,
- coceira severa da pel que non pode estar satisfeita con nada,
- náuseas, vómitos
- patoloxías infecciosas, como enfermidades da pel pustulares, tordido frecuente na boca ou na vaxina, etc.
Non é necesario que unha persoa teña todos os síntomas inducidos, pero se se observan polo menos 2-3 ao mesmo tempo, paga a pena continuar o exame.
Cómpre destacar que coa diabetes tipo 1, todos os síntomas desenvólvense rapidamente e o paciente pode lembrar a data exacta do inicio dos síntomas, e algúns pacientes quedan tan inesperados que acaban en coidados intensivos en estado de coma diabético. Os pacientes con este tipo de diabete son normalmente persoas menores de 40-45 anos ou nenos.
O curso latente é máis característico da diabetes mellitus tipo 2, polo que trataremos máis adiante o diagnóstico desta forma particular de trastorno do metabolismo dos carbohidratos.
De gran importancia para o diagnóstico da diabetes tipo 2 son os factores de risco, que inclúen:
- idade de máis de 40-45 anos,
- prediabetes ou tolerancia á glucosa prexudicada,
- sobrepeso, obesidade (IMC maior de 25 anos),
- aumento do perfil de lípidos sanguíneos,
- presión arterial alta, presión arterial superior a 140/90 mm RT. Art.,
- baixa actividade física
- as mulleres que no pasado tiveron un trastorno no metabolismo dos carbohidratos durante o embarazo ou deron a luz a un fillo que pesaba máis de 4,5 kg,
- ovario poliquístico.
Todas as persoas maiores de 40-45 anos deben examinarse de azucre elevado na sangue unha vez cada 3 anos, e as persoas con obesidade e con polo menos un factor de risco, unha vez ao ano.
Na aparición da diabetes tipo 2, a herdanza xoga un papel importante. A existencia desta enfermidade en familiares aumenta as posibilidades de desenvolver diabetes tipo 2. As estatísticas din que unha persoa con un pai diabético tamén estará enferma nun 40% dos casos.
Forma de dosificación
Comprimidos recubertos con película de 25 mg, 50 mg ou 100 mg
Unha tableta contén
substancia activa - fosfatato de sitagliptina monohidrato 32,13 mg, 64,25 mg ou 128,5 mg (equivalente a 25 mg, 50 mg ou 100 mg de sitagliptina),
excipientes: celulosa microcristalina, fosfato de hidróxeno cálcico (anhidro), non mesturado, sodio croscarmelosa, estearato de magnesio, fumarato de estearilo sódico,
composición de revestimento de películas Opadray® II Pink 85F97191 (para dosificación 25 mg), Opadray® II Beige claro 85F17498 (para a dosificación 50 mg), Opadray® II Beige 85F17438 (para dosificación 100 mg): alcohol polivinilico, dióxido de titanio E171, macrogol / polietilenglicol 3350, talco, ferro (III) óxido amarelo E172, ferro (III) óxido vermello E172.
Comprimidos de 25 mg - As láminas son redondas, biconvexas, cubertas cunha funda de película rosa, gravadas cun "221" por un lado e lisas polo outro.
Comprimidos de 50 mg - As tabletas son redondas, biconvexas, recubertas cunha membrana de película de cor beige claro, co gravado "112" por un lado e liso polo outro.
Comprimidos de 100 mg - Tabletas de forma redonda, biconvexas, cubertas cunha cuncha de película beige, co gravado "277" por un lado e liso polo outro.
Métodos de investigación de laboratorio
Para o diagnóstico da diabetes tipo 2 úsanse varios tipos de probas. Algunhas técnicas úsanse como proxeccións. O cribado é un estudo dirixido a identificar a enfermidade nas primeiras etapas, realizado por un gran número de persoas que a miúdo non presentan síntomas evidentes da enfermidade. O método máis fiable para diagnosticar a diabetes é a determinación da hemoglobina glicosilada.
A hemoglobina glicosilada é a hemoglobina eritrocitaria que uniu unha molécula de glicosa.O grao de glicosilación depende da concentración de glicosa no sangue, que nos eritrocitos permanece inalterada durante a súa vida de tres meses. A norma de hemoglobina glicosilada é do 4,5-6,5% da cantidade total de hemoglobina.
A este respecto, en calquera momento, a porcentaxe de tal hemoglobina reflicte o nivel medio de azucre no sangue do paciente durante 120 días antes do estudo. Isto axuda non só a revelar a diabetes mellitus tipo 2 latente, senón tamén a determinar o grao de control da enfermidade e a avaliar a adecuación da terapia.

Os métodos para detectar a diabetes divídense en básicos e adicionais.
Os principais métodos inclúen os seguintes:
- determinación do nivel de azucre no sangue realizado: nun estómago baleiro, dúas horas despois de comer antes de durmir,
- un estudo sobre a cantidade de hemoglobina glicosilada,
- proba de tolerancia á glicosa - durante o estudo, o paciente bebe unha certa cantidade de glicosa e doa sangue do dedo antes e dúas horas despois de tomar o cóctel de diagnóstico. Esta proba axuda a aclarar o tipo de trastorno do metabolismo dos carbohidratos, permítelle distinguir os prediabetes da verdadeira diabetes,
- determinación da presenza de azucre nos ouriños: a glicosa entra nos ouriños cando a concentración supera os 8 a 9,
- análise do nivel de fructosamina: permite descubrir o nivel de azucre nas últimas 3 semanas,
- estudos da concentración de cetonas na urina ou no sangue - determina o inicio agudo da diabetes ou as súas complicacións.
Chámanse métodos adicionais que determinan os seguintes indicadores:
- insulina no sangue - para determinar a sensibilidade dos tecidos do corpo á insulina,
- autoanticorpos para células pancreáticas e insulina - revela unha causa autoinmune de diabetes,
- proinsulina: mostra a funcionalidade do páncreas,
- grelina, adiponectina, leptina, resistina - indicadores do fondo hormonal do tecido adiposo, avaliación das causas da obesidade,
- Péptido C: permítelle coñecer a taxa de consumo de insulina por células,
- Teclado HLA: usado para identificar patoloxías xenéticas.
A estes métodos recórrese en caso de dificultade durante o diagnóstico da enfermidade nalgúns pacientes, así como para a selección da terapia. O nomeamento de métodos adicionais é decidido só polo médico.
Propiedades farmacolóxicas
Farmacocinética
Despois da administración oral de 100 mg de sitagliptina, conséguese a concentración máxima (Cmax) no intervalo de 1 a 4 horas desde o momento da administración. A área baixo a curva de concentración-tempo (AUC) aumenta en proporción á dose e ascende a 8,52 μmol · hora cando se toma 100 mg por vía oral, Cmax é 950 nmol, a semivida (T1 / 2) é de 12,4 horas. A AUC plasmática de sitagliptin aumentou aproximadamente un 14% despois da seguinte dose de 100 mg de fármaco ao chegar ao estado de equilibrio despois de tomar a primeira dose. Os coeficientes de variabilidade AUC intra e interindividual de sitagliptin son insignificantes (5,8% e 15,1%). A farmacocinética da sitagliptina en xeral en individuos sans e pacientes con diabetes tipo 2 é similar. Absorción A biodisponibilidade absoluta de sitagliptin é aproximadamente do 87%. Dado que a inxestión combinada de sitagliptina e alimentos graxos non ten efecto na farmacocinética, o medicamento pode prescribirse independentemente da comida.
Distribución. O volume medio de distribución en equilibrio despois de tomar unha única dose de 100 mg de sitagliptin é de aproximadamente 198 L. A fracción de sitagliptina que se une ás proteínas do plasma é relativamente baixa, ao 38%.
Metabolismo. Só se metaboliza unha pequena fracción do medicamento recibido no corpo. Aproximadamente o 79% da sitagliptina excrétase sen cambios na orina. Aproximadamente o 16% do fármaco se excreta baixo a forma dos seus metabolitos.Atopáronse rastros de seis metabolitos que probablemente non afectasen á actividade do efecto inhibidor da sitagliptina DPP-4 no plasma. A enzima principal implicada no metabolismo limitado de sitagliptin atopouse CYP3A4 que implicaba CYP2C8.
A cría. Despois da administración oral de sitagliptina marcada con 14C por voluntarios sans, aproximadamente o 100% do medicamento foi excretado durante 1 semana con feces e ouriños do 13% e o 87%, respectivamente. A vida media de eliminación para a administración oral dunha única dose de 100 mg de sitagliptin é de aproximadamente 12,4 horas; a eliminación renal é de aproximadamente 350 ml / min.
A excreción de sitagliptina realízase principalmente por excreción polos riles mediante o mecanismo de secreción tubular activa. A sitagliptin é un substrato para o transportador de anións humanos orgánicos de tipo III (hOAT-3), que pode estar implicado na excreción de sitagliptina polos riles. A implicación de HOAT-3 no transporte de sitagliptin non foi estudada clínicamente. A sitagliptina é tamén un substrato da p-glicoproteína, que tamén pode estar implicado na eliminación renal da sitagliptina. Non obstante, a ciclosporina, un inhibidor da p-glicoproteína, non reduce a eliminación renal da sitagliptina. A sitagliptina non é un substrato para un transportador catiónico orgánico (OCT2), un transportador aniónico orgánico (OAT1) ou transportadores de proteínas (PEPT1 / 2).
Nos estudos envitroA sitagliptina non inhibe a transferencia mediada por OAT3 (IC50 = 160 μM) ou p-glicoproteína (ata 250 μM) a concentracións plasmáticas significativas terapéuticamente. Nos estudos clínicos, a sitagliptina ten poucos efectos sobre as concentracións plasmáticas de digoxina. Non obstante, a sitagliptina pode ser un inhibidor leve da p-glicoproteína.
Pacientes con insuficiencia renal. En pacientes con insuficiencia renal leve (liberación de creatinina KK 50-80 ml / min) non houbo un aumento clínicamente significativo da concentración de sitagliptina no plasma sanguíneo en comparación co grupo control de voluntarios sans. Observouse un aumento do AUC aproximadamente de 2 veces para a sitagliptina en pacientes con insuficiencia renal moderada (CC 30-50 ml / min), observouse un aumento de 4 veces de AUC en pacientes con insuficiencia renal grave (CC menos de 30 ml / min) e pacientes con insuficiencia renal en fase final que estiveron en hemodiálise, en comparación co grupo control. Por iso, para conseguir unha concentración terapéutica do medicamento no plasma sanguíneo en pacientes con insuficiencia renal moderada a grave, é necesario un axuste da dose. A sitagliptina é reducida en pequena medida durante a hemodiálise (o 13,5% da dose durante unha sesión de diálise de 3-4 horas, que comezou 4 horas despois de tomar o medicamento).
Pacientes con insuficiencia hepática. En pacientes con insuficiencia hepática moderada (7-9 puntos na escala Child-Pugh), non se precisa axuste da dose. Non hai datos clínicos sobre o uso de sitagliptina en pacientes con insuficiencia hepática grave (máis de 9 puntos na escala Child-Pugh). Non obstante, debido a que a sitagliptina é principalmente excretada polos riles, non se debe esperar un cambio significativo na farmacocinética de sitagliptina en pacientes con insuficiencia hepática grave.
A vellez. Non é necesario axustar a dose segundo a idade. En pacientes anciáns (65-80 anos), as concentracións plasmáticas de sitagliptin son un 19% máis altas que en pacientes máis novos.
Nenos. Non se realizaron estudos sobre o uso de sitagliptina en nenos.
Xénero, raza, índice de masa corporal. Non é necesario axustar a dose do medicamento segundo o sexo, a raza ou o IMC. Estas características non tiveron un efecto clínicamente significativo na farmacocinética da sitagliptina.
Diabetes tipo 2. A farmacocinética da sitagliptina é xeralmente a mesma en individuos sans e en pacientes con diabetes tipo 2. Os estudos clínicos descubriron que o xénero, a raza e o peso corporal non teñen un efecto clínico significativo na farmacocinética de sitagliptin.
Farmacodinámica
Xanuvia é un membro da clase de fármacos hipoglicémicos orais denominados inhibidores da dipeptidil peptidase 4 (DPP-4), que melloran o control glicémico en pacientes con diabetes tipo 2 aumentando os niveis das hormonas activas da familia de incretinas. As hormonas da familia das incretinas, incluído o péptido-1 (GLP-1) e o péptido insulinotrópico dependente da glicosa (HIP), están secretadas no intestino durante o día, o seu nivel aumenta en resposta á inxestión de alimentos. As incretinas forman parte do sistema fisiolóxico interno para regular a homeostase da glicosa. Con niveis de glicosa no sangue normais ou elevados, as hormonas da familia das incretinas contribúen a un aumento da síntese de insulina, así como á súa secreción por células beta pancreáticas debido aos mecanismos intracelulares de sinalización asociados con AMP cíclico (adenosina monofosfato).
Estudos de inhibidores de GLP-1 ou DPP-4 en modelos animais con diabetes tipo 2 demostraron unha mellor sensibilidade á glicosa das células β e a estimulación da síntese de insulina. Houbo un aumento da absorción de glicosa cun aumento da produción de insulina. O GLP-1 tamén axuda a suprimir o aumento da secreción de glucagón polas células alfa pancreáticas. Unha diminución da concentración de glucagón no fondo dun aumento dos niveis de insulina contribúe a unha diminución da produción de glicosa por parte do fígado, o que finalmente leva a unha diminución da glicemia.
A unha baixa concentración de glicosa no sangue, non se observan os efectos listados das incretinas sobre a liberación de insulina e unha diminución da secreción de glucagón. O efecto da estimulación de GLP-1 e GUI depende do nivel de glicosa no sangue. Non se estimula a produción de insulina nin a supresión da produción de glucagón GLP-1 cun baixo nivel de glicosa no sangue. GLP-1 e HIP estimulan a produción de insulina só cando o nivel de glicosa no sangue comeza a superar a norma. GLP-1 e HIP non afectan a liberación de glucagón como resposta á hipoglucemia. En condicións fisiolóxicas, a actividade das incretinas está limitada pola encima DPP-4, que hidroliza rapidamente as incretinas coa formación de produtos inactivos.
Xanuvia impide a hidrólise das incretinas por encima DPP-4, aumentando así as concentracións plasmáticas das formas activas de GLP-1 e HIP. Ao aumentar o nivel de incretinas, Januvia aumenta a liberación de insulina dependente da glicosa e axuda a reducir a secreción de glucagón. En pacientes con diabetes mellitus tipo 2 con hiperglicemia, estes cambios na secreción de insulina e glucagón conducen a unha diminución do nivel de hemoglobina glicosilada НbА11 e unha diminución da concentración plasmática de glicosa, determinada no estómago baleiro e despois dun test de estrés. O efecto dependente da glicosa da sitagliptin é diferente dos efectos das sulfonilureas, que aumentan a liberación de insulina incluso a niveis baixos de glicosa e poden levar a hipoglucemia en pacientes con diabetes tipo 2 e suxeitos saudables. A sitagliptin é un inhibidor altamente selectivo do encima DPP-4, e a concentracións terapéuticas non inhibe os encimas estreitamente relacionados DPP-8 ou DPP-9.
Resumo dun artigo científico sobre medicina e asistencia sanitaria, autor dun traballo científico - Kim S.S., Kim Yin Zhuo, Lee K.D., Park C.H., Kim Y.I., Lee Y.S., Chung S.Ch. ., Lee S.Ch.
Para o tratamento da diabetes mellitus tipo 2 (T2DM), recoméndase o inicio precoz da terapia combinada con fármacos hipoglucémicos. Nun ensayo aleatorizado multicéntrico, dobre cego, en grupos paralelos, a eficacia e a seguridade da sitagliptina e metformina administradas como combinación fixa (Sit / Met) foron comparadas con glimepirida como o tratamento inicial para pacientes con diabetes tipo 2. Métodos Os pacientes con T2DM (con idade> 18 anos) foron aleatorizados para recibir Sith / Met ou glimepirida dentro das 30 semanas despois do período inicial de lavado.O punto principal principal foi o cambio no nivel de HbA1 desde a liña de base. Os endpoints secundarios incluíron datos de pacientes que alcanzaron o obxectivo de tratar glimepirida HbA1c (n = 145). Despois de 30 semanas de tratamento, a combinación Sit / Met superou o glimepirida ao baixar o nivel de HbA1c (1,49 e 0,71%, respectivamente, a diferenza entre os grupos do 0,78%, p de glimepirida (40,1%, p de glimepirida) (diferenza no rango medio de 23,5 mg / dl, p de hipoglucemia e aumento de peso estatisticamente significativamente máis baixos no grupo Sit / Met en comparación co glimepirida (5,5% en comparación con 20,1%, 0,83 kg en comparación con +0,90 kg, respectivamente, para de ambas comparacións, o valor de p con glimepirida, o nomeamento de Sit / Met como terapia inicial 30 semanas despois do inicio do estudo, proporcionou máis mellora significativa do control glicémico e do peso corporal, mentres que se reduciu a incidencia de hipoglucemia.
Texto dun artigo científico sobre o tema "A eficacia e seguridade dunha combinación fixa de sitagliptin / metformina en comparación con glimepirida en pacientes con diabetes mellitus tipo 2: un estudo de dobre cego aleatorizado multicéntrico"
Eficacia e seguridade dunha combinación fixa de sitagliptina / metformina en comparación con glimepirida en pacientes con diabetes mellitus tipo 2: dobre aleatorizado multicéntrico
Kim S. SL 2, Kim I. CHL 2, Lee C.D. 3, Park C.H. 4, Kim Y.I. 5, Lee Y.S. 7, Chung S.Ch. 6, Lee S. 8ª parte
1 Departamento de Endocrinoloxía e Metabolismo, Departamento de Terapia, Busan State University Hospital, Corea do Sur
2 Instituto de Investigación Biomédica, Busan State University Clinic, Corea do Sur
3 Departamento de Endocrinoloxía e Metabolismo, Departamento de Terapia, Hospital de Daedong, Corea do Sur
4 Departamento de Endocrinoloxía e Metabolismo, Departamento de Terapia, Busan Peck Hospital, Universidade de Inje, Colexio de Medicina, Universidade de Inje, Busan, Corea do Sur
5 Departamento de Endocrinoloxía e Metabolismo, Departamento de Terapia, Hospital Universitario Ulsan, Corea do Sur
6 Departamento de Endocrinoloxía e Metabolismo, Departamento de Terapia, Dongkang Medical Center, Corea do Sur
7 Departamento de Endocrinoloxía e Metabolismo, Departamento de Terapia, Facultade de Medicina da Universidade de Dongguk, Gyeongju, Corea do Sur
8 MSD Korea Ltd, Seúl, Corea do Sur
Para o tratamento da diabetes mellitus tipo 2 (T2DM), recoméndase o inicio precoz da terapia combinada con fármacos hipoglucémicos. Nun ensayo aleatorizado multicéntrico, dobre cego, en grupos paralelos, a eficacia e a seguridade da sitagliptina e metformina administradas como combinación fixa (Sit / Met) foron comparadas con glimepirida como o tratamento inicial para pacientes con diabetes tipo 2.
Métodos Os pacientes con T2DM (con idade> 18 anos) foron aleatorizados para recibir Sith / Met ou glimepirida durante 30 semanas despois do período inicial de lavado. O punto principal principal foi o cambio no nivel de HbA1 desde a liña de base. Os endpoints secundarios incluían datos do paciente
* Este artigo está dispoñible publicamente de acordo cos termos da licenza non comercial Creative Creative Attribution, que permite usar, distribuír e reproducir datos de calquera xeito, sempre que se faga referencia correctamente á obra orixinal.
Provedores de tratamento HbA1c Non podo atopar o que necesitas? Proba co servizo de selección de literatura.
8 MSD Korea Ltd, Seúl, Corea do Sur e Corea do Sur
Recoméndase a iniciación temperá da terapia combinada con axentes antihiperglicémicos para tratar a diabetes tipo 2 (T2D). O presente estudo multicéntrico do grupo paralelo aleatorizado de dobre cego examinou a eficacia e seguridade dunha combinación de dose fixa sitagliptina e metformina (Sita / Met) en comparación con glimepirida en pacientes con T2D como tratamento inicial.
Métodos Os pacientes con diabetes tipo 2 (con idades superiores aos 18 anos) foron aleatorizados a Sita / Met ou glimepirida durante 30 semanas despois do período de lavado. O punto final principal foi o cambio da base (CFB) en HbA1c. Os obxectivos secundarios incluían a proporción de pacientes que alcanzaban o obxectivo HbA1c
Conclusións. En comparación con gLimepiride, Sita / Met como tratamento inicial levou a melloras significativas no control glicémico e cambios de peso corporal, cunha menor incidencia de hipoglucemia durante máis de 30 semanas.
glimepirida, hipoglucemia, metformina, fosfato de sitagliptina
J Diabetes. 2017, 9: 412-422. doi: 10.1111 / 1753-0407.12432
A carga clínica e económica da diabetes e o seu tratamento seguen a ser un problema importante para a comunidade médica 1, 2. A prevalencia total de diabetes en 2014 entre adultos foi do 9%, o 90% destes casos foron diabetes tipo 2 (T2DM ) En Corea do Sur, segundo o Programa nacional de verificación de saúde e nutrición, en 2011.a prevalencia estimada de diabetes mellitus en pacientes con idades superiores aos 30 anos foi do 10,5% en base a datos sobre a glicosa plasmática en xaxún (presión sanguínea en xaxún) e do 12,4% en base a datos sobre o nivel de glicosa en sangue e HbA1c.
Para a diabetes mellitus, existe unha forte correlación da presenza da enfermidade co desenvolvemento de complicacións micro e macro-vasculares que danan a órganos e tecidos, estas complicacións rexístranse nun 30-50% dos pacientes e o seu risco está asociado en gran medida a hipoglucemia previamente identificada. Dado que a terapia glicémica está principalmente orientada á prevención de complicacións microvasculares, a relación entre o control glicémico e as complicacións macrovasculares é 7-10 menos lixeira. Non obstante, a vantaxe de lograr un control glicémico intensivo nas etapas iniciais do tratamento da diabetes é a posibilidade de manter o control durante unha década ou máis incluso cun tratamento adicional menos intensivo 10, 11. Estes últimos resultados apoian un cambio nos principios de tratamento cara á consecución temperá de obxectivos glicémicos en pacientes con diabetes tipo 2.
O algoritmo de tratamento desenvolvido pola Asociación Americana de Endocrinólogos Clínicos (AACE) recomenda o inicio precoz da terapia combinada con metformina cun nivel inicial de HbA1c> 7,5% (58 mmol / mol), xa que alcanzar un nivel de HbA1c do 9,0% (75 mmol / mol), xa que é pouco probable que estes pacientes acaden o nivel obxectivo de HbA1c con monoterapia con metformina. Así, o inicio temperán do combinado
A terapia con fármacos hipoglicémicos con diversos mecanismos de acción pode ser unha opción especialmente eficaz para pacientes con diabetes tipo 2.
Na práctica clínica actual, os derivados 17-19 de sulfonil-urea úsanse a miúdo como terapia inicial para estimular a secreción de insulina en pacientes con diabetes tipo 2. Debido á súa capacidade para mellorar a secreción de insulina (que é un problema moi coñecido na T2DM), a glimepirida foi usada como monoterapia de primeira liña en moitos países, incluída Corea. Non obstante, debido ás taxas máis altas de mortalidade global en comparación coa metformina, xurdiu a preocupación pola seguridade dos derivados da sulfonilurea 20, 21. Ademais, destácase o desenvolvemento de hipoglucemia e un aumento do peso corporal co uso de glimepirida. Sitagliptin, un potente inhibidor da dipeptidil peptidasa (DPP) moi selectivo oral, foi o primeiro medicamento rexistrado desta clase para tratar pacientes adultos con diabetes tipo 2. A sitagliptina aumenta a secreción de insulina e reduce a concentración de glucagón a través dunha nova vía de sinalización hormonal. O mecanismo de acción deste fármaco depende do nivel de glicosa 23, 24. As sinerxías, a alta eficacia e a boa tolerabilidade da combinación de sitagliptina e metformina (Sit / Met) demostraron pacientes. con T2DM 25, 26. Non obstante, anteriormente non se realizaron estudos sobre a combinación fixa Sit / Met en Corea.
O obxectivo do estudo presentado en Corea foi estudar a eficacia e seguridade do tratamento inicial de Sit / Met FDC en comparación con glimepirida en pacientes con diabetes tipo 2.
O estudo de dobre cego aleatorio multicéntrico presentado en grupos paralelos realizouse do 6 de maio de 2010 ao 29 de outubro de 2013 en 21 centros clínicos de Corea do Sur durante 39 semanas (número de identificación CLinicaLtriaLs.gov Ш: NCT00993187, protocolo da empresa Merk MK-0431A -202). Os pacientes foron aleatorizados 1: 1 para unha terapia de 30 semanas despois dun período de indución / lavado de 6 semanas opcional e un período de indución obrigatorio de 2 semanas para a terapia placebo simple cega (Fig. 1, A). Este estudo realizouse de acordo
Fig. 1. Deseño do estudo e distribución do paciente
A - información detallada sobre a distribución dos pacientes, B - Sit / Met EyO - sitagliptin e metformina nunha combinación fixa, AE - un fenómeno indesexable, SNA - un fenómeno indesexable grave.
* O centro de ensaios clínicos foi pechado porque o investigador foi despedido do seu propio albedrío e era imposible trasladar o paciente a outro centro clínico. O patrocinador decidiu pechar este centro clínico e excluír ao paciente durante o período de selección para o estudo clínico.
coas normas das regras para a realización de ensaios clínicos de calidade, as disposicións da Declaración de Helsinki e as leis e regulacións estatais e / ou locais aplicables. Antes do estudo, a comisión de ética independente obtivo a aprobación en cada centro de investigación, así como o consentimento informado por escrito de cada paciente.
segundo os requisitos da investigación ou expoñer ao paciente ao risco segundo o investigador ou observación médica. Os pacientes foron excluídos do estudo durante o período introdutorio do placebo ou durante a aleatorización se o nivel de GPN ou os resultados dunha análise da glicosa capilar do xexún nun centro clínico foron inferiores a 110 mg / dl ou superiores a 300 mg / dl, respectivamente.
O período introdutorio inicial incluíu pacientes adultos (> 18 anos) con T2DM que non estaban embarazadas, non amamantaron e para os que había unha probabilidade de concepción extremadamente baixa durante o estudo ou período de observación clínica. Os criterios de selección na visita de cribado incluíron un nivel de HbA1c de> 7,0 (53 mmol / mol) a 6,5 (48 mmol / mol) a 7,0 (53 mmol / mol) ata 14 días, fármacos inmunomoduladores, cirurxía para anestesia xeral (dentro dos 30 días antes do inicio do estudo ou intervencións previstas), así como calquera opcións de terapia experimental (dentro de 8 semanas antes do inicio do estudo).
Outros criterios de exclusión incluían hipersensibilidade ou contraindicacións ao uso de derivados de sulfonilurea, inhibidores de DPP-4 ou biguanidas, creatinina sérica> 1,5 mg / dl en homes e> 1,4 mg / dl en mulleres, triglicéridos por encima de 500 mg / dl, desequilibrio da hormona estimulante da tiroide, enfermidade hepática en fase activa (excepto a hepatose graxa), enfermidades cardiovasculares, resultado positivo dunha análise do virus da inmunodeficiencia humana, trastornos do sistema hematopoietico, antecedentes de neoplasias malignas, unha proba positiva de embarazo de orina, índice de masa corporal (IMC)> 35 kg / m2 ou condicións que poidan levar a incumprimentos
Ao longo do período introdutorio / de lavado, os pacientes foron aconsellados sobre a dieta e o exercicio e instruíronse sobre o uso dos contadores de glicosa. Durante o período de placebo, os pacientes tomaron comprimidos placebo correspondentes a Sit / Met nunha combinación fixa (FDC) 50/500 mg (1 comprimido durante as comidas de mañá e noite), en combinación cun comprimido placebo correspondente a 1 mg de glimepirida (1 vez ao día ata a comida da mañá).
Durante o período de tratamento, o grupo experimental tomou Sit / Met nunha combinación fixa (Yanumet, Merck & Co., Inc., West Point, PA, EE. UU.) 50/500 mg 2 veces ao día por vía oral durante as comidas cunha titulación de dose de ata 50. / 1000 mg 2 veces ao día durante un período de 4 semanas. Ata a oitava semana despois do período inicial de 4 semanas, a titulación permitíase cunha redución da dose de Sit / Met FDC en caso de intolerancia, entón non se permitiron cambios de dosificación. Os comprimidos placebo correspondentes a glimepirida (Merck & Co., Inc., InvaGen Pharmaceuticals, Happodge, Nova York, EUA) foron necesarios para tomar unha vez ao día. Os pacientes do grupo control recibiron glimepirida nunha dose inicial de 1 mg / día cunha valoración de ata 6 mg / día durante as 8 primeiras semanas a criterio do investigador, segundo as recomendacións da ADA (American Diabetes Association, American Association of Diabetologists). Os comprimidos placebo correspondentes á Sit / Met FDC foron necesarios para tomar dúas veces ao día.Para asegurar un réxime cego, empregouse un enfoque con dous tipos de placebo: (1) pacientes do grupo Cit / Met FDC recibiron comprimidos Cit / Met FDC 50/500 mg e / ou Sit / Met FDC 50/1000 mg e comprimidos placebo correspondentes á glimepirida, ( 2) os pacientes do grupo glimepirida recibiron 2 comprimidos placebo correspondentes a Sit / Met FDC 50/500 mg e / ou Sit / Met FDC 50/1000 mg e comprimidos de glimepirida (a dose determinouse en función da valoración) 1 ou 2 mg.
Adherencia ao tratamento
Para cumprir os criterios de selección durante o período introdutorio, requiriuse un 85% de adhesión ao tratamento (calculado en función do cálculo de comprimidos placebo tomados nun réxime cego simple). Ao longo do período de tratamento, avaliouse a adherencia á terapia mediante a seguinte fórmula: porcentaxe de adhesión = (número real de días de tratamento / número de días de tratamento requirido) x 100.
Modo aleatorio / Distribución / Cego
Un estatístico que non participou no estudo preparou os esquemas de aleatorización. Ao final do período introdutorio do placebo (visita 5), todos os pacientes cuxos datos cumprían os criterios de selección foron asignados un número de asignación veciño do catálogo adecuado proporcionado por DreamCIS (Seúl, Corea). Merck Sharp e Dohme (West Point, PA, EUA) fornecéronlle os preparativos do modo cego e os sobres selados con códigos. Este estudo foi dobre cego, é dicir. Os investigadores, enfermeiros, farmacéuticos e pacientes non tiveron información sobre o tratamento recibido.
Avaliación e criterios de rendemento
A avaliación da eficacia hipoglicémica da terapia baseouse no nivel de HbA1c, GPN e no nivel de tolerancia do medicamento que estuda. O obxectivo principal de eficacia foi o cambio no nivel de HbAlc desde a liña base na semana 30 da terapia. Os endpoints secundarios incluíron cambios nos niveis de GPN desde a liña base ata os niveis na semana 30 e a proporción de pacientes que alcanzaron un nivel HbA1c obxectivo inferior ao 7% (53 mmol / mol) na semana 30.
Os extremos de seguridade incluíron a incidencia de episodios de hipoglucemia e cambios no peso corporal desde a liña base. A seguridade e tolerabilidade global foron avaliadas en función do número de eventos adversos relacionados co tratamento (EEs), resultados dunha proba de sangue bioquímica (incluído o nivel de alanina aminotransferase, aspartato minotransferase, bilirrubina total e fosfatase alcalina), proba de sangue hematolóxica (incluída a conta xeral de sangue, fórmula de leucocitos) e o número absoluto de neutrófilos), os principais indicadores do estado do corpo e a análise xeral da orina.
Aproximadamente 139 pacientes de cada grupo terapéutico (un total de 278 pacientes) foron necesarios para determinar o verdadeiro valor medio de diferenza do 0,4% do cambio no nivel de HbA1c desde a liña base ata a 30ª semana de tratamento entre os grupos Sit / Met FDC e os grupos de glimepirido cun nivel de significación bilateral. e 0,05. Este cálculo baseouse nunha estimación da desviación estándar (SD) do 1% para medir o cambio no nivel de HbA1c desde a liña base ata a 30 semana de tratamento, tendo en conta a asunción do 90% de potencia e o 5% dos pacientes cuxos datos non se poden avaliar.
Unha análise de punto final para comparar grupos terapéuticos para confirmar a superioridade dun tratamento foi realizada mediante a análise de covarianza (ANCOVA) para unha mostra completa de pacientes para a análise (FAS) cun valor p i. Non podes atopar o que necesitas? Proba co servizo de selección de literatura.
Dos 628 pacientes con diabetes tipo 2 que foron examinados para participar neste estudo, excluíron os datos; os 292 restantes foron aleatorizados (147 ao grupo Sit / Met FDC e 145 ao grupo glimepirida). 229 pacientes completaron o estudo (ver Fig. 1, B). A taxa de abandono abandonado foi do 17,7% no grupo Sit / Met FDC e do 25,5% no glimepirido.
As características básicas foron xeralmente comparables entre os dous grupos (ver Táboa 1), coa excepción dunha duración lixeiramente máis longa do T2DM no grupo Sit / Met FDC (4,6 e 3,9 anos).A idade media dos pacientes foi de 54,8 e 53,1 anos nos grupos Sith / MetFDC e glimepirida, respectivamente; o nivel medio de HbA1c foi do 8,0% (64 mmol / mol) no grupo Sith / Met FDC e do 8,1% (64 mmol / mol) no grupo glimepirido. Inicialmente, o 38,8 e o 43,3% dos pacientes non recibiron previamente terapia hipoglucémica nos grupos Sit / Met FDC e grupos glimepiridos, respectivamente. Información sobre tomar a droga
Táboa 1. Características demográficas e clínicas iniciais dos pacientes
Indicador I Sentado / Met FDC (n = 147) 1 Glimepirida (n = 145) 1 Total (n = 292) 1
Idade, anos 54,8 ± 8,5 53,1 ± 9,2 53,9 ± 8,9
Xénero Homes Mulleres 81 (55,1) 66 (44,9) 84 (57,9) 61 (42,1) 165 (56,5) 127 (43,5)
Peso corporal, kg 67,3 ± 8,8 67,7 ± 10,4 67,5 ± 9,6
IMC, kg / m2 25,2 ± 2,7 25,0 ± 2,8 25,1 ± 2,7
Duración da diabetes mellitus tipo 2 anos 4,6 ± 4,6 3,9 ± 3,7 4,2 ± 4,2
HbA1c% mmol / mol 8,0 ± 0,9 64,0 ± 9,8 8,1 ± 0,9 65,0 ± 9,8 8,0 ± 0,8 64,0 ± 8,7
GPN, mg / dl 171,5 ± 41,2 168,3 ± 39,4 169,9 ± 40,3
GFR 75,9 ± 11,7 76,7 ± 16,2 76,2 ± 13,3
Colesterol total, mg / dl 176,1 ± 34,9 171,0 ± 32,4 173,5 ± 33,7
Colesterol LDL, mg / dl 97,3 ± 33,0 95,0 ± 28,1 96,2 ± 30,6
HDL colesterol, mg / dL 48,2 ± 11,0 48,8 ± 10,1 48,5 ± 10,5
Triglicéridos, mg / dl 150,5 ± 88,2 134,1 ± 72,1 142,3 ± 80,8
XARDÍN, mmHg 125,3 ± 11,2 126,3 ± 13,2 125,8 ± 12,2
DBP, mmHg 76,7 ± 8,1 77,7 ± 8,5 77,2 ± 8,3
Terapia hipoglucémica anterior Si Non 90 (61,2) 57 (38,8) 82 (56,6) 63 (43,4) 172 (58,9) 120 (41,1)
Terapia anterior 118 (80,3) 123 (84,8) 241 (82,5)
Medicamentos hipolipidémicos 65 (44,2) 66 (45,5) 131 (44,9)
Inhibidores da PAC 43 (29,3) 43 (29,7) 86 (29,5)
Medicamentos antiplaquetas 57 (38,8) 53 (36,6) 110 (37,7)
Nota Salvo que se indique o contrario, os datos presentáronse como media ± desviación estándar (Por) ou n (%). Sit / Met EyO - sitagliptin e metformina nunha combinación fixa, DBP - presión arterial diastólica, GPN - glicosa plasmática en xaxún, RAS - sistema renina-angiotensina, CAD - presión arterial sistólica, IMC - índice de masa corporal, GFR - taxa de filtración glomerular, colesterol O colesterol LDL é lipoproteína de baixa densidade, o colesterol HDL é colesterol lipoproteíno de alta densidade.
Táboa 2. Resumo das doses máximas, finais e medias de glimepirida
Número de pacientes con 141 dispoñibles
Dose media ± RMS
desviación (jeje) 2,0 ± 1,3
Número de pacientes (%) como máximo
O número de pacientes (%) coa dose final
O 80,3% dos pacientes do grupo Sit / Met FDC e o 84,8% dos pacientes do grupo glimepirida presentaron o historial dos fármacos, os fármacos de baixada de lípidos máis mencionados, seguidos da frecuencia de antitrombóticos e drogas que afectan o sistema renina-angiotensina.
En ambos os grupos, entre os pacientes houbo un alto nivel de adhesión ao tratamento (> 90%). A maioría dos pacientes tomaron o medicamento para o estudo durante máis de 24 semanas. A duración media do medicamento en calquera dose foi similar en ambos os grupos terapéuticos (175,6 días no grupo Sit / Met FDC e 166,6 días no grupo glimepirida).
Tituación da dose no grupo de glimepirido
A dose media prescrita de glimepirido foi de 2,0 mg (rango: 1,0-6,0 mg). A dose máxima de 1 mg foi asignada ao 46,1% (65/141) de pacientes e só o 17,7% (25/141) de pacientes recibiron unha dose máxima de 6 mg (táboa 2). A dose final de glimepirida foi de 1 mg no 49,6% (70/141) e 6 mg no 17,0% (24/141) dos pacientes.
Análise de rendemento (FAS)
Endpoint primario
Na semana 30, o valor medio de HbA1c diminuíu do valor inicial: 8% (64 mmol / mol) a 6,5%
Sitagliptin / Metformin FDC A
90 80 70 60 50 40 30 20 10
p Non podo atopar o que necesitas? Proba co servizo de selección de literatura.
- Sitagliptin / Metformin FDC - Glimepirida
5 6 7 8 (0W) (2W) (4W) (8W)
- Sitagliptin / Metformin FDC - Glimepirida
Fig. 2. Indicadores de eficacia e seguridade durante o período de tratamento nos grupos de sitagliptina e metformina nunha combinación fixa (FDC) ou glimepirida (A, B, G)
Cambios en comparación cos valores iniciais de (A) HbA1c da poboación de análise completa (FAS), (B) glicosa plasmática en xaxún (GPN) en FAS e (D) peso corporal na poboación de pacientes que recibiron polo menos unha dose do medicamento estudado (APaT). A proporción de pacientes que alcanzaron o obxectivo HbA1c de 7 e 6,5% na semana 30 (FAS) (B). Número de pacientes con polo menos 1 episodio de hipoglucemia (poboación APaT) (D). Os datos son media ± erro estándar da media (SEM) (B, D, D) ou media ± SEM (A, C).
Diferencia = -14,7% p Non podo atopar o que necesitas? Proba co servizo de selección de literatura.
Na semana 30, alcanzouse o nivel HbA1 ^ inferior a un 7,0% (53 mmol / mol) nunha proporción estadísticamente significativamente maior de pacientes no grupo FDC Sit / Met.
en comparación co grupo glimepirida (81,2 e 40,1%, mediana p (36,5 meses)
Tempo tomado para diagnosticar a diabetes: medianas (24,8 kg / m2) IMC: 65 anos: medianas (56 anos) idade: mediana (7,8%)
■ Valor inicial HbA1c (%): Non atopo o que necesitas? Proba co servizo de selección de literatura.
■ Estrato: sen drogas hipoglucémicas
■ Estrato: tomar drogas hipoglucémicas
Fig. 3. Análise de subgrupos
A gráfica mostra as diferenzas entre as opcións de tratamento (glimepirida menos sitagliptina con metagina nunha combinación fixa) en relación ao nivel de HbA1c en diferentes subgrupos, determinado en función das características demográficas e antropométricas iniciais. Observouse unha diminución significativa en comparación co valor inicial en todos os subgrupos de ambos grupos terapéuticos. En ambos os grupos terapéuticos, con valores HbA1c iniciais máis altos, notouse unha diminución máis pronunciada deste indicador desde o nivel inicial. As diferenzas entre grupos entre os cambios no límite medio desde a liña inicial ata a semana 30 foron xeralmente as mesmas en todos os subgrupos identificados en función da idade, sexo, índice de masa corporal (IMC) e duración máis longa da diabetes mellitus tipo 2.
Táboa 3. Resumo de eventos adversos
Tamiz / Met Glimepiride FDC
(n = 146) (n = 144) glimepirida (95% CI +)
Resultado fatal 0 (0) 0 (0)
Eventos adversos graves 8 (5.5) 9 (6.3) -0.8 (-7.7, 5.0)
Eventos adversos asociados á toma do medicamento * 37 (25.3) 39 (27.1) -1,7 (-11.9.8.4)
Eventos adversos (pacientes con> 1 ocorrencia) 88 (60,3) 101 (70,1) -9,9 (-20,6, 1,1)
Eventos adversos detectados durante o tratamento (> 5% dos pacientes)
Trastornos gastrointestinais 51 (34,9) 27 (18,8) 16,2 (6,0, 26,0)
Dispepsia 19 (13,0) 9 (6,3)
Diarrea 15 (10,3) 4 (2,8)
Náuseas 10 (6,8) 4 (2,8)
Dor abdominal 4 (2,7) 0 (0,0)
Enfermidades infecciosas e parasitarias 31 (21.2) 32 (22.2) -1.0 (-9.0, 11.0)
Nasofaringitis 13 (8,9) 17 (11,8)
Infeccións das vías respiratorias superiores 12 (8.2) 4 (2.8)
Trastornos metabólicos e alimentarios 14 (9,6) 33 (22,9) -13,3 (5,0, 22,0)
Hipoglicemia 8 (5.5) 29 (20.1)
Diminución do apetito 6 (4.1) 0 (0.0)
Os resultados de estudos de laboratorio e instrumentais 8 (5.5) 15 (10.4) -4.9 (-1,0, 12,0)
Aumento de glicosa no sangue 0 (0,0) 6 (4,2)
Violacións do sistema nervioso 14 (9.6) 9 (6.3) 3.3 (-10.0, 3.0)
Mareos 5 (3.4) 2 (1.4)
Trastornos músculo-esqueléticos e do tecido conectivo 10 (6,8) 11 (7,6) 2,0 (-7,0, 2,0)
Violacións da pel e do tecido subcutáneo 4 (2,7) 10 (6,9) -4,2 (-1,0, 10,0)
Interrupción da terapia prescrita por eventos adversos 8 (5.5) 8 (5.6) -0.1 (-5.8, 5.6)
Interrupción da terapia por eventos adversos relacionados coa terapia. 7 (4.8) 3 (2.1) 2.7 (-1,8, 7,8)
Interrupción da terapia por graves eventos adversos 1 (0,7) 1 (0,7) 0
Nota A menos que se indique o contrario, preséntase o número de participantes en cada grupo, as porcentaxes danse entre parénteses. Aínda que o paciente podería ter dous ou máis eventos adversos, os datos do paciente en cada categoría rexistráronse só 1 vez. * Definido polo investigador como posible, probablemente ou definitivamente relacionado coa administración de fármacos. Calculáronse intervalos de confianza (CI) do 95% segundo o método de M1eSpep e IgtPep. Sit / Met EyO, sitagliptin e metformina nunha combinación fixa.
Para outros indicadores (funcións vitais, análise bioquímica de sangue, lípidos plasmáticos ou outros parámetros hematolóxicos), non se rexistraron cambios clínicamente significativos desde o nivel inicial nin diferenzas entre os grupos.
O estudo multicéntrico de dobre cego en pacientes coreanos con diabetes tipo 2 demostrou a superioridade de Sith / Met FDC sobre glimepirida en termos de baixar os niveis de HbA1c e GPN despois dun tratamento inicial de 30 semanas. Logrouse un nivel de HbA1c inferior a un 7,0% (53 mmol / mol) nunha proporción estadisticamente significativamente maior de pacientes do grupo Sit / Met FDC. Aínda que ambas as opcións de tratamento melloraron o control glicémico, a terapia con glimepirida provocou un aumento do peso corporal, mentres que con Sit / Met, observouse unha lixeira diminución con hipoglucemia menos pronunciada. En xeral, ambas as opcións de tratamento foron ben toleradas.
Para a terapia combinada con sitagliptina e metformina, demostrouse previamente eficacia en termos de lograr unha glicemia adecuada
control, boa tolerancia, efecto neutral sobre o peso corporal e baixo risco de hipoglucemia 25, 26, 28. No presente estudo obtivéronse datos adicionais sobre o uso de Sit / Met nunha combinación fixa en pacientes con diabetes tipo 2. De acordo coa práctica clínica actual en Corea, o glimepirido é un fármaco de primeira liña para a diabetes tipo 2. Os resultados do estudo actual suxiren que Sit / Met FDC ten unha vantaxe no nomeamento do tratamento inicial para pacientes con diabetes tipo 2 sobre monoterapia con glimepirida. Dadas as recomendacións actuais sobre o uso da terapia combinada nas etapas iniciais do tratamento en pacientes que non alcanzan os niveis diana de HbA1c, estes resultados son de gran importancia clínica para o manexo de pacientes diabéticos en Corea.
En estudos anteriores que avalían a eficacia e a seguridade da terapia combinada con sitagliptina e metformina na poboación coreana, confirmouse a eficacia e a boa tolerabilidade desta combinación. Un estudo recente comparou a eficacia do control glicémico da terapia combinada baseada en metformina coa sitagliptina, un derivado da sulfonilurea (glimepirida ou
con gliclazida de liberación modificada) ou pioglitazona en 116 pacientes coreanos non tratados previamente, demostrouse un control glicémico similar destas tres combinacións nunha ampla gama de niveis de HbA1c base. Noutro estudo, os pacientes coreanos que xa recibiron anteriormente terapia combinada (dobre ou triple combinación con metformina) recibiron unha mellora estadísticamente significativa no control glicémico durante o tratamento con sitagliptina a unha dose de 100 mg / día. No grupo que pasou de glimepirida a sitagliptina, a frecuencia de episodios de hipoglucemia diminuíu, polo que, en pacientes con hipoglucemia en xaxún recorrente, pode considerarse unha opción de cambio de tratamento similar. A pesar da eficacia demostrada da terapia combinada, non houbo estudos de Sit / Met nunha combinación fixa anteriormente en Corea, e o estudo presentado é o primeiro deste tipo.
Os efectos beneficiosos do uso de combinacións de dose fixa demostráronse previamente para outras combinacións de medicamentos de dous compoñentes para o tratamento da T2DM. Nun estudo multicéntrico aleatorio e aberto en grupos paralelos, 209 pacientes coreanos non lograron un control adecuado da T2DM, a pesar da monoterapia con metformina, glimepirida / metformina FDC usouse en doses baixas ou titulación cunha maior dose de metformina (nun prazo de 24 semanas), o glimepirido / metformina FDC superou a titulación doses de metformina en relación co control glicémico. Unha revisión empíricamente concluíu que a metformina / pioglitazona FDC é eficaz en pacientes con diabete resistente á insulina, que non lograron obxectivos de tratamento que cumpriron os estándares de atención recomendados durante a monoterapia. Nunha extensa análise retrospectiva dunha base de datos de 16.928 pacientes, descubriuse que coa rosiglitazona / metformina FDC, houbo unha mellora estadísticamente significativa na adherencia ao tratamento en comparación cos réximes de tratamento que incluían 2 fármacos. En xeral, o uso de FDC non só pode mellorar a adhesión á terapia, senón que tamén ten un perfil de tolerancia máis favorable, ser máis conveniente para os pacientes e ter un rendemento potencialmente maior. O uso de Sit / Met FDC no estudo presentado podería ser un dos factores que influíron na alta adhesión ao tratamento (
Case o 40% dos pacientes incluídos no estudo non recibiron previamente terapia hipoglucémica. En varios estudos anteriores 35-37 avaliouse a eficacia do tratamento inicial con Sit / Met FDC en pacientes anteriormente sen tratamento.A eficacia e seguridade da Sit / Met FDC en comparación coa pioglitazona foi estudada recentemente en dous estudos extensos que implicaron aproximadamente 500 pacientes, cada un dos cales confirmou unha mellora estadística significativa no control glicémico con Sit / Met 35, 37. Ademais,
Dos pacientes do grupo Sit / Met observouse unha diminución do peso corporal, mentres que nos pacientes do grupo pioglitazona aumentou o peso corporal. Noutro estudo randomizado dobre cego de 1250 pacientes previamente tratados, tomaron Sith / Met FDC ou metformina, segundo os seus resultados, a terapia inicial con Sith / Met FDC en comparación coa monoterapia con metformina foi máis beneficiosa en termos de control glicémico e rexistráronse indicadores similares de perda de peso. e unha menor incidencia de dor abdominal e diarrea. Dous ensaios clínicos antes deseñados en pacientes previamente sen tratamento con T2DM despois de 18 ou 24 semanas de terapia Sit / Met mostraron unha mellora máis pronunciada do control glicémico que no caso da monoterapia cun fármaco e / ou placebo. E este efecto positivo persistiu durante todo o período de tratamento, que durou ata 2 anos. Dado o período introdutorio de lavado requirido polo deseño do estudo, o efecto Sieve / Met FDC superior rexistrado no estudo actual pode reflectir parcialmente o feito de que moitos pacientes non recibiron tratamento antes.
No grupo glimepirida, observouse unha maior incidencia de hipoglucemia en comparación co grupo Sit / Met FDC (20,1 e 5,5%). Dado que en máis do 46% dos pacientes a dose máxima ou final do medicamento foi de 1 mg e só aproximadamente o 17% dos pacientes recibiron 6 mg como dose máxima ou total, estes resultados son bastante esperados. Aínda que o estudo actual permitiu a valoración dunha dose de glimepirida a criterio dos médicos, cómpre sinalar que debido á natureza dobre cego do estudo, os médicos non tiñan información sobre o tratamento específico. Así, este estudo reflicte a práctica real de aumentar de forma pasiva a dose de glimepirida. Un dato interesante é que no grupo glimepirida, ao aplicar doses relativamente baixas, observouse unha maior incidencia de hipoglucemia. Dadas as preocupacións asociadas á hipoglucemia, o uso dun réxime de terapia derivada con sulfonilurea pode demorar a consecución do nivel glicémico diana. Ademais, para a hipoglucemia provocada por derivados de sulfonil-urea, demostrouse unha dependencia da dose, así como unha correlación inversa co aumento do IMC, que pode ser unha explicación plausible para o aumento do peso corporal no grupo glimepirido no presente estudo.
No grupo Sit / Met FDC, observouse unha frecuencia relativamente baixa de interrupción da terapia en comparación co grupo glimepirida (17,7 e 25,5%). Aínda que a taxa de abandono escolar en ambos grupos parece alta, dada a duración do estudo (39 semanas), este valor está nun rango aceptable.
O estudo presentado comparou a eficacia e a seguridade da monoterapia (glimepirida) e da terapia de dous compoñentes (Sit / Met FDC). Algúns estudos anteriores tamén compararon a monoterapia e a terapia combinada 31, 36, 37, así
as dúbidas sobre a elección de medicamentos neste estudo non teñen fundamento. Ademais, o feito de que o glimepirido é actualmente un medicamento de primeira liña en pacientes con diabetes tipo 2 en Corea é un motivo adicional para o seu uso no grupo de comparación do presente estudo.
Aínda que se estudaron 628 pacientes para este estudo, só 292 persoas foron aleatorias a calquera grupo terapéutico.A maioría dos casos nos que os pacientes non foron incluídos nos resultados do cribado debéronse a valores moi baixos ou altos de HbA1c, baixa depuración de creatinina e outros parámetros que non cumpriron os criterios de selección. As características de moitos pacientes non cumpriron os criterios especificados durante o período introdutorio debido a baixos niveis de HbA1c, probablemente debido aos cambios no estilo de vida dos pacientes durante o período introdutorio de 6 semanas. Isto confirma os efectos beneficiosos dun estilo de vida saudable sobre a diabetes. Ademais, como se comentou anteriormente, a valoración con doses crecentes de glimepirida podería ser insuficiente, o que tamén podería afectar aos resultados do estudo.
En conclusión, cabe sinalar que o uso da terapia combinada nas primeiras etapas do tratamento cumpre as normas modernas de atención médica para a diabetes. O estudo actual é o primeiro en avaliar a seguridade e eficacia de Sit / Met nunha combinación fixa en comparación coa glimepirida en pacientes coreanos con T2DM como terapia inicial. Os resultados deste estudo suxiren que Sit / Met FDC pode ser unha boa opción de tratamento inicial para pacientes con diabetes tipo 2 en comparación coa monoterapia con glimepirida. Son necesarios máis estudos para avaliar os efectos a longo prazo da Sit / Met FDC e o efecto desta combinación nos puntos finais do sistema cardiovascular, así como a mortalidade entre pacientes con T2DM.
A combinación de Sit / Met como a terapia inicial proporcionou unha mellora máis pronunciada do control glicémico en xaxún e da glicosa plasmática en xaxún (GPN) 30 semanas despois do inicio en comparación coa glimepirida. Ademais, co uso de Sit / Met, observouse unha lixeira diminución do peso corporal e unha hipoglucemia menos pronunciada en comparación coa terapia con glimepirida.
■ O estudo actual avalía por primeira vez a seguridade e eficacia de Sit / Met de forma fixa
combinación con glimepirida en pacientes coreanos con diabetes mellitus tipo 2 (T2DM) como terapia inicial.
■ Resultados estadísticamente significativos do estudo: a combinación de Sit / Met como terapia inicial proporcionou unha mellora máis pronunciada dos niveis de HbA1c e GPN 30 semanas despois do inicio en comparación con glimepirida. A terapia con glimiririda provocou un aumento do peso corporal, mentres que o uso de Sit / Met mostrou unha lixeira diminución e unha hipoglicemia menos pronunciada.
■ Que ofrece este estudo: este estudo avalía por primeira vez a seguridade e eficacia da combinación Sit / Met en comparación coa monoterapia con glimepirida como tratamento inicial en pacientes coreanos con diabetes tipo 2.
Este estudo foi financiado por MSD International GmbH, unha filial de Merck & Co., Inc. (Kenilworth, Nova Xersei, EUA). O patrocinador participou no desenvolvemento de proxectos de investigación, recollida, revisión e análise de datos, así como na redacción do informe. Tejas Tirodkar (Cactus Communications, Mumbai, India) foi axudada para redactar o texto médico. Esta asistencia foi financiada por MSD Korea Ltd. Os autores agradecen a todos os investigadores que participaron no estudo: Young Sik Choi (Clínica evanxélica da Universidade de Kosin), Jong Ryeal Hahm (Clínica da Universidade Estatal de Gyeongsang), Mi Kyung Kim (Centro Médico Maryknoll), Parque Ja Young (Clínica Santa María Busan ), Sung Rae
Cho (Clínica Fatima en Changwon), Kyung Mook Choi (Clínica Guro na Universidade de Corea), Dae Jung Kim (Clínica da Universidade de Aju), Ki Young Lee (Centro Médico Gil da Universidade Gachon), Chong Hwa Kim (Clínica Ilsan, Servizo Estatal de Seguros de Saúde) ), Dong Jun Kim (Clínica Ilsan Peck, Universidade de Inje), Choon Hee Chung (Clínica cristiá separada para Wongju), Ji Oh Mok (Hospital Phocong da Universidade Sun-Chun-hyang) e Sung Hee Choi (Clínica Bundang, Universidade Estatal de Seúl).
SJL é empregada de MSD Korea Ltd, e todos os demais autores non teñen ningún conflito de interese.
Este estudo está rexistrado na base de datos Cli-nicalTrials.gov (ID: NCT00993187).
INFORMACIÓN DO AUTOR PRINCIPAL
Kim In Joo, Departamento de Endocrinoloxía e Metabolismo, Departamento de Terapia, Busan State University Hospital, Corea do Sur Correo electrónico: [email protected]
1. Asociación Americana da Diabetes. Diagnóstico e clasificación da diabetes mellitus. Coidado da diabetes. 2014, 37 (SuppL 1): S81-90.
2. Miller B.R., Nguyen H., Hu C.J., Lin C., Nguyen Q.T. Drogas e obxectivos novos e emerxentes para a diabetes tipo 2: Revisar a evidencia. Beneficios de drogas para a saúde. 2014, 7: 452-63.
3. Organización Mundial da Saúde. Ficha informativa sobre a diabetes. 2015. URL: http: // www.who.int/mediacentre/factsheets/fs312/en/ (data de acceso o 1 de febreiro de 2016).
4. Jeon J.Y., Ko S.H., Kwon H.S., et al. Prevalencia da diabetes e prediabetes segundo a glicosa plasmática en xaxún e HbA1c. Diabetes Metab J. 2013, 37: 349-57.
5. Cade W.T. Enfermidades microvasculares e macrovasculares relacionadas coa diabetes no ámbito da terapia física. Phys Ther. 2008, 88: 1322-35.
6. Stratton I.M. Adler A.I., Neil H.A.W., et al. Asociación de glicemia con complicacións macrovasculares e microvasculares de diabetes tipo 2 (UKPDS 35): estudo observacional prospectivo. BMJ 2000, 321: 405-12.
7. Acción para controlar o risco cardiovascular no grupo de estudo da diabetes, Gerstein H.C., Miller M.E., et al. Efectos da redución intensiva de glicosa na diabetes tipo 2. N Engl J Med. 2008, 358: 2545-59.
8. ADVANCE Collaborative Group, Patel A., MacMahon S. et al. Control intensivo da glicosa e resultados vasculares en pacientes con diabetes tipo 2. N Engl J Med. 2008, 358: 2560-72.
9. Duckworth W., Abraira C., Moritz T., et al. Control da glicosa e complicacións vasculares en veteranos con diabetes tipo 2. N Engl J Med. 2009, 360: 129-39.
10. Grupo de estudos prospectivos sobre a diabetes (UKPDS) do Reino Unido. Control intensivo da glicosa en sangue con sulfonilureas ou insulina en comparación co tratamento convencional e risco de complicacións en pacientes con diabetes tipo 2 (UKPDS 33). Lanceta 1998, 352: 837-53.
11. Holman R.R., Paul S.K., Bethel M.A., Matthews D.R., et al. Seguimento a 10 anos do control intensivo da glicosa na diabetes tipo 2. N Engl J Med. 2008, 359: 1577-89.
12. Riddle M.C., Yuen K.C. Obxectivos de reevaluación da insulinoterapia: perspectivas de grandes ensaios clínicos. Endocrinol Metab Clin North Am. 2012, 41: 41-56.
13. Algoritmo de xestión integral da diabetes da AACE. Foro de traballo do novo algoritmo completo de diabetes. Endocr Práctica. 2013, 19 (suplemento 2): 1-48.
14. Derosa G., Maffioli P. Consideracións do paciente e utilidade clínica dunha combinación de dose fixa de saxagliptina / metformina no tratamento da diabetes tipo 2. Diabetes Metab Syndr Obes. 2011, 4: 263-71.
15. American Diabetes Association. Enfoques do tratamento glicémico. Coidado da diabetes. 2015, 38 (suplemento 1): S41-88.
16. Defronzo R.A. Conferencia aburrante. Do triunvirateto o nefasta octeto: un novo paradigma para o tratamento da diabetes mellitus tipo 2. Diabetes. 2009, 58: 773-95.
17. Suk J.H., Lee C.W., Son S.P., et al. Estado actual da prescrición en pacientes diabéticos tipo 2 de hospitais xerais en Busan. Diabetes Metab J. 2014, 38: 230-9.
18. Davis S.N. O papel do glimepirido no manexo eficaz da diabetes tipo 2. J Complicacións da diabetes. 2004, 18: 367-76.
19. Korytkowski M.T. Tratamento con sulfonilurea da diabetes mellitus tipo 2: céntrase na glimepirida. Farmacoterapia 2004, 24: 606-20.
20. Currie C. J., Poole C. D., Evans M., Peters J. R., et al. Mortalidade e outros resultados importantes relacionados coa diabetes con insulina fronte a outros
terapias antihiperglucémicas na diabetes tipo 2. J Clin Endocrinol Metab. 2013, 98: 668-77.
21. Morgan C. L., Mukherjee J., Jenkins-Jones S., Holden S. E., et al. Asociación entre monoterapia de primeira liña con sulfonilurea fronte a metformina e risco de mortalidade por causas cardiovasculares: estudo retrospectivo e observacional. Diabetes Obes Metab. 2014, 16: 957-62.
22. Xénero S. ¿Deberían as sulfonilureas un complemento aceptable de primeira liña para a terapia con metformina en pacientes con diabetes tipo 2? Non, é hora de seguir adiante! Coidado da diabetes. 2015, 38: 170-5.
23. Plosker G.L. Sitagliptin: Unha revisión do seu uso en pacientes con diabetes mellitus tipo 2. Drogas 2014, 74: 223-42.
24. Herman G.A., Bergman A., Stevens C., et al. Efecto das doses orais de sitagliptin, un inhibidor da dipeptidil peptidase-4, sobre os niveis de incretina e glicosa plasmática despois dunha proba de tolerancia oral á glicosa en pacientes con diabetes tipo 2. J Clin Endocrinol Metab. 2006, 91: 4612-9.
25. Goldstein B.J., Feinglos M.N., Lunceford J.K. Johnson J., et al., Sitagliptin 036 Grupo de estudo. Efecto da terapia de combinación inicial con sitagliptin, un inhibidor de dipeptidil peptidase-4, e metformina no control glicémico en pacientes con diabetes tipo 2. Coidado da diabetes. 2007, 30: 1979-87.
26. Charbonnel B., Karasik A., Liu J., Wu M., et al., Sitagliptin Study 020 Group. A eficacia e a seguridade do inhibidor da dipeptidil peptidase-4 sitagliptin engadiuse á terapia con metformina en curso en pacientes con diabetes tipo 2 controlada inadecuadamente só con metformina. Coidado da diabetes. 2006, 29: 2638-43.
27. Miettinen O., Nurminen M. Análise comparativa de dúas taxas. Med Med. 1985, 4: 213-26.
28. Chwieduk C.M. Combinación de dose fixa de sitagliptin / metformina: en pacientes con diabetes mellitus tipo 2. Drogas 2011, 71: 349-61.
29. Lee Y.K., Song S.O., Kim K.J., et al. Eficacia glicémica de terapias de dobre combinación baseadas en metformina con sulfonilurea, pioglitazona ou inhibidor de DPP4 en pacientes diabéticos tipo coreano inxenuos con drogas. Diabetes Metab J. 2013, 37: 465-74.
30. Chung H.S., Lee M.K. Eficacia da sitagliptina cando se engade á terapia en curso en suxeitos coreanos con diabetes mellitus tipo 2. Diabetes Metab J. 2011, 35: 411-7.
31. Kim H.S., Kim D.M., Cha B.S., et al. Eficacia da combinación de glimepirida / metformina con dose fixa vs uptitración de metformina en pacientes diabéticos tipo 2 controlados inadecuadamente en monoterapia de dose baixa con metformina: un estudo paralelo, aleatorio e aberto, de grupo paralelo, en multicéntrico en Corea. J Diabetes Investigación. 2014, 5: 701-8.
32. Derosa G., Salvadeo S.A. Combinación de dose fixa de pioglitazona e metformina en diabetes mellitus tipo 2: unha revisión baseada na evidencia do seu lugar en terapia. Núcleo Evid. 2008, 2: 189-98.
33. Vanderpoel D.R., Hussein M.A., Watson-Heidari T., Perry A. A adhesión a unha combinación de dose fixa de maleato de rosiglitazona / clorhidrato de metformina en suxeitos con diabetes mellitus tipo 2: unha análise de base de datos retrospectiva. Clin Ther. 2004, 26: 2066-75.
34. Bain S.C. Tratamento da diabetes mellitus tipo 2 con axentes administrados por vía oral: avances na terapia combinada. Endocr Práctica. 2009, 15: 750-62.
35. Perez-Monteverde A., Seck T., Xu L., et al. Eficacia e seguridade da sitagliptina e da combinación de dose fixa de sitagliptin e metformina vs. pioglitazona en pacientes inxenuos con drogas tipo diabete. Pr. Clinica Int J. 2011, 65: 930-8.
Terapia de diabetes mellitus tipo 2
| í Amaryl '1 * 1 I Amaryl' j Amaryl ■ Amaryl '
II 1 tmr-lm ■ "I Ts 1 IM HTM", p. "Anos, n!
I 1 iHNOF '^ yifiÖ ^ O
Máis de 15 anos de uso en Rusia1
Mecanismo de acción dobre: estimulación da secreción de insulina e diminución da resistencia á insulina2
Reducir a glicemia en combinación cun baixo risco de hipoglucemia con glimepirida na práctica clínica real en Rusia 3-5
Administración conveniente: 1 comprimido 1 vez ao día2
Variedade de dosificación para unha valoración conveniente2
Forma económica de liberación: 90 comprimidos nun paquete6 *
Breves instrucións para a práctica médica
D da droga AMARIL®
Nome comercial da preparación: Amaril®. Nome non propietario internacional: glimepirido. Forma e composición dosificación: comprimidos. Amaryl® 1.2.3.4 mg: 1 comprimido contén 1.2.3.4 mg de glimepirida, respectivamente. Grupo farmacoterapéutico: axente hipoglucémico para a administración oral do grupo sulfonilurea de xeración III. Indicacións de uso: diabetes mellitus tipo 2 (en monoterapia ou como parte da terapia combinada con metformina ou insulina). Dose e administración: Os comprimidos Amaril® tómanse enteiros sen masticar, bebendo moito líquido ™ (aproximadamente 0,5 cuncas). A dose inicial é de 1 mg de glimepirido 1 vez ao día. Recoméndase que o aumento da dose se realice baixo control regular da concentración de glicosa no sangue e de acordo co seguinte paso de aumento da dose: 1 mg-2 mg-Zmg-4 mg-6 mg-8 mg con intervalos de 1-2 semanas. Tómase antes dun almorzo completo ou comida principal. Contraindicacións: diabetes mellitus tipo 1, cetoacidosis diabética, precoma e coma diabéticos, hipersensibilidade ao glimepirido ou a calquera dos compoñentes auxiliares do fármaco, a outras sulfonilureas ou sulfonamidas, embarazo e lactación, deficiencia hepática grave, insuficiencia renal grave, nenos idade (falta de datos clínicos sobre o uso), raras enfermidades hereditarias (intolerancia a galactosa, deficiencia de lactasa ou malabsor de glicosa-galactosa btsiya). Con precaución: nas primeiras semanas de tratamento, ante factores de risco para o desenvolvemento da hipoglucemia (ver as instrucións completas para o uso médico do medicamento), para enfermidades intercurrentes, cambios no estilo de vida dos pacientes, deficiencia de glicosa-6-fosfato deshidroxenase e malabsorción gastrointestinal (intestinal obstrución, paresis intestinal).Instrucións especiais: nas primeiras semanas de tratamento, o risco de hipoglucemia pode aumentar - é necesario un coidadoso control da glicemia. En caso de condicións estresantes clínicas especiais (trauma, intervencións cirúrxicas, infeccións con febre febril), pode ser necesaria unha transferencia temporal á insulinoterapia. Interacción con outros fármacos: o glimepirido metabolízase polo citocromo P4502C9 (CYP2C9), que se debe ter en conta cando se usa simultaneamente con indutores (por exemplo rifampicina) ou inhibidores (por exemplo, fluconazol) CYP2C9. Para obter interacción con outros fármacos, consulte as instrucións completas para o uso médico do medicamento. Efecto secundario: hipoglucemia. En casos raros: náuseas, vómitos, molestias no epigastrio, diarrea, un aumento transitorio da actividade de encimas hepáticas e / ou colestase, hepatite, deficiencia visual transitoria debido a un cambio na concentración de glicosa en sangue, trombocitopenia, leucopenia, anemia hemolítica, eritrocitopenia, granulocitopenia , agranulocitosis, panitopenia, prurito, urticaria, erupción cutánea, vasculite alérxica, fotosensibilidade. Sobredose: unha sobredose aguda, así como un tratamento prolongado con doses demasiado altas de glimepirida poden levar ao desenvolvemento de hipoglucemia grave, que pode poñer en risco a vida. En canto se detecte unha sobredose, deberá informar inmediatamente ao seu médico. A hipoglicemia case sempre pode ser parada rapidamente pola inxestión inmediata de hidratos de carbono. Código ATX: A10BB12. Data de caducidade: 3 anos. Antes da cita, debes ler as instrucións de uso médico da droga
1. Certificado de rexistro do medicamento Amaril® para uso médico П П N015530 / 01. 2. Instrucións para o uso médico de Amaril®, por, número P N015530 / 01-131216.3. Ametov A.C. con eoavt. Posibilidades de usar glimepirida para iniciar a terapia para reducir o azucre. Resultados dun estudo observacional Amaril-MONO. Diabetes mellitus, 2013: nº 3. 4. Glinkina I.V. et al., Eficacia e seguridade da combinación libre de glimepirida e metformina en pacientes con diabetes mellitus tipo 2 na práctica clínica real: un programa de observación // Farmacoterapia eficaz. Endocrinoloxía 2/2012: 16-20,5. Zaitseva N.V. et al., <Terapia combinada con glimepirida e metformina en pacientes con diabetes tipo 2. Os resultados do estudo observacional ruso // Farmateka. - 2014. - Nº 16.6. www.apteka.ru, último acceso ao sitio - 06/07/2017. "O custo dun comprimido nun paquete nº 90 é un 25% menor que o dun comprimido nun paquete nº 30 para dosificación comparable. # A aproximación clásica ao tratamento da diabetes mellitus tipo 2: estimulación da secreción de insulina e> redución da resistencia á insulina. A información está destinada aos profesionais sanitarios.
Representación do cadáver de Sanofi-aventis JSC (Francia) 125009, Moscova, ul. Tverskaya, d. 22. Teléfono: (495) 721-14-00, fax: (495) 721-14-11, www.sanofi.ru.SARU.GLI.17.06.0953
36. Reasner C., Olansky L., Seck T. L., et al. O efecto da terapia inicial coa combinación de dose fixa de sitagliptina e metformina en comparación coa monoterapia con metformina en pacientes con diabetes mellitus tipo 2. Diabetes Obes Metab. 2011, 13: 644-52.
37. Wainstein J., Katz L., Engel S.S., et al. A terapia inicial coa combinación de dose fixa de sitagliptina e metformina produce unha mellora do control glicémico en comparación coa pioglitazona
monoterapia en pacientes con diabetes tipo 2. Diabetes Obes Metab. 2012, 14: 409-18.
Farmacoloxía
Metformin + sitagliptin é unha combinación de dúas substancias activas (DV) cun mecanismo de acción complementario (complementario) - sitagliptin, un inhibidor de DPP-4, e metformina, un representante da clase biguanida. Utilízase para mellorar o control glicémico en pacientes con diabetes tipo 2.
Cando se administra por vía oral, sitagliptin é un inhibidor activo de DPP-4 activamente selectivo, destinado ao tratamento da diabetes mellitus tipo 2. Os efectos farmacolóxicos da clase de fármacos - Os inhibidores de DPP-4 están mediados pola activación de incretinas. Ao inhibir a DPP-4, a sitagliptina aumenta a concentración de dúas hormonas activas coñecidas da familia de incretinas: GLP-1 e HIP.As incretinas forman parte do sistema fisiolóxico interno para regular a homeostase da glicosa. A concentracións de glicosa no sangue normal ou elevadas, GLP-1 e GUI aumentan a síntese e secreción de insulina polas células beta pancreáticas. O GLP-1 tamén suprime a secreción de glucagón polas células alfa pancreáticas, reducindo así a síntese de glicosa no fígado. Este mecanismo de acción difire do mecanismo de acción dos derivados da sulfonilurea, que estimulan a liberación de insulina incluso a baixas concentracións de glucosa en sangue, que está cheo do desenvolvemento da hipoglucemia sulfonilinducada non só en pacientes con diabetes mellitus tipo 2, senón tamén en individuos sans. Sendo un inhibidor altamente selectivo e eficaz do encima DPP-4, a sitagliptina en concentracións terapéuticas non inhibe a actividade dos encimas relacionados DPP-8 ou DPP-9. A sitagliptina difire na estrutura química e na acción farmacolóxica dos análogos de GLP-1, insulina, derivados da sulfonilurea ou meglitinidas, biguanidas, agonistas do receptor gamma activados polo proliferador de peróxisis (PPARγ), inhibidores da alfa-glucosidasa e análogos da amilina.
A metformina é un medicamento hipoglucémico que aumenta a tolerancia á glicosa en pacientes con diabetes tipo 2, reducindo a concentración de glucosa en sangue basal e posprandial. Os seus mecanismos farmacolóxicos de acción difiren dos mecanismos de acción dos axentes hipoglucemicos orais doutras clases.
A metformina reduce a síntese de glicosa no fígado, a absorción de glicosa nos intestinos e aumenta a sensibilidade á insulina aumentando a captación periférica e a utilización de glicosa. A diferenza dos derivados da sulfonilurea, a metformina non causa hipoglucemia en pacientes con diabetes mellitus tipo 2 ou en persoas saudables (con excepción dalgunhas circunstancias, consulte "Restricións ao uso", Metformina) e non causa hiperinsulinemia. Durante o tratamento con metformina, a secreción de insulina non cambia, mentres que a concentración de insulina nun estómago baleiro e o valor diario da concentración plasmática de insulina poden diminuír.
A administración oral dunha única dose de sitagliptina a pacientes con diabetes mellitus tipo 2 leva a unha supresión da actividade do encima DPP-4 durante 24 horas, que se acompaña dun aumento de dúas a tres veces na concentración de GLP-1 e HIP activos circulantes, un aumento da concentración plasmática de insulina e péptido C, unha diminución da concentración de glucagón e C-péptido. concentración de glucosa no plasma de xexún, así como unha diminución da amplitude das flutuacións glicémicas tras a carga de glicosa ou alimentos.
A administración de sitagliptin nunha dose diaria de 100 mg durante 4-6 meses mellorou significativamente a función das células beta pancreáticas en pacientes con diabetes mellitus tipo 2, como o demostran os correspondentes cambios en marcadores como HOMA-β (valoración da homeostase no modelo β), a relación proinsulina / insulina, avaliación da reacción das células beta pancreáticas segundo o panel de probas repetidas para a tolerancia alimentaria. Segundo estudos clínicos das fases II e III, a eficacia do control glicémico da sitagliptina no réxime de 50 mg dúas veces ao día foi comparable coa eficacia do réxime de 100 mg unha vez ao día.
Nun estudo aleatorio, controlado con placebo, dobre cego, dobre simulado de 4 períodos cruzados, voluntarios sans estudaron os efectos da sitagliptina en combinación con metformina, ou só sitagliptina, ou só metformina, ou placebo en cambios nas concentracións plasmáticas do GLP-1 activo e total e da glicosa despois da administración comida. Os valores medios ponderados da concentración de GLP-1 activo 4 horas despois da comida aumentaron aproximadamente 2 veces despois de tomar só sitagliptin ou só metformina en comparación co placebo. A administración combinada de sitagliptina e metformina asegurou un resumo do efecto cun aumento de 4 veces na concentración de GLP-1 activo en comparación coa dinámica do grupo placebo.
A recepción de sitagliptina en solitario foi acompañada dun aumento da concentración de GLP-1 só activo debido á inhibición do encima DPP-4, mentres que a administración de metformina só foi acompañada dun aumento simétrico na concentración do GLP-1 total e activo. Os datos obtidos reflectiron varios mecanismos que subxacen ao aumento da concentración de GLP-1 activo despois de tomar estes dous fármacos. Os resultados do estudo tamén demostraron que era a sitagliptina, e non a metformina, que proporcionaba un aumento na concentración de GLP-1 activo.
En estudos realizados en voluntarios sans, tomar sitagliptina non estivo acompañado dunha diminución da concentración de glicosa e non provocou hipoglucemia, o que confirma a natureza dependente da glicosa do efecto insulinotrópico e a supresión da síntese de glucagón.
Nun estudo aleatorio, controlado con placebo, en pacientes con hipertensión arterial, o uso combinado de fármacos antihipertensivos (un ou máis da lista: inhibidores da ACE, ARA II, BKK, beta-bloqueantes, diuréticos) con sitagliptina foi xeralmente ben tolerado polos pacientes. Nesta categoría de pacientes, a sitagliptina mostrou un lixeiro efecto hipotensivo: nunha dose diaria de 100 mg, sitagliptin reduciu o valor medio diario de ambulatorio de SBP en 2 mm Hg. en comparación co grupo placebo. En pacientes con presión arterial normal, non se observou efecto hipotensivo.
Efecto na electrofisioloxía cardíaca
Nun estudo aleatorio, cruzado controlado con placebo en voluntarios sans, utilizouse sitagliptin unha vez a unha dose de 100 ou 800 mg (o 8 veces máis da dose recomendada) ou o placebo. Despois de tomar a dose terapéutica recomendada de calquera efecto do fármaco na duración do intervalo QT, como no momento do seu plasma Cmáx , e noutros puntos de verificación ao longo do estudo, non se observaron. Tras a inxestión de 800 mg, o aumento máximo do cambio medio axustado co placebo na duración do intervalo QT en comparación co valor inicial 3 horas despois de tomar o medicamento foi de 8 ms. Un aumento similar foi clínicamente insignificante. Despois de tomar 800 mg, o valor do plasma Cmáx A sitagliptin foi aproximadamente 11 veces maior que o valor correspondente tras tomar unha dose terapéutica de 100 mg.
Os resultados dun estudo de bioequivalencia en voluntarios sans demostraron que as tabletas combinadas (metformina + sitagliptin) 500/50 mg e 1000/50 mg son bioequivalentes á administración por separado das doses apropiadas de sitagliptina e metformina.
Dada a bioequivalencia comprobada dos comprimidos con doses máis baixas e altas de metformina, os comprimidos cunha dose intermedia de metformina (metformina + sitagliptin) tamén obtiveron bioequivalencia a 850/50 mg, sempre que se combinase a combinación de dose fixa no comprimido.
Sitagliptin. A biodisponibilidade absoluta de sitagliptin é aproximadamente do 87%. Tomar sitagliptina ao mesmo tempo que unha comida graxa non afecta a farmacocinética da combinación.
Metformina. A biodisponibilidade absoluta de metformina cando se toma sobre o estómago baleiro a unha dose de 500 mg é do 50-60%. Os resultados dos estudos dunha única dose de metformina en doses de 500 a 1500 mg e de 850 a 2550 mg indican unha violación da proporcionalidade á dose coa dose crecente, que é máis probable debido a unha absorción reducida que a unha excreción acelerada. O uso concomitante con alimentos reduce a taxa e cantidade de metformina absorbida, como evidencia unha diminución do plasma Cmáx ao redor do 40%, unha diminución da ASC de aproximadamente o 25% e un retraso de 35 minutos en alcanzar a Cmáx despois dunha única dose de metformina nunha dose de 850 mg simultaneamente cos alimentos en comparación cos valores dos parámetros correspondentes despois de tomar unha dose similar do medicamento no estómago baleiro. Non se estableceu a importancia clínica de baixar os parámetros farmacocinéticos.
Sitagliptin. Medio Vss despois dunha única inxección iv, 100 mg de sitagliptina en voluntarios sans son aproximadamente 198 l. A fracción de sitagliptina ligada reversiblemente ás proteínas do plasma é relativamente pequena (38%).
Metformina. Vd metformina despois dunha única dose oral de 850 mg de media (654 ± 358) l. A metformina só en moi pequena relación únese ás proteínas do plasma. A metformina distribúese parcial e temporalmente nos glóbulos vermellos. Cando se usa metformina en doses e modos recomendados, plasma Css (normalmente Cmáx non superaron os 5 μg / ml incluso despois de tomar as doses máximas.
Sitagliptin. Aproximadamente o 79% da sitagliptina é excretada sen cambios polos riles, a transformación metabólica é mínima.
Despois de que se administrou oralmente sitagliptina marcada con 14 C, aproximadamente o 16% da radioactividade administrada foi excretada como metabolitos de sitagliptin. Identificáronse as concentracións de rastro de 6 metabolitos de sitagliptin que non contribuíron á actividade inhibidora plasmática de DPP-4 de sitagliptin. Nos estudos in vitro As isoenzimas do sistema citocromo CYP3A4 e CYP2C8 identifícanse como as principais implicadas no metabolismo limitado da sitagliptina.
Metformina. Despois dunha única administración de iv a voluntarios sans de metformina, case toda a dose administrada foi excretada sen cambios polos riles. Non se producen cambios metabólicos no fígado e excreción coa bilis.
Sitagliptin. Despois de que a sitagliptina marcada con 14 C foi inxerida por voluntarios sans, case toda a radioactividade introducida eliminouse do corpo dentro dunha semana, incluída O 13% polos intestinos e o 87% polos riles. T media1/2 sitagliptin con administración oral de 100 mg é de aproximadamente 12,4 horas, a eliminación renal é de aproximadamente 350 ml / min.
A excreción de sitagliptina realízase principalmente por excreción renal polo mecanismo de secreción tubular activa. A sitagliptina é un substrato do transportador de anións humanos orgánicos do terceiro tipo (hОAT-3), que está implicado na eliminación de sitagliptina polos riles. Non se estableceu a importancia clínica da implicación de hOAT-3 no transporte de sitagliptin. P-gp pode estar implicado na eliminación renal de sitagliptin (como substrato), con todo, o inhibidor da P-gp ciclosporina non reduce a eliminación renal de sitagliptin.
Metformina. A eliminación renal da metformina supera a clearance da creatinina en 3,5 veces, o que indica a secreción renal activa como principal vía de excreción. Despois de tomar metformina, preto do 90% do medicamento absorbido é excretado polos riles durante as primeiras 24 horas nun plasma T1/2 aproximadamente 6,2 horas, no sangue este valor esténdese a 17,6 horas, o que indica a posible participación de glóbulos vermellos como compartimento de distribución potencial.
Farmacocinética en grupos de pacientes individuais
Pacientes con diabetes tipo 2
Sitagliptin. A farmacocinética de sitagliptin en pacientes con diabetes tipo 2 é similar á farmacocinética en individuos sans.
Metformina. Con función renal conservada, os parámetros farmacocinéticos despois dunha administración repetida de metformina en pacientes con diabetes mellitus tipo 2 e individuos sans son os mesmos, o fármaco non se acumula ao tomar doses terapéuticas.
A combinación de metformina + sitagliptin non se debe prescribir a pacientes con insuficiencia renal (ver "Contraindicacións").
Sitagliptin. En pacientes con insuficiencia renal moderada, notouse un aumento de dúas veces aproximadamente na AUC plasmática de sitagliptina, e en pacientes con estadios severos e terminais (na hemodiálise), o aumento da ASC foi de 4 veces en comparación cos valores de control en individuos sans.
Metformina. En pacientes con función renal reducida (eliminación da creatinina) T1/2 alonga, e a eliminación renal diminúe en proporción a unha diminución da eliminación da creatinina.
Sitagliptin. En pacientes con insuficiencia hepática moderada (7-9 puntos na escala Child-Pugh), os valores medios de AUC e Cmáx sitagliptin despois dunha única dose de 100 mg aumenta aproximadamente 21 e 13%, respectivamente, en comparación con individuos sans. Esta diferenza non é clínicamente significativa. Non hai datos clínicos sobre o uso de sitagliptina en pacientes con insuficiencia hepática grave (máis de 9 puntos na escala Child-Pugh). Non obstante, en función da vía de excreción predominantemente renal, non se prevén cambios significativos na farmacocinética de sitagliptina en pacientes con insuficiencia hepática grave.
Metformina. Non se realizaron estudos sobre os parámetros farmacocinéticos da metformina en pacientes con insuficiencia hepática.
Sitagliptin. Segundo a análise dos datos farmacocinéticos dos ensaios clínicos de fase I e II, o xénero non tivo un efecto clínicamente significativo nos parámetros farmacocinéticos de sitagliptin.
Metformina. Os parámetros farmacocinéticos da metformina non diferían significativamente en individuos sans e en pacientes con diabetes mellitus tipo 2 en función do xénero. Segundo ensaios clínicos controlados, os efectos hipoglucémicos da metformina en homes e mulleres foron similares.
Sitagliptin. Segundo a análise farmacocinética da poboación de ensaios clínicos de fase I e II, a idade dos pacientes non tivo un efecto clínicamente significativo nos parámetros farmacocinéticos de sitagliptin. A concentración de sitagliptin en pacientes anciáns (65-80 anos) foi aproximadamente un 19% maior que en pacientes novos.
Metformina. Os datos limitados procedentes de estudos farmacocinéticos controlados de metformina en individuos anciáns saudables suxiren que se reduce a súa eliminación de plasma total, T1/2 alongamentos e o valor de Cmáx aumenta en comparación cos novos individuos sans. Estes datos significan que os cambios relacionados coa idade na farmacocinética da metformina débense a unha diminución da función excretora renal.
O tratamento coa combinación de metformina + sitagliptin non está indicado para anciáns á idade de ≥80 anos, coa excepción de persoas cuxa depuración de creatinina indica que a función renal non se reduce (ver "Precaucións", Metformina).
Non se realizaron estudos sobre a combinación de metformina + sitagliptin en nenos.
Sitagliptin. Segundo a análise de datos farmacocinéticos procedentes de ensaios clínicos de fase I e II, a raza non tivo un efecto clínicamente significativo nos parámetros farmacocinéticos de sitagliptin, incluído representantes das razas caucásicas e mongoloides, representantes de países latinoamericanos e doutros grupos étnicos e raciais.
Metformina. Non se realizaron estudos sobre o efecto potencial da raza sobre os parámetros farmacocinéticos da metformina. Segundo estudos controlados de metformina en pacientes con diabetes mellitus tipo 2, o efecto hipoglucémico foi comparable en representantes das razas do Cáucaso, das razas Negroid e dos países latinoamericanos.
Sitagliptin. Segundo a análise complexa e poboacional de parámetros farmacocinéticos de ensaios clínicos de fase I e II, o IMC non tivo un efecto clínicamente significativo sobre os parámetros farmacocinéticos de sitagliptin.
O uso de substancias Metformin + Sitagliptin
A combinación de metformina + sitagliptin está indicada como terapia inicial para pacientes con diabetes mellitus tipo 2 para mellorar o control glicémico, se a dieta e o réxime de exercicios non permiten un control adecuado.
A combinación de metformina + sitagliptina indícase como complemento á dieta e réxime de exercicios para mellorar o control glicémico en pacientes con diabetes tipo 2 que non lograron un control adecuado no fondo da monoterapia con metformina ou sitagliptina, ou despois dun tratamento combinado sen éxito con dúas DV.
A combinación de metformina + sitagliptina está indicada para pacientes con diabetes mellitus tipo 2 para mellorar o control glicémico en combinación con derivados de sulfonilurea (triple combinación: derivado de metformina + sitagliptin + sulfonilurea) cando a dieta e o réxime de exercicios se combinan con dous destes tres fármacos: metformina, sitagliptina ou os derivados da sulfonilurea non conducen a un control glicémico adecuado.
A combinación de metformina + sitagliptin está indicada para pacientes con diabetes mellitus tipo 2 para mellorar o control glicémico en combinación con tiazolidinediones (agonistas do receptor PPARγ activados polo proliferador peroxisoma), cando a dieta e o réxime de exercicios son combinados con dous destes tres fármacos: metformina, sitagliptina ou tiazolidina non levar a un control glicémico adecuado.
A combinación de metformina + sitagliptin está indicada para pacientes con diabetes mellitus tipo 2 para mellorar o control glicémico en combinación con insulina, cando a dieta e o réxime de exercicios en combinación con insulina non conducen a un control glicémico adecuado.
Restricións de aplicación
Uso na terceira idade
A combinación de metformina + sitagliptina. Dado que a principal vía de eliminación de sitagliptina e metformina son os riles e a función excretora dos riles diminúe coa idade, as medidas de precaución ao prescribir a combinación de metformina + sitagliptina aumentan en proporción á idade. Os pacientes anciáns experimentan unha selección coidadosa da dose e un control regular da función renal (ver "Precaucións", Monitorización da función renal).
Sitagliptin. Segundo estudos clínicos, a eficacia e seguridade da sitagliptina en pacientes anciáns (> 65 anos) foi comparable á eficacia e seguridade en pacientes novos (PM, non recomendado para o seu uso durante o embarazo.
Non se realizaron estudos experimentais sobre a combinación de metformina + sitagliptin para avaliar o efecto sobre a función reprodutiva.
Sitagliptin. A sitagliptin non mostrou teratoxenicidade durante a organoxénese cando se administrou por vía oral a ratas a doses diarias de ata 250 mg / kg ou a coellos a doses de ata 125 mg / kg (o que supera a exposición ao plasma en humanos entre 32 e 22 veces, respectivamente, despois de tomar a dose terapéutica diaria recomendada de 100 mg) . Notouse un lixeiro aumento da frecuencia de malformación das costelas na descendencia (ausencia, hipoplasia, curvatura) cando se administra por vía oral en doses diarias de 1000 mg / kg (o que supera a exposición en humanos unhas 100 veces despois de tomar a dose diaria recomendada de 100 mg). Houbo unha lixeira diminución do peso corporal na descendencia de ratas de ambos sexos durante a lactación e unha diminución da taxa de aumento de peso ao finalizar a lactación en homes con administración oral de 1000 mg / kg de dose diaria de sitagliptina en mulleres embarazadas. Non obstante, os estudos reprodutivos experimentais non sempre se correlacionan directamente cos efectos da sitagliptina sobre a función reprodutora humana.
Metformina. A metformina non demostrou teratoxenicidade cando se administrou por vía oral en ratas en doses diarias de ata 600 mg / kg. Isto supera en 2 e 6 veces a exposición ao plasma dos humanos (en ratas e coellos, respectivamente) despois de tomar a dose terapéutica diaria recomendada máxima de 2000 mg. Os valores da concentración plasmática no feto indican transferencia parcial da placentaria.
Non se realizaron estudos experimentais para determinar a secreción dos compoñentes da combinación de metformina + sitagliptin no leite materno. Segundo estudos sobre os compoñentes individuais, tanto a sitagliptina como a metformina son secretadas no leite materno das ratas. Non hai datos sobre a secreción de sitagliptina no leite materno humano. Polo tanto, a combinación de metformina + sitagliptin non debe ser prescrita durante a lactación.
Efectos secundarios de Metformin + Sitagliptin
En estudos controlados con placebo, o tratamento combinado con sitagliptina e metformina foi xeralmente ben tolerado por pacientes con diabetes mellitus tipo 2. A incidencia de efectos secundarios con tratamento combinado con sitagliptina e metformina foi comparable á frecuencia cando se tomou metformina en combinación con placebo.
Tratamento combinado con sitagliptina e metformina
Nun estudo factorial controlado con placebo durante 24 semanas de terapia de combinación inicial con sitagliptina e metformina (sitagliptin 50 mg + metformina 500 ou 1000 mg 2 veces ao día) no grupo de terapia combinada en comparación con grupos de monoterapia de metformina (500 ou 1000 mg 2 veces ao día) , sitagliptin (100 mg unha vez ao día) ou placebo, observáronse as seguintes reaccións adversas asociadas ao fármaco, observadas cunha frecuencia de ≥1% no grupo de tratamento combinado e máis frecuentemente que no grupo placebo: diarrea (sitagliptina + metformina - 3,5%, metformina - 3,3%, sitagliptina - 0%, placebo - 1,1%), náuseas (1,6, 2,5, 0 e 0,6%), dispepsia (1,3, 1,1, 0 e 0%), flatulencias (1,3, 0,5, 0 e 0%), vómitos (1,1, 0,3, 0 e 0%), cefalea (1,3, 1,1, 0,6 e 0%) e hipoglucemia (1,1, 0,5, 0,6 e 0%).
Engadindo sitagliptin á terapia con metformina actual
Nun estudo controlado con placebo durante 24 semanas, cando se engadiu sitagliptina a unha dose de 100 mg / día ao tratamento actual con metformina, a única reacción adversa asociada á coadministración foi observada cunha frecuencia de ≥1% no grupo de tratamento con sitagliptina e máis a miúdo que no grupo placebo, houbo náuseas (sitagliptin + metformin - 1,1%, placebo + metformin - 0,4%).
Hipoglicemia e reaccións adversas do tracto gastrointestinal
En estudos controlados con placebo de tratamento combinado con sitagliptina e metformina, a incidencia de hipoglucemia (independentemente da relación causal) nos grupos de terapia combinada foi comparable á frecuencia nos grupos de tratamento de metformina combinada con placebo (1,3-1,6 e 2,1% respectivamente). A frecuencia das reaccións adversas controladas do tracto gastrointestinal (independentemente da relación causa-efecto) nos grupos de tratamento combinados de sitagliptin e metformina foi comparable á frecuencia nos grupos de monoterapia de metformina: diarrea (sitagliptina + metformina - 7,5%, metformina - 7,7%), náuseas (4,8, 5,5%), vómitos (2,1, 0,5%), dor abdominal (3, 3,8%). En todos os estudos, rexistráronse reaccións adversas en forma de hipoglucemia con base en todos os informes de síntomas clínicos de hipoglucemia, non foi necesaria unha medición adicional da concentración de glicosa no sangue.
Tratamento combinado con sitagliptina, metformina e un derivado da sulfonilurea
Nun estudo de 24 semanas controlado con placebo usando sitagliptin a unha dose de 100 mg / día fronte ao fondo do tratamento combinado actual con glimepirida a unha dose de ≥4 mg / día e metformina a unha dose de ≥1500 mg / día, observáronse as seguintes reaccións adversas cunha frecuencia de ≥1% no grupo de tratamento con sitagliptina e máis a miúdo que no grupo placebo: hipoglucemia (sitagliptin - 13,8%, placebo - 0,9%), estreñimiento (1,7 e 0%).
Tratamento combinado con sitagliptin, metformina e agonista de PPARγ
Segundo un estudo controlado con placebo empregando sitagliptin a unha dose de 100 mg / día fronte aos antecedentes do tratamento combinado actual con rosiglitazona e metformina, na 18ª semana do tratamento observáronse as seguintes reaccións adversas asociadas á toma, observada cunha frecuencia de ≥1% no grupo de tratamento con sitagliptina e máis a miúdo. que no grupo placebo: cefaléia (sitagliptina - 2,4%, placebo - 0%), diarrea (1,8, 1,1%), náuseas (1,2, 1,1%), hipoglucemia (1 , 2, 0%), vómitos (1,2, 0%). Na 54ª semana do tratamento combinado, observáronse as seguintes reaccións adversas asociadas á administración, observadas cunha frecuencia de ≥1% no grupo de tratamento con sitagliptina e máis frecuentemente que no grupo placebo: cefalea (sitagliptin - 2,4%, placebo - 0%) , hipoglucemia (2,4, 0%), infeccións das vías respiratorias superiores (1,8, 0%), náuseas (1,2, 1,1%), tose (1,2, 0%), infeccións fúngicas da pel ( 1,2, 0%), edema periférico (1,2, 0%), vómitos (1,2, 0%).
Tratamento combinado con sitagliptina, metformina e insulina
Nun estudo de 24 semanas controlado con placebo utilizando sitagliptin a unha dose de 100 mg / día fronte aos antecedentes do tratamento combinado actual con metformina a unha dose de ≥1500 mg / día e unha dose constante de insulina, a única reacción adversa asociada á toma do medicamento e observada cunha frecuencia de ≥1%. o grupo de tratamento con sitagliptina e máis a miúdo que o grupo con placebo tiña hipoglucemia (sitagliptin - 10,9%, placebo - 5,2%). Noutro estudo de 24 semanas no que os pacientes recibiron sitagliptina como terapia adxuntiva con insulinoterapia (con ou sen metformina), a única reacción adversa observada cunha frecuencia de ≥1% no grupo de tratamento con sitagliptina e metformina, e máis a miúdo que no grupo placebo e a metformina foi vómito (sitagliptina e metformina - 1,1%, placebo e metformina - 0,4%).
Nunha análise xeneralizada de 19 ensaios clínicos aleatorios de dobre cego, do uso de sitagliptin (a unha dose de 100 mg / día) ou dun medicamento control (activo ou placebo), a incidencia de pancreatite aguda foi de 0,1 casos por cada 100 pacientes anos de tratamento en cada grupo (ver "Medidas precaucións ").
Non se observaron desviacións clínicamente significativas nos signos vitais ou ECG (incluída a duración do intervalo QTc) con terapia combinada con sitagliptin e metformina.
Reaccións adversas debidas ao uso de sitagliptina
Os pacientes non experimentaron reaccións adversas por mor da sitagliptina, cuxa frecuencia foi ≥1%.
Reaccións adversas debidas ao uso de metformina
As reaccións adversas observadas no grupo metformina en> 5% dos pacientes e máis frecuentemente que no grupo placebo son diarrea, náuseas / vómitos, flatulencia, astenia, dispepsia, molestias abdominais e dor de cabeza.
Durante o seguimento post-rexistro do uso da combinación de metformina + sitagliptin ou sitagliptin, que forma parte dela, en monoterapia e / ou en terapia combinada con outros fármacos hipoglucemicos, reveláronse eventos adversos adicionais. Dado que estes datos foron obtidos voluntariamente dunha poboación de tamaño incerto, non se pode determinar a frecuencia e relación causal destes sucesos adversos coa terapia. Estes efectos adversos inclúen reaccións de hipersensibilidade, incluíndo anafilaxia, angioedema, erupción cutánea, urticaria, vasculite cutánea, enfermidades exfoliativas da pel, incluída a síndrome de Stevens-Johnson, pancreatite aguda, incluíndo formas hemorráxicas e necróticas con desenlace fatal e non fatal, función renal deteriorada, incluída a insuficiencia renal aguda (a veces é necesaria a diálise. ), infección das vías respiratorias superiores, nasofaringitis, estreñimiento, vómitos, cefalea, artralxia, mialxia, dor nas extremidades, dor nas costas, coceira.
Cambios de laboratorio
Sitagliptin. A frecuencia das desviacións dos parámetros de laboratorio nos grupos de tratamento con sitagliptina e metformina foi comparable coa frecuencia nos grupos de tratamento con placebo e metformina. A maioría, pero non todos os ensaios clínicos, observaron un lixeiro aumento do número de glóbulos brancos (aproximadamente 200 / µl en comparación co placebo, o contido medio no inicio do tratamento 6600 / µl), debido ao aumento do número de neutrófilos. Este cambio non se considera clínicamente significativo.
Metformina. En estudos clínicos controlados de metformina que teñen unha duración de 29 semanas, reduciuse a concentración normal de cianocobalamina (vitamina B)12) a valores anormais no soro sanguíneo en aproximadamente o 7% dos pacientes, sen manifestacións clínicas. Unha diminución similar debido á malabsorción selectiva da vitamina B12 (é dicir, unha violación da formación dun complexo co factor interno de Castle necesario para a absorción de vitamina B12), moi raramente leva ao desenvolvemento de anemia e corríxese facilmente pola abolición da metformina ou unha inxestión adicional de vitamina B12 (ver "Precaucións").
Interacción
Sitagliptina e metformina
A administración simultánea de múltiples doses de sitagliptina (50 mg 2 veces ao día) e metformina (1000 mg 2 veces ao día) non estivo acompañada de cambios significativos nos parámetros farmacocinéticos de sitagliptina ou metformina en pacientes con diabetes mellitus tipo 2.
Non se realizaron estudos do efecto interdrográfico sobre os parámetros farmacocinéticos da combinación de metformina + saxagliptina. Non obstante, se realizaron un número suficiente de estudos similares para cada un dos compoñentes da combinación: sitagliptin e metformina.
En estudos sobre interaccións con outros fármacos, a sitagliptina non tivo un efecto clínicamente significativo na farmacocinética de metformina, rosiglitazona, glibenclamida, simvastatina, warfarina ou anticonceptivos orais. A partir destes datos, sitagliptin non inhibe os isoenzimos de CYP3A4, CYP2C 8 ou CYP2C 9. Datos in vitro indican que a sitagliptina tampouco suprime CYP2D6, CYP1A 2, CYP2C 19 e CYP2B 6 isoenzimas e non induce CYP3A4.
Segundo unha análise farmacocinética da poboación en pacientes con diabetes tipo 2, a terapia concomitante non tivo un efecto clínicamente significativo na farmacocinética de sitagliptina. O estudo evaluou unha serie de medicamentos máis usados por pacientes con diabetes tipo 2, incluído fármacos hipocolesterolémicos (estatinas, fibratos, ezetimibe), axentes antiplaquetarios (clopidogrel), antihipertensivos (inhibidores da ACE, ARA II, beta-bloqueantes, BKK, hidroclorotiazida, analxésicos e AINEs (naproxeno, diclofenac, anticropressin, anti-anticorroso, anticorroso, anticorroso, anticorroso, anticorroso, anticorroso, anticorroso, anticorroso, anticorroso) ), antihistamínicos (cetirizina), inhibidores da bomba de protóns (omeprazol, lansoprazol) e para o tratamento da disfunción eréctil (sildenafil).
Notouse un aumento da ASC (11%) e da media de Cmáx (18%) digoxina cando se combina con sitagliptina. Este aumento non se considera clínicamente significativo, sen embargo, mentres se controla a digoxina, recoméndase un seguimento do paciente.
Notouse un aumento da AUC e Cmáx sitagliptin nun 29 e 68%, respectivamente, coa administración oral única combinada de saxagliptina a unha dose de 100 mg e ciclosporina (un forte inhibidor de P-gp) a unha dose de 600 mg. Estes cambios nos parámetros farmacocinéticos de sitagliptin non son clínicamente significativos.
Glibenclamida: nun estudo da interacción fármaco-fármaco de doses individuais de metformina e glibenclamida en pacientes con diabetes mellitus tipo 2, non se observaron cambios nos parámetros farmacocinéticos e farmacodinámicos da metformina. Cambios en AUC e Cmáx glibenclamida eran altamente variables. A información insuficiente (unha única dose) e a inconsistencia da concentración plasmática de glibenclamida cos efectos farmacodinámicos observados cuestionan a importancia clínica desta interacción.
Furosemida: Nun estudo da interacción entre fármacos de doses individuais de metformina e furosemida en voluntarios sans, observouse un cambio nos parámetros farmacocinéticos de ambos os dous fármacos. Furosemida aumentou o valor de Cmáx metformina no plasma e sangue enteiro nun 22%, o valor AUC da metformina en sangue enteiro nun 15%, sen cambiar a eliminación renal do medicamento. Valores Cmáx e a AUC de furosemida, á súa vez, diminuíu un 31 e un 12%, respectivamente, e T1/2 diminuíu un 32% sen cambios significativos na eliminación renal de furosemida. Non hai información sobre a interacción entre fármacos de dous fármacos con uso conxunto prolongado.
Nifedipina: ao estudar a interacción medicamento-nifedipina e metformina despois dunha única dose de fármacos por voluntarios sans, un aumento do plasma Cmáx e AUC de metformina nun 20 e 9%, respectivamente, así como un aumento da cantidade de metformina excretada polos riles. Tmáx e T1/2 A metformina non cambiou. Baséase nun aumento da absorción de metformina en presenza de nifedipina. O efecto da metformina na farmacocinética da nifedipina é mínimo.
Preparaciones catiónicas: Os fármacos catiónicos (é dicir, amilorida, digoxina, morfina, procainamida, quinidina, quinina, ranitidina, triamtereno, trimetoprim ou vancomicina) secretados por secreción tubular poden teóricamente interactuar coa metformina, competindo por un sistema de transporte tubular renal compartido. Unha competencia similar foi observada coa administración simultánea de metformina e cimetidina por voluntarios sans en estudos de dose única e múltiple, cun aumento do 60% na concentración Cmáx metformina en plasma e sangue enteiro e un aumento do 40% na AUC de metformina en plasma e sangue enteiro. Nun estudo de dose T única1/2 a metformina non cambiou. A metformina non afectou a farmacocinética da cimetidina. E aínda que estas interaccións entre fármacos son principalmente de importancia teórica (con excepción da cimetidina), recoméndase un control minucioso do paciente e axuste da dose da combinación de metformina + sitagliptin e / ou dos fármacos catiónicos anteriormente excretados polos túbulos renais proximais en casos de administración simultánea.
Outros: algúns fármacos teñen potencial hiperglicémico e poden interferir co control establecido sobre a glicemia. Estes inclúen tiazida e outros diuréticos, corticosteroides, fenotiazinas, hormonas tiroideas, estróxenos, anticonceptivos orais, fenitoína, ácido nicotínico, simpatomiméticos, BKK e isoniazida. Ao prescribir os medicamentos enumerados a un paciente que recibe unha combinación de metformina + sitagliptin, recoméndase un control minucioso dos parámetros de control glicémico.
Mentres que voluntarios saudables tomaban metformina e propranolol ou metformina e ibuprofeno, non se observaron parámetros farmacocinéticos destes fármacos.
Só unha parte insignificante da metformina se une ás proteínas plasmáticas, polo tanto, as interaccións entre fármacos da metformina con fármacos que se unen activamente ás proteínas do plasma (salicilatos, sulfonamidas, cloramfenicol e probenecid) son pouco probables, a diferenza das sulfonilureas, que tamén se unen ás proteínas plasmáticas.
Dosificación e administración
Xanuvia pódese tomar sen ter en conta as comidas.
A dose inicial recomendada é de 100 mg unha vez ao día.
Non se precisa axuste da dose cando se usa Januvia en combinación con metformina e / ou un agonista de PPARγ (tiazolidinediones). As drogas deben tomarse ao mesmo tempo.
Cando se usa Januvia en combinación con sulfonilurea ou insulina, pódense considerar doses máis baixas de sulfonilurea ou insulina que reducen o risco de hipoglucemia.
Ao saltar unha dose de Januvia, o paciente debe tomala en canto recorde isto. Non tome unha dobre dose de fármaco o día do ingreso.
Pacientes con insuficiencia renal. Os pacientes con insuficiencia renal leve (CC ≥50 ml / min, aproximadamente correspondente a un nivel de creatinina plasmática de ≤1,7 mg / dL nos homes, ≤ 1,5 mg / dL nas mulleres) non requiren axuste da dosificación de Januvia.
Para pacientes con insuficiencia renal moderada (CC ≥30 ml / min, pero 1,7 mg / dl, pero ≤3 mg / dl nos homes,> 1,5 mg / dl, pero ≤ 2,5 mg / dl nas mulleres), a dose de Januvia é de 50 mg. unha vez ao día.
Para pacientes con insuficiencia renal grave (CC 3 mg / dl en homes,> 2,5 mg / dl en mulleres), así como cunha etapa terminal de patoloxía renal, que require hemodiálise ou diálise peritoneal, a dose de Januvia é de 25 mg unha vez ao día. Xanuvia pódese usar independentemente do tempo de diálise.
Pacientes con insuficiencia hepática. Non se precisa axuste da dosificación para Januvia en pacientes con insuficiencia hepática leve ou moderada. Non se estudou a droga en pacientes con insuficiencia hepática grave.
Pacientes anciáns. Non se precisa axuste da dose para pacientes maiores. Non se estudou o uso de Januvia en pacientes maiores de 75 anos.
Idade infantil. Non se recomenda usar Januvia para nenos e adolescentes menores de 18 anos debido á falta de estudos clínicos sobre seguridade e eficacia neste grupo de idade.
Posibilidade de aplicación complexa
A sitagliptin non inhibe a actividade de Rosiglitazona, Simvastatina, Metformina e Warfarina. Pode ser usado por mulleres que usan regularmente anticonceptivos orais. Se se prescribe en paralelo coa Dioxina, as posibilidades deste último aumentan lixeiramente, con todo, tales cambios non precisan axuste da dosificación.
"Sitagliptin" pódese usar simultaneamente con inhibidores (por exemplo, con "Ketoconazol") e con ciclosporina. O efecto da droga en tales situacións non é crítico e non cambia as condicións do seu uso.
Dado que no tratamento da diabetes tipo 2 faise unha dobre carga nos riles, escollendo un complexo de drogas, é necesario ter en conta as súas capacidades e estado.
"Sitagliptin" é o nome internacional da droga, o seu sinónimo comercial é "Januvia".

Durante os ensaios clínicos, os medicamentos baseados na sitagliptina non tiveron un efecto significativo e significativo na cinética farmacolóxica de Rosiglitazon, Simvastatin, Metformin, anticonceptivos orais, Warfarina e Glibenclamida.
Cando se usan preparados baseados en sitagliptin, non se produce a inhibición dos isoenzimas CYP2C9, CYP3A4 e CYP2C8. Ademais, estes fármacos non inhiben os seguintes encimas: CYP2C19, CYP1A2, CYP2B6 e CYP2D6. "
O uso simultáneo de "Metformin" e "Sitagliptin" non trae cambios significativos na farmacocinética da sustancia activa deste último na diabetes mellitus.
O Yanumet combinado pode considerarse un análogo de Sitagliptinum Sitagliptin, inclúe metformina e sitagliptin.
Hai unha droga coas mesmas substancias activas - metformina e sitagliptina - esta "Velmetia." Outros análogos de "Yanumet" teñen unha acción similar e un código ATC:
- Avandamet
- Glibometro,
- Douglimax
- Tripride.
De acordo coas revisións dos pacientes que usan estes fármacos para o tratamento, afectan significativamente o nivel de azucre no corpo humano, con todo, precisan un control estrito da afección debido á posible aparición de moitos efectos secundarios.

O custo do medicamento depende do envase e da rexión do país. Varía entre 1596-1724 rublos. O prezo do análogo de Sitagliptin Yanumet é de 1.680 rublos.
Segundo informes de varios foros, o medicamento é o máis prescrito a miúdo aos diabéticos nun estadio inicial da patoloxía. As revisións de especialistas e pacientes demostran que hai un gran número de sutilezas no uso da incretinomimética.
"Sitagliptin" é un medicamento de nova xeración, non todos os médicos teñen moita experiencia no seu uso. Ata hai pouco, a metformina era moi utilizada, pero agora Januvia prescríbese como monoterapia. Con un número suficiente de posibilidades, non é adecuado complementalo con medicamentos como Metformin.

O análogo de "Sitagliptin" "Yanumet" móstrase como un complemento ao réxime de actividade física e dieta, o que contribúe a un mellor control da glicemia na diabetes tipo 2. As críticas sobre el son maioritariamente positivas.Non obstante, os diabéticos din que o medicamento e os seus análogos non sempre cumpren todos os requisitos, a súa eficacia diminúe co paso do tempo. O punto aquí non é a adicción, senón as características da enfermidade: o segundo tipo de diabetes é unha patoloxía crónica que está progresando.
Revisamos o prezo da droga "Sitagliptin", críticas e análogos.
Sobredose
Durante os ensaios clínicos, unha única dose de sitagliptin a unha dose de ata 800 mg foi xeralmente ben tolerada por voluntarios sans. Observáronse cambios mínimos no intervalo QT, non considerados clínicamente significativos, nun dos estudos de sitagliptina nunha dose diaria de 800 mg (ver "Farmacodinámica", Efecto na electrofisioloxía cardíaca) Non se estudou a dose superior a 800 mg / día en humanos.
Nos ensaios clínicos de administración repetida de sitagliptin (fase I), non se observaron reaccións adversas asociadas ao tratamento con sitagliptin cunha dose diaria de ata 400 mg durante 28 días.
En caso de sobredose, é necesario iniciar medidas estándar de apoio: eliminación da sitagliptina aínda non absorbida do tracto dixestivo, seguimento de signos vitais, incluído o ECG, así como o nomeamento de terapia sintomática se é necesario.
A sitagliptina está mal dializada: segundo estudos clínicos, só o 13,5% da dose foi excretada durante unha sesión de diálise de 3-4 horas. En caso de necesidade clínica, prescríbese hemodiálise prolongada. Non hai datos sobre a eficacia da diálise peritoneal.
Houbo casos de sobredose de metformina, incluída a administración en cantidades superiores a 50 g (50.000 mg). A hipoglicemia foi observada en aproximadamente o 10% de todos os casos de sobredosis. Non obstante, non se estableceu un vínculo claro cunha sobredose de metformina. O desenvolvemento da acidosis láctica acompañou aproximadamente o 32% de todos os casos de sobredosis de metformina (ver "Precaucións", Metformina) É posible unha hemodiálise de emerxencia (a metformina está dializada a unha velocidade de ata 170 ml / min en condicións de boa hemodinámica) para acelerar a eliminación do exceso de metformina nos casos de sospeita de sobredose.
Precaucións Metformina + Sitagliptin
Combinación de metformina + sitagliptina
No período de observación posterior ao rexistro, recibíronse informes sobre o desenvolvemento de pancreatitis aguda, incluída hemorráxica ou necrótica con resultado fatal e non fatal, en pacientes que toman sitagliptina (ver "Efectos secundarios", Observacións posteriores ao rexistro).
Dado que estas mensaxes foron recibidas voluntariamente dunha poboación de tamaño incerto, é imposible estimar de forma fiable a frecuencia destas mensaxes ou establecer unha relación causal coa duración do medicamento. Os pacientes deben ser informados sobre os síntomas característicos da pancreatite aguda: dor abdominal grave persistente. As manifestacións clínicas de pancreatite desapareceron despois da interrupción da sitagliptina. En caso de sospeita de pancreatite, é necesario deixar de tomar a combinación de metformina + sitagliptin e outros medicamentos potencialmente perigosos.
Monitorización da función renal
A vía preferida para eliminar metformina e sitagliptina é a excreción renal. O risco de acumulación de metformina e o desenvolvemento de acidosis láctica aumenta en proporción ao grao de función renal deteriorada, polo tanto, a combinación de metformina + sitagliptina non debe prescribirse a pacientes cunha concentración sérica de creatinina superior á VGN relacionada coa idade. En pacientes anciáns, debido a unha diminución da función renal relacionada coa idade, débese esforzar por lograr un control glicémico adecuado na dose mínima de combinación de metformina + sitagliptin. En pacientes anciáns, especialmente os maiores de 80 anos, controlan regularmente a función renal. Antes de comezar o tratamento cunha combinación de metformina + sitagliptin, e tamén polo menos unha vez ao ano despois de comezar o tratamento, coa axuda de probas adecuadas, confirman a función renal normal.Cunha maior probabilidade de desenvolver disfunción renal, a monitorización da función renal realízase con máis frecuencia e, cando se detecta, a combinación de metformina + sitagliptin cancelase.
O desenvolvemento de hipoglucemia con uso simultáneo con sulfonilureas ou insulina
Do mesmo xeito que ocorre con outros axentes hipoglucémicos, a hipoglucemia foi observada co uso simultáneo de sitagliptina e metformina en combinación con derivados de insulina ou sulfonilurea (ver "Efectos secundarios"). Para reducir o risco de hipoglucemia provocada por insulina ou inducida pola insulina, debe reducirse a dose de sulfonilurea ou derivado da insulina.
O desenvolvemento de hipoglucemia con uso simultáneo con sulfonilureas ou insulina
En estudos clínicos de sitagliptina, tanto en monoterapia como en combinación con fármacos que non conducen ao desenvolvemento de hipoglucemia (é dicir, metformina ou agonistas PPARγ - tiazolidinediones), a incidencia da hipoglucemia no grupo de pacientes que tomaban sitagliptina estivo preto da frecuencia no grupo de pacientes. tomando un placebo. Do mesmo xeito que ocorre con outros axentes hipoglucémicos, a hipoglucemia foi observada co uso simultáneo de sitagliptin en combinación con insulina ou derivados da sulfonilurea (ver "Efectos secundarios"). Para reducir o risco de hipoglucemia provocada por insulina ou inducida pola insulina, debe reducirse a dose de sulfonilurea ou derivado da insulina.
Durante o seguimento post-rexistro da utilización da combinación de metformina + sitagliptin ou sitagliptin, que forma parte dela, en monoterapia e / ou en terapia combinada con outros axentes hipoglucémicos, detectáronse reaccións de hipersensibilidade. Estas reaccións incluían anafilaxis, angioedema, enfermidades exfoliativas da pel, incluída a síndrome de Stevens-Johnson. Dado que estes datos se obtiveron voluntariamente dunha poboación de tamaño incerto, non se pode determinar a frecuencia e relación causal coa terapia destas reaccións adversas. Estas reaccións producíronse durante os primeiros 3 meses despois do inicio do tratamento con sitagliptin, algunhas observáronse despois de tomar a primeira dose. Se se sospeita o desenvolvemento dunha reacción de hipersensibilidade, é necesario deixar de tomar a combinación de metformina + sitagliptin, avaliar outras posibles causas do desenvolvemento do suceso adverso e prescribir outra terapia de redución de lípidos (ver "Contraindicacións" e "Efectos secundarios", Observacións posteriores ao rexistro).
A acidosis láctica é unha complicación metabólica rara pero grave que se produce debido á acumulación de metformina durante o tratamento coa combinación de metformina + sitagliptin. A mortalidade na acidosis láctica alcanza aproximadamente o 50%. O desenvolvemento de acidosis láctica tamén pode producirse no fondo dalgunhas enfermidades somáticas, en particular a diabetes mellitus ou calquera outra condición patolóxica, acompañada de hipoperfusión grave e hipoxemia de tecidos e órganos. A acidosis láctica caracterízase por unha maior concentración de lactato no plasma sanguíneo (> 5 mmol / l), un pH sanguíneo reducido, alteracións de electrólitos cun aumento do intervalo de anión, un aumento da relación de lactato / piruvato. Se a metformina é a causa da acidosis, a súa concentración plasmática normalmente é> 5 μg / ml. Segundo os informes, a acidosis láctica no tratamento da metformina desenvolvíase moi raramente (nuns 0,03 casos por cada 1000 pacientes anos, cunha taxa de mortalidade de aproximadamente 0,015 casos por cada 1000 pacientes anos). Durante 20.000 anos pacientes de tratamento con metformina, non se informaron casos de acidosis láctica nos ensaios clínicos.Casos coñecidos producíronse principalmente en pacientes con diabetes mellitus con insuficiencia renal grave, incluíndo patoloxía grave e hipoperfusión renal, a miúdo en combinación con enfermidades somáticas / cirúrxicas múltiples e simultaneas. O risco de desenvolver acidosis láctica en pacientes con insuficiencia cardíaca que requira unha corrección importante dos fármacos, especialmente con inestabilidade de angina pectoral / insuficiencia cardíaca no estadio agudo, acompañado de hipoperfusión grave e hipoxemia, aumenta significativamente. O risco de desenvolver acidosis láctica aumenta proporcionalmente ao grao de función renal deteriorada e á idade do paciente, polo tanto, un seguimento adecuado da función renal, así como o uso da dose mínima efectiva de metformina, pode reducir significativamente o risco de acidosis láctica. Un control coidadoso da función renal é especialmente necesario no tratamento de pacientes anciáns e, para os pacientes maiores de 80 anos, o tratamento con metformina comeza só despois da confirmación da función renal adecuada segundo os resultados da valoración da depuración da creatinina, xa que estes pacientes teñen máis risco de desenvolver acidosis láctica. Ademais, en calquera condición acompañada do desenvolvemento de hipoxemia, deshidratación ou sepsis, a metformina debe ser inmediatamente cancelada. Dado que coa función hepática deteriorada, a excreción de lactato é significativamente reducida, a metformina non debe ser prescrita a pacientes con signos clínicos ou de laboratorio de enfermidade hepática. Durante o tratamento con metformina, a inxestión de alcohol debe limitarse, xa que o alcol potencia o efecto da metformina no metabolismo do lactato. Ademais, o tratamento con metformina interrompeuse temporalmente durante a duración de estudos de radiopaque intravasculares e intervencións cirúrxicas.
A aparición de acidosis láctica adoita ser difícil de detectar e só se acompaña de síntomas non específicos como malestar, mialxia, síndrome de angustia respiratoria, aumento da somnolencia e síntomas dispepticos non específicos. Con un agravamento do curso da acidosis láctica, a hipotermia, a hipotensión arterial e a bradiriortmia resistentes poden unirse aos síntomas antes mencionados. O médico e paciente deben ser conscientes do posible significado destes síntomas e o paciente deberá informar inmediatamente ao médico do seu aspecto. O tratamento con metformina cancelouse ata que se aclare a situación.
Determinanse as concentracións plasmáticas de electrólitos, cetonas, glicosa, así como (segundo as indicacións) o valor de pH do sangue, a concentración de lactato. Ás veces a información sobre concentración plasmática de metformina tamén pode ser útil. Despois de que o paciente se acostumase á dose óptima de metformina, os síntomas gastrointestinais característicos das etapas iniciais do tratamento deberían desaparecer. Se aparecen tales síntomas, é probablemente un sinal de desenvolvemento de acidosis láctica ou outra enfermidade grave.
Se durante o tratamento con metformina, a concentración de lactato no plasma sanguíneo venoso supera a VGN, non sendo superior a 5 mmol / l, isto non é patognomónico para a acidosis láctica e pode deberse a condicións como a diabetes mellitus ou a obesidade mal controlada ou un esforzo físico excesivo ou un erro de medición técnico. . En calquera paciente con diabetes e acidosis metabólica a falta de confirmación de cetoacidosis (ketonuria e ketonemia), existe o risco de acidosis láctica.
A acidosis láctica é unha enfermidade que require atención médica de urxencia nunha instalación médica. O tratamento con metformina é cancelado e inmediatamente realízanse as medidas necesarias para a terapia de mantemento. Dado que a metformina se dializa a unha velocidade de ata 170 ml / min en condicións de boa hemodinámica, recoméndase unha hemodialise inmediata para corrixir a acidosis e eliminar a metformina acumulada.Estas medidas a miúdo levan á rápida desaparición de todos os síntomas da acidosis láctica e á restauración do estado do paciente (ver. "Contraindicacións").
En condicións normais, con monoterapia con metformina, a hipoglucemia non se produce, pero o seu desenvolvemento é posible contra o fondo da fame, despois dun importante esforzo físico sen compensación posterior das calorías consumidas, mentres que o uso doutros axentes hipoglucemicos (derivados da sulfonilurea e insulina) ou o alcol. En maior medida, o desenvolvemento de hipoglucemia afecta a pacientes maiores, debilitados ou esgotados, pacientes que abusan de alcol, pacientes con insuficiencia suprarrenal ou pituitaria. A hipoglicemia é difícil de recoñecer en pacientes anciáns e pacientes que toman beta-bloqueantes.
A farmacoterapia concomitante pode afectar negativamente á función renal ou á distribución de metformina. O uso simultáneo de fármacos que afectan negativamente a función renal, a hemodinámica ou a distribución de metformina (como os fármacos catiónicos que son excretados do corpo por secreción tubular) deben prescribirse con precaución (ver "Interacción", Metformina).
Estudos radiolóxicos con administración intravascular de axentes de contraste que conteñen iodo (por exemplo, urografía iv, colangiografía iv, angiografía, tomografía computada con administración iv de axentes de contraste)
A administración intravascular de axentes de contraste que contén iodo asociouse co desenvolvemento de acidosis láctica en pacientes que toman metformina e pode causar alteración renal aguda (ver "Contraindicacións"). Polo tanto, os pacientes que están programados para un estudo deberán deixar temporalmente de tomar a combinación de metformina + sitagliptin 48 horas antes e dentro das 48 horas posteriores ao estudo. A continuación do tratamento só é posible despois da confirmación do laboratorio da función renal normal.
O colapso (choque) vascular de calquera etioloxía, insuficiencia cardíaca aguda, infarto agudo de miocardio e outras condicións acompañadas do desenvolvemento da hipoxemia poden desencadear o desenvolvemento de acidosis láctica e azotemia renal. Se as condicións listadas se desenvolven no paciente durante o tratamento coa combinación de metformina + sitagliptin, a combinación debe deterse inmediatamente.
O uso da combinación de metformina + sitagliptin debería ser interrompido durante a duración de calquera intervención cirúrxica (coa excepción de pequenas manipulacións que non precisan restricións no réxime de bebida e fame) e ata que se reanude a comida normal, sempre que se obteña a confirmación de laboratorio da función renal normal.
O alcol potencia o efecto da metformina no metabolismo do ácido láctico. O paciente debe ser advertido sobre os perigos do abuso de alcol (unha única dose de grandes cantidades ou a inxestión constante de pequenas doses) durante o período de tratamento coa combinación de metformina + sitagliptin.
Función hepática deteriorada
Dado que se coñecen casos de desenvolvemento de acidosis láctica en pacientes con alteración da función hepática, non se recomenda prescribir unha combinación de metformina + sitagliptina en pacientes con signos clínicos ou de laboratorio de enfermidade hepática.
A concentración de cianocobalamina (vitamina B12) no plasma sanguíneo
En estudos controlados de metformina que duraron 29 semanas, o 7% dos pacientes mostrou unha diminución da concentración normal inicial de cianocobalamina (vitamina B12) no plasma sanguíneo sen o desenvolvemento de síntomas clínicos de deficiencia. Unha diminución similar pode deberse á malabsorción selectiva da vitamina B12 (é dicir, unha violación da formación do complexo co factor interno de Castle necesario para a absorción de vitamina B12), moi raramente leva ao desenvolvemento de anemia e corríxese facilmente pola abolición da metformina ou unha inxestión adicional de vitamina B12. Cando se trata coa combinación de metformina + sitagliptin, recoméndase comprobar anualmente os parámetros hematolóxicos do sangue, debendo estudar e corrixir calquera desviación. Pacientes con deficiencia de vitamina B12 (debido á reducida inxestión ou absorción de vitamina B12 ou calcio) recoméndase determinar a concentración plasmática de vitamina B12 a intervalos de 2-3 anos.
Cambio no estado clínico de pacientes con diabetes mellitus tipo 2 controlados adecuadamente
Se aparecen anomalías de laboratorio ou síntomas clínicos da enfermidade (en particular, calquera condición que non se poida identificar claramente) nun paciente con diabetes mellitus tipo 2 controlado previamente adecuadamente durante o tratamento coa combinación de metformina + sitagliptin, cetoacidosis ou acidosis láctica debe excluírse inmediatamente. A avaliación do estado do paciente debe incluír análises de sangue para electrólitos e cetonas, a concentración de glicosa no sangue, así como (segundo as indicacións) o pH do sangue, as concentracións plasmáticas de lactato, piruvato e metformina. Co desenvolvemento de acidosis de calquera etioloxía, debería deixar inmediatamente de tomar a combinación de metformina + sitagliptina e tomar as medidas adecuadas para corrixir a acidosis.
Perda de control glicémico
En situacións de estrés fisiolóxico (hipertermia, trauma, infección ou cirurxía) nun paciente con control glicémico previamente estable, é posible unha perda temporal de control glicémico. Nestes períodos, a substitución temporal da combinación de metformina + sitagliptin e insulinoterapia é aceptable e, tras resolver a situación aguda, o paciente pode retomar o tratamento anterior.
Influencia na capacidade para conducir vehículos e traballar con mecanismos. Non se realizaron estudos para estudar o efecto da combinación de metformina + sitagliptin na capacidade para conducir vehículos e traballar con mecanismos. Non obstante, deben terse en conta casos de mareos e somnolencia cando se toma sitagliptin.
Ademais, os pacientes deben ser conscientes do risco de hipoglucemia mentres usan unha combinación de metformina + sitagliptin con derivados de sulfonilurea ou insulina.
Normas de mostraxe de material e lecturas normais de glicosa
Valores normais de xaxún para o sangue integral - 3,3-5,5 mmol / L, para plasma - 4,0-6,1 mmol / L.
A mostraxe de sangue para esta sinxela análise ten as súas propias sutilezas. O sangue, xa sexa venoso ou capilar, debe tomarse para a súa análise pola mañá cun estómago baleiro. Non podes comer durante 10 horas, podes beber auga limpa, pero antes diso, a comida debería estar familiar.

Inmediatamente antes da manipulación é necesario evitar o estrés, o malestar, a actividade física, non se pode fumar. O resultado pode verse afectado por certos grupos de drogas (salicilados, representantes individuais dos antibióticos), vitamina C, así como por algúns outros fármacos, enfermidades e condicións que deben ser informados ao médico que o trate.
Un estudo recomendado para o cribado é o azucre en xaxún. Un método bastante rápido e sinxelo permítelle examinar grandes grupos de poboación para o metabolismo dos carbohidratos deteriorado. Esta análise refírese a aquelas que se poden realizar sen receita médica. É especialmente importante doar sangue dun dedo para o azucre a persoas en risco de diabetes tipo 2.
Sitagliptin para controlar o apetito e o peso corporal
Na patoxénese da diabetes tipo 2 distínguense tres mecanismos principais:
- Resistencia á insulina dos tecidos,
- Trastornos na produción de insulina endóxena,
- Síntese excesiva de glicosa polo fígado.
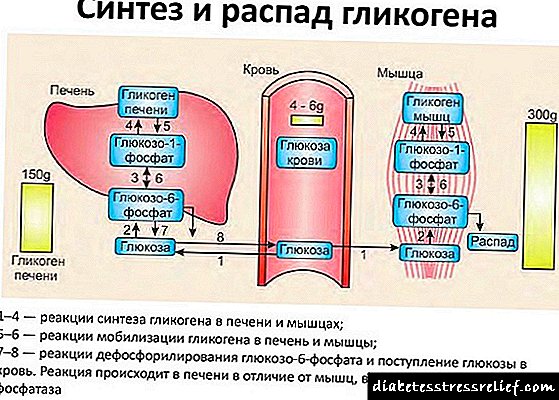
A responsabilidade para o desenvolvemento dunha enfermidade tan insidiosa recae nas células b e c do páncreas. Este último tamén produce unha hormona que estimula a conversión da glicosa en enerxía para os músculos e o cerebro. Se o ritmo da súa produción diminúe, isto provoca hiperglicemia.
As células B son as responsables da produción de glucagón, o seu exceso crea os requisitos previos para a excesiva secreción de glicosa polo fígado. O exceso de glucagón e a falta de insulina proporcionan as condicións para a acumulación de glucosa non procesada no torrente sanguíneo.
Non é posible un manexo eficaz da diabetes tipo 2 sen un control estable e a longo prazo (durante todo o período da enfermidade) do metabolismo dos carbohidratos. Numerosos ensaios internacionais confirman que só a compensación do azucre proporciona as condicións para a prevención de complicacións e aumentan a esperanza de vida dun diabético.
A pesar de toda a variedade de medicamentos antidiabéticos, non todos os pacientes conseguen unha compensación estable de hidratos de carbono coa súa axuda. Segundo un autoritario estudo UKPDS, o 45% dos diabéticos recibiron unha compensación do 100% pola prevención de microangiopatía despois de 3 anos e só un 30% despois de 6 anos.
Estas dificultades determinan a necesidade de desenvolver unha clase fundamentalmente nova de fármacos que non só axudarían a eliminar problemas metabólicos, senón tamén a manter o páncreas, estimulando o mecanismo fisiolóxico que permite regular a produción de insulina e a glicemia.
Os medicamentos da serie incretina, que poden controlar a diabetes tipo 2 sen estimular o páncreas, cambios bruscos de glicemia, o risco de hipoglucemia, son os últimos desenvolvementos por parte dos farmacéuticos.
O inhibidor da encima GLP-4, Sitagliptin, axuda a un diabético a controlar o apetito e o peso corporal, proporcionándolle ao corpo a capacidade de superar de forma independente o problema da toxicidade por glicosa.
Forma e composición de liberación
 O medicamento baseado en sitagliptin co nome comercial Januvia prodúcese en forma de comprimidos redondos cunha tonalidade rosa ou beige e marcado “227” para 100 mg, “112” para 50 mg, “221” para 25 mg. As tabletas están embaladas en caixas de plástico ou maletíns. Pode haber varias placas nunha caixa.
O medicamento baseado en sitagliptin co nome comercial Januvia prodúcese en forma de comprimidos redondos cunha tonalidade rosa ou beige e marcado “227” para 100 mg, “112” para 50 mg, “221” para 25 mg. As tabletas están embaladas en caixas de plástico ou maletíns. Pode haber varias placas nunha caixa.
A sustancia activa básica hidratado de fosfato sitagliptina complétase con croscarmelosa sódica, estearato de magnesio, celulosa, fumarato de estearil sódico, fosfato de calcio non definido.
Para a sildagliptina, o prezo depende do paquete, en particular para 28 comprimidos que ten que pagar 1.596-1724 rublos. Dálle un medicamento baixo receita, a vida útil é de 1 ano. O medicamento non require condicións especiais para o seu almacenamento. Os envases abertos almacénanse na porta do frigorífico durante un mes.
Farmacocinética de sitagliptina
A absorción do medicamento prodúcese rapidamente, cunha biodisponibilidade do 87%. A taxa de absorción non depende do tempo de inxestión e composición do alimento, en particular, os alimentos graxos non cambian os parámetros farmacocinéticos da incretina mimética.
En equilibrio, o uso adicional dunha tableta de 100 mg aumenta a área baixo a curva AUC, o que caracteriza a dependencia dos volumes de distribución a tempo, nun 14%. Unha única dose de comprimidos de 100 mg garante un volume de distribución de 198 l.
Unha parte relativamente pequena da incretina mimética é metabolizada. Identificáronse seis metabolitos que carecen de capacidade para inhibir o DPP-4. Limpeza renal (QC) - 350 ml / min. A parte principal do fármaco é eliminada polos riles (79% en forma non modificada e 13% en forma de metabolitos), o resto é excretado polos intestinos.
Á vista da gran carga que ten os riles en diabéticos con forma crónica (CC - 50-80 ml / min.), Os indicadores son idénticos, con CC 30-50 ml / min. observouse unha duplicación dos valores de AUC, cun CC por baixo dos 30 ml / min. - catro veces. Tales condicións suxiren a valoración da dose.
Con patoloxías hepáticas de gravidade moderada, Cmax e AUC aumentan un 13% e un 21%. En formas graves, a farmacocinética da sitagliptina non cambia significativamente, xa que o medicamento é principalmente excretado polos riles.
Quen se amosa incretinomimético
O medicamento prescríbese para a diabetes tipo 2 ademais dunha dieta baixa en carbohidratos e unha actividade muscular adecuada.
Úsase como fármaco único e terapia conxunta con metformina, preparados de sulfonilurea ou tiazolidinediones. Tamén é posible empregar esquemas de inxección de insulina se esta opción axuda a resolver o problema da resistencia á insulina.
Para o tratamento de articulacións, os nosos lectores usaron con éxito DiabeNot. Vendo a popularidade deste produto, decidimos ofrecelo á súa atención.
Eventos adversos
A xulgar polas revisións, a maioría de diabéticos están preocupados pola dispepsia e as feces molestas. Nas probas de laboratorio obsérvase hiperuricemia, unha diminución da eficiencia da glándula tiroide e leucocitosis.
Entre outros efectos imprevistos (non se probou unha conexión coa mimética de incretina): infeccións respiratorias, artralxia, enxaqueca, nasofaringite). A incidencia de hipoglucemia é similar aos resultados no grupo control que recibiu placebo.
Resultados de interacción con drogas
Co uso simultáneo de sitagliptina con metformina, rosiglitazona, anticonceptivos orais, glibenclamida, warfarina, simvastatina, a farmacocinética deste grupo de medicamentos non cambia.
A administración simultánea de sitagliptina con digoxina non implica un cambio na dosificación de medicamentos. Recomendacións similares ofrecen a instrución e a interacción de sitagliptin e ciclosporin, ketoconazol.
Sildagliptin - análogos
Sitagliptin é o nome internacional da droga; o seu nome comercial é Januvius. Un análogo pode considerarse o medicamento combinado Yanumet, que inclúe sitagliptina e metformina. Galvus pertence ao grupo de inhibidores de DPP-4 (Novartis Pharma AG, Suíza) co compoñente activo vildagliptin, prezo de 800 rublos.
Os medicamentos hipoglicémicos tamén son adecuados para o código ATX do nivel 4:
- Nesina (Takeda Pharmaceuticals, EUA, baseada na alogliptina),
- Onglisa (Bristol-Myers Squibb Company, baseada en saxagliptin, prezo - 1800 rublos),
- Trazhenta (Bristol-Myers Squibb Company, Italia, Gran Bretaña, coa sustancia activa linagliptin), prezo - 1700 rublos.
Estas drogas graves non están incluídas na lista de medicamentos preferentes, ¿paga a pena experimentar no seu propio risco e arriscar co seu orzamento e saúde?
Sitagliptin - críticas
A xulgar por informes sobre foros temáticos, Januvius adoita prescribirse a diabéticos na fase inicial da enfermidade. Sobre a sitagliptina, as revisións de médicos e pacientes demostran que o uso de incretinomimética ten moitos matices.
Januvia é un medicamento de nova xeración e non todos os médicos teñen bastante experiencia no seu uso. Ata hai pouco, a metformina era o fármaco de primeira liña; agora, Januvia tamén se prescribe como monoterapia. Se as súas capacidades son suficientes, non é aconsellable complementalo con metformina e outros fármacos.
Os diabéticos quéixanse de que o medicamento non sempre cumpre cos requisitos establecidos, co tempo a súa efectividade diminúe. O problema aquí non se acostuma ás pílulas, senón nas características da enfermidade: diabetes tipo 2: unha patoloxía crónica e progresiva.
Todos os comentarios levan á conclusión de que a introdución na práctica clínica da sitagliptina, que é unha clase fundamentalmente nova de fármacos, proporciona unha ampla oportunidade para o manexo da diabetes tipo 2 en calquera fase, desde o prediabetes ata a terapia adicional, con resultados insatisfactorios da aplicación de esquemas de compensación glicémicas tradicionais.
Informe do profesor A.S. Ametov, endocrinólogo-diabetólogo sobre a teoría e práctica da utilización de sitagliptina - en vídeo.
Doce para diabetes
A pregunta sobre o uso de produtos de repostería doce por parte de pacientes con diabetes segue a ser, se non a máis, a máis relevante durante moitas décadas. Sen dúbida, todos os que nin sequera estaban enfermos desta enfermidade endócrina polo menos unha vez na súa vida escoitaron que os doces son prexudiciais para os diabéticos e poden causar danos irreparables ao corpo.Non obstante, non esquezas que vivimos nun mundo moderno e progresivo onde moitos problemas son completamente solucionables ou polo menos poden ser corrixidos. A diabetes mellitus non é unha sentenza e comer doces para un paciente diabético non está prohibido en absoluto, pero primeiro debes estudar algunhas das características e matices dunha deliciosa dieta.
Si, si! Oíches ben: un alimento de dieta saborosa e incluso doce, seguido racionalmente por consellos, non danará ao corpo de ningún xeito, pero, pola contra, permitirache axustar mellor os procesos metabólicos perturbados como consecuencia da diabetes.
Dieta doce
Estamos acostumados a comprender o termo "dieta" e "dieta alimentaria" - un proceso acompañado de todo tipo de intentos de vontade, conciencia e limitacións que nos molestan, pero isto non é completamente certo. Na comunidade médica, o termo "dieta" refírese a un complexo nutricional especializado, cunha lista de recomendacións e produtos adicionais máis adecuados para unha determinada enfermidade. A dieta non exclúe os doces e engade substancias especiais á dieta - edulcorantes e edulcorantes.
Pode un paciente cun diagnóstico establecido de diabetes usar algo? Por suposto, pode, pero como isto afectará á súa condición é un problema completamente diferente e, moi probablemente, a nutrición descontrolada levará á progresión da enfermidade, especialmente tendo en conta que a gran maioría dos pacientes con diabetes teñen un segundo tipo de enfermidade, que se forma como resultado dun estilo de vida inadecuado, desnutrición e, por suposto, unha predisposición a ela.
A dieta número 9 é baixa en carbohidratos e baséase nos logros do médico estadounidense Richard Bernstein. Esta dieta inclúe todos os alimentos básicos e rica en calorías, e en canto ao doce, non exclúe o uso de froitas e verduras doces, que conteñen unha substancia como a glicosa - a sacarosa, pero os carbohidratos facilmente dixeribles (azucre, fariña) substitúense por edulcorantes. que non están incluídos no metabolismo dos carbohidratos. Elaboráronse receitas especiais para unha variedade de deliciosos e doces pratos que se poden preparar coas súas propias mans e, ao mesmo tempo, cumprirán os criterios para a dieta nº 9.
Hidratos de carbono simples - dano
Os carbohidratos sinxelos son hidratos de carbono facilmente dixeribles que se descompoñen case ao instante no tracto gastrointestinal e son absorbidos na circulación sistémica. A partir de hidratos de carbono simples prodúcese un aumento da secreción de insulina. Se un paciente con esta enfermidade endocrina come moitos carbohidratos sinxelos á vez, isto provocará un forte aumento da glicosa no sangue. O que provocará un deterioro do benestar. O carbohidrato simple máis común é o azucre.
Os carbohidratos sinxelos inclúen tamén:
- Produtos de panadaría e repostería
- Doces, chocolate, cacao,
- Algunhas froitas, como o plátano, a sandía e o melón,
- Xarope, mermelada, mel.
Todos estes produtos teñen un alto índice glicémico, xa que crean un forte aumento da concentración de glicosa no sangue, prexudicial para calquera persoa. Especialmente para un diabético. ¿Pode haber diabete nunha persoa que consuma constantemente hidratos de carbono simples? É posible, xa que o risco do seu desenvolvemento aumenta significativamente. Trátase de hidratos de carbono sinxelos que se recomenda que sexan substituídos por diabéticos por edulcorantes e edulcorantes. É importante facer unha pequena nota, os doces para diabéticos tipo 1 deben estar sempre a man, porque cunha sobredose de insulina axudarán a desfacerse dos efectos secundarios da hipoglucemia.
Hidratos de carbono complexos: beneficios
Os hidratos de carbono complexos son un complexo dos mesmos hidratos de carbono sinxelos. Non obstante, as características estruturais non permiten que esas moléculas se descompoñan rapidamente e sexan absorbidas no sangue. Non teñen un sabor tan doce, pero teñen un baixo índice glicémico e son ideais para diabéticos como dieta principal.O sabor dos hidratos de carbono complexos pódese resolver facilmente engadindo edulcorantes que non están implicados no metabolismo dos carbohidratos.
Que son os substitutos dos carbohidratos doces?
Aínda así, que doces poden ter as persoas con diabetes? A industria farmacéutica e alimentaria moderna non permanece en pé. Desenvolveuse unha ampla gama de diversos compostos que imitan o sabor doce nas papilas gustativas, pero non son carbohidratos. Hai dous grupos principais de tales compostos químicos:
Falaremos con máis detalle de cada un deles, e tamén entenderemos as propiedades útiles e nocivas destes compostos.
Edulcorantes
Estas substancias conteñen hidratos de carbono, pero teñen un menor contido calórico que o azucre. Os edulcorantes teñen un sabor máis intenso e cun menor volume poden conseguir as mesmas propiedades gustativas dun prato.
Entre os substitutos inclúense substancias como:
- O sorbitol é un suplemento dietético común nos alimentos da dieta E420.
- Manitol: atopado en plantas e usado na industria alimentaria como aditivo alimentario E421.
- Fructosa: presente en todas as froitas e verduras doces. Chega ata un 80% de mel.
- O aspartame é 300 - 600 veces máis doce que o azucre, corresponde ao complemento alimenticio E951.
Unha propiedade valiosa dos edulcorantes é un sabor máis rico en comparación co azucre, o que lles permite empregar en concentracións moito máis baixas, mentres que o produto alimenticio non perde a súa dozura. Non obstante, os edulcorantes cando son absorbidos transfórmanse en glicosa e aumentan o seu nivel no sangue, polo tanto é imposible empregalos en grandes cantidades, isto debe terse en conta na diabetes.
Edulcorantes
Como o azucre e os edulcorantes, os edulcorantes teñen un sabor doce, con todo, a súa estrutura química non é en absoluto carbohidratos. Existen edulcorantes naturais e artificiais. Os naturais inclúen: miraculina, osladina, ernandulcin. A artificial: sacarina, ciclamato, neotam. Os edulcorantes teñen contido en calorías cero e son recomendables para o uso tanto para diabéticos tipo 2 como para diabéticos de tipo 1.
Hai máis de 30 tipos de edulcorantes, a maioría deles de carácter péptido ou proteico. As propiedades do sabor tamén son diversas, desde identidade completa a azucres, ata doces e centos de veces de dozura superior. Os doces para diabéticos tipo 2, baseados en edulcorantes, poden ser un excelente substituto para a repostería convencional.
Danos dos edulcorantes
A pesar de todos os beneficios de usar edulcorantes e edulcorantes, o uso destas substancias aínda ten un lado negativo. Así, os científicos demostraron que co uso constante e excesivo de substitutos do azucre, a dependencia psicolóxica se desenvolve. Se hai moitos edulcorantes. Entón nas neuronas do cerebro desenvólvense novas vías asociativas que contribúen á violación do valor calórico dos alimentos, en particular, a orixe dos carbohidratos. Como resultado, unha avaliación inadecuada das propiedades nutricionais dos alimentos leva á formación de alimentación excesiva, que afecta negativamente aos procesos metabólicos.
Cal é o segredo de comer doces para diabéticos
Todo inxenioso é sinxelo! En primeiro lugar, cómpre coñecer claramente a forma da diabetes e o grao de compensación das súas manifestacións. Para iso, a determinación do nivel de hemoglobina glicada e a valoración das complicacións microvasculares da diabetes (exame do fondo no oftalmólogo) son excelentes.
En segundo lugar, se decides comer pratos cun alto índice glicémico, necesitas calcular con antelación a cantidade de hidratos de carbono que entrarán no corpo e convertelos en unidades de pan (XE) co fin de calcular oportunamente a dose racional de insulina.
En terceiro lugar, os produtos cun alto índice glicémico sempre poden ser substituídos por outros de poucas calorías coa adición dun edulcorante, o que lle aforrará o cálculo de carbohidratos comidos e a dosificación de insulina.
O desenvolvemento da diabetes a partir de doces
A diabetes mellitus pode desenvolverse a partir de doces? A resposta a esta pregunta molestaralle, pero quizais. Se o equilibrio entre o alimento consumido e, en consecuencia, a enerxía subministrada con ela e a actividade física non se observa, aumenta a probabilidade de desenvolver diabete. Cando usa fariña, repostería e bebidas carbonatadas en gran cantidade, corre o risco de desenvolver obesidade, o que ás veces aumenta o risco de desenvolver diabetes tipo 2.
Que pasará se unha persoa que ten sobrepeso continúa este estilo de vida? No corpo de tal persoa comezarán a producirse substancias que reducen a sensibilidade dos tecidos á insulina, como resultado diso, as células beta do páncreas comezarán a producir moita máis insulina e, como consecuencia, esgotaranse os mecanismos de produción de reserva e a persoa terá que recorrer á terapia con insulina.
A partir da información recibida, pódense extraer as seguintes conclusións:
- Non teñas medo dos doces, só tes que saber a medida.
- Se non tes diabetes, non levas o corpo ao extremo.
- Para os diabéticos, hai varias opcións alternativas para unha vida "doce" sen riscos innecesarios, estamos a falar de edulcorantes, edulcorantes e un enfoque racional para o tratamento da diabetes.
Non teñas medo da enfermidade, pero aprendes a convivir con ela e entón comprenderás que todas as restricións só están na túa cabeza.