Insulina Apidra Solostar: instrucións de uso
A insulina por ultrasonido comeza a actuar 5-15 minutos despois da administración, e o efecto máximo ocorre nunha hora. Válido na cantidade de aproximadamente 4 horas. Polo tanto, cómpre introducilo 15 minutos antes de comer, pero non antes, pode que se poida producir hipoglucemia.
Suxiro ler artigos que atopei na rede sobre o tema da insulina ultrahort Apidra.
Apidra® (Apidra®)
Substancia activa: insulina glulisina
Forma de dosificación: solución para administración subcutánea
1 ml de solución contén:
- substancia activa: insulina glulisina 100 UNIDADES (3,49 mg), excipientes: metacresol (m-cresol) 3,15 mg, trometamol (trometamina) 6,0 mg, cloruro sódico 5,0 mg, polisorbato 20 0,01 mg , hidróxido sódico a pH 7,3, ácido clorhídrico a pH 7,3, auga para inxección ata 1,0 ml.
Descrición: Líquido claro e incoloro.
Grupo farmacoterapéutico: axente hipoglucémico - análogo de insulina de acción curta.
ATX: A.10.A.B.06 Insulina glulisina
Farmacodinámica
A insulina glulisina é un análogo recombinante da insulina humana, que é igual a forza da insulina humana común. Despois da administración subcutánea de insulina, a glulisina comeza a actuar máis rápido e ten unha duración de acción menor que a insulina humana soluble.
Estudos realizados en voluntarios saudables e pacientes con diabetes mellorable demostraron que coa administración subcutánea de insulina, a glulisina comeza a actuar máis rápido e ten unha duración de acción menor que a insulina humana soluble. Con administración subcutánea, baixando a concentración de glicosa no sangue, a acción da insulina glulisina comeza en 10-20 minutos.
Cando se administra por vía intravenosa, os efectos de reducir a concentración de glicosa no sangue da insulina glulisina e da insulina humana soluble son iguais en forza. Unha unidade de insulina glulisina ten a mesma actividade de redución de glicosa que unha unidade de insulina humana soluble.
Nun estudo de fase I en pacientes con diabetes mellitus tipo 1, administráronse subcutáneamente perfís de redución da glicosa da insulina glulisina e insulina humana soluble a unha dose de 0,15 U / kg en diferentes momentos respecto a unha comida estándar de 15 minutos.
Os resultados do estudo demostraron que a insulina glulisina administrada 2 minutos antes dunha comida proporcionou o mesmo control glicémico despois dunha comida como a insulina humana soluble administrada 30 minutos antes da comida. Cando se administrou 2 minutos antes da comida, a insulina glulisina proporcionou un mellor control glicémico despois dunha comida que a insulina humana soluble administrada 2 minutos antes da comida.
A insulina en glulisina administrada 15 minutos despois do inicio da comida deu o mesmo control glicémico despois da comida que a insulina humana soluble, administrada 2 minutos antes da comida.
Un estudo de fase I realizado con insulina glulisina, insulina lispro e insulina humana soluble nun grupo de pacientes obesos demostrou que nestes pacientes a insulina glulisina conserva as súas características de acción rápida.
Neste estudo, o tempo para alcanzar o 20% do AUC total foi de 114 minutos para a insulina glulisina, 121 min para a insulina lispro e 150 min para a insulina humana soluble e AUC (0-2H), que tamén reflectían a actividade de redución da glicosa precoz, respectivamente, foi de 427 mg / kg para a insulina glulisina, 354 mg / kg para a insulina lispro e 197 mg / kg para a insulina humana soluble.
Estudos clínicos
Diabetes tipo 1
Nun ensayo clínico de 26 semanas da fase III, que comparou a insulina glulisina coa insulina lyspro, administrada subcutaneamente pouco antes das comidas (0-15 minutos), os pacientes con diabetes tipo 1 que usan insulina glargina como insulina basal, a insulina glulisina foi comparable. con insulina lispro para o control glicémico, que se evaluou polo cambio na concentración de hemoglobina glicosilada (HbA1c) no momento do punto final do estudo en comparación co resultado.
Un ensaio clínico en fase III de 12 semanas realizado en pacientes con diabetes mellitus tipo 1 que recibiron insulina glargina como terapia basal demostrou que a eficacia da administración de insulina glulisina inmediatamente despois das comidas era comparable á da insulina glulisina inmediatamente antes das comidas (para 0 -15 min) ou insulina humana soluble (30-45 min antes das comidas).
Na poboación de pacientes que completou o protocolo de estudo, no grupo de pacientes que recibiron insulina glulisina antes das comidas, houbo unha diminución significativamente maior de HbA1C en comparación co grupo de pacientes que recibiron insulina humana soluble.
Diabetes tipo 2
Realizouse un ensaio clínico en fase III de 26 semanas seguido por un seguimento de 26 semanas en forma de estudo de seguridade para comparar a insulina glulisina (0-15 minutos antes das comidas) coa insulina humana soluble (30-45 minutos antes das comidas), que se inxectaron subcutáneamente en pacientes con diabetes mellitus tipo 2, ademais de usar insulina isófana como insulina basal.
Neste estudo, a maioría dos pacientes (79%) mesturou a súa insulina de acción curta coa insulina insulina inmediatamente antes da inxección. 58 pacientes no momento da aleatorización empregaron medicamentos hipoglucémicos orais e recibiron instrucións para seguir tomando a mesma dose (sen cambios).
Durante a infusión continua de insulina subcutánea usando un dispositivo de acción bomba (para diabetes mellitus tipo 1), en 59 pacientes tratados con Apidra® ou insulina aspart, observouse unha baixa incidencia de oclusión de catéter nos dous grupos de tratamento (0,08 oclusións ao mes con Apidra® e 0,15 oclusións por mes ao usar insulina aspart), así como unha frecuencia similar ás reaccións no lugar da inxección (10,3% ao usar Apidra® e 13,3% ao usar insulina aspart).
Ao mesmo tempo, despois de 26 semanas de tratamento, os pacientes que recibiron tratamento con insulina glulisina para conseguir un control glicémico comparable á insulina lispro requiriron un aumento significativamente menor das doses diarias de insulina basal, insulina de acción rápida e a dose total de insulina.
Raza e xénero
Nos ensaios clínicos controlados en adultos non houbo diferenzas na seguridade e eficacia da insulina glulisina na análise de subgrupos distinguidos por raza.
Absorción e biodisponibilidade
As curvas farmacocinéticas de concentración no tempo en voluntarios sans e pacientes con diabetes mellitus tipo 1 e tipo 2 demostraron que a absorción de insulina glulisina en comparación coa insulina humana soluble foi aproximadamente 2 veces máis rápida e a concentración máxima de plasma alcanzada (Cmax) foi de aproximadamente 2. veces máis.
Nun estudo realizado en pacientes con diabetes mellitus tipo 1, despois da administración subcutánea de insulina glulisina a unha dose de 0,15 UI / kg, Tmax (tempo de inicio da concentración máxima do plasma) foi de 55 minutos e Cmax foi de 82 ± 1,3 μU / ml. en comparación con Tmax de 82 minutos e Cmax de 46 ± 1,3 μU / ml para insulina humana soluble. O tempo medio de residencia na circulación sistémica para a insulina glulisina foi menor (98 minutos) que para a insulina humana soluble (161 minutos).
Nun estudo realizado en pacientes con diabetes mellitus tipo 2 despois da administración subcutánea de insulina glulisina a unha dose de 0,2 U / kg, Cmax foi de 91 mkU / ml cunha latitud interquartil de 78 a 104 mkU / ml.
Coa administración subcutánea de insulina glulisina na rexión da parede abdominal anterior, da coxa ou do ombreiro (na rexión do músculo deltoide), a absorción foi máis rápida cando se introduciu na rexión da parede abdominal anterior en comparación coa administración do medicamento na coxa. A taxa de absorción da rexión deltoide foi intermedia.
A biodisponibilidade absoluta de insulina glulisina despois da administración subcutánea foi aproximadamente do 70% (73% da parede abdominal anterior, 71 do músculo deltoide e 68% da rexión femoral) e presentaron unha baixa variabilidade en diferentes pacientes.
Distribución e retirada
A distribución e excreción da insulina glulisina e da insulina humana soluble despois da administración intravenosa son similares, con volumes de distribución de 13 litros e 21 litros e semivida de 13 e 17 minutos, respectivamente.
Nunha análise transversal dos estudos de insulina glulisina tanto en individuos sans como en diabete tipo 1 e tipo 2, a vida media aparente oscilou entre 37 e 75 minutos.
Grupos especiais de pacientes
Pacientes con insuficiencia renal
Nun estudo clínico realizado en individuos sen diabetes cun amplo rango de estado funcional dos riles (limpieza de creatinina (CC)> 80 ml / min, 30-50 ml / min, indicacións
A diabetes mellitus que require tratamento con insulina en adultos, adolescentes e nenos maiores de 6 anos.
Contraindicacións
- Hipersensibilidade á insulina glulisina ou a algún dos compoñentes do medicamento. Hipoglicemia. Precaucións: Durante o embarazo. Embarazo e lactación: embarazo
Non hai estudos clínicos controlados sobre o uso de Apidra® en mulleres embarazadas. Unha cantidade limitada de datos obtidos sobre o uso de insulina glulisina en mulleres embarazadas (informáronse menos de 300 resultados do embarazo) non indica o seu efecto adverso sobre o embarazo, o desenvolvemento intrauterino do feto ou o bebé recentemente nado.
O uso de Apidra® SoloStar® en mulleres embarazadas debe realizarse con precaución. É necesario un coidadoso control da concentración de glicosa no sangue e manter o control glicémico.
Os pacientes con diabetes pre-embarazo ou gestacional deben manter o control glicémico durante todo o seu embarazo. Durante o primeiro trimestre do embarazo, a necesidade de insulina pode diminuír e, durante o segundo e terceiro trimestre, normalmente pode aumentar. Inmediatamente despois do nacemento, a demanda de insulina diminúe rapidamente.
Dosificación e administración
Apidra® debe administrarse pouco despois (0-15 minutos) antes ou pouco despois da comida.
Apidra® debe usarse en esquemas de tratamento que inclúen insulina de acción media ou insulina de acción longa ou un análogo de insulina de acción longa. Ademais, Apidra® pode usarse en combinación con medicamentos hipoglucémicos orais. O réxime de dosificación do fármaco Apidra® está seleccionado individualmente.
Administración de drogas
Apidra® está destinado á inxección subcutánea ou á infusión continua subcutánea de insulina mediante un dispositivo de bombeo adecuado para a administración de insulina.
A taxa de absorción e, en consecuencia, o inicio e a duración da acción poden verse afectadas por: o lugar de administración, a actividade física e outras condicións de cambio. A administración subcutánea á rexión da parede abdominal anterior proporciona unha absorción algo máis rápida que a administración ás outras partes do corpo indicadas anteriormente (ver sección Farmacocinética).
Deben observarse precaucións para evitar que o fármaco entre directamente nos vasos sanguíneos. Despois da administración do medicamento, é imposible facer masaxes na área de administración. Os pacientes deben formarse coa técnica de inxección correcta.
Mezcla de insulina hipodérmica
- Apidra® pode mesturarse con insulina-isófano humano. Ao mesturar Apidra® con insulina-isófano humano, primeiro débese introducir Apidra® na xeringa. A inxección subcutánea debe facerse inmediatamente despois da mestura. As insulinas mesturadas anteriormente non se poden administrar por vía intravenosa.
O uso de Apidra® cun dispositivo de acción bomba para a infusión continua de insulina subcutánea
Apidra® tamén se pode administrar mediante un dispositivo de bombeo para infusión continua de insulina subcutánea. Ao mesmo tempo, o conxunto de infusión e o depósito usado con Apidra® deben ser substituídos por regras asépticas polo menos cada 48 horas.
Estas recomendacións poden diferir das instrucións xerais dos manuais de bomba. É importante que os pacientes sigan as instrucións especiais anteriores para o uso de Apidra®. O non seguir estas instrucións especiais para o uso de Apidra® pode levar ao desenvolvemento de eventos adversos graves.
Ao usar Apidra® cun dispositivo de acción bomba para a infusión continua de insulina subcutánea. Apidra® non debe mesturarse con outras insulinas ou disolventes.
Os pacientes que se administran Apidra® por infusión continua subcutánea deberán ter sistemas alternativos para a administración da insulina e deben adestrarse para administrar a insulina por inxección subcutánea (en caso de avería do dispositivo bomba usado).
Cando se usa Apidra® con dispositivos de bomba para infusión continua de insulina subcutánea, a interrupción do dispositivo bomba, o mal funcionamento do conxunto de infusión ou erros no manexo poden levar rapidamente ao desenvolvemento de hiperglicemia, cetose e cetoacidosis diabética. No caso do desenvolvemento de hiperglicemia ou cetose ou cetoacidosis diabética, é necesaria a identificación e eliminación rápida das causas do seu desenvolvemento.
Grupos especiais de pacientes
Función renal deteriorada: A necesidade de insulina na insuficiencia renal pode diminuír.
Función hepática deteriorada: en pacientes con función hepática deteriorada, a necesidade de insulina pode diminuír debido á capacidade reducida de gluconeoxénese e unha desaceleración do metabolismo da insulina.
Pacientes anciáns: Os datos farmacocinéticos dispoñibles en pacientes anciáns con diabetes mellitus son insuficientes. A deterioración da función renal na vellez pode levar a unha diminución dos requirimentos de insulina.
Nenos e adolescentes: Apidra® pode usarse en nenos maiores de 6 anos e adolescentes. A información clínica sobre o uso da droga en nenos menores de 6 anos é limitada.
Siga coidadosamente as instrucións para o manexo adecuado das plumas xeringas precargadas (consulte a sección "Instrucións de uso e manipulación").
Efectos secundarios
- As reaccións adversas observadas foron reaccións coñecidas por esta clase farmacolóxica e, polo tanto, comúns a calquera insulina. Trastornos metabólicos e nutricionais A hipoglicemia, o efecto indesexable máis común da terapia con insulina, pode ocorrer se se usan doses demasiado altas de insulina que exceda a necesidade desta.
Os síntomas da hipoglucemia adoitan ocorrer de súpeto.Non obstante, normalmente os trastornos neuropsiquiátricos debidos a neuroglicopenia (sensación de cansazo, cansazo ou debilidade inusual, diminución da capacidade de concentración, somnolencia, trastornos visuais, dor de cabeza, náuseas, confusión ou perda de consciencia, síndrome convulsiva) están precedidos de síntomas de contrarregulación adrenérxica (activación de simpatía sistema suprarrenal en resposta á hipoglucemia): fame, irritabilidade, excitación nerviosa ou tremor, ansiedade, palidez da pel, suor "fría", tach icardia, palpitacións graves (canto máis rápido se desenvolve a hipoglucemia e máis difícil é, máis pronunciados son os síntomas da contraregulación adrenérxica).
Trastornos do sistema inmune
Pode producirse reaccións de hipersensibilidade local (hiperemia, inchazo e picazón no lugar de inxección de insulina). Estas reaccións normalmente desaparecen despois duns días ou semanas de usar o medicamento. Nalgúns casos, estas reaccións poden non estar relacionadas coa insulina, pero poden deberse á irritación da pel provocada por un tratamento antiséptico antes da inxección ou a unha inxección subcutánea inadecuada (se a técnica adecuada para a inxección subcutánea está deteriorada).
Reaccións sistémicas de hipersensibilidade á insulina
Tales reaccións á insulina (incluída a insulina glulisina) poden, por exemplo, ir acompañadas dunha erupción cutánea en todo o corpo (incluíndo picazón), tensión no peito, asfixia, diminución da presión arterial, aumento da frecuencia cardíaca ou sudoración excesiva. Os casos graves de alerxias xeneralizadas, incluídas as reaccións anafilácticas, poden poñer en perigo a vida do paciente.
Trastornos da pel e do tecido subcutáneo
Lipodistrofia. Como ocorre con calquera outra insulina, a lipodistrofia pode desenvolverse no lugar da inxección, o que pode retardar a absorción de insulina. O desenvolvemento da lipodistrofia pode contribuír á violación da alternancia de lugares de administración de insulina, xa que a introdución do medicamento no mesmo lugar pode contribuír ao desenvolvemento da lipodistrofia.
A alternancia constante de sitios de inxección dentro dunha das áreas de inxección (coxa, ombreiro, superficie anterior da parede abdominal) pode axudar a reducir e evitar o desenvolvemento desta reacción indesexable.
Outro
A administración accidental doutras insulinas foi informada por erro, en particular insulinas de longa duración, en lugar da insulina glulisina.
Sobredose
Cun exceso de dose de insulina en relación coa necesidade desta, determinada pola inxestión de alimentos e o consumo de enerxía, pode producirse unha hipoglucemia.
Non hai datos específicos sobre unha sobredose de insulina glulisina. Non obstante, coa súa sobredose, o desenvolvemento da hipoglucemia é posible. Os episodios de hipoglucemia leve poden deterse tomando glicosa ou alimentos que conteñan azucre. Por iso, recoméndase que os pacientes con diabetes leven sempre anacos de azucre, doces, galletas ou zume de froitas doces.
Despois de recuperar a conciencia, recoméndase dar aos pacientes carbohidratos cara ao interior para evitar a recorrencia da hipoglucemia, o que é posible despois dunha aparente mellora clínica. Despois da administración de glucagón, para establecer a causa desta hipoglucemia grave e evitar o desenvolvemento doutros episodios similares, o paciente debe ser observado nun hospital.
Interacción
Non se realizaron estudos sobre interaccións farmacocinéticas. A partir dos coñecementos empíricos existentes sobre outros fármacos similares, é pouco probable a aparición de interaccións farmacocinéticas clínicamente significativas. Algúns medicamentos poden afectar o metabolismo da glicosa, o que pode requirir o axuste da dose de insulina glulisina e especialmente un control minucioso do tratamento.
Entre as substancias que poden reducir o efecto hipoglucémico da insulina inclúense: glucocorticosteroides, danazol, diazoxido, diuréticos, glucagón, isoniazido, derivados de fenotiazina, somatropina, simpatomiméticos (por exemplo, adrenalina epinefrina, salbutamol, hormonas tiroideas, p. en anticonceptivos hormonais), inhibidores de proteasas e antipsicóticos atípicos (por exemplo, olanzapina e clozapina).
Os beta-bloqueantes, clonidina, sales de litio ou etanol poden potenciar ou debilitar o efecto hipoglucémico da insulina. A pentamidina pode provocar hipoglucemia seguida de hiperglicemia. Ademais, baixo a influencia de fármacos con actividade simpatolítica, como beta-bloqueantes, clonidina, guanetidina e reserpina, os síntomas da activación adrenérxica reflexa en resposta á hipoglucemia poden ser menos pronunciados ou ausentes.
Directrices de compatibilidade
Debido á falta de estudos de compatibilidade, a insulina glulisina non debe mesturarse con ningún outro fármaco, coa excepción da insulina insulina humana. Cando se administra utilizando un dispositivo de bomba de infusión, Apidra® non debe mesturarse con disolventes ou outras preparacións de insulina.
Instrucións especiais
Debido á curta duración da acción do medicamento Apidra®, os pacientes con diabetes mellitus tamén requiren a introdución de insulinas de acción media ou a infusión de insulina usando unha bomba de insulina para manter un control glicémico adecuado.
Calquera cambio na insulinoterapia debe facerse con precaución e só baixo a supervisión dun médico. Cambio na concentración de insulina, produtor de insulina, tipo de insulina (insulina humana soluble, insulina-isófano, análogos de insulina), especies de insulina (insulina animal, insulina humana) ou método de produción de insulina (insulina ADN recombinante ou insulina de orixe animal) pode requirir un cambio na dose de insulina. Tamén pode ser necesario cambiar as doses de axentes hipoglucémicos orais tomados simultaneamente.
A necesidade de insulina pode cambiar durante enfermidades intercurrentes, como consecuencia dunha sobrecarga emocional ou do estrés. O uso de doses inadecuadas de insulina ou a interrupción do tratamento, especialmente en pacientes con diabetes tipo 1, pode levar ao desenvolvemento de hiperglicemia e cetoacidosis diabética - condicións potencialmente mortais.
Hipoglicemia
O tempo en que se desenvolve a hipoglucemia depende da taxa de inicio do efecto da insulina usada e, polo tanto, cambia cando cambia o réxime de tratamento.
Entre as condicións que poden cambiar ou facer menos pronunciadas os precursores do desenvolvemento da hipoglucemia son: intensificación da terapia con insulina e mellora significativa do control glicémico, desenvolvemento gradual da hipoglucemia, paciente ancián, presenza de neuropatía do sistema nervioso autónomo, existencia a longo prazo de diabetes mellitus e uso de certos medicamentos (ver sección “Interacción con outros medicamentos”).
Tamén pode ser necesaria a corrección das doses de insulina se os pacientes aumentan a actividade física ou cambian o seu horario habitual de alimentación. O exercicio realizado inmediatamente despois de comer pode aumentar o risco de hipoglucemia. En comparación coa insulina humana soluble, a hipoglucemia pode desenvolverse máis cedo despois da inxección de análogos de insulina de acción rápida.
As reaccións hipoglicémicas ou hiperglicémicas non compensadas poden levar á perda de consciencia, coma ou morte.
Insuficiencia renal
A necesidade de Apidra®, do mesmo xeito que con todas as outras insulinas, pode diminuír a medida que avance a insuficiencia renal.
Insuficiencia hepática
En pacientes con insuficiencia hepática, a necesidade de insulina redúcese debido á diminución da capacidade de gluconeoxénese no fígado e unha desaceleración do metabolismo da insulina.
Pacientes anciáns
A deterioración da función renal na vellez pode levar a unha diminución dos requirimentos de insulina. Os pacientes de idade avanzada poden ter dificultades para recoñecer signos de desenvolvemento de hipoglucemia.
Nenos e adolescentes
Apidra® pode usarse en nenos e nenas maiores de 6 anos e adolescentes. A información clínica sobre o uso da droga en nenos menores de 6 anos é limitada.
As propiedades farmacocinéticas e farmacodinámicas da insulina glulisina estudáronse en nenos (7-11 anos) e adolescentes (12-16 anos) con diabetes tipo 1. Nos dous grupos de idade, a insulina glulisina foi absorbida rapidamente e a súa taxa de absorción non difería da dos adultos (voluntarios sans e pacientes con diabetes mellitus tipo 1).
Despois do inicio do uso, garde os frascos, xeringas OptiSet®, cartuchos ou cartuchos OptiKlik® con unha temperatura non superior a +25 ° C nun lugar protexido da luz e do alcance dos nenos. Non arrefriarse (a administración de insulina refrixerada é máis dolorosa). Para protexerse da exposición á luz, debes gardar a botella, a pluma de xiringa OptiSet® previamente cuberta, os cartuchos OptiClick® ou cartuchos nos seus propios envases de cartón.
O prazo de conservación da droga nunha botella, cartucho, sistema de cartuchos OptiKlik® ou pluma de xeringa OptiSet® despois do primeiro uso é de 4 semanas. Recoméndase marcar na etiqueta a data da primeira inxección do medicamento.
Instrucións de uso e manexo
Dado que Apidra® é unha solución, non se necesita resuspensión antes do uso.
Viales
Os frascos Apidra® están deseñados para o uso con xeringas de insulina coa escala unitaria adecuada e para o seu uso co sistema de bombas de insulina. Inspeccione a botella antes do uso. Só debe usarse se a solución é clara, incolora e non contén partículas visibles.
O conxunto de infusión e depósito deben ser substituídos cada 48 horas cumprindo as regras asépticas. Os pacientes que reciben Apidra® a través de NPII deberían ter en stock insulina alternativa no caso de fallos no sistema de bombas.
Bolígrafos de xiringa OptiSet® pre-recheos
Antes do uso, inspeccione o cartucho dentro da pluma de xeringa. Debe usarse só se a solución é transparente, incolora, non contén partículas sólidas visibles e, en coherencia, aseméllase á auga.
As xeringas baleiras OptiSet® non deben reutilizarse e hai que desaloxalas. Para previr a infección, un bolígrafo pre-cuberto só o debe usar un paciente e non debe ser transferido a outra persoa.
Antes de usar a seringa OptiSet®, lea atentamente a información de uso.
Información importante sobre o uso da seringa Pen OptiSet®
- Use sempre unha nova agulla para cada seguinte uso. Use só agullas axeitadas para a pluma de xiringa OptiSet®. Antes de cada inxección, proba sempre para ver se a pluma de xiringa está preparada para o seu uso (ver máis abaixo). Se se emprega unha nova pluma xeringa OptiSet®, a proba de preparación para o uso debe realizarse usando 8 unidades preestablecidas polo fabricante. O selector de dose só se pode xirar nunha dirección. Non xire nunca o selector de dose (cambio de dose) despois de premer o botón de inicio da inxección. Esta pluma de xiringa de insulina é para uso do paciente. Non podes traizoalo a outra persoa. Se a inxección a fai outra persoa, débese ter especial coidado para evitar lesións accidentais de agulla e infección por unha enfermidade infecciosa. Non use nunca a pluma xeringa OptiSet® danada, nin se está seguro da súa reparación. Ten sempre unha pluma de xiringa OptiSet® de reposición no caso de que a súa xeringa OptiSet® estea danada ou perdida.
Proba de insulina
Despois de retirar a tapa da xeringa, hai que revisar as marcas no depósito de insulina para asegurarse de que conteña a insulina adecuada. Tamén debe comprobarse o aspecto da insulina: a solución de insulina debe ser transparente, incolora, libre de partículas sólidas visibles e ter unha consistencia similar á auga. Non empregue a pluma xeringa OptiSet® se a solución de insulina está turbia, ten cor ou partículas alleas.
Fixación de agullas
Despois de quitar a tapa, conecte con coidado e firmemente a agulla á xeringa. Comprobación da preparación da pluma xiringa para o seu uso. Antes de cada inxección, é necesario comprobar a dispoñibilidade do bolígrafo para ser usado. Para unha pluma de xeringa nova e sen uso, o indicador de dose debe situarse no número 8, como o estableceu anteriormente o fabricante.
Se se usa unha pluma de xeringa, o dispensador debe xirarse ata que o indicador de dose pare no número 2. O dispensador xira nun só sentido. Saque completamente o botón de inicio para facer a dose. Nunca xire o selector de dose despois de extraer o botón de inicio.
- Débense retirar os tapóns de agulla exteriores e internos. Garda a tapa exterior para eliminar a agulla usada. Mentres mantén a pluma xeringa coa agulla orientada cara arriba, toque suavemente o depósito de insulina co dedo para que as burbullas de aire se levanten cara á agulla. Despois diso, prema completamente o botón de inicio. Se se desprende unha pinga de insulina da punta da agulla, a pluma de xiringa e a agulla funcionan correctamente. Se non aparece unha pinga de insulina na punta da agulla, debería repetir a proba de preparación da xeringa para ser utilizada ata que a insulina apareza na punta da agulla.
Selección de dose de insulina
Pódese establecer unha dose de 2 unidades a 40 unidades por incrementos de 2 unidades. Se se precisa unha dose superior a 40 unidades, debe administrarse en dúas ou máis inxeccións. Asegúrese de ter suficiente insulina para a súa dose.
- A escala de insulina residual nun recipiente transparente para a insulina mostra a cantidade de insulina que queda aproximadamente na pluma de xeringa OptiSet®. Esta escala non se pode usar para tomar unha dose de insulina. Se o pistón negro está ao comezo da tira de cores, hai aproximadamente 40 unidades de insulina. Se o pistón negro está no extremo da tira coloreada, hai aproximadamente 20 unidades de insulina. O selector de dose debe virar ata que a frecha de dose indique a dose desexada.
A inxestión de dose de insulina
- Hai que tirar o botón de inicio da inxección ata o límite para encher o bolígrafo de insulina. Comprobe se a dose correcta está completamente cuberta. Teña en conta que o botón de inicio cambia segundo a cantidade de insulina que queda no tanque de insulina. O botón de inicio permite comprobar que dose se está marcando. Durante a proba, o botón de inicio debe manterse activado. A última liña ancha visible no botón de inicio mostra a cantidade de insulina tomada. Cando se mantén o botón de inicio, só é visible a parte superior desta liña ampla.
Administración de insulina
O persoal especializado debe explicar ao paciente a técnica de inxección.
- A agulla debe introducirse subcutaneamente. Débese premer ata o límite o botón de inicio da inxección. O clic deterase cando se preme todo o botón de inicio da inxección. A continuación, debe manterse presionado o botón de inicio da inxección durante 10 segundos antes de tirar a agulla da pel. Isto asegurará a introdución de toda a dose de insulina.
Eliminación de agullas
Despois de cada inxección, a agulla debe ser eliminada da pluma de xiringa e descartada.Isto evitará infeccións, así como fugas de insulina, entrada de aire e posibles obstrucións da agulla. Non se deben reutilizar as agullas. Despois diso, volva a colocar a tapa na xeringa.
Cartuchos
Os cartuchos deben usarse cunha pluma de insulina, como OptiPen® Pro1 ou ClickSTAR® e de acordo coas recomendacións da información proporcionada polo fabricante do dispositivo. Non se deben empregar con outras plumas de xeringa recargables, xa que a precisión de dosificación só se estableceu con OptiPen® Pro1 e ClickSTAR® xeringas.
As instrucións do fabricante para usar o xeringuete OptiPen® Pro1 ou ClickSTAR® sobre a carga dun cartucho deben ser seguidas exactamente. Inspeccione o cartucho antes do uso. Debe usarse só se a solución é clara, incolora, non contendo partículas sólidas visibles.
Antes de introducir o cartucho na xeringa recargable, o cartucho debe estar a temperatura ambiente durante 1-2 horas. Antes da inxección, deberán eliminar as burbullas de aire do cartucho (ver instrucións de uso da xeringa). As instrucións de uso da pluma xeringa deben ser estritamente. Non se poden volver cargar cartuchos baleiros. Se a pluma de xiringas OptiPen® Pro1 ou ClickSTAR® está danada, non se pode usar.
- Se o bolígrafo non funciona correctamente, pódese extraer a solución do cartucho nunha xeringa de plástico adecuada á insulina a unha concentración de 100 PECES / ml e administrada ao paciente. Para evitar a infección, débese empregar unha xeringa reutilizable só no mesmo paciente.
Sistema de cartuchos Opticlick®
O sistema de cartuchos OptiClick® é un cartucho de vidro que contén 3 ml de solución de insulina glulisina, que se fixa nun recipiente de plástico transparente cun mecanismo de pistón unido.
Se a pluma xeringa OptiClick® está danada ou mal por un defecto mecánico, debe substituírse por outra.
Antes de instalar o sistema de cartuchos na pluma xeringa OptiClick®, debe estar a temperatura ambiente durante 1-2 horas. Inspeccione o sistema de cartuchos antes da instalación. Debe usarse só se a solución é clara, incolora, non contendo partículas sólidas visibles.
Antes de realizar unha inxección, as burbullas de aire deben eliminarse do sistema de cartuchos (ver instrucións de uso da xeringa). Non se poden volver cargar cartuchos baleiros. Se o bolígrafo non funciona correctamente, a solución pódese extraer do sistema de cartuchos nunha xeringa de plástico axeitada para a insulina a unha concentración de 100 pezas / ml e inxectada ao paciente.
Para previr a infección, debe utilizarse unha xeringa reutilizable só para un paciente.
Influencia sobre a capacidade de conducir transp. Mércores e peles.
A capacidade do paciente para concentrarse e a velocidade das reaccións psicomotrices poden verse afectadas por hipoglucemia ou hiperglicemia, así como por trastornos visuais. Isto pode supoñer certo risco en situacións nas que estas habilidades son importantes, por exemplo, cando se conduce vehículos ou outros mecanismos.
Forma / dosificación de liberación
Solución para administración subcutánea, 100 pezas / ml.
- 10 ml de fármaco nunha botella de vidro transparente e incoloro (tipo I). A botella está tapada, espremida cunha tapa de aluminio e cuberta cunha tapa protectora. 1 botella xunto coas instrucións de uso nunha caixa de cartón.
- 3 ml de fármaco nun cartucho de vidro claro e incoloro (tipo I). O cartucho está enrolado por un lado cun tapón e espremido cunha tapa de aluminio, por outra banda - cun émbolo.
- 5 cartuchos por ampolla de película de PVC e papel de aluminio. 1 embalaxe en forma de blister xunto coas instrucións de uso nunha caixa de cartón. O cartucho está montado nunha pluma xeringuilla OptiSet® desbotable. Cada 5 plumas xeringas OptiSet® xunto coas instrucións de uso nunha caixa de cartón equipada cunha pinza de cartón. O cartucho insírese no sistema de cartuchos OptiClick®. En 5 sistemas de cartuchos OptiKlik® xunto coas instrucións de uso nun paquete de cartón equipado cunha pinza de cartón.
Insulina "Apidra" - para nenos con diabetes
O Ministerio de Sanidade israelí aprobou o uso de insulina Apidra (insulina Glulisin), un análogo da insulina de acción rápida para uso por nenos de 6 anos con diabetes.
Recentemente, a insulina Apidra rexistrouse nos Estados Unidos e está permitida para nenos a partir de 4 anos, nos países da UE - para nenos e adolescentes a partir dos 6 anos.
A insulina Apidra, desenvolvida pola compañía farmacéutica internacional Sanofi Aventis, é un análogo da insulina de acción rápida, que ten un inicio rápido e unha curta duración de acción. Está indicado para pacientes con diabetes tipo 1 e tipo 2, a partir dos 6 anos. O medicamento existe en forma de xiringa ou inhalador.
Apidra ofrece aos pacientes unha maior flexibilidade en canto ás horas de inxección e comida. Se é necesario, pódese usar insulina Apidra con insulina de acción longa como Lantus.
Sobre a diabetes
A diabetes mellitus é unha enfermidade crónica e xeneralizada causada por unha diminución da secreción da hormona insulina ou a súa baixa actividade biolóxica. A insulina é unha hormona necesaria para converter a glicosa (azucre) en enerxía.
Dado que o páncreas non produce case ou completamente insulina, os pacientes con diabetes tipo 1 necesitan inxeccións diarias de insulina ao longo da súa vida. Na diabetes mellitus tipo 2, o páncreas segue producindo insulina, pero o corpo reacciona mal á influencia da hormona, o que leva a unha relativa deficiencia de insulina.
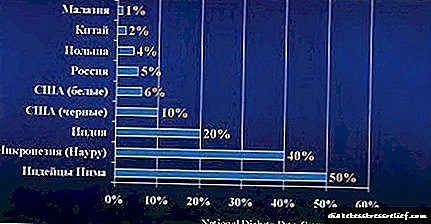
Segundo as estatísticas, 35.000 nenos con diabetes viven en Israel. A Federación Internacional de Diabetes (IDF) estima que hai 440.000 nenos menores de 14 anos con diabetes tipo 1 en todo o mundo que son diagnosticados con 70.000 casos novos cada ano.
Insulina de acción rápida (ultra curto)
A insulina de acción rápida (ultrashort) inclúe hoxe tres tipos de novos fármacos:
- lispro (Humalog), aspart (NovoRapid), glulisina (Apidra).
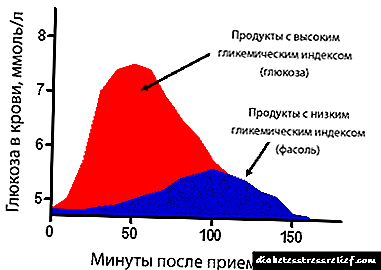
A principal característica de insulina de acción rápida é o comezo rápido e o final da súa acción en comparación con insulinas "sinxelas". O efecto de redución da glicosa neste caso producirase moito máis rápido, o que se debe á absorción acelerada de insulina da graxa subcutánea.
O uso desta insulina de acción rápida pode reducir significativamente o intervalo de tempo entre as inxeccións e a inxestión directa de alimentos. Debido a isto, o nivel de glicemia despois da comida é reducido e a incidencia de hipoglucemia.
A aparición da acción da insulina rápida prodúcese entre 5 e 15 minutos despois da administración e o pico de acción, é dicir, o seu efecto máximo conséguese aos 60 minutos. A duración total de acción deste tipo de insulina é de 3-5 horas. A insulina de acción rápida debe administrarse entre 5 e 15 minutos antes da comida ou xusto antes da comida. Ademais, a administración de insulina rápida inmediatamente despois dunha comida tamén fai posible un bo control glicémico.
Cómpre ter en conta que a introdución de insulina rápida antes de 20 a 30 minutos antes da comida pode levar á hipoglucemia.
Ao cambiar a introdución deste tipo de insulina, é necesario controlar máis frecuentemente o nivel de glicemia para aprender a correlacionar correctamente a dose de insulina administrada e a cantidade de carbohidratos consumidos. As doses do medicamento en cada caso establécense de xeito individual.
Unha única dose de insulina de acción rápida non debe superar as 40 unidades. Máis información sobre como calcular a súa dose de insulina.
A insulina pódese producir en frascos e cartuchos. Se empregas insulina en frascos, entón podes mesturar insulina de acción rápida e unha preparación de insulina humana de acción prolongada nunha soa xeringa. Neste caso, a insulina de acción rápida ponse por primeira vez na xiringa. As insulinas de cartucho non están destinadas á preparación de mesturas con outro tipo de insulinas.
Paga a pena prestar especial atención a que a insulina de acción rápida se debe usar só en conexión directa coa inxestión de alimentos.
Epidera. Apidra Glulisina insulina. Insulina glulisino. Contén insulina glulisina (INN - Insulinum glulisinum), elaborada coa tecnoloxía de ADN recombinante empregando E. coli.
A forma de liberación da droga. Solución de inxección 100 UI / ml cartucho 3 ml, inxección para 100 UI / ml botella, inxección para 100 IU / ml xeringa OptiSet 3 ml.
O uso e a dose da droga. Epidera é administrado inmediatamente antes (0-15 minutos) ou inmediatamente despois dunha comida. Epidera debe usarse no réxime de insulinoterapia, que inclúe insulina de acción media ou longa ou un análogo da insulina basal, e pode usarse simultaneamente con axentes hipoglucemicos orais.
A dose de Epidera é seleccionada e corrixida individualmente.
O grao de absorción e, probablemente, o inicio e a duración da acción poden depender do sitio da inxección, a súa aplicación e outros indicadores. A inxección subcutánea na parede abdominal proporciona unha absorción máis rápida que con outros sitios de inxección.
Debe evitarse o dano aos vasos sanguíneos. Despois da inxección, non realice masaxes no lugar da inxección. Aos pacientes se lles debe ensinar a técnica correcta de inxección. As propiedades farmacocinéticas de Epidera presérvanse xeralmente en pacientes con insuficiencia renal. Non obstante, en caso de deterioración da función renal, a necesidade de insulina pode diminuír.
Non se estudaron as propiedades farmacocinéticas de Epidera en pacientes con diminución da función hepática. En pacientes con alteración da función hepática, a necesidade de insulina pode ser menor debido á diminución da gluconeoxénese e á capacidade da insulina para ser metabolizada.
Determinar a función hepática pode levar a unha diminución dos requirimentos de insulina. Non hai información clínica adecuada sobre o uso de Epidera en nenos e adolescentes.
Acción da medicina. A insulina glulisina é un análogo recombinante da insulina humana, similar en potencia. A insulina glulisina actúa máis rápido e por menos tempo que a insulina natural humana. A acción principal da insulina e os seus análogos, incluída a insulina glulisina, está dirixida a regular o metabolismo da glicosa.
A insulina reduce os niveis de glicosa no sangue ao estimular a acumulación periférica de glicosa, especialmente no músculo esquelético e no tecido adiposo e inhibindo a síntese de glicosa hepática. A insulina prevén a lipólise nos adipocitos, proteólise e potencia a síntese de proteínas.
Con administración subcutánea de insulina glulisina e insulina humana normal a unha dose de 0,15 U / kg en diferentes momentos respecto á comida estándar de 15 minutos, atopouse que o control glicémico post-prandial é similar ao habitual A insulina humana usada 30 minutos antes das comidas.
Ao comparar a insulina glulisina e a insulina humana normal 2 minutos antes das comidas, a insulina glulisina proporcionou un control posprandial mellor que a insulina de acción curta humana. O uso de insulina glulisina 15 minutos despois da comida proporciona un control glicémico, similar ao da insulina humana convencional, administrada 2 minutos antes das comidas.
A glulisina insulina preserva o inicio do efecto en pacientes con obesidade. Os indicadores do tempo para alcanzar o 20% dos valores totais de AUC e AUC0-2 h, que son indicadores do efecto hipoglucemático precoz das insulinas, foron 114 min e 427 mg / kg respectivamente para insulina glulisina e 121 min e 354 mg / kg para insulina lispro, 150 min e 197 mg / kg para insulina humana de acción curta.
En ensaios clínicos controlados en adultos, a insulina glulisina non mostrou diferenzas de seguridade e eficacia en subgrupos que diferían por raza e xénero. A absorción máis rápida da insulina glulisina proporcionase substituíndo o aminoácido asparagina na posición B3 da insulina humana pola lisina e a lisina na posición B29 polo ácido glutámico.
Os perfís farmacocinéticos en voluntarios sans e pacientes con diabetes mellitus tipo I ou tipo 2 demostraron que a absorción de insulina glulisina foi 2 veces máis rápida cunha concentración máxima de aproximadamente 2 veces a concentración de insulina humana de acción curta.
Despois da administración subcutánea de insulina, a glulisina é excretada máis rápido que a insulina humana regular, cunha vida media de 42 minutos para a insulina glulisina e 86 minutos para a insulina común. En individuos sans ou pacientes con diabetes tipo I ou tipo 2, a vida media media foi de 37 a 75 minutos.
En caso de deterioración da función renal, a necesidade de insulina pode diminuír, non obstante, queda a capacidade da insulina glulisina de ter un efecto rápido. Non se estudaron as propiedades farmacocinéticas da insulina glulisina en pacientes con alteración da función hepática. Os datos sobre a farmacocinética do fármaco en pacientes anciáns con diabetes son moi limitados.
O uso de insulina glulisina inmediatamente antes das comidas en nenos e adolescentes proporciona un mellor control glicémico posprandial en comparación coa insulina humana convencional, similar a como sucede en pacientes adultos. As flutuacións nos niveis de glicosa (AUC) son 641 mg / h / dl para a insulina glulisina e 801 mg / h / dl para a insulina humana común.
Indicacións de uso. Diabetes mellitus.
Posibles efectos secundarios. O efecto secundario máis común da terapia con insulina é a hipoglucemia, que se produce como consecuencia dunha sobredose de insulina.
Contraindicacións. Hipersensibilidade á insulina glulisina ou outros compoñentes do fármaco, hipoglucemia.
Insulina Apidra (Epidera, Glulisina) - revisión
Quero dicir unhas palabras, por así dicilo en busca, sobre a transición do humalogo á apidra. Volvo a ela hoxe e agora mesmo. Estiven sentado no Humalog + Humulin NPH hai máis de 10 anos. Estudei todas as vantaxes e os inconvenientes do humalogo, dos que hai moitos. Hai un par de anos fun trasladado a apidra durante 2-3 meses, xa que houbo interrupcións na clínica co humalogo.
Segundo o entendo, non fun o único. E xa sabes, moitos dos problemas cos que xa me reconciliara desapareceron de súpeto. O principal problema é o efecto da madrugada. O azucre no estómago baleiro no apidra de súpeto fíxose estable. Non obstante, cun humalogo non tiveron éxito ningún experimento coa dosificación do humalogo e NPH, nin unha proba de azucre durante toda a noite.
En definitiva, pasei unha chea de probas, pasei por moitos médicos e o noso endocrinólogo por fin escribiume un apidra no canto dun humalogo. Hoxe é o primeiro día que fun traballar con el. O resultado é tan malo. Fixo todo hoxe absolutamente coma se lle inxectara un humalogo e por se lle botase máis azucre nos petos. Antes do almorzo, ás 8:00 horas había 6,0, que creo que é normal.
Fun apuñalada de apidra, almorzou, todo é como é habitual segundo XE, chego ao traballo ás 10:00. Azucre 18,9! Lavar este é o meu "record" absoluto! Parece que non me inxectou. Incluso unha simple insulina curta daría un mellor resultado. Por suposto, fixen de inmediato outras 10 unidades, porque considero razoable ir con tales azucres. Ao mediodía, ás 13:30, o sk era xa o 11,1. Hoxe reviso o azucre cada hora e media.
Tipos de insulina ultra-curtos: actúan máis rápido que ninguén
Os tipos de insulina por ultrasonido son Humalog (Lizpro), NovoRapid (Aspart) e Apidra (Glulizin). Son producidos por tres compañías farmacéuticas diferentes que compiten entre si.
A insulina curta habitual é humana e os ultrashort son análogos, é dicir. alterado, mellorado, en comparación coa insulina humana real. A mellora reside no feito de que comezan a baixar o azucre no sangue aínda máis rápido que as curtas habituais - 5-15 minutos despois da inxección.
Apidra para embarazadas
O nomeamento do medicamento no caso de mulleres embarazadas debe realizarse con extrema precaución. Ademais, no marco deste tratamento, o control sobre a relación de azucre no sangue debe levarse a cabo coa maior frecuencia posible. Recoméndase encarecidamente que:
- aos pacientes diagnosticados de diabetes mellitus inmediatamente antes do embarazo ou que desenvolveron a chamada diabetes gestacional das mulleres embarazadas, recoméndase encarecidamente durante todo o período manter un control glicémico uniforme,
- durante o primeiro trimestre do embarazo, a necesidade de representantes femininos de usar insulina pode diminuír rapidamente,
- normalmente, no segundo e no terceiro trimestre aumentará,
- despois do parto, a necesidade do uso dun compoñente hormonal, incluído Apidra, volverá a diminuír significativamente.
Tamén hai que ter en conta que as mulleres que planean un embarazo están simplemente obrigadas a informar ao seu propio médico.
Tamén é necesario recordar que non se sabe completamente se a insulina-glulisina é capaz de pasar directamente ao leite materno.
Este análogo da insulina humana pódese tomar durante o embarazo, pero actúa con coidado, controlando coidadosamente o nivel de azucre e, segundo iso, axuste a dose da hormona. Por regra xeral, no primeiro trimestre do embarazo, a dose do medicamento diminúe, e no segundo e terceiro, aumenta gradualmente.
Despois do parto, a necesidade dunha gran dose de Apidra desaparece, polo que a dose volve reducirse.
Non hai estudos clínicos sobre o uso de Apidra durante o embarazo. Os datos limitados sobre o uso desta insulina por mulleres embarazadas non indican o seu efecto negativo sobre a formación intrauterina do feto, o curso do embarazo ou o recentemente nado.
As probas de reprodución en animais non demostraron diferenzas entre a insulina humana e a insulina glulisina en relación ao desenvolvemento embrionario / fetal, embarazo, parto e desenvolvemento postnatal.
As mulleres embarazadas deberían prescribir Apidra con precaución co control constante obrigatorio dos niveis de glucosa no plasma e control glicémico.
As mulleres embarazadas con diabetes gestacional deben ser conscientes dunha posible redución da demanda de insulina durante o primeiro trimestre do embarazo, un aumento no segundo e terceiro trimestre e unha rápida diminución despois do parto.
Durante todo o embarazo é necesario manter un estado de equilibrio metabólico en pacientes con diabetes preexistente ou xestacional. A necesidade de insulina no primeiro trimestre do embarazo pode diminuír, normalmente aumenta no segundo e no terceiro trimestre. Inmediatamente despois do nacemento, a demanda de insulina diminúe rapidamente.
Non se dispón de información relativa ao uso de insulina-glulisina por mulleres embarazadas. Os experimentos reprodutivos en animais non mostraron diferenzas entre a insulina soluble humana e a insulina-glulisina en relación ao embarazo, o desenvolvemento fetal do feto, o parto e o desenvolvemento postparto.
Non obstante, as mulleres embarazadas deberían prescribir a droga con moito coidado. Durante o período de tratamento, debe controlarse regularmente o control do azucre no sangue.
Os pacientes que tiveron diabetes antes do embarazo ou que desenvolveron diabetes gestacional en mulleres embarazadas necesitan manter o control glicémico durante todo o período.
No primeiro trimestre do embarazo, a necesidade de insulina do paciente pode diminuír. Pero, por regra xeral, nos trimestres posteriores, aumenta.
Despois do parto, a necesidade de insulina diminúe de novo. As mulleres que planean un embarazo deberán informar ao seu proveedor sanitario.
Interacción farmacolóxica
O fármaco debe administrarse por inxección subcutánea, así como por infusión continua. Recoméndase facelo exclusivamente no tecido graxo subcutáneo e usando un sistema especial de acción de bomba.
As inxeccións subcutáneas deben realizarse en:
A introdución de Apidra insulina mediante infusión continua no tecido subcutáneo ou gordo debe realizarse no abdome. Os expertos recomendan alternar entre si para as novas implementacións do compoñente, non só de inxeccións, senón tamén de infusións nas áreas presentadas anteriormente.
Factores como a área de implantación, a actividade física e outras condicións "flotantes" poden ter un efecto no grao de aceleración da absorción e, como consecuencia, no lanzamento e extensión do impacto.
A implantación subcutánea na parede da rexión abdominal convértese nunha garantía de absorción moito máis acelerada que a implantación noutras zonas do corpo humano. Asegúrese de seguir as normas de precaución para excluír a entrada do medicamento nos vasos sanguíneos do tipo sanguíneo.
Non se realizaron estudos de interacción farmacolóxica. Con base na experiencia adquirida con outros fármacos similares, é improbable que as interaccións farmacolóxicas de importancia clínica.
Informa ao teu médico sobre TODOS os medicamentos que toma, aínda que suceda caso por caso.
Algunhas substancias afectan o metabolismo da glicosa, polo que pode ser necesario un axuste da dose da insulina glulisina e un control particularmente coidado.
As substancias que poden aumentar o efecto de redución da glicosa no sangue e aumentar a tendencia á hipoglucemia inclúen medicamentos hipoglucemicos orais, inhibidores da enzima que converten a angiotensina, disopiramidas, fibratos, fluoxetina, inhibidores de MAO, pentoxifilina, propoxifeno, salicilatos e sulfibamida.
Os beta-bloqueantes, clonidina, sales de litio e o alcohol poden potenciar e debilitar a actividade de redución da glicosa da insulina no sangue. A pentamidina pode provocar hipoglucemia, que ás veces entra en hiperglicemia.
Ademais, baixo a influencia de fármacos simpatolíticos como ß-bloqueantes, clonidina, guanetidina e reserpina, os signos de antirregulación adrenérxica poden ser leves ou ausentes.
Directrices de compatibilidade
Debido á falta de estudos de compatibilidade, este medicamento non debe mesturarse con drogas distintas da insulina NPH humana.
Necesita Apidra
A corona "14 de novembro de 2008, 19:51
Connie »14 de novembro de 2008 19:55.
Realmente o buscador non funciona?
A corona "14 de novembro de 2008, 19:58
Hork ™ »14 de novembro de 2008 20:22
A corona "14 de novembro de 2008, 20:48
Hork ™ "14 de novembro de 2008, 20:57